骨骼肌介導的運動神經保護效應:作用途徑和分子機制
王少堃 ,王世強 , ,王一杰 ,郭凱林 ,胥祉涵
運動作為一種簡便易行的非藥物干預手段,惠及大腦及機體的多個器官。骨骼肌是機體運動系統的動力部分,傳統上僅被認為是一種效應器官,在神經-體液的雙重調節作用下通過收縮、牽拉骨骼帶動肢體完成機體的動作執行。研究發現,骨骼肌還能夠產生和分泌數百種生物活性分子,即肌細胞因子(myokines)。這些肌細胞因子以自分泌、旁分泌以及內分泌的方式,廣泛參與調節機體的多種生理活動和病理過程(Kim et al.,2019)。肌細胞因子的發現,為探究骨骼肌與大腦之間的信息交流提供了重要基礎。
由于受到血腦屏障(blood-brain barrier,BBB)的保護,大腦是一個相對獨立的器官。作為運動誘導神經保護效應的關鍵性機制,運動狀態下的骨骼肌收縮如何從外周對大腦產生效益仍缺乏系統研究。許多研究證實了骨骼肌在運動刺激下會產生并分泌多種肌細胞因子,這些肌細胞因子進入血液循環后以激素形式發揮生物學功能,其可透過BBB 作用于腦組織,產生促進神經發生、提高突觸可塑性、增加腦血流量等一系列神經保護效應(Kim et al.,2019)。鑒于運動通過調控骨骼肌內分泌功能產生神經保護效應的機制,本研究探究運動時骨骼肌與大腦之間的其他分子聯系,系統總結骨骼肌介導運動神經保護效應的作用途徑和分子機制,從運動方式、運動強度和運動持續時間3 個方面進一步探討促進腦健康的運動干預策略,旨在為運動神經保護效應的應用提供理論基礎,為神經系統疾病的運動療法提供更多可能性。
1 運動通過骨骼肌內分泌途徑產生神經保護效應
1.1 腦源性神經營養因子
腦源性神經營養因子(brain-derived neurotrophic factor,BDNF)是神經營養因子家族的一員,除在神經系統廣泛表達外,骨骼肌也可表達和分泌BDNF,是目前研究成果相對較多的肌細胞因子(Kim et al.,2019)。
BDNF 與運動對神經系統疾病,如阿爾茨海默病(Alzheimer’s disease,AD)、帕金森病(Parkinson’s disease,PD)和亨廷頓病(Huntington’s disease,HD)等的保護作用密切相關(任可欣,2021)。成熟的BDNF 能通過特異性結合位于神經細胞膜上的高親和力酪氨酸激酶受體B(tyrosine kinase receptor B,Trk B),激活磷脂酰肌醇3-激酶(phosphatidylinositol 3-kinase,PI3K)/蛋 白 激 酶B(protein kinase B,Akt)、絲裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)及其下游的環磷腺苷效應元件結合蛋白(cAMP-response element binding protein,CREB)、磷脂酶Cγ(phospholipase Cγ,PLCγ)及其下游的蛋白激酶C(protein kinase C,PKC)等信號轉導通路,促進神經元生長、存活和樹突發育,增強突觸可塑性,從而增強認知功能,提 高 學 習 記憶與情 緒 調 控 能 力(Kowiański et al.,2018)。此外,BDNF 通過結合低親和力p75 神經營養因子受體(p75 neurotrophin receptor,p75NTR)誘導神經元凋亡和樹突萎縮,起到清除異常或突觸可塑性受損的神經元的作用(Kowiański et al.,2018)。
運動可提高骨骼肌BDNF 的表達量,提高幅度與運動強度呈正相關,同時可以改善中樞神經系統的功能(宗博藝 等,2019)。運動還能夠提高海馬BDNF 的水平,促進海馬細胞增殖,伴隨海馬體積增大,認知功能增強,可降低神經系統疾病的患病風險(Ma?czyńska et al.,2019)。由此推測,由于循環中完整的BDNF 可以通過一種高容量、可飽和的轉運系統透過BBB 進入腦組織,骨骼肌來源的BDNF可能會對大腦產生效益(Ma?czyńska et al.,2019)。因此,盡管BDNF 主要在大腦產生,但運動誘導的神經保護效應至少可以部分解釋為骨骼肌源性BDNF 的有益作用。
1.2 鳶尾素
鳶尾素(irisin)是2012 年發現的一種肌細胞因子,它在過氧化物酶體增殖物激活受體-γ 共激活因子-1α(peroxisome proliferator-activated receptor-γ coactivator-1α,PGC-1α)的調控下,由含Ⅲ型纖連蛋白結構域蛋白5(fibronectin type III domain-containing protein 5,FNDC5)在合成后迅速被蛋白水解酶剪切修飾而成,隨后分泌進入血液循環(Young et al.,2019)。作為運動敏感基因,正常生理狀態下,骨骼肌PGC-1α 表達水平較低,但當受到運動刺激時,PGC-1α 的表達水平會迅速提高,同時顯著提高FNDC5 和鳶尾素的表達水平(Jodeiri Farshbaf et al.,2021)。
研究發現,鳶尾素在調節腦內BDNF 的表達中發揮了重要作用。在海馬體中,PGC-1α 結合雌激素受體α 后能上調FNDC5 和BDNF 的表達,敲除PGC-1α 基因會使FNDC5和BDNF 表達量均降低(Wrann et al.,2013)。在初級皮質神經元中,過表達FNDC5 能使BDNF 表達增加,若采用RNA 干擾對FNDC5 表達進行干擾,會引起BDNF 表達下降(Wrann et al.,2013)。外周鳶尾素具有激活其他組織中PGC-1α 基因的作用(Young et al.,2019)。因此,運動時骨骼肌產生的鳶尾素經血液循環透過BBB 進入腦組織,能激活PGC-1α/FNDC5/BDNF 通路,促進BDNF 表達。
除了調節BNDF 表達外,循環鳶尾素進入腦組織后,還參與維持神經元的功能穩態。鳶尾素通過激活信號轉導和轉錄激活因子3(signal transducer and activator of transcription 3,STAT3)通路誘導神經元增殖,促進海馬神經發生(Moon et al.,2013);通過激活Akt 和細胞外調節蛋白激酶(extracellular regulated protein kinases,ERK)1/2 信號通路抑制炎癥信號通路,減少大腦缺血情況下由氧化應激和炎癥造成的神經元損傷(Li et al.,2017)。
研究發現,不同的運動強度會對外周鳶尾素水平產生不同的影響。在一次性急性跑臺運動中,高強度運動(80%V˙O2max)可引起受試者外周鳶尾素水平升高,但低強度運動(40%V˙O2max)卻不能使鳶尾素水平發生變化(Tsuchiya et al.,2014)。L?ffler 等(2015)指出,急性大強度的運動能引起血清鳶尾素水平迅速、短暫升高,而長期的運動訓練對血清鳶尾素水平沒有顯著影響。因此,一定的運動強度可能是調控骨骼肌鳶尾素表達進而產生運動神經保護效應的必要條件。
1.3 組織蛋白酶B
組織蛋白酶B(cathepsin B,CTSB)是一種蛋白水解酶。Moon 等(2016)發現,CTSB 是一種肌細胞因子,且與運動促進海馬神經元的生長、存活以及空間記憶的形成密切相關。在Moon 等(2016)的體外實驗中,將腺苷酸活化蛋白激酶(AMP-activated protein kinase,AMPK)激動劑AICAR 加入L6 成肌細胞培養基中以模擬運動效果,發現培養液中CTSB 水平升高;動物實驗方面,運動可以誘導小鼠骨骼肌CTSB 基因的表達,提高血漿的CTSB 水平,同時增強海馬BDNF 的表達和神經發生,提高空間記憶能力。敲除了骨骼肌CTSB 基因的小鼠在自愿運動后沒有出現這種情況,并在被強迫游泳時表現出抑郁癥狀。當外周靜脈注射重組CTSB 至CTSB 基因敲除小鼠體內15 min 后,血液和腦組織中CTSB 蛋白水平均明顯提高,并引起BDNF mRNA 和蛋白水平的提高;在人體實驗中,運動可提升受試者外周CTSB 水平,同時提高其記憶力。研究顯示,運動時CTSB 促進海馬神經元存活和遷移、增強突觸可塑性,是通過多功能蛋白P11 依賴性機制上調海馬BDNF 和雙皮質激素(doublecortin,DCX)表達實現的(Moon et al.,2016)。綜上所述,運動可通過激活骨骼肌AMPK 通路誘導CTSB表達,CTSB 經血液循環透過BBB 引起海馬BDNF 和DCX水平提高,產生促進神經發生、增強學習記憶等神經保護效應。
1.4 胰島素樣生長因子1
胰島素樣生長因子1(insulin-like growth factor 1,IGF-1)是胰島素多肽家族的一員。IGF-1 在調節神經系統的結構與功能中發揮關鍵作用,并與運動改善神經系統疾病患者的認知功能和學習記憶能力密切相關(Lewitt et al.,2019)。
運動能刺激骨骼肌產生并分泌IGF-1,提升循環IGF-1水平(Kim et al.,2019)。IGF-1 水平的變化常伴有BDNF水平的變化,如1 型糖尿病患者血清IGF-1 和BDNF 的基礎水平均低于正常個體,高強度間歇運動則能同時提高循環IGF-1 和腦組織BDNF 的水平(?ebrowska et al.,2018)。通過頸動脈注射IGF-1 會引起腦組織BDNF 水平的提高,而IGF-1 抗體或IGF-1 受體拮抗劑的中和作用則會抑制由運動誘導的海馬BDNF 表達上調和神經元再生(于濤,2020)。研究顯示,IGF-1 能通過激活海馬MAPK 激酶(mitogen-activated protein kinase kinase,MEK)/ERK 和PI3K/Akt 通路誘導BDNF 表達和神經元增殖、分化,以發揮神經保護作用(Yuan et al.,2015)。
1.5 血管內皮生長因子
血管內皮生長因子(vascular endothelial growth factor,VEGF)是一種血管生成調節因子,在誘導血管內皮細胞增殖、遷移和存活,提高血管通透性,促進血管再生中發揮重要作用(Fournier et al.,2012)。運動能誘導骨骼肌產生和分泌VEGF,同時引起海馬VEGF 水平升高和神經元增殖。特異性敲除小鼠骨骼肌VEGF 基因或用靜脈注射攜帶嵌合型VEGFR1 受體的腺相關病毒載體(adeno-associated virus,AAV)阻斷循環VEGF 的信號轉導,會導致小鼠海馬血流量減少,削弱運動對海馬VEGF 水平提高和神經發生的誘導作用(Lee et al.,2021; Rich et al.,2017)。VEGF 可以通過與海馬血管內皮細胞以及神經元前體細胞的受體胎肝激酶-1(fetal liver kinase-1,Flk-1)結合,激活MEK/ERK 和PI3K/Akt 等信號通路,調控血管內皮細胞增殖、分化、遷移和通透性的改變,促進大腦血管生成和神經發生(Fournier et al.,2012)。若抑制Flk-1 的表達,會損害海馬突觸可塑性和情感、記憶的鞏固(De Rossi et al.,2016)。
可見,骨骼肌源性VEGF 是誘導大腦血管生成、促進神經元增殖和分化、提高突觸可塑性的重要因子,是運動神經保護效應的關鍵介質。
1.6 成纖維細胞生長因子21
成纖維細胞生長因子21(fibroblast growth factor 21,FGF21)是機體代謝穩態的關鍵調節因子。骨骼肌可通過激活mTOR 蛋白復合體1(mTOR complex 1,mTORC1)和Akt 通路調控FGF21 的表達,循環FGF21 能透過BBB,結合位于下丘腦的受體FGFR1,使共受體β-Klotho 與FGFR1 發生二聚化和自磷酸化(Guridi et al.,2015),從而調節機體的交感神經活動和晝夜節律(Bookout et al.,2013)。若特異性敲除腦組織中的β-Klotho 基因,FGF21 則無法發揮上述生理作用(Bookout et al.,2013)。動物研究表明,FGF21在腦中能通過改善外周胰島素敏感性、增強海馬可塑性、恢復腦線粒體功能和減少神經元凋亡,增強胰島素抵抗肥胖大鼠的認知能力(Sa-Nguanmoo et al.,2016)。
雖然抗阻訓練和高強度間歇訓練均能引起骨骼肌FGF21 水平的顯著提升(He et al.,2018),但有研究顯示,除了運動刺激外,饑餓和胰島素刺激也可上調骨骼肌FGF21 的表達,在線粒體肌病小鼠模型中,骨骼肌FGF21的表達水平亦顯示提高(Keipert et al.,2014)。因此,盡管骨骼肌源性FGF21 能在中樞神經系統中發揮重要調節作用,但可能較多的是由除運動外的其他應激誘導的,未來需要進一步揭示運動如何通過調控骨骼肌FGF21 的表達產生神經保護效應。
1.7 肌源性脂肪細胞因子
1.7.1 瘦素
瘦素(leptin)是一種多肽類激素,許多神經系統疾病的發病過程涉及瘦素的代謝異常(Guo et al.,2017; Watanabe et al.,2021)。運動可使骨骼肌產生瘦素,運動后循環瘦素的水平顯著提升(田振軍 等,2013)。中樞神經系統存在大量瘦素受體,循環瘦素可通過BBB 上的LepRa 受體可飽和轉運機制或者腦脊液進入中樞神經系統,與相應受體結合后參與大腦生理功能的調節(Schulz et al.,2010)。瘦素通過與位于下丘腦的受體LepRb 結合,激活Janus 酪氨酸激酶2(Janus family tyrosine kinases-2,JAK2)/STAT3、PI3K 和ERK1/2 通路,調控機體能量平衡和代謝穩態(彭瑾 等,2021);與海馬神經元上的受體結合,激活JAK2/STAT3 和PI3K/Akt 通路,促進神經祖細胞增殖和海馬神經發生,調節突觸功能,提高情緒調控和學習記憶能力(Garza et al.,2012)。瘦素還可通過激活AMPK 和PGC/過氧化物酶體增殖活化受體(peroxisome proliferators-activated receptors,PPAR)通路,改善神經元線粒體功能,增強神經元存活,減少神經元凋亡(程瑾 等,2014)。
1.7.2 脂聯素
脂聯素(adiponectin,ADN)是一種生物活性多肽,參與了神經系統疾病的發病機制(張小曼 等,2012)。運動能夠誘導骨骼肌產生ADN,ADN 透過BBB 進入腦組織后,通過與海馬體上的受體ADNR1結合,激活ADNR1/AMPK通路,發揮促進神經元增殖和神經發生的作用(Yau et al.,2014)。ADN 還能通過AMPK 途徑降低ROS 水平以減少神經元凋亡,并促進腦血管內皮細胞產生一氧化氮,使腦血管發生擴張,提高腦血流量(Qiu et al.,2011)。ADN基因敲除會削弱運動對海馬神經發生的誘導能力(Qiu et al.,2011)。
綜上所述,瘦素和ADN 與神經系統疾病密切相關。運動可刺激骨骼肌產生并分泌瘦素和ADN,瘦素和ADN進入腦組織后能發揮一系列神經保護作用,其有望成為治療神經系統疾病的新靶點。
運動通過骨骼肌內分泌途徑產生神經保護效應的機制如圖1 所示。
2 運動通過骨骼肌能量代謝途徑產生神經保護效應
2.1 乳酸
乳酸是常見的能量代謝產物,其可借助單羧酸轉運蛋白(monocarboxylate transporters,MCTs)透過BBB 進入腦組織(El Hayek et al.,2019),發揮以下神經保護作用:1)乳酸可激活神經元中的N-甲基-D-天冬氨酸(N-methyl-D-aspartic acid,NMDA)受體及其下游ERK 信號通路,刺激突觸可塑性相關基因的表達,促進長時程增強和記憶的形成(Yang et al.,2014)。2)乳酸可通過結合BBB 上的羥基羧酸受體1(hydroxycarboxylic acid receptor 1,HCAR1)促進腦內VEGF 的表達和血管再生,敲除了HCAR1 基因的小鼠在運動后沒有出現這種情況(Morland et al.,2017)。乳酸結合HCAR1 后,還能抑制腺苷酸環化酶活性,降低海馬cAMP 水平,有助于緩解認知功能障礙(Morland et al.,2015)。3)乳酸可提高神經元BDNF 的表達水平,增強認知功能。在El Hayek 等(2019)的動物實驗中,將乳酸注射至小鼠腹腔,會引起海馬BDNF 和Trk B 水平的提高,同時增強小鼠的學習記憶能力。若用MCT 抑制劑阻礙外周乳酸進入腦組織,運動后小鼠腦中BDNF 的表達水平不會升高。進一步研究顯示,乳酸對腦內BDNF 的調控作用是通過NAD+依賴的組蛋白去乙酰化酶沉默信息調節因子1(sirtuin 1,SIRT1)介導的,運動和腹腔注射乳酸均可引起海 馬SIRT1 表 達 增 加,SIRT1 通 過 激 活PGC-1α/FNDC5/BDNF 通路來提高腦內BDNF 的水平(Müller et al.,2020)。
綜上所述,運動時骨骼肌通過無氧代謝產生的乳酸在進入血液循環后,可透過BBB 作用于大腦,上調BDNF 和VEGF 的表達,從而增強神經可塑性,提高血管再生能力,改善認知功能。
2.2 α-酮戊二酸
α-酮戊二酸是一種能量代謝中間產物,運動時骨骼肌中的三羧酸循環和谷氨酸脫氨基反應均可產生大量的α-酮戊二酸。α-酮戊二酸能通過調節TET 蛋白的酶活性來影響中樞神經系統的結構與功能(Lio et al.,2019)。TET蛋白是一類依賴于α-酮戊二酸和二價鐵離子起催化作用的雙加氧酶,通過參與調節DNA 甲基化和DNA 去甲基化之間的動態平衡,在機體的生長、發育和衰老過程中發揮至關重要的作用。TET 可通過調控神經發育相關基因中5-羥甲基胞嘧啶(5-hydroxymethylcytosine,5hmC)的含量來影響大腦的發育(Li et al.,2014)。TET 基因敲除的小鼠神經元活性基因失調,出現神經元凋亡和突觸可塑性嚴重受損的情況(Rudenko et al.,2013)。TET 還能催化腦內BDNF 基因啟動子上的5-甲基胞嘧啶(5-methylcytosine,5mC)生成5hmC,引起DNA 去甲基化,促使BDNF 基因表達(Ambigapathy et al.,2015)。TET 基因缺失會導致海馬神經元生成受到抑制,空間記憶和認知能力受損(Rudenko et al.,2013)。
TET 發揮作用的酶活性受到α-酮戊二酸水平的影響(Lio et al.,2019)。運動可通過提高骨骼肌α-酮戊二酸的水平增加TET 活性,促進BDNF 表達和海馬神經發生,從而促進大腦發育,增強認知功能和學習記憶(Yuan et al.,2020)。
運動通過骨骼肌能量代謝途徑產生神經保護效應的機制如圖2 所示。
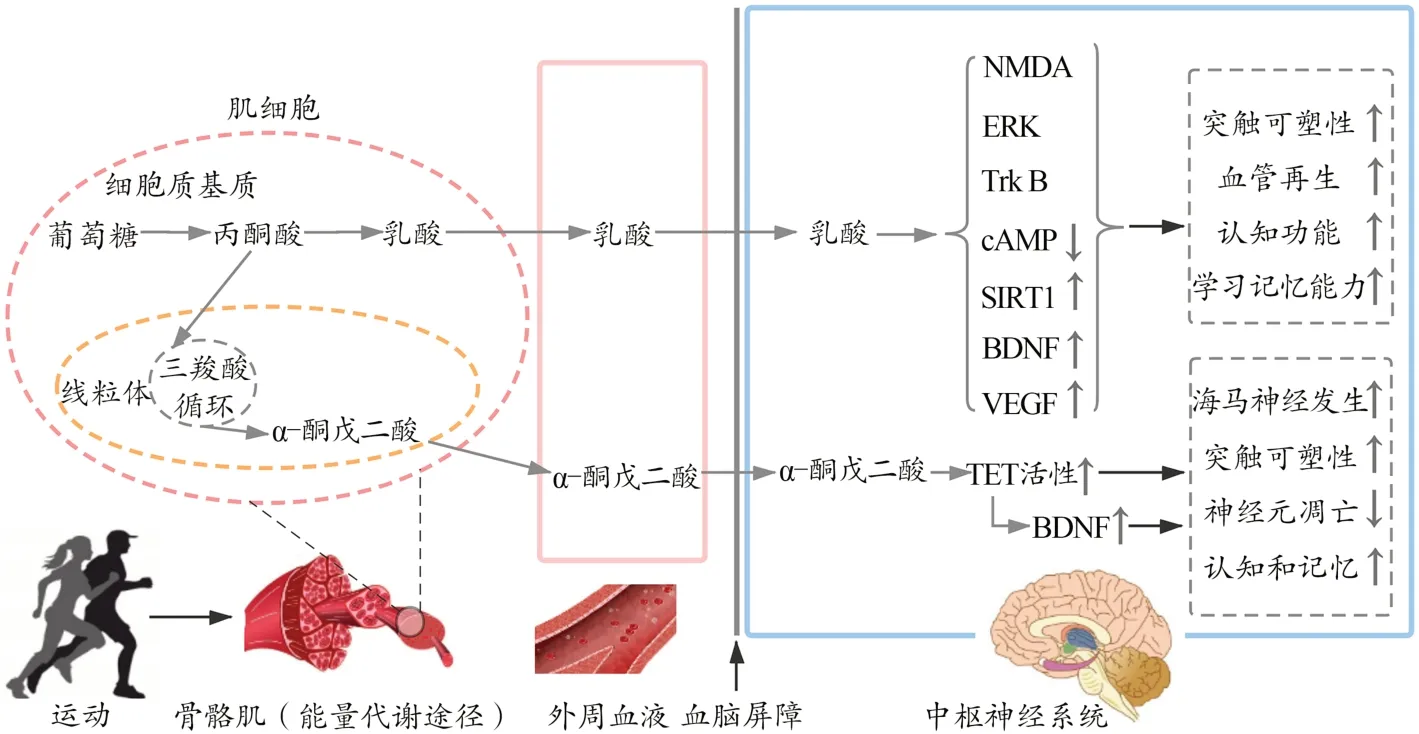
圖2 運動通過骨骼肌能量代謝途徑產生神經保護效應Figure 2.Exercise Induces Neuroprotective Effects through Skeletal Muscle Energy Metabolism
3 運動通過骨骼肌抗炎途徑產生神經保護效應
神經炎癥是指在中樞神經系統中發生的局部炎癥,神經炎癥功能紊亂會引起認知功能障礙,誘發神經系統疾病。外周炎癥可通過多種機制破壞BBB 的正常功能,從而使外周炎癥細胞和促炎細胞因子易于通過BBB 或淋巴管進入腦組織,導致神經炎癥的發生和發展(黃曉雯 等,2021)。運動可通過誘導骨骼肌產生外周抗炎效應來緩解神經炎癥,進而改善神經系統疾病。
3.1 運動通過調控骨骼肌IL-6 表達發揮抗炎作用
運動能夠通過調控多種肌細胞因子的表達參與機體免疫功能的調節過程,以白細胞介素-6(interleukin-6,IL-6)最具代表性。IL-6 作為一種促炎細胞因子參與了神經炎癥反應,并與多種神經系統疾病的發病過程密切相關(劉秋燕 等,2019)。
研究發現,靜息狀態時人體骨骼肌IL-6 處于非常低的水平,急性運動可使循環IL-6 水平呈指數型升高,運動結束時或不久后能達到近基礎水平100 倍的峰值(Pedersen,2013)。急性運動誘導IL-6 的驟升,能觸發外周抗炎級聯反應,促進抗炎細胞因子(如IL-1ra 和IL-10)的產生,抑制IL-1α、IL-1β 和TNF-α 等促炎細胞因子的釋放,降低機體的氧化應激(章嵐 等,2014)。慢性運動對骨骼肌IL-6 的調控有所不同。流行病學研究顯示,體力活動水平與循環IL-6 的基礎水平呈負相關(Sponder et al.,2017)。耐力訓練會降低IL-6 基礎水平,也會降低急性運動引起骨骼肌IL-6 水平升高的幅度,卻上調了IL-6R 受體的表達,據此推測耐力運動使得骨骼肌對IL-6 的分泌產生適應(Sponder et al.,2017)。
綜上所述,不同類型的運動可作用于IL-6 的不同方面,從而改善機體的炎癥狀態。急性運動刺激骨骼肌釋放大量的IL-6,可引發外周抗炎效應,間接緩解神經炎癥;慢性運動可使骨骼肌對IL-6 產生適應,降低IL-6 基礎水平,阻礙其進入腦組織。
3.2 運動通過調控犬尿氨酸代謝過程發揮抗炎作用
色氨酸是一種必需氨基酸,通常在肝臟中代謝為犬尿氨酸(kynurenine,KYN)。KYN 有2 條代謝途徑:一條是大部分的KYN 代謝為3-羥基犬尿氨酸(3-hydroxykynurenine,3-HKYN),并進一步代謝為喹啉酸(quinolinic acid,QA);另一條途徑是代謝為犬尿喹啉酸(kynurenic acid,KYNA)。QA 極具神經毒性,能通過誘發神經元損傷引起神經功能退行性改變(秦宇 等,2020)。KYNA 能夠對抗QA 產生的神經毒性作用。KYN 向KYNA 的轉化,是由犬尿氨酸氨基轉移酶(kynurenine aminotransferase,KAT)催化的(秦宇 等,2020)。正常情況下,KYN 和KYNA 維持著動態平衡。當機體處于炎癥或應激狀態時,促炎細胞因子可促使KYN 向QA 方向代謝,損害BBB 的完整性,導致外周QA易于進入腦組織。因此,KYN代謝通路被認為是連接神經炎癥與神經系統疾病的主要途徑(Agudelo et al.,2014)。
運動能通過激活骨骼肌PGC-1α/PPARα/δ 通路上調KAT 表達,循環KAT 水平的提高促使外周組織中的能借助L 型 氨 基 酸 轉 運 蛋 白1(L-type aminoacid transporter 1,LAT1)輕松透過BBB 的KYN 代謝為不能透過BBB 的KYNA,緩解神經炎癥(Agudelo et al.,2014)。KYNA 還可通過激活G 蛋白偶聯受體35(G protein coupled receptor 35,GPR35)刺激脂肪組織中抗炎基因的表達,減少外周炎癥反應,降低病理性谷氨酸的水平以發揮保護BBB 的作用,維持神經系統微環境的穩態(Fallarini et al.,2010)。
可見,運動刺激下的骨骼肌可作為抗炎器官為機體創造良好的抗炎環境,通過調控IL-6 表達和KYN 代謝過程緩解外周和神經炎癥,降低神經毒害作用,進而減少認知功能損傷,預防和改善神經系統疾病(圖3)。
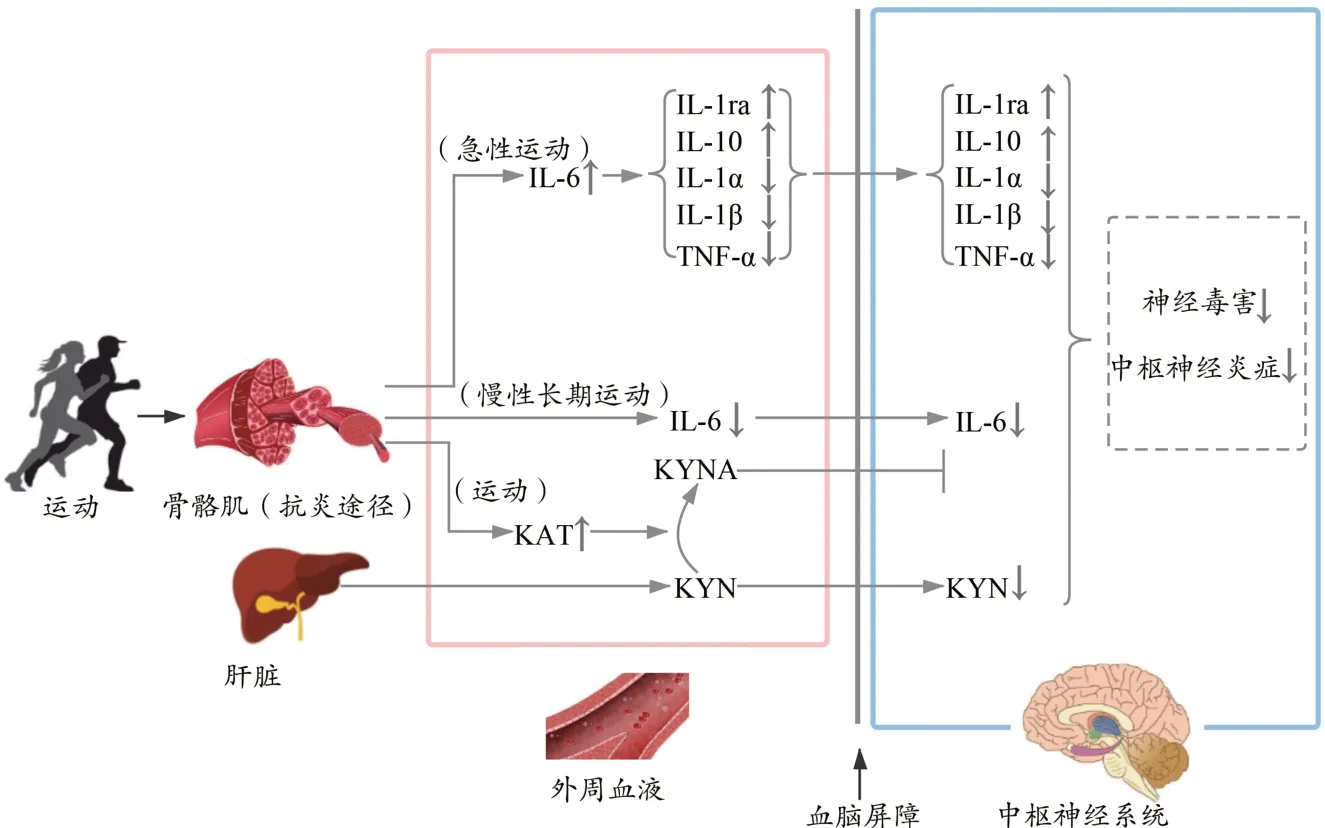
圖3 運動通過骨骼肌抗炎途徑產生神經保護效應Figure 3.Exercise Induces Neuroprotective Effect through Skeletal Muscle Anti-inflammatory Pathway
4 骨骼肌介導的運動神經保護效應途徑及基于該途徑的運動干預策略
4.1 骨骼肌介導的運動神經保護效應途徑
基于以上分析,骨骼肌介導運動神經保護效應有以下3 條途徑:1)運動通過調控骨骼肌內分泌功能上調肌細胞因子相關基因的表達,肌細胞因子以激素的形式作用于腦組織,產生神經保護效應;2)運動可促進骨骼肌能量代謝,代謝產物乳酸和α-酮戊二酸可進入中樞神經系統,產生神經保護效應;3)運動可誘導骨骼肌外周抗炎效應,緩解神經炎癥。這3 條途徑均顯示骨骼肌在運動神經保護效應中發揮了重要的介導作用。在這3 條途徑中,存在對運動具有敏感性的骨骼肌基因或蛋白(如PGC-1α、AMPK 等),作為該途徑的啟動者,通過調控目的基因的表達和代謝產物的合成,從外周向腦組織傳遞神經保護性調節信號,從而改善神經系統疾病(圖4)。
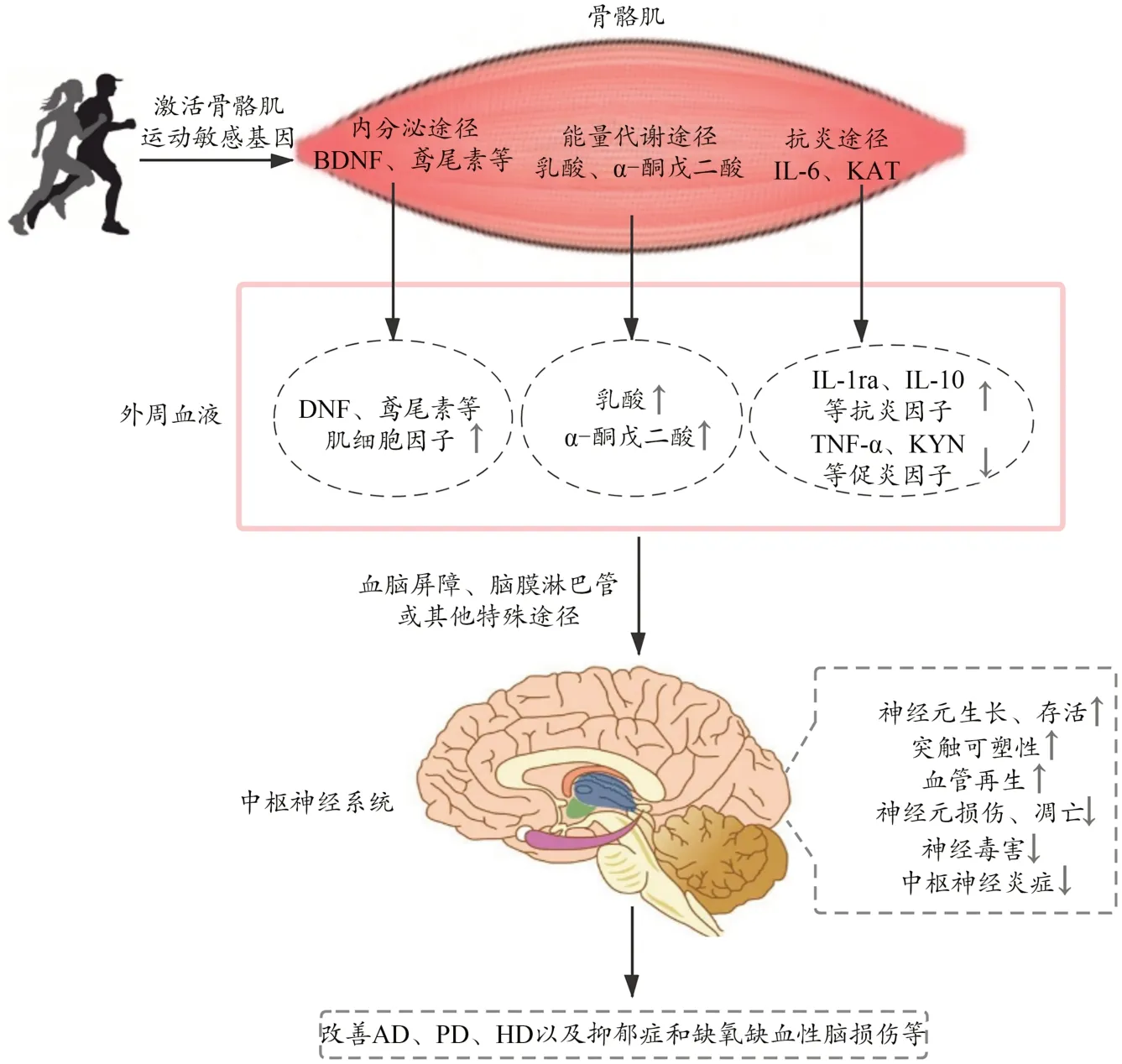
圖4 骨骼肌介導的運動神經保護效應途徑Figure 4.The Pathways of the Skeletal Muscle Mediated Exercise-Induced Neuroprotective Effects
4.2 骨骼肌介導的神經保護效應運動干預策略
4.2.1 運動方式
有氧運動與抗阻運動是臨床上常見的2 種促進腦健康的運動方式。有氧運動被廣泛證實具有促進骨骼肌分泌細胞因子、改善認知記憶相關腦區結構與功能、延緩認知衰退的作用(Kwon et al.,2020)。規律性的有氧運動還能有效改善機體慢性炎癥狀態,降低神經系統疾病的患病風險(周永戰 等,2019);抗阻運動可對炎癥進行有效干預,相較于有氧運動,其是改善由肥胖和肌肉丟失導致的慢性炎癥的較佳運動方式(徐唯,2016)。抗阻運動能夠明顯地誘導神經肌肉適應,增加骨骼肌的肥厚程度,提高骨骼肌基礎代謝率,預防骨骼肌萎縮,從而對骨骼肌功能和大腦認知等產生效益(Chow et al.,2021)。研究發現,將有氧運動與抗阻運動相結合,無論是對于機體炎癥反應(徐唯,2016)、骨骼肌能量代謝(田野 等,2015)還是大腦認知(Sumińska,2021),其干預效果均比單一運動方式更佳。因此,將有氧運動與抗阻運動相結合,可為神經保護效應運動干預策略的臨床應用提供更多新思路。
4.2.2 運動強度
運動強度是制定運動干預策略的關鍵要素,不同的運動強度表現出不同的干預效果。相較于低強度運動,中等強度和高強度運動能顯著提高血清BDNF、IGF-1 等肌細胞因子的水平,改善認知功能和學習記憶能力(Fernández-Rodríguez et al.,2021; Jeon et al.,2017)。在許多神經系統疾病的運動干預中,中等強度和高強度運動顯示出比低強度運動更明顯的改善效果(Balchin et al.,2016)。從骨骼肌能量代謝的角度來說,運動負荷越高,機體血乳酸水平越高,產生的神經保護效應更加持久。研究證實,單次高強度間歇訓練能使血乳酸水平和循環BDNF、VEGF水平顯著提高;長期高強度間歇訓練有利于改善腦血管功能,提高認知和記憶能力(胡靜蕓 等,2021;宗博藝 等,2021)。此外,高強度間歇訓練和中等強度持續訓練均能激活IL-6 抗炎效應,提高外周抗炎細胞因子的水平,降低機體的氧化應激和炎癥反應(Hoekstra et al.,2017)。可見,中等強度和高強度的運動在骨骼肌介導的神經保護效應中能夠發揮更好的誘導作用。
4.2.3 運動持續時間
在骨骼肌介導的運動神經保護效應中,無論是內分泌、能量代謝還是抗炎途徑,均通過骨骼肌產生的生物分子向腦組織傳遞調節信號來實現。研究證實,運動后這些生物分子的外周水平會依次呈現出升高、到達峰值、降低的總體變化趨勢(He et al.,2018)。因此,若想獲得長久的運動神經保護效應,應通過長期的骨骼肌活動使有益的外周生物分子處于較高水平。事實上,許多研究表明,相較于短時間的運動,長時間的運動對延緩認知衰退、提高學習記憶等具有更好的效果(張連成 等,2020)。
綜上所述,長時間、中高強度、有氧與抗阻相結合的運動,可能會最大限度地發揮骨骼肌介導的神經保護效應。由于技術上的限制,目前大多數相關研究是在動物模型和體外系統中進行的,臨床證據相對缺乏,較多的流行病學和臨床關注運動對大腦結構和功能產生的直接影響。未來需進一步明確不同的運動方式、運動強度、運動持續時間和頻率等對骨骼肌內分泌、能量代謝和抗炎功能的影響及其與腦健康之間的聯系,綜合考慮年齡、性別、疾病和遺傳等影響因素,探索針對不同人群的個性化運動干預策略。
5 總結與展望
5.1 總結
運動不僅是促進認知功能、提高學習記憶和情緒調控能力的有效方式,更是預防和改善神經系統疾病的重要手段。本研究以“運動-骨骼肌-大腦”為主線,系統地總結運動通過骨骼肌產生神經保護效應的3 條途徑和分子機制,指出長時間、中高強度、有氧與抗阻相結合的運動是促進腦健康的有效干預策略。
5.2 展望
雖然國內外相關研究為骨骼肌介導運動神經保護效應提供了依據,但仍然存在一些問題:1)蛋白質組學研究發現,骨骼肌能合成并分泌數百種肌細胞因子,現有對肌細胞因子的認識和研究可能只是“冰山一角”,未來還需進一步篩選其他能夠參與介導運動神經保護效應的肌細胞因子,并探索其相應受體;2)由于人體是一個有機整體,運動刺激骨骼肌產生的生物活性分子是否通過作用于機體的其他組織調節其靶向大腦的相關因子活性從而改善大腦功能,仍需進一步研究;3)目前對于運動通過骨骼肌誘導神經保護效應的炎癥機制知之甚少,隨著腦膜淋巴管的發現,今后需更加深層次地揭示外周炎癥與神經系統疾病的聯系。

