術中冰凍病理在立體定向腦深部病變活檢中的應用
陳志杰 林濤 劉妲 鄧斌 張旭標 曾永親 鄧少勇 羅似亮 李海南 成白杰
【摘要】 目的 探討術中冰凍病理檢查在立體定向腦病變活檢的應用價值。方法 回顧性分析2015年6月—2021年10月收治的44例接受神經外科機器人輔助立體定向活檢的腦深部病變患者臨床資料。所有患者行術中冰凍病理,必要時行術中冰凍免疫組化檢查。常規病理結果作為診斷金標準,判斷冰凍結果的確診率、延遲診斷率和誤診率,分析術中冰凍病理的診斷陽性率、診斷符合率及其影響因素。結果 44例患者接受46次活檢手術,有9例患者首次術中冰凍結果為陰性,其中7例調整穿刺深度再次活檢后取得冰凍陽性結果。23例患者通過術中免疫組化及時判斷腫瘤類別。最終44例患者(96.65%)術中冰凍結果陽性,診斷符合率91.3%(35例確診+7例延遲診斷)。穿刺活檢結果為膠質瘤27例(WHO Ⅰ-Ⅱ級6例,WHO Ⅲ-Ⅳ級21例),淋巴瘤12例,生殖細胞瘤4例,淀粉樣變性1例。結論 雖然術中冰凍病理會導致手術耗時增多,但能快速判斷立體定向活檢標本的性質,避免了過度取材,提高手術效率,減少活檢損傷,可應用在神經外科機器人引導下腦病變活檢手術中。
【關鍵詞】 立體定向;腦活檢術;精確診斷;術中冰凍;診斷陽性率
【中圖分類號】 R651;R602 【文獻標志碼】 A 【文章編號】 1672-7770(2023)02-0135-06
Abstract: Objective To explore the application value of intraoperative frozen section analysis in stereotactic biopsy of brain lesions. Methods The clinical data of 44 patients with brain lesions from June 2015 to October 2021 were analyzed retrospectively. Intraoperative frozen pathology analysis was applied in all 46 procedures,immunohistochemical examination was applied if necessary. Regular pathological results were used as the gold standard for diagnosis, and the diagnostic rate, delayed diagnostic rate and misdiagnosis rate of frozen results were judged. The diagnostic positive rate, diagnostic coincidence rate and influencing factors of frozen pathology during operation were analyzed. Results Of the 44 patients who underwent 46 biopsies, 9 patients had negative results in the first intraoperative freezing, and 7 of them had positive results after adjusting the depth of puncture and re-biopsy. 23 patients were diagnosed by intraoperative immunohistochemistry. In the end, 44 patients(96.65%) had positive intraoperative freezing results, and the diagnostic accuracy rate was 91.3%(35 cases were confirmed+7 cases were delayed). The results of puncture biopsy included 27 cases of glioma(6 cases of WHO grade Ⅰ- Ⅱ, 21 cases of WHO grade Ⅲ - Ⅳ), 12 cases of lymphoma, 4 cases of germinoma, and 1 case of amyloidosis. Conclusions Although intraoperative frozen pathology leads to more operation time consuming, it can quickly uncover the pathology of biopsy specimens, avoid excessive sampling, ??improve operation efficiency and reduce surgical complications. Intraoperative frozen pathology can be applied in robot-assisted stereotactic brain lesion biopsy.
Key words: brain biopsy; intracranial tumor; stereotactic biopsy; intraoperative frozen-section; diagnostic yield
基金項目:廣東省醫學科學技術研究基金項目(A2020505);廣東省醫學科學技術研究基金項目(B2023418)
作者單位:510510 廣州,廣東三九腦科醫院神經外二科(陳志杰,林濤,劉妲,鄧斌,張旭標,曾永親),外七科(鄧少勇,羅似亮),病理科(李海南,成白杰)
通信作者: 林濤
立體定向活檢在腦內病變活檢具有微創和精準的優勢,臨床醫生能依據病理結果做出合適的診療策略。神經外科機器人是立體定向活檢技術的常用設備,但是在實際操作中穿刺脫靶后會出現漏診或者誤診。文獻報道的腦立體定向活檢確診率在72.8%~100%,其中采用術中冰凍病理的確診率均在87.6%以上[1-4],應用術中冰凍能夠保證活檢標本的可靠性。但有學者認為術中冰凍耗時且增加取材[5]。鑒于術中冰凍的優勢和潛在不足的一些爭議,本研究回顧性分析2015年6月—2021年10月廣東三九腦科醫院收治的44例腦深部病變活檢患者資料,探討術中冰凍病理在神經外科機器人引導的無框架立體定向腦深部病變活檢中的應用價值。
1 資料與方法
1.1 一般資料 共納入44例患者,其中男26例,女18例;年齡7~76歲,平均(42.52±19.47)歲。有2例患者首次活檢常規病理診斷陰性,各行第二次機器人輔助下活檢,故共行46次活檢手術。采用2016年美國麻醉醫師協會(American Society of Anesthesiologists,ASA)分級標準進行術前風險評估,其中ASA Ⅰ-Ⅱ級37例,ASA Ⅲ級6例,ASA Ⅳ級1例。所有的病變均在腦內深部,多發或者彌漫性(累及多個腦葉)病變者16例,單發病變28例。病變平均直徑為(4.46±2.52)cm (1.5~11.47 cm)。所有患者術前完善頭顱CT及MRI(T1、T2、T2 FLAIR及增強掃描)檢查,部分患者行PET-CT、MRS和ASL等檢查,必要時行腰椎穿刺做腦脊液檢查。納入標準:(1)深部病變且影像診斷困難;(2)病變位于功能區,手術風險極高;(3)影像診斷相對明確,放療前行病理確診,如生殖細胞瘤;(4)病變惡性程度高或者良性腫瘤術后復發并提示惡化,家屬拒絕再次開顱手術切除;(5)顱內腫瘤綜合治療后需鑒別腫瘤進展或放射性壞死;(6)患者及家屬同意行機器人輔助下活檢。排除標準:(1)患者存在基礎疾病,全身情況不能耐受麻醉或手術,ASA為Ⅳ級或以上;(2)凝血功能存在手術禁忌;(3)影像提示腦疝形成;(4)患者及家屬拒絕使用機器人輔助下活檢[6]。
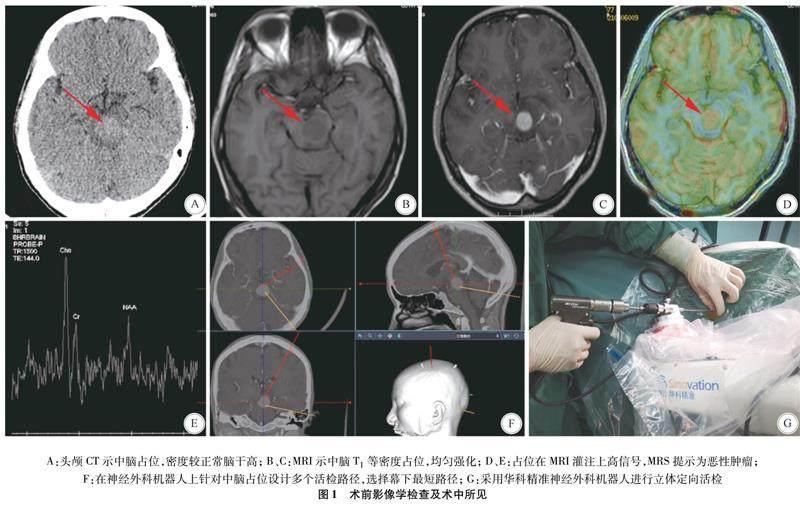
1.2 術前準備與規劃 術前共為20例患者組織由神經外科、神經內科、影像科、腫瘤放療科和病理科參加的多學科討論,為26例患者組織神經外科科內術前疑難病例討論。單個巨大占位或者多發占位的活檢部位優先選擇在非功能區的病變作為活檢靶點。具體手術操作步驟參見本研究前期文獻[6]。本研究中,16 次手術由ROSA神經外科機器人(法國,Medtech)輔助下完成穿刺活檢,30次手術由SINO神經外科機器人(北京華科精準)輔助下完成穿刺活檢。見圖1。
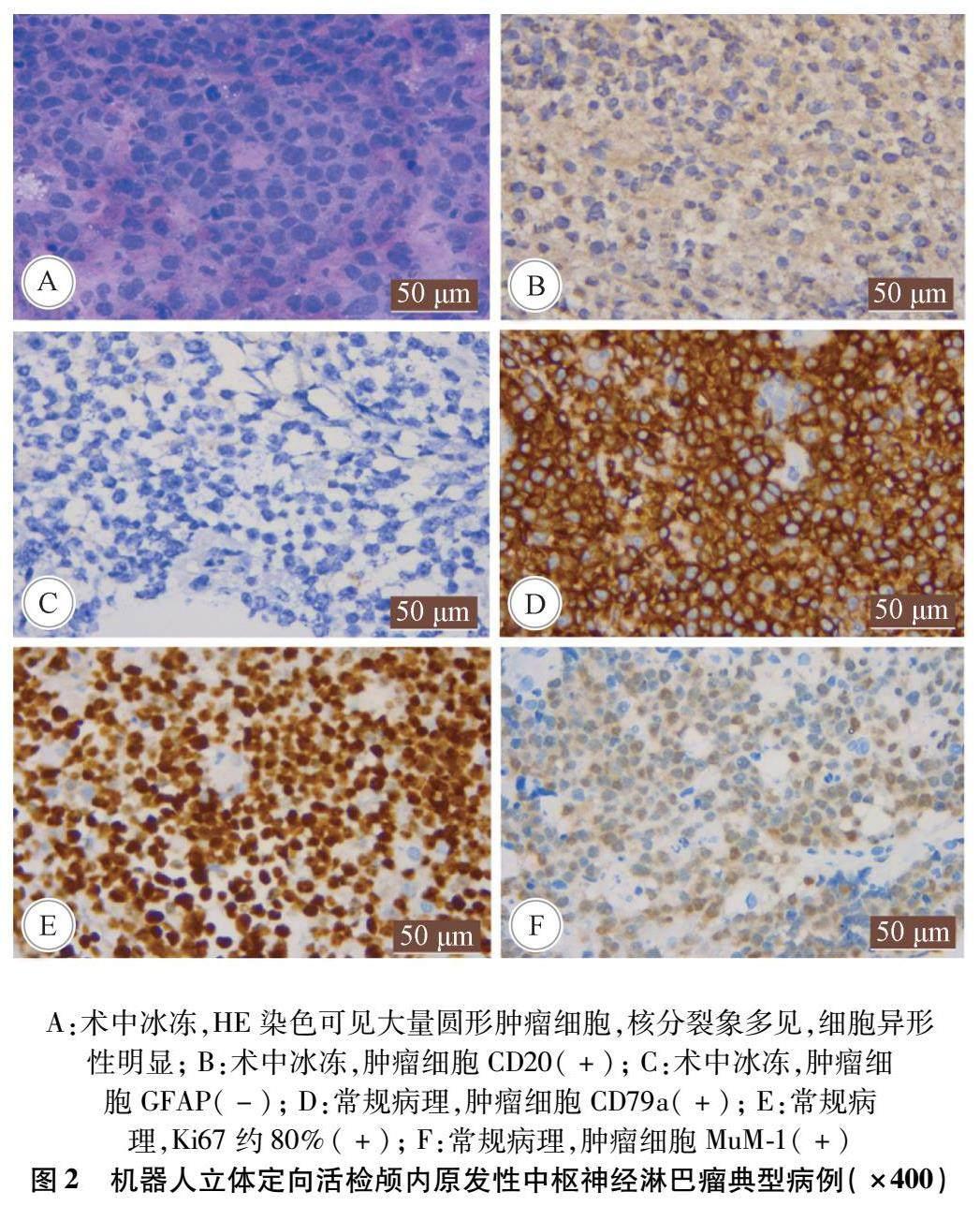
1.3 標本送檢和冰凍病理方法 穿刺獲得標本后觀察其性質和顏色,先送檢1~2條約0.1 cm×1 cm大小的外觀異常(一般為膠凍樣,魚肉狀,圖2)的標本行術中冰凍病理檢查。在等待術中冰凍結果時繼續穿刺活檢,留取2~4條標本作為常規病理,留取標本后在穿刺針的末端滴注生理鹽水,借助水壓對病灶壓迫止血。常規病理檢查如無法確診,則補充行基因檢測包括熒光原位雜交(fluorescence in situ hybridization,FISH)檢測、基因重排等。
術中冰凍的處理采取0.2 cm間隔的書頁狀平行方式切開,仔細關注標本形態。儀器采取冰凍切片機(LEICA CM1950,德國徠卡),溫度設置成-19~-20 ℃,切片厚度為4 μm,1個組織切片2~3張,HE染色后用光鏡予以觀察。如冰凍HE染色診斷困難,立即補充行免疫組化;剩余的組織行石蠟切片處理。
1.4 指標觀察 本研究以常規病理整合診斷(組織學表型和基因表型)以及炎癥診斷結果為金標準,比較術中冰凍病理在機器人立體定向活檢中的診斷價值。結果分為三種:(1)確診:術中冰凍病理診斷和整合診斷的結果符合或基本符合的,術中和術后均符合炎癥診斷的;(2)延遲診斷:術中冰凍判斷腫瘤WHO分級與常規病理不一致;(3)誤診:術中冰凍切片診斷出現假陽性結果、假陰性結果。其中確診和延遲診斷歸類為診斷符合。腫瘤患者病理診斷依據2016版WHO中樞神經系統腫瘤分類標準。如多靶點活檢病理結果相同,則合并為一個結果;如患者同時存在高級別膠質瘤和低級別膠質瘤,則診斷為高級別膠質瘤。
1.5 統計學分析 采用統計學軟件SPSS 21.0進行檢驗,合計數值采取例數(n)或率(%)表示,行χ2檢驗,以P<0.05 認為差異具有統計學意義。
2 結 果
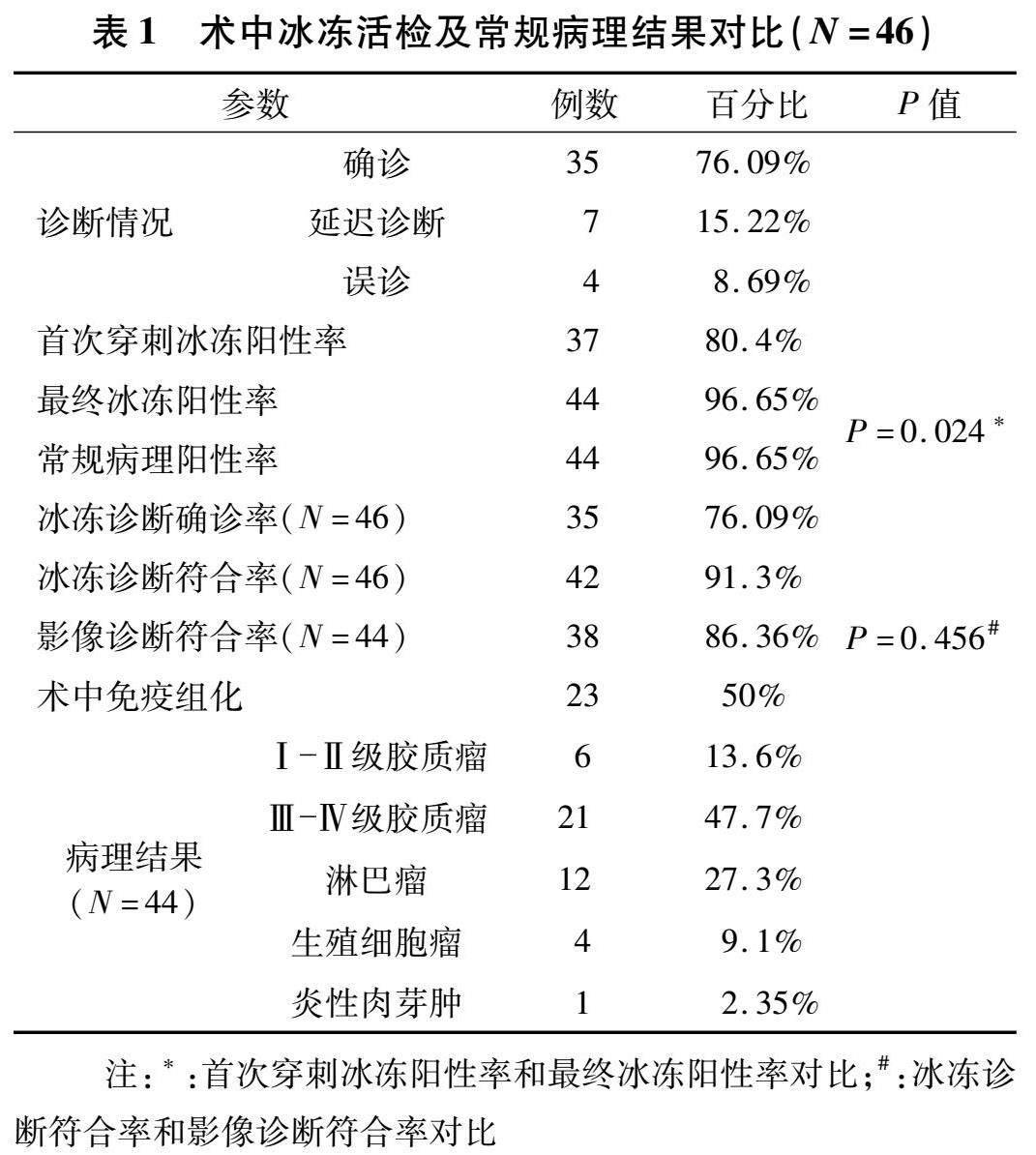
2.1 手術情況和術中冰凍結果 44例患者共接受46次手術,行52個靶點的穿刺活檢,術中冰凍病理平均耗時(26±5.6)min (20~41 min)。有9例(19.56%)患者首次術中冰凍結果為陰性,其中7例術中調整穿刺深度或更換靶點后取得陽性結果,另有2例患者再次術中冰凍病理仍為陰性,術后通過常規病理和(或)基因重排得到確診。每例患者送檢術中冰凍1~4次(中位數1次),共行60次穿刺活檢行術中冰凍病理檢查。單次手術術中冰凍陽性率從80.44%(37/46)提高到95.65%(44/46),具有明顯差異(P=0.024,表1)。將術中冰凍與常規病理對比,診斷符合率91.3%(35例確診+7例延遲診斷),誤診4例(包含2例術中冰凍陰性)。另外,共有23例患者的冰凍切片做了術中免疫組化進一步明確病變性質。6例患者術后出現術區血腫,包括5例患者出現無癥狀性小出血和1例嚴重遲發性腦出血導致死亡。除這例腦出血致死亡患者外,其余患者均未發生手術相關性神經功能障礙或者顱內感染,并接受下一步的專科治療。見表1。
2.2 術后病理結果 病理整合診斷結果為膠質瘤27例(WHO Ⅰ-Ⅱ級6例,WHO Ⅲ-Ⅳ級21例),淋巴瘤12例,生殖細胞瘤4例,淀粉樣變性1例。其中1例患者術中連續送檢4次冰凍病理均為陰性,最終依靠基因測序診斷為膠質母細胞瘤 WHO Ⅳ級。
3 討 論
神經外科機器人國內的應用達20多年,進口品牌ROSA和國產品牌包括SINO、Tirobot Cranial、睿米(Remebot)機器人等已廣泛應用在神經外科的多種手術中[7-9],包括立體定向活檢手術。因受到取材、制片、閱片等相關因素的影響會出現假陰性和假陽性診斷,很多立體定向活檢手術并未采用術中冰凍病理(表2)。Shooman等[5]認為術中冰凍不會提高診斷率,反而會導致手術時間延長,并增加腦出血和功能障礙的發生率。本研究者認為,在無術中冰凍病理的情況下為了保證常規診斷陽性率,術者可能會過度取材,從而增加并發癥的發生率。因此本研究在開展神經外科機器人立體定向腦深部病變活檢手術中,均采用了術中冰凍病理來及時判斷病變性質。
本研究中的首次穿刺活檢術中冰凍陽性率為80.4%(37例次),通過調整靶點或者穿刺深度,最終單次手術術中冰凍病理陽性率提高到96.65%(44例次)。出現首次穿刺陰性的原因是很多病變在重要功能區(如腦干、丘腦和基底節等),所以在設計活檢靶點的時候偏于保守,有時將靶點定位在病變周邊導致穿刺標本缺少病變特征。本研究的最終常規病理陽性率達96.65%,如無術中冰凍病理協助判斷活檢組織性質的話,診斷陽性率可能會低于此。
很多研究為提高立體定向活檢的診斷陽性率做了很多的嘗試,包括術中冰凍病理、術中組織涂片、增加活檢標本量以及采用機器人輔助手術等[10]。術中冰凍病理檢查在開顱腦病變切除手術中應用廣泛,但是在立定定向活檢中的還比較有限。限制該技術的原因包括,病損組織少,對冰凍切片技術要求比較高。有研究認為單個靶點至少4條活檢標本方能確保診斷的準確性[11]。本研究中,如果術中冰凍結果陽性,則留取2~4條標本送常規病理(圖2),避免了過度取材。本研究總結了近15年來各類技術實施的立體定向活檢的文獻,發現只有6個(6/22)研究采用了術中冰凍病理檢查,其中僅有2個研究的所有病例均采用該方法[2,12](表2)。上述研究的術中冰凍病理活檢陽性率在70.1%~97.2%之間,最終的常規病理結果陽性率達87.6%~98.7%[1-3,13-14]。Verploegh等[15]認為隨著操作的熟練和經驗的積累,術者可以不依賴術中冰凍病理,但是本研究認為,患者及家屬在決定接受立體定向活檢手術時,便對手術結果有很大的期待,應盡量在單次手術即獲得正確的病理診斷。
本研究單次手術術中冰凍診斷符合率為91.3%(42/46)。近15年來,國內外文獻報道立體定向活檢的術中冰凍的診斷符合率在70%~81%之間(表2),這些研究的手術設備包括機器人、框架和非機器人的無框架立體定向儀器等[2-3,13]。在不采用術中冰凍切片情況下,為了提高診斷陽性率,有學者建議采用多個靶點活檢提高陽性率[2-3,5],但這種方法耗時會更多,而且增加腦出血的風險。如果采用框架行多個靶點活檢時調整靶點的操作較為繁雜,則會耗時更多,神經外科機器人操作簡化,適合多靶點活檢并行術中冰凍病理檢查。此外,本組中有1例誤診患者的術中冰凍結果陽性,但是常規病理結果為陰性,究其原因可能是冰凍標本和常規病理標本不是同一條穿刺標本。后來,本研究改進了這種送檢方法,穿刺活檢的單個標本一半送術中冰凍切片,另一半送常規病理檢查。將2~3條標本的各一半合起來送術中冰凍檢查,既能保證充足的標本量,又能保證常規病理和術中冰凍病理的一致性。
廣東三九腦科醫院影像科對所有的患者術前影像進行了定性診斷,診斷符合率為72.73%(32/44,表2)。得益于影像科的高確診率,本研究及時調整了治療方法,讓很多被誤診為自身免疫性腦炎或脫髓鞘的患者接受立體定向活檢。此外,通過合理安排,術前1 d和病理科同事預約術中冰凍事宜,以便他們做好工作安排盡早作出診斷。這些患者通過活檢明確腦腫瘤后,轉至腫瘤科行綜合治療。
雖然神經外科機器人定位精準,但實際操作中仍有可能出現偏差,和其他立體定向活檢一樣出現脫靶的情況[5]。脫靶是導致術中冰凍病理漏診或者誤診的主要因素,出現該情況的原因包括:(1)病變過小,活檢針側切口沒有正對病變組織;(2)操作者對影像的解讀不到位,將非典型區域定位為靶點;(3)操作者為了避開重要功能區而選擇周邊的靶點;(4)機器人操作不當。一旦術中冰凍的結果為陰性,術者應馬上分析原因,立即調整靶點深度或更改靶點。本研究中,有3例患者的病變小于2 cm,最小的病變約1.5 cm,對這類小病灶進行穿刺時,如果活檢針側切口沒有正對病變組織,那術中冰凍的結果可能就是陰性的。術中在對小病灶進行活檢時,應當盡量穿刺到病灶中心,如冰凍結果陰性,則活檢針側切口方向即可,不需要調整穿刺深度。有研究認為深部病變活檢是影響診斷率的重要因素[2],而有研究則認為是淺部病變容易脫靶[16],這可能和術者操作不同的活檢設備有關。
標本不合格和病理醫生閱片錯誤,是術中冰凍病理結果陰性兩個重要主觀因素。標本不合格包括送檢不合格標本(外科醫生取出了多份標本,但送檢了腦組織部分)和病理科技師處理標本不合格。一般腦腫瘤標本呈魚肉狀,這與乳白色的腦組織有明顯的外觀差異,術者應當觀察后選擇合適的標本送檢。病理醫生對的標本解讀具有較強的主觀性,閱片失誤在所難免,建議術中冰凍病理由多位有經驗的病理醫生共同閱片診斷。
由于部分淋巴瘤和膠質瘤的形態學上不易區分,本研究中出現診斷困難時病理科醫生會立即做2~5項術中免疫組化,耗時約20~30 min。共有23例次的患者行術中免疫組化及時為腫瘤定性,其中3例為低級別膠質瘤,10例為高級別膠質瘤, 9例為淋巴瘤,1例為生殖細胞瘤。通過做免疫組化獲得較為準確的病理結果(圖2),術者能夠在手術當天告知患者家屬病理結果,并且盡早為淋巴瘤患者開始化學治療,可改善患者生存質量和延長生存期[17]。有研究者總結2005年以前的文獻發現,術中冰凍的診斷符合率約為73 % (51%~91 %)[4]。本研究中,對定性診斷困難的標本采用了術中免疫組化檢查,雖然耗時增多,但最終診斷符合率達91.3%,達到理想的診斷陽性率和診斷符合率。
本研究為回顧性分析,所有患者均行術中冰凍病理檢查,未設立無術中冰凍組作為對照研究。本研究中,首次術中冰凍病理陰性率較高,平均耗時較多,需要術者今后在手術中提高手術技巧。雖然術中冰凍病理會導致手術耗時增加,但能快速判斷立體定向活檢標本的性質,及時行下一步治療,避免了過度取材,提高手術效率,減少活檢損傷,可應用在神經外科機器人引導下腦病變活檢手術中。
[參 考 文 獻]
[1]Zanello M,Roux A,Senova S,et al.Robot-assisted stereotactic biopsies in 377 consecutive adult patients with supratentorial diffuse gliomas:diagnostic yield,safety,and postoperative outcomes[J].World Neurosurg,2021,148(4):e301-e313.
[2]Woodworth GF,McGirt MJ,Samdani A,et al.Frameless image-guided stereotactic brain biopsy procedure:diagnostic yield,surgical morbidity,and comparison with the frame-based technique[J].J Neurosurg,2006,104(2):233-237.
[3]Taweesomboonyat C,Tunthanathip T,Sae-Heng S,et al.Diagnostic yield and complication of frameless stereotactic brain biopsy[J].J Neurosci Rural Pract,2019,10(1):78-84.
[4]Khatab S,Spliet W,Woerdeman PA.Frameless image-guided stereotactic brain biopsies:emphasis on diagnostic yield[J].Acta Neurochir(Wien),2014,156(8):1441-1450.
[5]Shooman D,Belli A,Grundy PL.Image-guided frameless stereotactic biopsy without intraoperative neuropathological examination[J].J Neurosurg,2010,113(2):170-178.
[6]劉妲,陳志杰,山常國,等.神經外科機器人輔助立體定向活檢在腦深部病變的應用(附26例臨床分析)[J].立體定向和功能性神經外科雜志,2021,34(1):4-8.
[7]吳世強,焦利武,肖群根,等.Remebot機器人輔助下立體定向活檢術的臨床應用[J].中國臨床神經外科雜志,2017,22(11):751-753.
[8]王逸鶴,單永治,趙國光,等.ROSA機器人輔助下立體定向活檢術在腦內病變診斷中的作用[J].中國臨床神經外科雜志,2017,22(1):11-13.
[9]劉德峰,王秀,張勇,等.Tirobot Cranial立體定向手術機器人輔助腦深部電極植入定位精度的研究[J].臨床神經外科雜志,2018,15(2):81-84.
[10]Jain D,Sharma MC,Sarkar C,et al.Correlation of diagnostic yield of stereotactic brain biopsy with number of biopsy bits and site of the lesion[J].Brain Tumor Pathol,2006,23(2):71-75.
[11]Brainard JA,Prayson RA,Barnett GH.Frozen section evaluation of stereotactic brain biopsies:diagnostic yield at the stereotactic target position in 188 cases[J].Arch Pathol Lab Med,1997,121(5):481-484.
[12]楊帆,董超,湯其華,等.立體定向活檢術在丘腦病變診斷的作用[J].中國微侵襲神經外科雜志,2021,26(8):384-385.
[13]Mader MMD,Rotermund R,Martens T,et al.The role of frameless stereotactic biopsy in contemporary neuro-oncology:molecular specifications and diagnostic yield in biopsied glioma patients[J].J Neurooncol,2019,141(1):183-194.
[14]Legnani FG,Franzini A,Mattei L,et al.Image-guided biopsy of intracranial lesions with a small robotic device(iSYS1):a prospective,exploratory pilot study[J].Oper Neurosurg(Hagerstown),2019,17(4):403-412.
[15]Verploegh ISC,Volovici V,Haitsma IK,et al.Contemporary frameless intracranial biopsy techniques:might variation in safety and efficacy be expected?[J].Acta Neurochir(Wien),2015,157(11):2011-2016.
[16]趙思源,劉娟,張劍寧,等.384例立體定向腦活檢術診斷率的影響因素分析[J].立體定向和功能性神經外科雜志,2014,27(6):327-330.
[17]梁肖歡,楊超,林佳平,等.63例原發性顱內惡性淋巴瘤臨床分析[J].臨床神經外科雜志,2016,13(4):272-275,280.
[18]Dammers R,Schouten JW,Haitsma IK,et al.Towards improving the safety and diagnostic yield of stereotactic biopsy in a single centre[J].Acta Neurochir(Wien),2010,152(11):1915-1921.
[19]Dlaka D,Sˇvaco M,Chudy D,et al.Frameless stereotactic brain biopsy:a prospective study on robot-assisted brain biopsies performed on 32 patients by using the RONNA G4 system[J].Int J Med Robot,2021,17(3):e2245.
[20]王俊文,吳世強,趙愷,等.Remebot機器人輔助立體定向活檢術診斷率的影響因素分析[J].中國耳鼻咽喉顱底外科雜志,2021,27(3):321-324.
[21]Wu SQ,Wang JW,Gao P,et al.A comparison of the efficacy,safety,and duration of frame-based and Remebot robot-assisted frameless stereotactic biopsy[J].Br J Neurosurg,2021,35(3):319-323.
[22]Terrier L,Gilard V,Marguet F,et al.Stereotactic brain biopsy:evaluation of robot-assisted procedure in 60 patients[J].Acta Neurochir(Wien),2019,161(3):545-552.
[23]Dawes W,Marcus HJ,Tisdall M,et al.Robot-assisted stereotactic brainstem biopsy in children: prospective cohort study[J].J Robot Surg,2019,13(4):575-579.
[24]Georgiopoulos M,Ellul J,Chroni E,et al.Efficacy,safety,and duration of a frameless fiducial-less brain biopsy versus frame-based stereotactic biopsy:a prospective randomized study[J].J Neurol Surg A Cent Eur Neurosurg,2018,79(1):31-38.
[25]Carai A,Mastronuzzi A,De Benedictis A,et al.Robot-assisted stereotactic biopsy of diffuse intrinsic pontine glioma:a single-center experience[J].World Neurosurg,2017,101(2):584-588.
[26]De Benedictis A,Trezza A,Carai A,et al.Robot-assisted procedures in pediatric neurosurgery[J].Neurosurg Focus,2017,42(5):E7.
[27]Nishihara M,Takeda N,Harada T,et al.Diagnostic yield and morbidity by neuronavigation-guided frameless stereotactic biopsy using magnetic resonance imaging and by frame-based computed tomography-guided stereotactic biopsy[J].Surg Neurol Int,2014,5(Suppl 8):S421-S426.
[28]Gempt J,Buchmann N,Ryang YM,et al.Frameless image-guided stereotaxy with real-time visual feedback for brain biopsy[J].Acta Neurochir(Wien),2012,154(9):1663-1667.
(收稿2022-04-10 修回2022-07-14)