莓茶提取物對2型糖尿病大鼠糖脂代謝及肝臟SIRT1、AMPK、PGC-1α蛋白表達的影響
肖穎馥 王能 盛文 劉露梅 孫天松 李波男 何清湖
〔摘要〕 目的 探索莓茶提取物對2型糖尿病(type 2 diabetes mellitus, T2DM)大鼠糖脂代謝及肝臟沉默信息調節(jié)因子1(silence information regulator 1, SIRT1)、AMP活化蛋白激酶(AMP activated protein kinase, AMPK)、過氧化物酶體增殖物激活受體γ輔助活化因子1α(peroxisome proliferator-activated receptor-γ coactivator-1α, PGC-1α)蛋白表達的影響。方法 高脂高糖喂養(yǎng)聯合鏈脲佐菌素(35 mg/kg)腹腔注射建立T2DM大鼠模型,建模成功后隨機分為模型組、莓茶低劑量組(0.4 g/kg)、莓茶高劑量組(0.8 g/kg),另設普通飼料喂養(yǎng)大鼠為正常組,每組8只。各組灌胃給藥6周后,行口服葡萄糖耐量試驗計算血糖-時間曲線下面積(area under the curve, AUC),ELISA法檢測空腹血胰島素(fasting insulin, FINS)水平,計算穩(wěn)態(tài)模型以評估胰島素抵抗指數(homeostatic model assessment for insulin resistance, HOMA-IR),全自動生化分析儀測定血清總膽固醇(total cholesterol, TC)、甘油三酯(triglycerides, TG)、高密度脂蛋白膽固醇(high density lipoprotein cholesterol, HDL-C)、低密度脂蛋白膽固醇(low density lipoprotein cholesterol, LDL-C)、超氧化物歧化酶(superoxide dismutase, SOD)、丙二醇(malondialdehyde, MDA)水平,HE染色觀察肝臟組織形態(tài)學變化,Western blot檢測肝臟SIRT1、AMPK、PGC-1α蛋白表達。結果 與正常組比較,模型組FBG、AUC、FINS、HOMA-IR、TC、TG、LDL-C、MDA均明顯升高(P<0.01),HDL-C、SOD和SIRT1、AMPK、PGC-1α蛋白表達均明顯降低(P<0.01),肝臟組織肝索排列紊亂,肝細胞間隙不清晰,呈脂肪變性改變。與模型組比較,莓茶低劑量組、莓茶高劑量組FBG、FINS、HOMA-IR、TG、MDA均明顯降低(P<0.05,P<0.01),SOD和SIRT1、AMPK、PGC-1α蛋白表達均明顯升高(P<0.05,P<0.01),肝臟組織肝索排列相對整齊,脂肪變性得到改善;莓茶高劑量組AUC、TC均明顯降低(P<0.05),HDL-C明顯升高(P<0.05)。與莓茶低劑量組比較,莓茶高劑量組FBG、AUC、FINS、TC、MDA均明顯降低(P<0.05),SIRT1、AMPK、PGC-1α蛋白表達均明顯升高(P<0.05)。結論 莓茶提取物能在一定程度上改善T2DM大鼠糖脂代謝,減輕胰島素抵抗,其機制可能與改善氧化應激,調節(jié)肝臟SIRT1、AMPK、PGC-1α蛋白表達有關。
〔關鍵詞〕 2型糖尿病;莓茶提取物;氧化應激;沉默信息調節(jié)因子1;AMP活化蛋白激酶
〔中圖分類號〕R285.5? ? ? ?〔文獻標志碼〕A? ? ? ? 〔文章編號〕doi:10.3969/j.issn.1674-070X.2023.05.008
Effects of ampelopsis grossedentata extract on glycolipid metabolism and SIRT1, AMPK and
PGC-1α expressions of liver in type 2 diabetes mellitus rats
XIAO Yingfu WANG Neng SHENG Wen LIU Lumei SUN Tiansong LI Bonan HE Qinghu
1. College of Chinese Medicine, Hunan University of Chinese Medicine, Changsha, Hunan 410208, China; 2. Laboratory of Andrology, Hunan University of Chinese Medicine, Changsha, Hunan 410208, China; 3. College of Integrated Chinese and Western Medicine, Hunan University of Chinese Medicine, Changsha, Hunan 410208, China; 4. Hunan University of Medicine, Huaihua, Hunan 418000, China
〔Abstract〕 Objective To explore the effects of ampelopsis grossedentata extract on glycolipid metabolism and silence information regulator 1 (SIRT1), AMP activated protein kinase (AMPK) and peroxisome proliferator-activated receptor-γ coactivator 1-α (PGC-1α) expressions of liver in type 2 diabetes mellitus (T2DM) rats. Methods T2DM rat model was established by high-fat/high-sugar diet combined with streptozotocin injection (STZ, 35 mg/kg) intraperitoneally. Then, T2DM rats were randomly divided into model group, low-dose ampelopsis grossedentata extract group (0.4 g/kg), and high-dose ampelopsis grossedentata extract group (0.8 g/kg), with 8 rats in each one. In addition, normal diet rats (n=8) were set as the normal group. After 6 weeks of gavage administration, oral glucose tolerance tests were performed to calculate the area under the curve (AUC) of glucose-time, fasting insulin (FINS) levels were measured by ELISA, and homeostatic model assessment for insulin resistance (HOMA-IR) was performed. Total cholesterol (TC), triglycerides (TG), high-density lipoprotein cholesterol (HDL-C), low-density lipoprotein cholesterol (LDL-C), superoxide dismutase (SOD) and malondialdehyde (MDA) levels were measured by automated biochemical analyzer. The morphological changes of liver were observed by HE staining, and the protein expressions of SIRT1, AMPK and PGC-1α in liver tissues were measured by Western blot. Results Compared with normal group, fasting blood glucose (FBG), AUC, FINS, HOMA-IR, TC, TG, LDL-C and MDA levels dramatically increased in model group rats (P<0.01), the expressions of HDL-C, SOD, SIRT1, AMPK and PGC-1α decreased significantly (P<0.01), the arrangement of hepatic cord in liver tissue was disordered, the hepatic intercellular space was unclear and hepatic steatosis was exhibited. Compared with model group, FBG, FINS, HOMA-IR, TG and MDA significantly decreased in low- and high-dose ampelopsis grossedentata extract groups (P<0.05, P<0.01), while the expressions of SOD, SIRT1, AMPK and PGC-1α significantly increased (P<0.05, P<0.01), the hepatic cord arrangement was relatively neat, and hepatic steatosis was alleviated. AUC and TC in high-dose ampelopsis grossedentata extract group were significantly lower (P<0.05), while HDL-C was notably higher (P<0.05). Compared with low-dose ampelopsis grossedentata extract group, FBG, AUC, FINS, TC and MDA were significantly reduced, while the expressions of SIRT1, AMPK and PGC-1α significantly increased (P<0.05) in high-dose ampelopsis grossedentata extract group (P<0.05). Conclusion Ampelopsis grossedentata extract can improve glucolipid metabolism and alleviate insulin resistance in T2DM rats to a certain extent. The mechanism may be related to mitigating oxidative stress and regulating expressions of SIRT1, AMPK and PGC-1α in liver.
〔Keywords〕 type 2 diabetes mellitus; ampelopsis grossedentata extract; oxidative stress; silence information regulator 1;AMP activated protein kinase
2型糖尿病(type 2 diabetes mellitus, T2DM)是以高血糖、胰島素抵抗和胰島素相對缺乏為主要特征的代謝性疾病,是最常見的糖尿病類型,占所有糖尿病的90%以上[1]。隨著疾病進展,可以引起心臟、腎臟、神經、眼部、血管等多種器官病變[2],嚴重威脅人們的健康,因此,防治糖尿病具有重要意義。目前,防治T2DM的藥物以雙胍類、α-葡萄糖苷酶抑制劑等為主要代表,長期使用副作用大[3],因此,尋找天然安全的植物替代藥具有重要價值和意義。
莓茶是土家族、瑤族、苗族等少數民族傳統藥茶,由我國民族特色植物——葡萄科顯齒蛇葡萄的嫩葉制作而成,已有數百年飲用歷史,被收載于《飲膳正要》《中草藥匯編》《中華本草》等多部著作中。莓茶味甘、淡,性涼,歸肺、肝、胃經,具有清熱解毒、平肝降壓、活血通絡的功效,適用于治療咽喉腫痛、風熱感冒、頭昏目脹等[4]。近期研究顯示,飲用莓茶可改善T2DM患者的血糖水平和腎功能[5],但其具體機制尚不明確。現代藥理研究發(fā)現,莓茶中富含的二氫楊梅素等黃酮類物質,可以激活骨骼肌細胞AMP活化蛋白激酶(AMP activated protein kinase, AMPK),AMPK是T2DM的關鍵信號通路,可以改善糖脂代謝、減輕胰島素抵抗[6]。沉默信息調節(jié)因子1(silenceinformation regulator 1, SIRT1)是與機體代謝密切相關的調節(jié)酶,與AMPK存在相互調控的關系,可影響過氧化物酶體增殖物激活受體γ輔助活化因子1α(peroxisome proliferator-activated receptor-γ coactivator-1α, PGC-1α)和叉頭轉錄因子O1等多種轉錄因子的表達[7],與活性氧(reactive oxygen species,ROS)的產生直接相關。因此,推測莓茶可能通過影響SIRT1、AMPK和PGC-1α的表達,減輕氧化損傷改善胰島素抵抗。
因此,本研究通過高脂高糖飼料聯合鏈脲佐菌素(streptozotocin injection, STZ)誘導T2DM大鼠模型,觀察莓茶提取物對T2DM大鼠糖脂代謝及胰島素抵抗的影響。肝臟是胰島素調節(jié)糖脂代謝、維持血糖穩(wěn)態(tài)的重要器官,以肝臟為研究對象,并初步探討了莓茶對肝臟SIRT1、AMPK和PGC-1α蛋白的影響,以期為后續(xù)進一步實驗研究提供依據。
1 材料與方法
1.1? 動物
32只SPF級Wistar雄性大鼠,8周齡,體質量(320±10)g,購自北京維通利華實驗動物技術有限公司,許可證號:SYXK(湘)2019-0009。動物飼養(yǎng)于湖南中醫(yī)藥大學實驗動物中心,室內溫度(24±2) ℃,相對濕度50%~70%。大鼠均自由攝食、飲水,適應性喂養(yǎng)1周后開始實驗。此實驗由湖南中醫(yī)藥大學動物實驗倫理委員會審核批準,倫理編號:LLBH-202109010001。
1.2? 主要藥物與試劑
莓茶提取物(湖南省乾坤生物有限公司,批號:20211201);血糖試紙(北京華益精點生物技術有限公司,批號:EC22E0708);STZ、檸檬酸鈉緩沖液、超氧化物歧化酶(superoxide dismutase, SOD)活性檢測試劑盒、丙二醛(malondialdehyde, MDA)含量檢測試劑盒均購自北京索萊寶科技有限公司(批號分別為S8050、C1013、BC0175、BC0025);總膽固醇(total cholesterol, TC)、低密度脂蛋白試劑盒(low-density lipoprotein cholesterol, LDL-C)、高密度脂蛋白測定試劑盒(high-density lipoprotein cholesterol, HDL-C)、甘油三酯(triglycerides, TG)測定試劑盒均購自南京建成生物研究所(批號分別為A111-1-1、A113-1-1、A112-1-1、A110-1-1);SIRT1抗體(英國Abcam公司,批號:ab189494);大鼠胰島素ELISA試劑盒、AMPKα抗體、PGC-1α抗體、β-actin抗體均購自美國Proteintech公司(批號分別為40001129、10929-2-AP、66369-1-Ig、66009-1-Ig)。
1.3? 主要儀器
血糖儀(北京華益精點生物技術有限公司,型號:EZ-8SIM);電子天平(美國雙杰公司,型號:JJ224BC);臺式高速冷凍離心機(湖南湘儀實驗室儀器開發(fā)有限公司,型號:H1650R);高速組織研磨儀、渦旋混合器均購自武漢賽維爾生物科技有限公司(型號分別為KZ-II、MX-F);電熱恒溫水槽(上海精宏實驗設備有限公司,型號:DK-8B);酶標檢測儀(美國伯騰儀器有限公司,型號:Epoch);全自動生化分析儀(山東博科生物產業(yè)有限公司,型號:BK280);搖床(海門市其林貝爾儀器制造有限公司,型號:TS-92);切片機(浙江金華益迪試驗器材,型號:YD-315);包埋機(常州中威電子儀器,型號:BMJ-A);精密pH計(上海雷磁儀器廠,型號:E-201-C);電泳儀、轉膜儀均購自北京六一儀器廠(型號分別為DYY-6C、DYCZ-40D);顯微鏡(麥克奧迪實業(yè)集團有限公司,型號:BA210T)。
2 方法
2.1? 動物造模分、組與給藥
Wistar大鼠適應性喂養(yǎng)1周后,隨機分成4組,選取1組為正常組,其余3組進行造模。正常組用普通飼料喂養(yǎng)6周,造模組用高脂飼料喂養(yǎng)6周。6周后,造模組大鼠空腹狀態(tài)下腹腔注射STZ溶液30 mg/kg(溶于檸檬酸鈉緩沖液,pH 4.5)建立T2DM模型[8],正常組腹腔注射30 mg/kg溶媒。注射3 d后,測隨機血糖≥16.7 mol/L表示造模成功[9]。血糖不達標的大鼠再次腹腔注射20 mg/kg STZ后,按前述步驟繼續(xù)觀察,若腹腔注射2次血糖仍未達標者,剔除造模組麻醉下處死。造模組大鼠成模后,隨機分為模型組、莓茶低劑量組、莓茶高劑量組。將莓茶提取物加入蒸餾水溶解,制成0.1 g/mL溶液,以李佳川等[10]的實驗劑量為依據,結合本課題組前期預實驗結果,莓茶低劑量組灌胃量為0.4 g/kg,莓茶高劑量組灌胃量為0.8 g/kg,正常組與模型組大鼠用等體積蒸餾水灌胃,1次/d,連續(xù)灌胃6周。
2.2? 空腹血糖(fasting blood glucose, FBG)及葡萄糖耐量
尾靜脈采血法測定大鼠FBG,用碘伏棉球消毒大鼠尾靜脈,一次性刺針刺破大鼠尾部毛細血管,試紙條測試區(qū)放置出血處,直至血液浸透測試區(qū),血糖儀讀取數據后進行記錄,連續(xù)檢測6周。干預6周末,行口服葡萄糖耐量試驗(oral glucose tolerance test, OGTT),各組大鼠隔夜禁食12 h,測定FBG后予2 g/kg無水葡萄糖溶液灌胃,分別于糖負荷后0.5、1、1.5、2 h測定血糖值,并根據各時間點血糖值計算血糖-時間曲線下面積(area under the curve, AUC)。
AUCOGTT=(0 h血糖+2×0.5 h血糖+3×1 h血糖+2×2 h血糖)/4[11]。
2.3? 空腹血胰島素(fasting insulin, FINS)及胰島素抵抗指數(insulin resistance index, HOMA-IR)檢測
第6周末次給藥前12 h,大鼠禁食不禁水,1.5%戊巴比妥鈉麻醉。腹主動脈采血,室溫靜置1 h,以3000 r/min(半徑8 cm)離心15 min,收集上清液,置于-80 ℃冰箱內保存。采用ELISA試劑盒檢測大鼠FINS,所有步驟按試劑盒說明書進行。根據各組FINS、FBG數值,計算HOMA-IR。
HOMA-IR=(FBG×FINS)/22.5[12]。
2.4? 血脂、氧化應激指標檢測
取血清操作同“2.3”,使用全自動生化分析儀測定大鼠血清中TC、TG、HDL-C、LDL-C、SOD、MDA水平。
2.5? HE染色觀察肝臟組織形態(tài)學變化
末次給藥結束后,大鼠禁食12 h,予以1.5%戊巴比妥鈉腹腔注射麻醉,冰上操作收集肝臟標本,稱量后放置于4%多聚甲醛溶液固定,經脫水,石蠟包埋切片,二甲苯脫蠟,酒精梯度脫水后,進行HE染色,顯微鏡下觀察大鼠肝臟病理形態(tài)學變化。
2.6? Western blot檢測肝臟SIRT1、AMPK、PGC-1?琢蛋白表達
收集肝臟標本操作同“2.5”。取肝臟組織剪碎,放入2 mL EP管中清洗,加入300 μL RIPA裂解液反復研磨,冰上裂解10 min,4 ℃。以12 000 r/min半徑8 cm離心15 min,收集上清液,BCA蛋白定量法測定蛋白濃度。配制10%分離膠、4.8%的濃縮膠,加入TEMED后搖勻灌膠,加入相應體積的總蛋白樣品與5×蛋白質凝膠電泳上樣緩沖液混合,煮沸變性后進行電泳,轉至PVDF膜,封閉液中封閉90 min,加入SIRT1、AMPKα和β-actin抗體,4 ℃過夜,TBST洗3次,每次10 min,加二抗孵育90 min,洗膜,ECL化學發(fā)光液與膜孵育1 min,凝膠成像系統成像。
2.7? 統計學分析
實驗數據使用SPSS 26.0統計軟件進行分析,GraphPad Prism 9進行作圖。正態(tài)分布計量資料以“x±s”表示,組間比較采用單因素方差分析;不滿足方差齊性時用非參數檢驗。以P<0.05表示差異有統計學意義。
3 結果
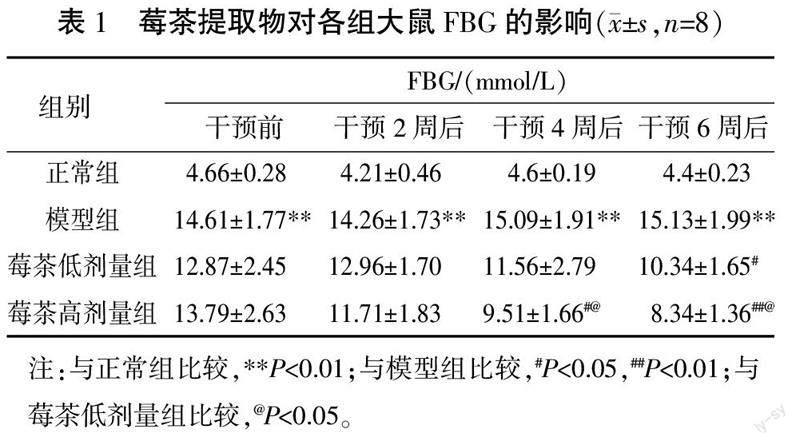
3.1? 莓茶提取物對各組大鼠FBG的影響
干預前后各時間點,模型組FBG明顯高于正常組(P<0.01)。干預4周后,莓茶高劑量組FBG明顯低于模型組(P<0.05)。干預6周后,莓茶高劑量組、莓茶低劑量組FBG均明顯低于模型組(P<0.05,P<0.01)。與莓茶低劑量組比較,莓茶高劑量組干預4周后、干預6周后FBG均明顯降低(P<0.05)。詳見表1。
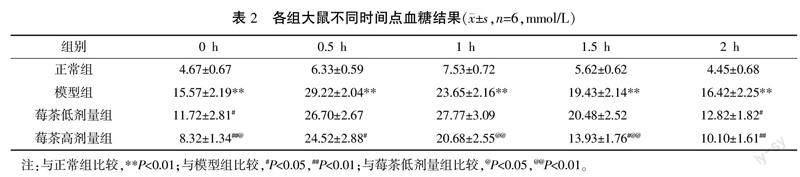
3.2? 莓茶提取物對各組大鼠血糖的影響
與正常組比較,模型組0、0.5、1、1.5、2 h血糖均明顯升高(P<0.01)。與模型組比較,莓茶低劑量組0、2 h血糖均明顯降低(P<0.05),莓茶高劑量組0、0.5、1.5、2 h血糖均明顯降低(P<0.05)。與莓茶低劑量組比較,莓茶高劑量組0、1、1.5 h血糖均明顯降低(P<0.05)。詳見表2。
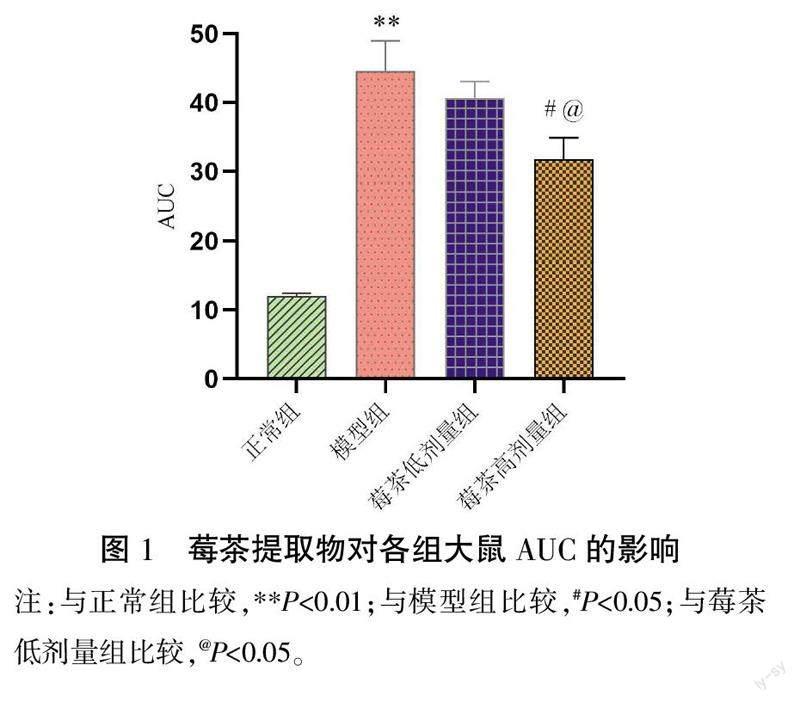
與正常組比較,模型組AUC明顯升高(P<0.01)。與模型組比較,莓茶高劑量組AUC明顯降低(P<0.05)。與莓茶低劑量組比較,莓茶高劑量組AUC明顯降低(P<0.05)。詳見圖1。
3.3? 莓茶提取物對各組大鼠FINS、HOMA-IR的影響
與正常組比較,模型組FINS、HOMA-IR均明顯升高(P<0.01)。與模型組比較,莓茶低劑量組、莓茶高劑量組FINS、HOMA-IR均明顯降低(P<0.05,P<0.01)。與莓茶低劑量組比較,莓茶高劑量組FINS明顯降低(P<0.05)。詳見圖2。
3.4? 莓茶提取物對各組大鼠血脂的影響
與正常組比較,模型組TG、TC、LDL-C均明顯升高(P<0.01),HDL-C明顯降低(P<0.01)。與模型組比較,莓茶低劑量組TG明顯降低(P<0.05);莓茶高劑量組TG、TC均明顯降低(P<0.05,P<0.01),HDL-C明顯升高(P<0.05)。與莓茶低劑量組比較,莓茶高劑量組TC明顯降低(P<0.05)。詳見圖3。
3.5? 莓茶提取物對各組大鼠氧化應激的影響
與正常組比較,模型組SOD含量明顯降低(P<0.01),MDA含量明顯上升(P<0.01)。與模型組比較,莓茶低劑量組、莓茶高劑量組MDA含量均明顯降低(P<0.05,P<0.01),SOD含量均明顯升高(P<0.05,P<0.01)。與莓茶低劑量組比較,莓茶高劑量組MDA含量明顯降低(P<0.05)。詳見圖4。
3.6? 莓茶提取物對各組大鼠肝臟組織的影響
正常組肝細胞大小均勻,以肝小葉為中心,肝索呈放射狀分布,細胞間無充血和水腫,未見明顯炎性細胞浸潤,偶見小泡性脂肪滴空泡。模型組肝臟組織結構被破壞,肝細胞間隙不清晰,呈脂肪變性改變,肝索排列紊亂,可見炎性細胞浸潤,伴有散在點狀肝細胞壞死。與模型組比較,莓茶低劑量組、莓茶高劑量組肝臟組織結構形態(tài)明顯恢復,肝索排列相對整齊,炎性細胞及脂肪變性均有減少。
3.7? 莓茶對各組大鼠肝臟組織SIRT1、AMPK、PGC-1α蛋白表達的影響
與正常組比較,模型組SIRT1、AMPK、PGC-1α蛋白表達均顯著降低(P<0.01)。與模型組比較,莓茶低劑量組、莓茶高劑量組SIRT1、AMPK、PGC-1α蛋白表達均明顯升高(P<0.05,P<0.01)。與莓茶低劑量組比較,莓茶高劑量組SIRT1、AMPK、PGC-1α蛋白表達均明顯升高(P<0.05)。詳見圖6。
4 討論
T2DM發(fā)病的兩大基本環(huán)節(jié)是胰島素抵抗和胰島素分泌相對不足,其中,胰島素抵抗貫穿于T2DM發(fā)生、發(fā)展的整個過程,糖代謝和脂代謝紊亂是T2DM發(fā)生的重要表型,與胰島素抵抗密切相關[13-14]。胰島素抵抗是引起糖、脂代謝紊亂的關鍵環(huán)節(jié),高血脂又可以啟動氧化應激,損傷胰島β細胞,影響糖代謝,加重胰島素抵抗[15]。本實驗通過高脂飲食聯合STZ成功建立T2DM大鼠模型,發(fā)現莓茶提取物可以降低T2DM大鼠的FBG和血脂,改善OGTT,并能夠明顯降低T2DM大鼠胰島素抵抗、HOMA-IR,改善其胰島素抵抗狀態(tài)。
氧化應激是導致胰島β細胞功能損傷及外周胰島素抵抗的重要因素,可以誘發(fā)糖尿病[7],在肥胖小鼠肝細胞研究中發(fā)現,高水平ROS可以刺激胰島素抵抗,過氧化氫的消耗則可以改善胰島素抵抗[16]。MDA是氧自由基攻擊生物膜中不飽和脂肪酸而形成的脂質過氧化物,是反應氧化應激損傷的重要指標,可反映機體內脂質過氧化程度和細胞受損傷的程度。SOD是一種抗氧化酶,主要功能是催化超氧陰離子自由基歧化為過氧化氫和氧可以直接捕獲和清除自由基,從而消除和減少細胞損傷[17],是反應抗氧化損傷能力的關鍵指標。本實驗結果表明,T2DM大鼠給予莓茶提取物治療后,MDA含量下降,SOD含量升高,提示莓茶提取物能夠增強機體的抗氧化能力有效減輕氧化應激損傷。
肝臟是胰島素作用的主要靶點之一,是調節(jié)糖脂代謝的重要器官。在胰島素抵抗過程中,肝臟胰島素信號通路受到破壞,胰島素不能發(fā)揮正常生理作用,造成糖脂代謝紊亂,最終發(fā)展為T2DM[18]。本實驗研究發(fā)現,莓茶提取物能夠明顯改善T2DM大鼠肝臟的病理變化,經莓茶提取物治療后,T2DM大鼠肝臟炎性細胞減少,脂肪變性得到改善。AMPK是機體維持細胞內能量平衡、調控全身能量代謝的一種關鍵能量調節(jié)元件。大量研究表明,AMPK在調節(jié)糖脂代謝、抗氧化應激等多方面發(fā)揮重要作用,AMPK可以促進抗氧化酶的轉錄表達,抑制ROS的生成,進而發(fā)揮抗氧化功能,改善胰島素抵抗,被認為是糖尿病防控的重要靶點[19-21]。本研究檢測了肝臟AMPK蛋白的表達,結果顯示莓茶提取物可上調肝臟AMPK的表達,因此,推測莓茶提取物可能通過上調AMPK的表達,改善胰島素抵抗狀態(tài)。
SIRT1可介導AMPK的激活[22]。SIRT1和AMPK介導了PGC-1α在葡萄糖代謝中的表達[23]。體內外實驗顯示,AMPK可以通過增加PGC-1α的表達,促進骨骼肌攝取利用葡萄糖[24]。此外,被激活的SIRT1通過激活PGC1α參與線粒體能量調節(jié),從而減輕氧化損傷。本實驗檢測了SIRT1、AMPK、PGC-1α蛋白表達的變化,實驗結果顯示莓茶提取物可以上調T2DM大鼠肝臟組織中SIRT1、AMPK、PGC-1α蛋白的表達,提示莓茶提取物可能通過干預肝臟SIRT1、AMPK、PGC-1α蛋白表達,改善氧化損傷和胰島素抵抗。
綜上所述,莓茶提取物對高糖高脂聯合STZ誘導的T2DM大鼠糖脂代謝具有改善作用,可改善胰島素抵抗、減輕氧化損傷,可能與影響肝臟AMPK、SIRT1、PGC-1α蛋白的表達相關。值得關注的是,糖尿病前期是糖尿病發(fā)展的前驅階段,對糖尿病前期進行有效干預可以減少甚至逆轉糖尿病的發(fā)生[25]。莓茶提取物是否可以改善糖尿病前期胰島素抵抗狀態(tài),減緩甚至逆轉糖尿病的發(fā)生,有待于進一步研究。
參考文獻
[1] ZHENG Y, LEY S H, HU F B. Global aetiology and epidemiology of type 2 diabetes mellitus and its complications[J]. Nature Reviews Endocrinology, 2018, 14(2): 88-98.
[2] 陳? 鋒, 張? 帆, 郝二偉, 等. 中藥多糖防治糖尿病及其并發(fā)癥的作用機制研究進展[J]. 中國實驗方劑學雜志, 2022, 28(12): 256-266.
[3] SIAVASH M, TABBAKHIAN M, SABZGHABAEE A M, et al. Severity of gastrointestinal side effects of metformin tablet compared to metformin capsule in type 2 diabetes mellitus patients[J]. Journal of Research in Pharmacy Practice, 2017, 6(2): 73-76.
[4] 何清湖, 王? 煒. 莓茶與健康[M]. 北京: 中國中醫(yī)藥出版社,2022: 30-35.
[5] RAN L, WANG X L, LANG H D, et al. Ampelopsis grossedentata supplementation effectively ameliorates the glycemic control in patients with type 2 diabetes mellitus[J]. European Journal of Clinical Nutrition, 2019, 73(5): 776-782.
[6] ENTEZARI M, HASHEMI D, TAHERIAZAM A, et al. AMPK signaling in diabetes mellitus, insulin resistance and diabetic complications: A pre-clinical and clinical investigation[J]. Biomedecine and Pharmacotherapie, 2022, 146: 112563.
[7] SINGH V, UBAID S. Role of silent information regulator 1 (SIRT1) in regulating oxidative stress and inflammation[J]. Inflammation, 2020, 43(5): 1589-1598.
[8] WANG L, WANG Z Y, YU Y, et al. Metabolomics analysis of stool in rats with type 2 diabetes mellitus after single-anastomosis duodenal-ileal bypass with sleeve gastrectomy[J]. Frontiers in Endocrinology, 2022, 13: 1013959.
[9] WANG Z, LI Q Q, HUANG C K, et al. Determination of CYP450 activities in diabetes mellitus rats by a UHPLC-MS/MS method[J]. Journal of Pharmaceutical and Biomedical Analysis, 2023, 224: 115191.
[10] 李佳川, 李思穎. 基于分子對接技術的藤茶總黃酮對高尿酸血癥腎功能損傷保護機制研究[J]. 中草藥, 2021, 52(3): 727-735.
[11] LINGVAY I, BEETZ N, SENNEWALD R, et al. Triple fixed-dose combination empagliflozin, linagliptin, and metformin for patients with type 2 diabetes[J]. Postgraduate Medicine, 2020, 132(4): 337-345.
[12] BIAGETTI B, SIM?譫 R. Acromegaly: Diabetes and HOMA-IR[J]. Endocrinologia, Diabetes y Nutricion, 2021, 68(1): 1-2.
[13] 鄭園園, 王? 健, 蔣劍平, 等. 玄參多糖對2型糖尿病大鼠糖脂代謝及肝胰島素信號通路的影響[J]. 中草藥, 2020, 51(6):1586-1592.
[14] 周? 楊, 高明松, 彭? 聰, 等. 五味子聯合阿卡波糖對2型糖尿病小鼠胰島素抵抗及降血糖作用機制研究[J]. 湖北中醫(yī)藥大學學報, 2022, 24(3): 12-15.
[15] STRINGER D M, ZAHRADKA P, TAYLOR C G. Glucose transporters: Cellular links to hyperglycemia in insulin resistance and diabetes[J]. Nutrition Reviews, 2015, 73(3): 140-154.
[16] AHMED B, SULTANA R, GREENE M W. Adipose tissue and insulin resistance in obese[J]. Biomedicine and Pharmacotherapy, 2021, 137: 111315.
[17] 王? 萍, 馮樹軍, 王? 宇, 等. 透刺經筋法對周圍性面癱患者血清SOD、NO水平及免疫功能的影響[J]. 陜西中醫(yī), 2022, 43(4): 527-530.
[18] HE F, HUANG Y R, SONG Z, et al. Mitophagy-mediated adipose inflammation contributes to type 2 diabetes with hepatic insulin resistance[J]. The Journal of Experimental Medicine, 2021, 218(3): e20201416.
[19] MENG Q H, QI X, FU Y, et al. Flavonoids extracted from mulberry (Morus alba L.) leaf improve skeletal muscle mitochondrial function by activating AMPK in type 2 diabetes[J]. Journal of Ethnopharmacology, 2020, 248: 112326.
[20] DINIZ T A, DE LIMA JUNIOR E A, TEIXEIRA A A, et al. Aerobic training improves NAFLD markers and insulin resistance through AMPK-PPAR-α signaling in obese mice[J]. Life Sciences, 2021, 266: 118868.
[21] WANG L, TANG J H, WANG L, et al. Oxidative stress in oocyte aging and female reproduction[J]. Journal of Cellular Physiology, 2021, 236(12): 7966-7983.
[22] 楊? 嫻, 阮金蘭. 雞血蓮黃酮通過調節(jié)AMPK/Sirt1/NF-κB信號通路改善小鼠非酒精性脂肪肝的實驗研究[J]. 中醫(yī)藥導報, 2021, 27(4): 10-14.
[23] ZHANG Y, ZHOU B, WEN M, et al. ZG02 improved hepatic glucose metabolism and insulin sensitivity via activation of AMPK/Sirt1 signaling pathways in a high-fat diet/streptozotocin-induced type 2 diabetes model[J]. Diabetes, Metabolic Syndrome and Obesity: Targets and Therapy, 2020, 13: 4333-4339.
[24] SANG A, WANG Y, WANG S, et al. Quercetin attenuates sepsis-induced acute lung injury via suppressing oxidative stress-mediated ER stress through activation of SIRT1/AMPK pathways[J]. Cellular Signalling, 2022, 96: 110363.
[25] MANGAN A, DOCHERTY N G, LE ROUX C W, et al. Current and emerging pharmacotherapy for prediabetes: Are we moving forward[J]. Expert Opinion on Pharmacotherapy, 2018, 19(15): 1663-1673.

