葛根素對LPS誘導的RAW264.7細胞炎癥反應的作用機制研究
孫輝 劉翠玲 姚靜 何秋婷 謝月 梁奇

〔摘要〕 目的 探討葛根素(puerarin, PUE)在脂多糖(lipopolysaccharide, LPS)誘導的RAW264.7巨噬細胞中的抗炎作用,并揭示其分子機制。方法 采用CCK-8比色法分別設置不同濃度的LPS和PUE,觀察對RAW264.7細胞活性的影響,篩選出合適的LPS造模濃度及PUE的給藥濃度。將細胞分為正常對照組、模型組(1 μg/mL)、PUE給藥組(12.5、25、50 μmol/L)。Griess法檢測一氧化氮(nitric oxide, NO)釋放量;ELISA法檢測腫瘤壞死因子-α(tumor necrosis factor-α, TNF-α)、白細胞介素-1β(interleukin-1β, IL-1β)和白細胞介素-6(interleukin-6, IL-6)的含量;qRT-PCR法檢測環氧化酶-2(cyclooxygenase-2, COX-2) mRNA水平;Western blot法檢測誘導型一氧化氮合酶(inducible nitric oxide synthase, iNOS)、COX-2、p-IκBα、p-p65蛋白表達水平。結果 與正常對照組比較,不同濃度的LPS誘導24 h,RAW264.7細胞存活率降低,但對細胞增殖無影響(P>0.05),PUE在濃度100 μmol/L及以下時對RAW264.7細胞增殖也無影響(P>0.05);與模型組相比,PUE給藥組(12.5、25、50 μmol/L)NO、TNF-α、IL-1β及IL-6的釋放量顯著降低(P<0.01),COX-2的蛋白及mRNA表達水平顯著降低(P<0.05),iNOS、p-IκBα、p-p65的蛋白表達水平呈濃度依賴性降低(P<0.01)。結論 PUE的體外抗炎作用機制與抑制核因子κB(nuclear factor-κB, NF-κB)信號通路相關。
〔關鍵詞〕 葛根素;脂多糖;RAW264.7細胞;炎癥;一氧化氮;一氧化氮合酶;NF-κB信號通路
〔中圖分類號〕R285.5 ? ? ?〔文獻標志碼〕A ? ? ? ?〔文章編號〕doi:10.3969/j.issn.1674-070X.2023.04.008
Anti-inflammatory effects and mechanisms of Puerarin on LPS-induced RAW264.7 macrophages
SUN Hui, LIU Cuiling, YAO Jing, HE Qiuting, XIE Yue, LIANG Qi*
Bao'an TCM Hospital of Guangzhou University of Chinese Medicine, Shenzhen, Guangdong 518101, China
〔Abstract〕 Objective To explore the anti-inflammatory potential of Puerarin (PUE) in lipopolysaccharide (LPS)-induced RAW264.7 macrophages and reveal its potential molecular mechanisms. Methods The effects of different concentrations of LPS and PUE on the viability of RAW264.7 cells were determined by CCK-8 colorimetric method, and the appropriate LPS modeling concentration and PUE administration concentration were screened. Cells were divided into normal control group, model group (1 μg/mL), and PUE administration group (12.5, 25, 50 μmol/L); Griess assay was used to assess the nitric oxide (NO) concentration; tumor necrosis factor-α (TNF-α), interleukin-1β (IL-1β) and interleukin-6 (IL-6) content was measured by ELISA; cyclooxygenase-2 (COX-2) mRNA levels were detected by qRT-PCR; the protein expression levels of inducible nitric oxide synthase (iNOS), COX-2, p-IκBα, and p-p65 were determined by Western blot. Results Compared with the normal control group, the survival rate of RAW264.7 cells decreased after 24 h of LPS induction at different concentrations, and there was no effect on cell proliferation (P>0.05), PUE has no significant cytotoxic effects at or below the concentrations of 100 μmol/L (P>0.05); Compared with the model group, PUE administration group (12.5, 25, 50 μmol/L) displayed favorable inhibitory effects on the release level of NO, TNF-α, IL-1β and IL-6 (P<0.01), and the protein and mRNA expression levels of COX-2 significantly decreased (P<0.05) in LPS-induced RAW264.7 cells, and it is the same for the expression levels of iNOS, p-IκBα, p-p65 (P<0.01). Conclusion The anti-inflammation mechanisms of PUE is related with nuclear factor-κB (NF-κB) signaling pathway.
〔Keywords〕 puerarin; lipopolysaccharide; RAW264.7 cells; inflammation; nitric oxide; inducible nitric oxide synthase; NF-κB signaling pathway
炎癥是機體對有害刺激(如病原體、受損細胞或刺激物)的復雜生物反應。炎癥反應導致疼痛、發熱、瘙癢、紅脹,甚至誘發過敏、哮喘及腫瘤等[1-2]。炎癥介導的關鍵因子核因子κB(nuclear factor-κB, NF-κB)是Toll樣受體(Toll-like receptor, TLR)通路中的重要信號分子。這些因子的調節被廣泛認為是抑制各種炎癥的良好策略。更具體地說,NF-κB是促炎基因轉錄調節的一個重要因素,如白細胞介素-6(interleukin-6, IL-6)、一氧化氮(nitric oxide, NO)誘導型一氧化氮合酶(inducible nitric oxide synthase, iNOS)和環氧化酶-2(cyclooxygenase-2, COX-2),也是NF-κB激活所必需的[3-4]。因此,NF-κB活化與炎癥性疾病密切相關,針對NF-κB的抗炎藥物的開發備受關注。
中藥葛根是解表退熱的代表性藥物之一,廣泛應用于治療臨床炎癥性疾病,如發熱[5]、疼痛[6-10]及類風濕關節炎[11-12]等。葛根素(puerarin, PUE)是葛根的主要有效成分,雖然其抗炎活性已有報道[13],但是PUE的抗炎活性所涉及的細胞機制仍有待闡明。本研究通過將PUE作用于脂多糖(lipopolysaccharide, LPS)誘導的RAW264.7巨噬細胞炎癥模型,研究PUE抗炎癥反應的作用及機制,為其進一步的開發及臨床應用提供實驗依據。
1 材料
1.1 ?細胞及藥品
小鼠RAW264.7巨噬細胞購自中國科學院武漢分院細胞庫。PUE(上海詩丹德標準服務技術有限公司,批號:110752-202013,純度≥98%);LPS(美國Sigma-Aldrich公司,批號:#028M4094V)。
1.2 ?主要試劑
CCK-8試劑盒(北京蘭杰柯科技有限公司,批號:21266840);胎牛血清(德國Nobimpex公司,批號:A115-500);DMEM培養基、PierceTM BCA蛋白檢測試劑盒(上海賽默飛世爾科技公司,批號:8122524、WK342259);UltraSYBR Mixture PCR試劑盒(北京康為世紀生物科技股份有限公司,批號:CW2601M);cDNA反轉錄試劑盒(上海翌圣生物科技股份有限公司,批號:H8203980);iNOS(上海Abcam公司,批號:ab178945);COX-2(批號:37843)、p-IκBα(批號:2859S)、IκBα(批號:4814S)、p65(批號:8242S)及p-p65(批號:3033S)均購自美國Cell Signaling Technology公司。
1.3 ?主要儀器
CO2細胞培養箱、高速冷凍離心機(上海賽默飛世爾科技有限公司,型號:371、Sorvall ST 16R);蛋白電泳儀(上海伯樂生命醫學產品有限公司,型號:Bio-Rad 1658029);化學發光熒光成像儀(上海天能科技有限公司,型號:5200Multi);醫用低溫保存箱(青島海爾特種電器有限公司,型號:HYC-198S);潔凈工作臺(蘇州安泰空氣技術有限公司,型號:SW-CJ-2FD)。
2 方法
2.1 ?細胞培養及傳代
RAW264.7細胞在37 ℃下于含10%胎牛血清、100 U/mL青霉素和100 μg/mL鏈霉素的DMEM中培養,細胞在37 ℃、5% CO2空氣環境中生長。待細胞密度長至90%時進行傳代,用細胞刮刀將貼壁細胞刮下,然后吹勻使細胞成單個懸浮狀態,再轉移至15 mL離心管,1000 r/min(離心半徑8 cm),離心5 min,棄上清液,加入新的培養基重懸,按照1∶3進行接種。
2.2 ?細胞分組及細胞存活率檢測
取對數生長的細胞,按照1×106個/mL接種于6孔板,設置正常對照組、模型組(0.01、0.1、1、10 μg/mL)、PUE給藥組(7.5、12.5、25、50、100 μmol/L)。待細胞貼壁過夜,正常對照組加入新鮮培養基,PUE給藥組加入不同濃度PUE,每組設3個復孔,培養24 h;每孔加入20 μL CCK-8,放入細胞培養箱內繼續孵育4 h,用酶標儀測定在450 nm處的吸光度(OD)值,計算細胞存活率。
2.3 ?細胞上清液中NO釋放量的檢測
取對數生長期的細胞,按照1×106個/mL接種于96孔板,設置正常對照組、模型組(1 μg/mL)、PUE給藥組(12.5、25、50 μmol/L),待細胞貼壁過夜,PUE給藥組加入PUE預處理0.5 h,除正常對照組,其余各組加入LPS(1 μg/mL)培養24 h。吸取各組細胞上清液50 μL,與Griess試劑混合,并在室溫下孵育15 min。使用NaNO2作為標準,在540 nm波長處測定NO濃度。
2.4 ?細胞上清液中炎性細胞因子的檢測
取對數生長期的細胞,按照1×106個/mL接種于6孔板,分組及處理同“2.3”,收集細胞上清液,按照ELISA試劑盒說明書定量檢測培養基中腫瘤壞死因子-α(tumor necrosis factor-α, TNF-α)、白細胞介素-1β(interleukin-1β, IL-1β)、IL-6的含量。
2.5 ?COX mRNA水平的檢測
細胞分組及給藥方法同“2.3”,收集細胞,使用TRIzol試劑提取總RNA,應用逆轉錄試劑盒制備cDNA。所有引物均由上海Invitrogen公司合成,使用Primer-BLAST(www.ncbi.nlm.nih.gov/tools/primer-blast)平臺設計COX-2、GAPDH引物序列(見表1)。使用RT-PCR試劑盒在羅氏LightCycler480實時系統(德國Roche Diagnostics公司)中進行qRT-PCR分析。
2.6 ?iNOS、COX-2、NF-κB信號通路蛋白表達的檢測
細胞分組及給藥方法同“2.3”,待細胞貼壁過夜,各給藥組加入PUE預處理0.5 h,除正常對照組,其余各組加入LPS(1 μg/mL)培養30 min,收集細胞,加入含有磷酸酶抑制劑和蛋白酶抑制劑的裂解液冰浴裂解30 min,在4 ℃條件下12 753 r/min離心15 min,離心半徑8 cm;收集上清后,按照BCA蛋白定量試劑盒說明進行蛋白定量,吸取部分蛋白液與5×蛋白質上樣緩沖液混勻,97 ℃金屬浴煮5 min,通過10%的十二烷基硫酸鈉聚丙烯酰胺凝膠電泳(sodium dodecyl sulfate polyacrylamide gel electrophoresis, SDS-PAGE)分離蛋白質提取物,并轉移至PVDF膜。脫脂奶粉封閉2 h,再加入iNOS、COX-2、p-IκBα、IκBα、NF-κB/p65、p-p65抗體稀釋液,4 ℃孵育過夜。用TBST洗滌3次,并與在封閉溶液中稀釋的過氧化物酶偶聯的二抗在室溫下孵育2 h,洗滌后,使用ECL發光液檢測蛋白質。
3 結果
3.1 ?LPS對RAW264.7細胞活性的影響
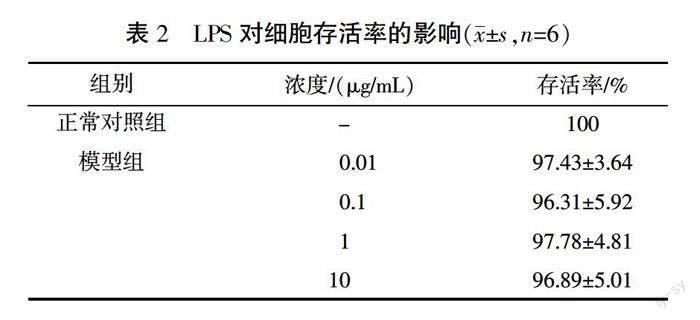
為了評估LPS對RAW264.7細胞的細胞毒性作用,將細胞與不同濃度的LPS(0.01、0.1、1、10 μg/mL)孵育24 h。CCK-8結果顯示,與正常對照組比較,在24 h內,LPS的濃度為0.01、0.1、1、10 μg/mL時,RAW264.7細胞存活率降低,但差異無統計學意義(P>0.05),說明各濃度下LPS對細胞無毒性或毒性不明顯。詳見表2。
3.2 ?PUE對RAW264.7細胞活性的影響
為了評估PUE對RAW264.7細胞的細胞毒性作用,將細胞與不同濃度的PUE(7.5、12.5、25、50、100 μmol/L)孵育24 h。CCK-8結果顯示,與正常對照組比較,在24 h內,PUE給藥組濃度為7.5、12.5、25、50、100 μmol/L時,RAW264.7細胞存活率逐漸降低,但差異無統計學意義(P>0.05),說明各濃度下PUE對細胞無毒性或毒性不明顯。詳見表3。最后,選擇12.5、25、50 μmol/L作為PUE的給藥濃度,用于進一步研究。
3.3 ?LPS對RAW264.7細胞中炎癥因子表達的影響
與正常對照組比較,除模型組(0.01 μg/mL)外,其余3個濃度(0.1、1、10 μg/mL)均可明顯誘導RAW264.7細胞產生炎癥因子TNF-α、IL-1β和IL-6(P<0.05),并呈現一定的濃度依賴關系。但由于1 μg/mL和10 μg/mL濃度之間誘導炎癥因子水平差異無統計學意義(P>0.05),故選擇1 μg/mL的LPS作為造模濃度。詳見表4。
3.4 ?PUE對LPS誘導的RAW264.7細胞中炎癥因子表達的影響
與正常對照組比較,模型組上清液中的TNF-α、IL-1β和IL-6水平明顯升高(P<0.05);與模型組比較,PUE給藥組上清液中TNF-α、IL-1β和IL-6的水平呈濃度依賴性降低(P<0.05)。詳見表5。
3.5 ?PUE對LPS誘導的RAW264.7細胞中NO和iNOS表達的影響
與正常對照組比較,模型組中NO的產生以及iNOS的表達明顯升高(P<0.05);與模型組比較,PUE給藥組LPS誘導的RAW264.7中NO的產生以及iNOS的蛋白表達水平降低(P<0.05)。詳見表6、圖1。
3.6 ?PUE對LPS誘導的RAW264.7細胞中COX-2表達的影響
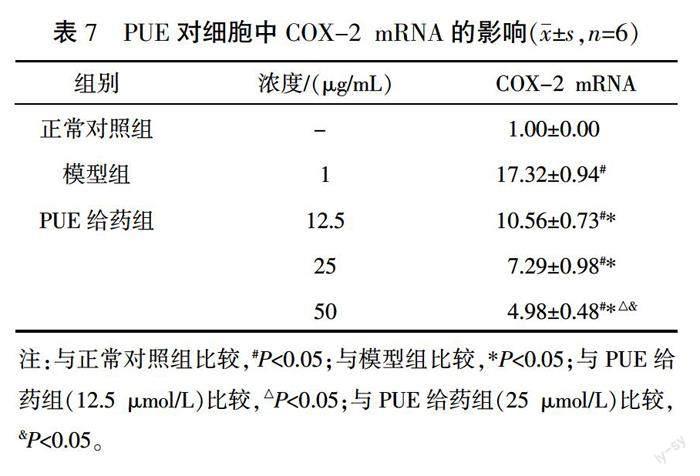
與正常對照組比較,模型組中COX-2的mRNA和蛋白表達明顯升高(P<0.05);與模型組相比,PUE給藥組COX-2的mRNA和蛋白表達明顯降低(P<0.05)。詳見圖2、表7。
3.7 ?PUE對NF-κB信號通路的影響
與正常對照組比較,模型組NF-κB信號通路中p-p65和p-IκBα表達明顯增加(P<0.05);與模型組相比,PUE給藥組p-p65和p-IκBα水平呈濃度依賴性降低(P<0.05)。詳見圖3。
4 討論
炎癥是病原體、受損細胞或刺激物攻擊機體產生的基本防御機制。炎癥反應有多種生理目的,如宿主防御、組織修復反應和穩態恢復。然而,這種反應會產生病理后果,導致炎癥組織損傷、化生和穩態設定點的改變。因此,機體需要對炎癥反應進行適當的調節。一些有害刺激,如病原體、受損細胞或刺激物可刺激機體產生NO,但過量產生NO會在巨噬細胞中誘導慢性炎癥反應[14]。慢性NO過量產生也涉及其他負面的細胞生理功能,如DNA損傷和誘變[15]。在本研究中,PUE抑制LPS刺激的RAW264.7細胞中NO的產生。其次,PUE還以劑量依賴的方式抑制LPS誘導的iNOS蛋白水平升高。這些結果表明,PUE可能是一種潛在的抗炎化學物質。前列腺素(prostaglandin, PG)是來源于花生四烯酸的類脂化合物。NO、iNOS和PG維持體內平衡功能并介導致病機制,包括炎癥反應。由促炎刺激物、細胞因子、激素和生長因子誘導的COX-2是炎癥中PG形成的重要來源[16-18]。COX-2酶抑制劑被開發用于治療與關節炎相關的炎癥[19-20]和疼痛[21-22]。促炎細胞因子往往會通過誘發機體產生發熱、炎癥、組織破壞或全身炎癥使疾病惡化。IL-6是一種關鍵的炎癥細胞因子,在誘導下游炎癥反應中起著重要作用。在這項研究中,我們發現PUE抑制LPS誘導的TNF-?琢、IL-1?茁和IL-6的上調。PUE處理以劑量依賴的方式減少LPS誘導的NO釋放。此外,PUE下調LPS誘導的iNOS、COX-2、p-IκBα、p-p65的表達。NF-κB可與κB的抑制劑IκBα結合,當給予誘導炎癥反應的刺激時,NF-κB被IκBα降解激活,并導致其易位到細胞核中,以促進炎癥基因的表達,包括iNOS、COX-2和IL-6。
綜上所述,體外實驗表明PUE可能是一種具有潛在抗炎作用的天然活性化合物,可以抑制炎癥因子的產生以及炎癥反應,這種抑制作用可能與調控NF-κB信號通路密切相關。本研究結果可為PUE用于治療相關炎癥性疾病以及進一步的研究利用提供科學參考。
參考文獻
[1] LOPEZ B, MAISONET T M, LONDHE V A. Alveolar NF-κB signaling regulates endotoxin-induced lung inflammation[J]. Experimental Lung Research, 2015, 41(2): 103-114.
[2] PFLUG K M, SITCHERAN R. Targeting NF-κB-inducing kinase (NIK) in immunity, inflammation, and cancer[J]. International Journal of Molecular Sciences, 2020, 21(22): 8470.
[3] LIN Y Q, LUO T Y, WENG A L, et al. Gallic acid alleviates gouty arthritis by inhibiting NLRP3 inflammasome activation and pyroptosis through enhancing Nrf2 signaling[J]. Frontiers in Immunology, 2020, 11: 580-593.
[4] HIRANO T, HIRAYAMA D, WAGATSUMA K, et al. Immunological mechanisms in inflammation-associated colon carcinogenesis[J]. International Journal of Molecular Sciences, 2020, 21(9): 3062.
[5] 管詠梅,龔麗霞,姜 ?鄂,等.葛根及其主要成分安全性研究進展[J].中華中醫藥學刊,2022,40(3):12-18.
[6] 朱 ?京,劉桂榮.張志遠運用葛根經驗[J].中醫雜志,2022,63(2): 111-114.
[7] 張文培.葛根湯在老年病臨床治療中的應用進展研究[J].內蒙古中醫藥,2021,40(12):124-125.
[8] 田利軍,郭宇松,劉 ?星,等.葛根湯聯合針刺治療青少年頸椎生理曲度異常所致頸源性頭痛療效及對患者腦血管功能狀況的影響[J].陜西中醫,2020,41(7):875-877,910.
[9] 樊俐慧,張 ?偉,王志剛,等.基于《傷寒雜病論》探討葛根的量效關系及用藥規律[J].中醫臨床研究,2021,13(21):28-30.
[10] 史晨旭,杜佳蓉,吳 ?威,等.葛根化學成分及藥理作用研究進展[J].中國現代中藥,2021,23(12):2177-2195.
[11] 婁 ?磊.葛根湯聯合腎著湯對類風濕性關節炎患者療效及免疫功能的影響[J].河北醫藥,2022,44(6):926-929.
[12] 楊小又,張麗萍,李 ?濤,等.李兆福教授運用桂枝加葛根湯治療類風濕關節炎合并外感風寒經驗[J].風濕病與關節炎,2020,9(11): 34-35,51.
[13] 孔令娟,計小清,劉 ?巖,等.葛根素通過調控AMPK/GSK-3β/β-catenin信號通路緩解糖尿病大鼠心肌損傷[J].中藥材,2023(2):474-478.
[14] LEE Y M, KIM D S. The extraction solvent influences the anti-inflammatory effects of jakyakgamcho-Tang in lipopolysaccharide-stimulated macrophages and mice with gouty arthritis[J]. International Journal of Molecular Sciences, 2020, 21(24): 9748.
[15] ZHAO W R, SHI W T, ZHANG J, et al. Tribulus terrestris L. extract protects against lipopolysaccharide-induced inflammation in RAW 264.7 macrophage and zebrafish via inhibition of Akt/MAPKs and NF-κB/iNOS-NO signaling pathways[J]. Evidence-Based Complementary and Alternative Medicine, 2021, 2021: 6628561.
[16] 陳詩潔,黃瀏姣.電針對缺血腦組織Survivin、COX-2表達及二者相關性影響的研究[J].湖北中醫藥大學學報,2022,24(4):5-9.
[17] LI T T, HAI L L, LIU B, et al. TLR2/4 promotes PGE2 production to increase tissue damage in Escherichia coli-infected bovine endometrial explants via MyD88/p38 MAPK pathway[J]. Theriogenology, 2020, 152: 129-138.
[18] 任天琦,劉澤霖,胡 ?海,等.甘草甜素對膝關節骨性關節炎大鼠軟骨細胞凋亡及PTEN/AKT/COX-2信號通路的影響[J].貴州醫科大學學報,2022,47(7):785-790,795.
[19] STILLER C O, HJEMDAHL P. Lessons from 20 years with COX-2 inhibitors: Importance of dose-response considerations and fair play in comparative trials[J]. Journal of Internal Medicine, 2022, 292(4): 557-574.
[20] WANG Q R, YE C Q, SUN S K, et al. Curcumin attenuates collagen-induced rat arthritis via anti-inflammatory and apoptotic effects[J]. International Immunopharmacology, 2019, 72: 292-300.
[21] ZHANG J Z, CHEN X Y, WU Y J, et al. Identification of active compounds from yi nationality herbal formula Wosi influencing COX-2 and VCAM-1 signaling[J]. Frontiers in Pharmacology, 2020, 11: 568585.
[22] GONZ?魣LEZ-BARNADAS A, CAMPS-FONT O, MART?魱N-FAT?魣S P, et al. Efficacy and safety of selective COX-2 inhibitors for pain management after third molar removal: A meta-analysis of randomized clinical trials[J]. Clinical Oral Investigations, 2020, 24(1): 79-96.
〔收稿日期〕2022-11-25
〔基金項目〕廣東省粵深青年聯合基金項目(2019A1515111192)。
〔第一作者〕孫 ?輝,男,碩士研究生,研究方向:中藥藥理研究。
〔通信作者〕*梁 ?奇,男,主任中藥師,E-mail:liangqi70@gzucm.edu.cn。

