電針與艾灸對佐劑性關節炎大鼠脾臟CD4+T細胞影響的對比研究
龍軼映 張亮 祁芳 艾坤 劉梨 趙凌云 瞿啟睿 謝輝 何可
〔摘要〕 目的 對比觀察電針和艾灸對佐劑性關節炎(adjuvant arthritis, AA)大鼠足跖容積測量、關節炎指數評分及分化簇4 淋巴細胞(cluster of differentiation-4+T-cell, CD4+T)水平的影響,評價兩種干預措施治療AA的效應機制。方法 選取健康雄性大鼠24只,隨機分為空白組、模型組、電針組和艾灸組,每組6只。艾灸組予以雙側“足三里”“關元”“阿是穴”懸灸20 min;電針組左側足三里與關元配穴,右側足三里與同側阿是穴配穴,干預20 min。于干預第21天進行足跖容積測量及關節炎指數評分,隔天于無菌操作臺進行脾臟取材,采用流式細胞術檢測脾臟CD4+T淋巴細胞。結果 與空白組相比,模型組的足跖容積、關節炎指數評分、CD4+T淋巴細胞數量均明顯增多(P<0.01);與模型組相比,電針組、艾灸組的足跖容積、關節炎指數評分、CD4+T淋巴細胞數量均明顯減少(P<0.05或P<0.01);與電針組相比,艾灸組的足跖容積、關節炎指數評分、CD4+T淋巴細胞數量差異均無統計學意義(P>0.05)。結論 電針與艾灸在改善類風濕關節炎癥狀及免疫方面的作用機制具有類似效應,均可抑制脾CD4+T淋巴細胞的增殖,維持機體免疫穩態,改善病情。
〔關鍵詞〕 佐劑性關節炎;類風濕關節炎;電針;艾灸;CD4+T細胞;免疫紊亂;療效對比
〔中圖分類號〕R245 ? ? ? 〔文獻標志碼〕A ? ? ? ?〔文章編號〕doi:10.3969/j.issn.1674-070X.2023.04.020
Comparative study of effects of electroacupuncture and moxibustion on spleen
CD4+T cells in rats with adjuvant arthritis
LONG Yiying1, ZHANG Liang1, QI Fang1, AI Kun1, LIU Li2, ZHAO Lingyun1, QU Qirui1, XIE Hui3*, HE Ke4*
1. College of Acupuncture & Tuina Rehabilitation, Hunan University of Chinese Medicine, Changsha, Hunan 410208, China;
2. The First Hospital of Hunan University of Chinese Medicine, Changsha, Hunan 410007, China; 3. The First People's Hospital of Chenzhou, Chenzhou, Hunan 423099, China; 4. The Second Hospital of Hunan University of Chinese Medicine, Changsha, Hunan 410005, China
〔Abstract〕 Objective To observe the effects of electroacupuncture and moxibustion on the plantar volume, arthritis index and the levels of cluster of differentiation-4+T-cell level in adjuvant arthritis (AA) rats. And to evaluate the mechanism of in the treatment of AA rats. Methods Twenty-four healthy male rats were randomly divided into blank group, model group, electroac?鄄upuncture group and moxibustion group, with 6 rats in each group. In the moxibustion group, the two sides of "Zusanli" (ST36), "Guanyuan" (BL26) and "Ashi" acupoints were suspended moxibustion for 20 min, while in the electroacupuncture group, the same acupoint intervention was performed for 20 min. The left ST36 was combined with BL26 point and the right ST36 was combined with the same side "Ashi" acupoints for 20 min. On the last day of intervention, plantar volume and arthritis index were scored. On the second day, spleen were taken from the sterile operation table, and CD4+T lymphocytes were detected by flow cytometry. Results Compared with blank group, plantar volume, arthritis index and number of CD4+T lymphocyte of model group (P<0.01). Compared with model group, plantar volume, arthritis index and number of CD4+T lymphocytes in electroacupuncture group and moxibustion group were significantly decreased (P<0.05, P<0.01). Compared with electroacupuncture group, the moxibustion group had no significant differences in plantar volume, arthritis index and number of CD4+T lymphocyte (P>0.05). Conclusion Electroacupuncture and moxibustion have similar effects on improving rheumatoid arthritis symptoms and immunity, both of which can inhibit the proliferation of CD4+T lymphocytes, maintain immune homeostasis and improve the disease.
〔Keywords〕 adjuvant arthritis; rheumatoid arthritis; electricacupuncture; moxibustion; CD4+T cells; immune disorders; comparison of curative effects
類風濕關節炎(rheumatoid arthritis, RA)是一種以侵蝕性關節滑膜炎癥為主要癥狀,病理過程難以控制的慢性、系統性自身免疫性疾病,且發病機制尚不明確[1-2]。該病目前尚無特效藥,患者需要長期服藥控制病情,費用昂貴,是現階段臨床相關領域研究的難點和熱點。
RA的特征是以大量CD4+T細胞浸潤為主的慢性滑膜炎癥反應。研究表明,針刺和艾灸治療RA均可以通過調節機體內免疫細胞的活性、細胞因子的表達等來調節RA患者自身的免疫反應,發揮其治療作用[3-4]。針灸治療RA免疫調節機制是近年來的研究熱點,艾灸屬于溫熱刺激,針刺屬于機械刺激,對于機體效應是否一致尚未明確。因此,本研究分別采用電針和艾灸“足三里”“關元”“阿是穴”干預佐劑性關節炎(adjuvant arthritis, AA)模型大鼠,以脾臟CD4+T細胞為切入點,觀察電針和艾灸治療AA大鼠免疫相關的對比療效,探討其對CD4+T細胞的影響。
1 材料與方法
1.1 ?實驗動物與分組
健康SPF級SD雄性大鼠24只,來源于湖南斯萊克景達實驗動物公司[動物合格證:4307272111
02588284,許可證號:SCXK(湘)2019-0004],體質量(100±10) g。24只大鼠以3只一籠飼養于湖南中醫藥大學動物實驗中心,設置12 h/12 h的晝夜明暗交替環境,飼養室溫(25.0±2) ℃,相對濕度50%±10%。適應性喂養1周后,根據隨機數字表法分為4組:空白組、模型組、電針組、艾灸組,每組6只。本實驗所有過程均遵從《關于善待實驗動物的指導性意見》(2006年版)中的相關規定[5]。
1.2 ?主要試劑與儀器
滅活結核分枝桿菌(美國Becton-Dickinson公司,批號:231141);礦物油(美國Sigma Aldrich公司,批號:M8410);抗鼠CD4 抗體(美國BioLegend公司,批號:201505);大鼠淋巴細胞分離液(深圳市達科為生物工程有限公司,批號:7211011);紅細胞裂解液(Biosharp公司,批號:BL503B);PBS溶液(北京索萊寶科技有限公司,批號:P1022);RPMI-1640培養基(美國Gibco公司,批號:21870076)。
35 mm培養皿(湖南比克曼生物公司,型號:110301019);200目尼農網(北京索萊寶科技有限公司,型號:YA0961);5 mL流式管(美國Becton公司,Dickinson and Company,型號:352235);移液槍(德國Eppendorf公司,型號:10~1000 μL);電針治療儀(蘇州醫療用品有限公司,型號:華佗牌 SDZ-Ⅱ型);足跖容積測量儀(濟南益延科技發展有限公司,型號:YLS-7C);高速低溫離心機(美國SCILOGEX公司,型號:D3024R);電熱恒溫槽(上海精宏實驗設備,型號:DK-8D);流式細胞儀(美國Becton-Dickinson公司,型號:Celesta)。
1.3 ?模型制備
本實驗采用以T細胞介導的免疫性炎癥動物模型——AA大鼠模型,免疫調節異常是其關鍵病理機制[6]。實驗第1天,模型組、電針組、艾灸組大鼠進行造模,將定量滅活結核分枝桿菌與礦物油放入高溫滅菌的研缽中充分研磨,直至溶液清透無雜質,配制成2.5 mg/mL的完全弗氏佐劑備用,使用時需震蕩以充分混勻。將大鼠呼吸麻醉后,在尾根部皮下用乙醇棉球消毒后注射佐劑,劑量為0.1 mL/只。空白組同法注射0.1 mL礦物油。通過觀察大鼠關節外表現,即模型大鼠造模第6天后出現尾根部紅腫,全身性關節繼發癥狀出現,第9~12天大鼠食欲減退、體質量減輕、皮溫變高,關節紅腫明顯加劇,其余關節也出現癥狀,則為模型制備成功的標志[7]。
1.4 ?干預方法
空白組、模型組大鼠不予任何治療,常規飼養,均僅以仰臥位固定于鼠板上20 min;電針組大鼠固定于自制的大鼠鼠板上,直刺雙后足“足三里”“關元”和“阿是穴”(雙側大鼠足跖關節腫脹明顯部位)[8],各穴均用30號1寸針,穴位參照“十五”國家規劃統編教材《實驗針灸學》中的大鼠標準穴位圖譜進行定位,針刺0.2~0.3寸,進針后接電子針療儀,左側足三里與關元配穴,右側足三里與同側阿是穴配穴,采用疏密波,強度通過觀察針柄端以出現輕微抖動,每次留針20 min;艾灸組大鼠固定于自制鼠板上(鼠板上安有固定艾條裝置)艾灸“足三里”“關元”和“阿是穴”,離穴位處皮膚2 cm處懸灸20 min。4組大鼠均于造模第2天開始干預,每天1次,7次為1個療程,共治療3個療程。
1.5 ?取材
干預結束后第2天,在無菌超凈臺下操作,將大鼠腹腔麻醉處死后開腹取出脾臟中段,放入裝有生理鹽水的試管備用。
1.6 ?指標檢測
1.6.1 ?右后足跖容積測量 ?干預第21天,使用足跖容積測量儀測量足跖關節容積,每只足測量3次,記錄讀數取平均數。
1.6.2 ?關節炎指數評分 ?炎癥出現后,每3天評估關節炎指數評分,以便觀察各組大鼠的繼發病變。評分標準[9]如下:0分,無紅腫;1分,跖關節出現輕微腫脹;2分,踝關節到跖關節或掌關節腫脹;3分,踝關節以下足爪出現腫脹;4分,包括踝關節及以下足爪出現腫脹。分別記錄四肢關節炎指數評分,統計總分,每只大鼠最多評12分。
1.6.3 ?流式細胞術檢測CD4+T淋巴細胞數據 ?此操作在無菌超凈臺上完成,首先分離出脾臟淋巴細胞懸浮液,將取出的脾臟組織(從大鼠體內取出脾臟到進行分離不能超過1 h)放入培養皿上的200目尼龍網上,使用移液槍放入4~5 mL淋巴細胞分離液(取用前搖勻)到脾臟上,進行研磨,研磨時幅度不宜過大,直至培養皿中的液體變色明顯且脾臟只剩些許結締組織。把研磨后懸有脾臟細胞的分離液轉移到15 mL離心管中,立即覆蓋200~500 μL的RPMI-1640培養基后,室溫,放入離心機以800 r/min、半徑約為8 cm離心30 min。離心結束后會出現細胞分層,吸出淋巴細胞層后,加入10 mL RPMI-1640培養基后顛倒洗滌。室溫,250 r/min、半徑約為8 cm離心10 min后立即收集細胞,傾倒上清液,用PBS溶液重懸細胞得到淋巴細胞懸浮液。然后,進行裂紅孵育,用移液槍將淋巴細胞懸浮液加入帶濾網的5 mL流式管中,加入1 μL CD4抗體;將樣本與抗體用渦旋振蕩器混勻,在室溫(25 ℃)下避光孵育15 min;所得混合物中加入3 mL PBS緩沖液,1000 r/min、半徑約為8 cm離心5 min,棄上清液;用500 μL PBS緩沖液重懸即得到待測樣品。同法不加抗體設置陰性管。最后,將待測樣品和陰性管冰上保存盡快進行上機檢測,得出CD4+T淋巴細胞數據結果,使用Flowjo軟件進行分析,得出結果。
1.7 ?統計學分析
數據分析應用SPSS 26.0軟件處理,本實驗所有數據均為計量資料,以“x±s”表示,符合正態分布且方差齊者,組間比較采用單因素方差分析,均以P<0.05表示差異有統計學意義。
2 結果
2.1 ?一般情況
空白組大鼠一般情況良好;模型組大鼠于造模第9天后足出現不均勻紅斑或紅腫,在第15~18天癥狀到達最高峰,全身出現繼發性炎癥,飲食減少,體質量與其他3組相比增長緩慢;電針組和艾灸組飲食正常,且肉眼可見大鼠后足跖腫脹度明顯小于模型組。
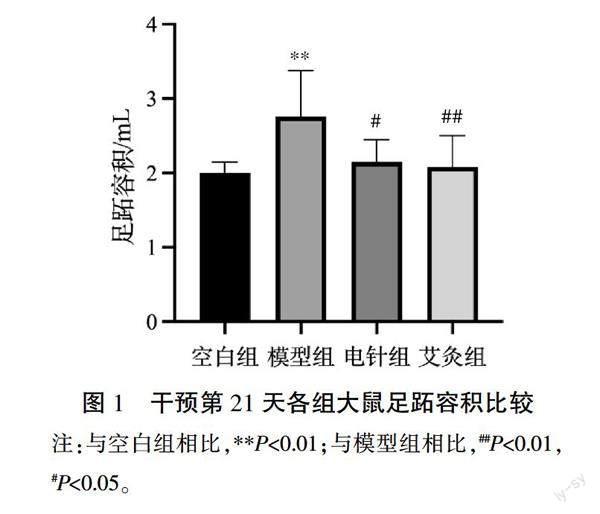
2.2 ?各組大鼠足跖容積比較
干預第21天,與空白組相比,模型組足跖容積明顯增大(P<0.01);與模型組相比,電針組足跖容積明顯減小(P<0.05),艾灸組顯著減少(P<0.01);而電針組與艾灸組足跖容積比較,差異無統計學意義(P>0.05)。詳見圖1。
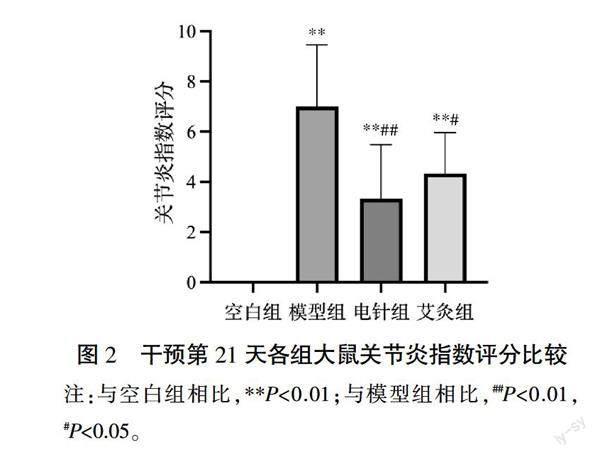
2.3 ?各組大鼠關節炎指數評分比較
干預第21天,空白組大鼠評分為0分,與空白組相比,模型組、電針組、艾灸組關節炎指數評分顯著增大(P<0.01);與模型組相比,電針組關節炎指數評分顯著減小(P<0.01),艾灸組明顯減少(P<0.05);而電針組與艾灸組比較,差異無統計學意義(P>0.05)。詳見圖2。
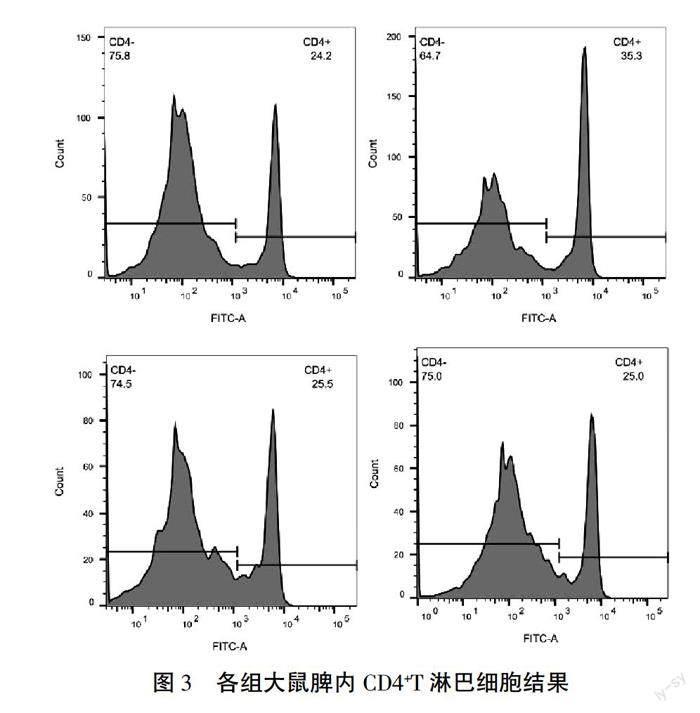
2.4 ?各組大鼠CD4+T淋巴細胞數量比較
干預第21天,與空白組相比,模型組大鼠CD4+T淋巴細胞數量顯著增多(P<0.01);與模型組相比,電針組、艾灸組CD4+T淋巴細胞數量均顯著減少(P<0.01);而電針組與艾灸組比較,差異無統計學意義(P>0.05)。詳見圖3—4。
3 討論
中醫學中,將RA歸入“痹病”范疇,病因多為正氣不足、復感外邪所致,中醫治療中針灸療效肯定,已成為重要治療手段之一。本課題組前期研究表明,電針治療AA大鼠能有效緩解大鼠足跖腫脹程度、降低致炎因子表達、緩解關節局部炎癥[10-11]。鐘玉梅等[12]發現艾灸通過調節脾臟膜型程序性細胞死亡配體1、血清可溶性程序性死亡蛋白1的表達,抑制T細胞的過度活化,緩解RA炎性反應。與這些研究結果一致,本實驗中模型大鼠足跖容積明顯增大(P<0.01)、關節炎指數評分顯著增大(P<0.01),經電針干預后足跖容積明顯降低(P<0.05)、關節炎指數評分明顯降低(P<0.01),艾灸干預后足跖容積明顯降低(P<0.01)、關節炎指數評分明顯降低(P<0.05);而電針組與艾灸組相比后足跖容積、關節炎指數評分差異均無統計學意義(P>0.05),提示電針與艾灸在緩解AA大鼠關節炎癥反應具有類似效果。
多因素相互作用導致的免疫耐受紊亂是RA發病的中心環節,RA的發病機制主要為T淋巴細胞等免疫細胞浸潤的慢性滑膜炎,且存在于滑膜下層的成纖維細胞增殖并導致軟骨損傷[13-14]。CD4+T細胞是其效應細胞,在一定程度上影響RA的發生與發展[15]。大部分RA病人外周血單個核細胞中均伴有CD4+T細胞活化[16],且在關節積液中存在CD4+T細胞的高度擴增[17],提示CD4+T細胞可能是緩解滑膜炎癥的靶點之一。大鼠AA模型是一種T細胞介導的免疫性炎癥動物模型[18-19],結核分枝桿菌中一個相對分子量為65 kDa熱休克蛋白(heat shock protein 65, HSP65)與大鼠關節軟骨(cartilago articularis, CII)的自身抗原60 kDa熱休克蛋白(heat shock protein 60, HSP60)有高度相似的保守序列,可以通過分子模擬或交叉反應,激活原來處于靜止狀態的針對CII抗原為主的T淋巴細胞克隆,從而引起關節的自身免疫反應[20-21]。研究證明,CD4+T細胞缺陷小鼠RA發病率更低[22]。進一步研究提示,CD4+T細胞在RA發病過程中的重要性,維持機體免疫穩態,對于維持正常免疫功能具有重要意義[23-24]。研究發現,懸灸法能夠降低RA大鼠血清抗體類風濕因子表達,從而改善免疫功能[25]。電針可以通過調節T淋巴細胞改善機體免疫功能[26]。本研究也發現,模型組大鼠脾臟CD4+T細胞顯著增多(P<0.01),電針、艾灸干預后,CD4+T細胞數量均顯著減少(P<0.01),提示電針與艾灸均可抑制CD4+T細胞增殖,緩解炎癥反應;同時,電針組與艾灸組比較,差異無統計學意義(P>0.05),這提示電針和艾灸在調節脾臟CD4+T細胞數量等方面表現出類似效應。因此,本研究認為電針、艾灸在改善RA炎性癥狀及其免疫方面的作用機制均與降低AA大鼠脾臟內CD4+T細胞數量,抑制其增殖,進而緩解炎性反應有關。
綜上所述,本研究認為電針和艾灸在改善RA癥狀及免疫方面的作用機制具有類似效應,即均可通過抑制脾臟CD4+T細胞增殖,減輕促炎效應,改善RA免疫功能,在一定程度上維持了機體免疫穩態,從而減輕病情,這為電針、艾灸治療RA提供了一定的證據基礎。此外,本研究尚存在一些局限性,CD4+T細胞的異常增殖、分化是RA早期免疫耐受紊亂的核心,本研究僅探討了電針與艾灸治療對CD4+T細胞增殖的影響,未涉及異常分化。因此,在后續的研究中,可增加CD4+T細胞異常分化相關指標如Th1/Th2、Th17/Treg的檢測來完善研究,同時進一步擴大樣本量進行重復,以增加信度。
參考文獻
[1] 李 ?佳,李柏村,蔡國偉,等.針灸足三里對佐劑性關節炎模型大鼠胃腸動力的調節作用[J].中國組織工程研究,2022,26(26):4141-4146.
[2] 武上雯,李 ?桓,李松偉.基于作用機制探討中藥復方與生物制劑治療類風濕關節炎概況[J].中華中醫藥學刊,2022,40(8):112-117.
[3] 黃亞蓉,耿 ?文,李 ?清,等.針灸對類風濕關節炎的免疫調節作用研究進展[J].國際中醫中藥雜志,2022,44(1):114-121.
[4] 王 ?萌,李 ?佳,李 ?靜.溫針灸足三里、腎俞對類風濕性關節炎模型RhoA蛋白表達的影響[J].湖北中醫藥大學學報,2016,18(6): 17-20.
[5] 關于發布《關于善待實驗動物的指導性意見》的通知[J].畜牧獸醫科技信息,2007(4):35-36.
[6] 于 ?坤,徐枝芳,余楠楠,等.佐劑性和膠原誘導性關節炎模型比較分析[J].遼寧中醫藥大學學報,2018,20(1):106-109.
[7] 楊俊玲,盧 ?軍,趙翡翠,等.類風濕性關節炎實驗動物模型的研究進展[J].西北藥學雜志,2015,30(3):329-332.
[8] AI K, LI Y L, QI F, et al. Effect of electroacupuncture on c-IAP1 mRNA and c-IAP2 mRNA in synovial tissues of rats with adjuvant arthritis[J]. Journal of Acupuncture and Tuina Science, 2019, 17(1): 16-23.
[9] ARSENAULT A L, LHOTAK S, HUNTER W L, et al. Taxol involution of collagen-induced arthritis: Ultrastructural correlation with the inhibition of synovitis and neovascularization[J]. Clinical Immunology and Immunopathology, 1998, 86(3): 280-289.
[10] 龍軼映,張 ?亮,祁 ?芳,等.電針對佐劑性關節炎大鼠滑膜組織中mTOR磷酸化水平的影響[J].湖南中醫藥大學學報,2021,41(12):1881-1885.
[11] 祁 ?芳,李艷玲,艾 ?坤,等.電針對佐劑性關節炎大鼠踝關節滑膜細胞胞漿內IκB磷酸化的影響[J].湖南中醫藥大學學報,2020, 40(12):1494-1498.
[12] 鐘玉梅,吳 ?菲,羅小超,等.基于PD-1/PD-L1信號通路艾灸治療類風濕性關節炎的機制研究[J].中國針灸,2020,40(9):976-982.
[13] WEYAND C M, GORONZY J J. Immunometabolism in the development of rheumatoid arthritis[J]. Immunological Reviews, 2020, 294(1): 177-187.
[14] LITTLEJOHN E A, MONRAD S U. Early diagnosis and treatment of rheumatoid arthritis[J]. Primary Care, 2018, 45(2): 237-255.
[15] 劉 ?健,文建庭,萬 ?磊,等.類風濕關節炎中醫學病機的分子生物學機制探討[J].風濕病與關節炎,2020,9(9):48-52.
[16] 黃自坤,李 ?雪,鄧 ?楨,等.類風濕關節炎患者外周血CD4+T和CD8+T細胞TIGIT的表達和意義[J].中華微生物學和免疫學雜志,2017,37(5):325-332.
[17] FISCHER J, DIRKS J, KLAUSSNER J, et al. Effect of clonally expanded PD-1highCXCR5-CD4+ peripheral T helper cells on B cell differentiation in the joints of patients with antinuclear antibody-positive juvenile idiopathic arthritis[J]. Arthritis & Rheumatology, 2022, 74(1): 150-162.
[18] ANDERTON S M, VAN DER ZEE R, PRAKKEN B, et al. Activation of T cells recognizing self 60-kD heat shock protein can protect against experimental arthritis[J]. The Journal of Experimental Medicine, 1995, 181(3): 943-952.
[19] HOLOSHITZ J, NAPARSTEK Y, BEN-NUN A, et al. Lines of T lymphocytes induce or vaccinate against autoimmune arthritis[J]. Science, 1983, 219(4580): 56-58.
[20] HOLMDAHL R, GOLDSCHMIDT T J, KLEINAU S, et al. Arthritis induced in rats with adjuvant oil is a genetically restricted, alpha beta T-cell dependent autoimmune disease[J]. Immunology, 1992, 76(2): 197-202.
[21] VAN EDEN W, HOLOSHITZ J, NEVO Z, et al. Arthritis induced by a T-lymphocyte clone that responds to Mycobacterium tuberculosis and to cartilage proteoglycans[J]. Proceedings of the National Academy of Sciences of the United States of America, 1985, 82(15): 5117-5120.
[22] EHINGER M, VESTBERG M, JOHANSSON?魡 C M, et al. Influence of CD4 or CD8 deficiency on collagen-induced arthritis[J]. Immunology, 2001, 103(3): 291-300.
[23] LI X Y, XU H H, HUANG J, et al. Dysfunctions, molecular mechanisms, and therapeutic strategies of regulatory T cells in rheumatoid arthritis[J]. Frontiers in Pharmacology, 2021, 12: 716081.
[24] ELYAHU Y, HEKSELMAN I, EIZENBERG-MAGAR I, et al. Aging promotes reorganization of the CD4 T cell landscape toward extreme regulatory and effector phenotypes[J]. Science Advances, 2019, 5(8): eaaw8330.
[25] 馬重兵,朱田田,劉安國,等.懸灸對濕熱痹阻型RA大鼠類風濕因子表達影響的研究[J].時珍國醫國藥,2018,29(11):2789-2791.
[26] 余曙光,唐 ?勇,劉旭光.電針對類風濕關節炎大鼠T細胞凋亡的影響[J].成都中醫藥大學學報,2002,25(1):25-27.
〔收稿日期〕2022-06-30
〔基金項目〕國家自然科學基金項目(82074565,82274627);湖南省研究生科研創新項目(CX20210704,CX20220798)。
〔第一作者〕龍軼映,女,碩士研究生,研究方向:常見疾病的中西醫結合康復的機理與臨床研究。
〔通信作者〕*何 ?可,男,副主任醫師,E-mail:178077878@qq.com;謝 ?輝,男,主任醫師,碩士研究生導師,E-mail:xiehui8663@163.com。

