BDNF信號通路在兒童孤獨癥譜系障礙中的作用機制及中醫(yī)藥干預研究進展
吳吉 裴方妤 張滌 朱沁泉
〔摘要〕 腦源性神經營養(yǎng)因子(brain-derived neurotrophic factor, BDNF)為細胞內信號通路轉導分子,調節(jié)眾多重要的生理過程。BDNF信號通路對于神經元的存活、形態(tài)發(fā)生和可塑性至關重要。目前,認為BDNF信號通路失調與孤獨癥譜系障礙(autism spectrum disorder, ASD)的發(fā)病機制密切相關,BDNF在外周血中的濃度可能成為評估ASD的潛在生物學指標。中醫(yī)藥治療ASD具有整體調節(jié)和多通道、多靶點的優(yōu)勢,可能通過調控BDNF信號通路改善ASD核心癥狀或伴隨癥狀。目前,研究存在的問題主要有:BDNF下游機制復雜,與ASD發(fā)病關系的相關機制未完全闡明;中醫(yī)藥治療兒童ASD的報道多為中藥復方的臨床觀察研究,尚缺乏中藥活性成分療效機制的動物實驗及針對BNDF信號通路的研究。今后的研究中,需進一步設計科學嚴謹的實驗方案,深入了解BDNF信號通路的作用機制。對BDNF信號通路在ASD發(fā)病機制中的作用及中醫(yī)藥研究進行綜述,以期為ASD的靶向治療提供理論依據。
〔關鍵詞〕 孤獨癥譜系障礙;腦源性神經營養(yǎng)因子;信號通路;中醫(yī)藥;靶點;兒童
〔中圖分類號〕R272 ? ? ? 〔文獻標志碼〕A ? ? ? ?〔文章編號〕doi:10.3969/j.issn.1674-070X.2023.04.030
Mechanisms of BDNF signaling pathway in autism spectrum disorder and
research progress of Chinese medicine intervention
WU Ji1, PEI Fangyu1, ZHANG Di2*, ZHU Qinquan2*
1. Hunan University of Chinese Medicine, Changsha, Hunan 410208, China;
2. The First Hospital of Hunan University of Chinese Medicine, Changsha, Hunan 410007, China
〔Abstract〕 Brain-derived neurotrophic factor (BDNF) is an intracellular signal transduction molecule that regulates important physiological processes. Furthermore, BDNF signaling pathway is essential for neuronal survival, morphogenesis and plasticity. Since the imbalance of BDNF signaling pathway is considered to be closely related to the pathogenesis of autism spectrum disorder (ASD), the concentration of BDNF in peripheral blood may become a potential biological index to evaluate ASD. Chinese medicine treatment of ASD can regulate overally with multiple channels and multiple targets. It may improve the core or concomitant symptoms of ASD by regulating BDNF signaling pathway. The main problems in its current research are as follows: the downstream mechanism of BDNF is complex and the ASD pathogenesis is not fully elucidated.Most reports on the treatment of children with ASD by Chinese medicine are clinical observation of formulas, but there is still a lack of animal experiment on the therapeutic mechanisms of active ingredients of formula and research on BDNF signaling pathway. In the future research, it is necessary to further design a scientific and rigorous experimental scheme to deeply understand the mechanisms of BDNF signaling pathway. This paper reviews the role of BDNF signaling pathway in the pathogenesis of ASD and the research of Chinese medicine, in order to provide a theoretical basis for the targeted treatment of ASD.
〔Keywords〕 autism spectrum disorder; brain-derived neurotrophic factor; signaling pathways; Chinese medicine; target; child
孤獨癥譜系障礙(autism spectrum disorder, ASD)是一組具有臨床異質性、可合并其他多種疾病的神經發(fā)育障礙癥候群,以社會交往障礙、重復刻板的行為-感覺異常與狹隘興趣為核心癥狀,是早期大腦發(fā)育和神經重組的結果[1]。本病全球發(fā)病率為1%~2%,男女比例約4∶1[2]。ASD也是我國0~6歲精神殘疾兒童致殘的首位原因,占比高達78%。本病可伴有其他發(fā)育障礙疾病,如智力障礙、發(fā)育性語言障礙、運動障礙等[3]。加之ASD的特征性表現(xiàn),使患兒在學校、社會交往、家庭生活、自我照護和未來工作等多方面面臨挑戰(zhàn)[4]。目前,ASD病因及發(fā)病機制尚不明確,以康復訓練、教育干預為主,藥物為輔的治療手段,旨在改善臨床癥狀,無法達到治愈目的,使得本病成為全世界共同面臨的重大公共衛(wèi)生難題及沉重的社會、家庭負擔。
腦源性神經營養(yǎng)因子(brain-derived neurotro?鄄phic factor, BDNF),屬于重要的神經營養(yǎng)因子之一,BDNF及其高親和力酪氨酸激酶受體B(tyrosine kinase receptor B, TrkB)在發(fā)育中和成年哺乳動物的大腦尤其是海馬和皮質中廣泛表達[5]。BDNF/TrkB刺激細胞內信號轉導對神經元的存活、形態(tài)發(fā)生和可塑性至關重要。近年來,研究表明BDNF通過與受體結合,激活下游信號通路,對神經元產生正向或負向的影響,涉及各種腦部疾病的病理生理學,如抑郁癥、阿爾茨海默病、帕金森病等[6]。同時研究也關注到,BDNF信號通路可能與ASD發(fā)病密切相關。因此,本文旨在初步總結BDNF信號通路在ASD發(fā)病過程中的作用機制,為發(fā)現(xiàn)治療ASD的藥物或手段提供新思路。
1 BDNF的概述
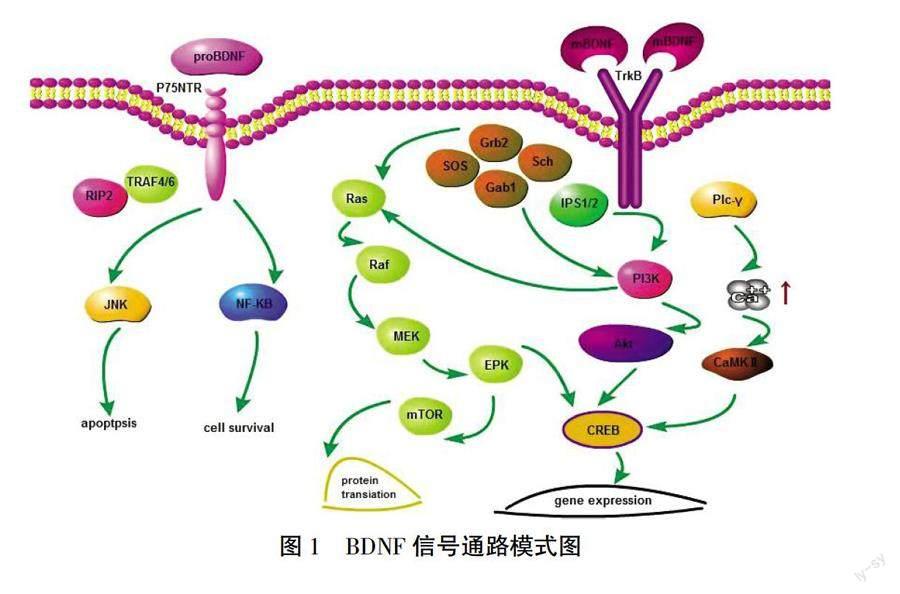
神經營養(yǎng)因子包括神經生長因子、BDNF、神經營養(yǎng)因子-3和神經營養(yǎng)因子-4/5,已知在神經元生長、分化、存活以及神經元結構和功能的調節(jié)中發(fā)揮關鍵作用[7-8]。BDNF的合成和成熟是一個多階段的過程,涉及幾種前體異構體的形成。BDNF首先是在內質網中以pre-pro-BDNF形式存在,運輸到高爾基體,在高爾基體中分裂后形成pro-BDNF。這種形式再次裂解,最終形成成熟的BDNF(m-BDNF)亞型。在大腦不同區(qū)域發(fā)育的不同階段,原始性與間源性BDNF的比例不同。在出生后早期,pro-BDNF的濃度較高,而m-BDNF在成年人中較為普遍[9]。因此,pro-BDNF可能是調節(jié)大腦功能的重要因素,而m-BDNF發(fā)揮重要作用的過程在成年階段,如神經保護和突觸可塑性。BDNF參與多種神經生理過程,其最關鍵的功能包括調節(jié)神經新生、糖原合成、突觸形成、神經保護、控制影響記憶和認知機制的長短突觸之間的相互作用[7]。而上述功能需要結合特定的Trk受體,通過各種細胞內信號通路激活。BDNF與磷酸化的TrkB結合可激活絲裂原活化蛋白激酶(mitogen-activated protein kinase, MAPK)/細胞外信號調節(jié)蛋白激酶(extracellular regulated protein kinases, ERK)、磷脂酶cγ(Recombinant Phospholipase C Gamma, PLCγ)和磷酸肌醇3激酶(Phosphoinositide 3-kinase, PI3K)/蛋白激酶B(protein kinase B, Akt)通路[10]。除了TrkB,低親和力的p75受體也參與神經元的存活和可塑性[11]。詳見圖1[12]。
2 BDNF與ASD
雖然ASD的病因、病理、生理機制尚不清楚,但研究證據表明,遺傳基因和環(huán)境因素損傷神經發(fā)育導致了ASD的產生。大腦中的BDNF可通過血腦屏障進入外周血,并與血清BDNF變化呈正相關。目前,認為外周BDNF水平可間接反映腦內BDNF水平變化。因此,BDNF在外周血中的濃度可以作為評價ASD個體的一個潛在的生物學指標[13]。基于這一理論,近年來,涌現(xiàn)越來越多的報道、動物實驗和薈萃分析來評估ASD動物模型或患者血液中BDNF水平的可能變化。然而,研究結果并不一致。這可能是方法學、樣本人群、不同疾病階段、性別、亞型、用藥史等方面的差異造成的。自2002年首次利用Fmr1基因敲除(knockout, KO)小鼠模型研究BDNF/TrkB信號通路以來[14],后續(xù)展開許多實驗對該模型小鼠神經祖細胞、海馬和皮質神經元進行研究,并對BDNF和TrkB的RNA和蛋白水平進行分析,總體證明BDNF、TrkB在幼年實驗小鼠中表達增加,但隨著年齡的增長而下降[15-16]。PIETROPAOLO等[17]和SUN等[18]通過實驗證明,應用BDNF或者TrkB激動劑可以增加Fmr1KO小鼠的BDNF水平,以改善或恢復其神經生物學和行為表型。近交系小鼠BTBRt+tf/j(black and tan, brachyuric, BTBR)由于模擬ASD核心特征的行為表型,也被用作該疾病的模型系統(tǒng)。REIM等[19]研究證實BTBR模型小鼠前腦中BDNF和TrkB下降。并且,這可能是一種年齡相關的現(xiàn)象,HWANG等[20]在胎兒BTBR小鼠大腦中觀察到BDNF水平升高。SKOGSTRAND等[21]采集了1981年至2004年收集的干血斑樣本,統(tǒng)計發(fā)現(xiàn)新生兒低血BDNF水平與ASD發(fā)生的概率顯著相關,提示新生兒較低的BDNF水平可能是ASD發(fā)病的原因之一。一項對0~19歲ASD患兒的研究表明,0~9歲ASD患兒血清BDNF水平低于對照組,而10~19歲ASD患兒血清BDNF水平高于對照組[22]。SAGHAZADEH等[23]通過對20項研究進行薈萃分析,發(fā)現(xiàn)ASD兒童的血液BDNF水平高于對照組。
3 BDNF與表觀遺傳
表觀遺傳機制,如DNA甲基化,在精神疾病中發(fā)揮關鍵作用。表觀遺傳學研究的是基因表達的可遺傳改變,其機制不會直接導致基礎DNA序列的改變。具有表觀遺傳調控功能的基因與ASD的易感性密切相關[24]。DUFFNEY等[25]對215個候選基因的研究發(fā)現(xiàn),19.5%是表觀遺傳調節(jié)因子,這表明幾個致病變異可能導致多種疾病表型。雙胞胎研究特別證明了表觀遺傳學可以調節(jié)疾病表型:一項針對50對同卵雙胞胎ASD的研究,報道了大量ASD相關的差異甲基化區(qū),在一些癥狀組常見的CpG位點有甲基化模式[26]。易感基因通常包括與甲基化有關的基因,如賴氨酸甲基轉移酶5B和賴氨酸去甲基化酶6B;染色質重塑蛋白包括甲基化CG結合蛋白2(methyl-CpG-binding protein 2, MeCP2)、染色質域解旋酶DNA結合蛋白8(chromodomain helicase DNA-binding protein 8, CHD8)等[27]。這些蛋白質的作用靶點從幾個到數百個不等,通常包括與ASD有關的通路,比如突觸形成。以MeCP2為例,MeCP2是一種染色質修飾劑,與ASD密切相關。在健康人中,MeCP2的結合作用可以調節(jié)許多具有突觸功能的基因,如BDNF、γ-氨基丁酸A受體β3亞基(gamma-aminobutyric acid receptor beta 3, GABRB3)、胰島素樣生長因子結合蛋白3(IGF binding protein 3, IGFBP3)[28-29]。另外,MeCP2是發(fā)育過程中調節(jié)谷氨酸能突觸形成的限速因子[30]。GO等[31]發(fā)現(xiàn),宮內暴露于丙戊酸的大鼠,通過上調Wnt1的表達和激活GSK-3β/β-catenin通路,導致大頭畸形,從而促進神經前體細胞的增殖和延遲神經發(fā)生。另一項研究發(fā)現(xiàn),丙戊酸通過兩種轉錄機制增加BDNF,這兩種轉錄機制涉及MeCP2和組織纖維蛋白溶酶原激活物(tissue-type plasminogen activator, tPA)。研究提出,BDNF的增加可以改變突觸的生長,損害突觸的形成[32]。因此,表觀遺傳學可以對生物體的轉錄組產生深遠地影響。即使是一個表觀遺傳調控基因中的致病變異,或環(huán)境影響都可能導致廣泛的基因失調。表觀遺傳調控因子本身可以引起疾病,但它們也可能通過影響危險基因的表達而加重或改善疾病表型。DNA甲基化作為表觀遺傳機制之一,可通過一些候選基因如MeCP2、泛素蛋白連接酶E3A(ubiquitin protein ligase E3A, UBE3A)、CHD8、活性依賴性神經保護蛋白同源框(activity-dependent neuroprotector, ADNP)和BDNF在ASD中發(fā)揮作用[33]。在DNA甲基化過程中,DNA甲基轉移酶(DNA methyltransferases, DNMTs)催化嘧啶環(huán)5位的胞嘧啶殘基上加入a-ch3基團。這些CpG二核苷酸序列通常位于基因調控區(qū)域內或周圍,稱為CpG島。DNA甲基化通常發(fā)生在這些調控區(qū)可導致轉錄抑制[34]。許多研究也闡明,DNA甲基化在成年人BDNF基因動態(tài)調節(jié)中的潛在作用:研究表明,DNA甲基化在活性依賴性BDNF調控中起著重要作用[35];研究還發(fā)現(xiàn),BDNF啟動子和基因內區(qū)域的甲基化改變與不同的行為趨勢有關,如恐懼學習、記憶形成、應激性社會交往等[36]。因此,DNA甲基化可能參與了ASD患者BDNF活性的動態(tài)調節(jié)。
4 BDNF信號通路的神經保護作用
ASD被認為是一組早期神經異質性疾病。目前,神經病理學病因機制尚不明確,但對ASD患者死后尸檢及大量動物實驗、臨床基因測序的研究表明,ASD患者存在神經元形態(tài)和細胞結構區(qū)域特異性異常。根據西蒙斯基金會自閉癥研究計劃基因數據庫,基因檢測技術的最新進展已經能夠鑒定出與ASD相關的1000多個候選基因和拷貝數變異(copy number variation, CNV)位點[37]。據估計,在高達25%的ASD病例、染色體重排(包括罕見和新生CNV)和編碼序列突變中可以確定遺傳原因,分別占ASD患者的10%~20%和5%~10%[38]。許多ASD候選基因涉及基本細胞功能的許多方面,如染色質重塑、代謝、mRNA翻譯可能會影響神經元過程,從神經發(fā)生到神經元遷移,軸突引導,樹突生長以及突觸形成和功能[39]。BDNF/TrkB在神經元存活、形態(tài)發(fā)生和可塑性中起著重要作用。BDNF與TrkB的結合激活多種細胞內信號通路,包括MAPK/ERK、PLCγ和PI3K/Akt通路[10]。MAPK/ERK信號級聯(lián)調節(jié)神經元分化過程中蛋白質的合成。MAPK相關的信號也是激活ERK1/2和環(huán)磷腺苷效應元件結合蛋白(cAMP-response element binding protein, CREB)所必需的。這一通路不僅對早期反應基因表達(如c-Fos和ARC)至關重要[40],而且對細胞骨架蛋白合成(如ARC和cypin)以及海馬神經元的樹突生長和分支也至關重要[41]。PI3K/Akt相關通路發(fā)揮抗凋亡和前生存活性,并能調節(jié)N-甲基-D-天門冬胺酸受體(N-methyl-D-aspartic acid receptor, NMDA)依賴性突觸可塑性。PI3K/Akt/mTOR級聯(lián)通過調節(jié)蛋白質合成和細胞骨架發(fā)育,促進樹突生長和分支[40]。PLCγ依賴途徑激活Ca2+調素依賴蛋白激酶(CAM kinase, CAMK)和蛋白激酶C蛋白激酶(protein kinase C, PKC),隨后增加1,2-二酰甘油(diacylglycerol, DAG)和Ca2+離子濃度。蛋白激酶C依賴途徑可以增強突觸可塑性[12]。BDNF/TrkB復合體激活代表Rho家族的GTP-ases,刺激肌動蛋白和微管的合成,從而導致神經纖維的生長[40]。
BDNF通過抑制gsk-3β和激活CREB來激活PI-3K/Akt和ERK通路發(fā)揮對細胞凋亡的保護作用[42]。BDNF能刺激CREB Ser133位點磷酸化而活化CREB,大量研究也表明,持續(xù)磷酸化活化的CREB才能與靶基因轉錄調控區(qū)CRE結合,而啟動下游CREB依賴基因的轉錄,使包括與細胞生長、存活、正常軸突的功能維持等有關靶基因開放[43]。其中,內源性BDNF表達的增加、TrkB受體水平的上調,激活CREB,可進一步激活抗凋亡基因表達程序,Bcl-2家族蛋白中促抗凋亡成員在線粒體上與其他凋亡蛋白的相互作用,調控線粒體結構與功能的穩(wěn)定性,促進神經營養(yǎng)因子介導的中樞神經存活,抑制神經元凋亡,發(fā)揮BDNF的神經保護作用[44]。BDNF和Ras蛋白的組成性激活可以阻止mk801誘導的未成熟神經元凋亡性死亡[45]。
神經遞質是在突觸傳遞中擔當信使的重要化學物質,其類型、分布和含量的不同會對人類的思維、情感和行為產生影響。興奮性(excitability, E)神經遞質和抑制性(inhibitory, I)神經遞質之間的平衡關系對腦功能的正常發(fā)揮起重要作用,E/I失衡可能與ASD發(fā)病密切相關[46]。在哺乳動物中樞神經系統(tǒng)(central nervous system, CNS)中,谷氨酸(glutamic acid, Glu)是最主要的興奮性神經遞質,也是一種潛在的神經毒素,其引起的興奮毒性可能導致神經細胞的死亡。為了保持突觸傳遞的敏感性,Glu必須被及時清除。BDNF對海馬神經元中Glu的保護作用是通過PI3K和MAPK信號通路介導。研究表明,低水平的NMDA受體刺激通過海馬神經元中BDNF自分泌環(huán)保護海馬神經元免受谷氨酸興奮毒性。GABA能神經元指的是能夠釋放抑制性神經遞質GABA的一類抑制性中間神經元的總稱。GABA能神經元在腦中主要發(fā)揮抑制神經元活性的作用,因此,其對于維持正常的神經環(huán)路功能至關重要。證據表明,BDNF在γ-氨基丁酸(γ-aminobutyric acid, GABA)能神經元發(fā)育方面具有重要作用。BDNF及其激活的下游信號通路中的分子起到調節(jié)GABA能神經元數量、胞體大小、神經元遷移、樹突軸突發(fā)育及突觸成熟等作用[47]。丙戊酸鈉(valproic acid, VPA)小鼠模型中不同發(fā)育時期E/I平衡的變化,參與E/I平衡的突觸前和突觸后興奮性和抑制功能的典型標志物在發(fā)育過程中顯著降低,反映了VPA暴露小鼠突觸可塑性發(fā)育障礙。BDNF在VPA暴露組中的表達嚴重降低。在關鍵的E/I失衡期間使用外源性BDNF治療改善了突觸功能和自閉癥樣行為[48]。
5 中醫(yī)藥治療ASD的研究進展
目前,治療兒童ASD的方法主要是行為干預訓練;配合利培酮等非典型抗精神藥物改善情緒、攻擊行為。本病康復周期漫長、照養(yǎng)負擔大、預后往往不夠理想。而中醫(yī)藥治療ASD具有整體調節(jié)和多通道、多靶點的優(yōu)勢。但目前國內中藥復方治療兒童ASD報道多為臨床觀察,相關作用機制的實驗研究主要涉及針灸療法。因此,本文僅對部分單味中藥、中藥復方干預BDNF信號通路改善與ASD相關的伴隨癥狀,或針灸干預BDNF信號通路改善兒童ASD核心癥狀進展的實驗研究進行歸納整理,為明確中醫(yī)藥治療ASD作用機制提供新思路。
5.1 ?單味中藥
5.1.1 ?姜黃 ?姜黃為姜科姜黃屬植物姜黃的干燥根莖。其味辛,苦,溫,歸脾、肝經,有破血行氣、通經止痛之功。姜黃素為其主要化學成分,現(xiàn)代藥理學研究證實,其活性成分具有抗氧化、抗炎等作用[49]。陳淑娟等[50]通過實驗研究發(fā)現(xiàn),通過2周腹腔注射姜黃素能有效改善ASD模型小鼠重復刻板行為及社會交流障礙;并且姜黃素干預后ASD模型鼠大腦顳葉皮質BDNF陽性細胞IOD值增加(P<0.05)。推測姜黃素通過增加BDNF表達,上調BDNF-Akt-Bcl2抗凋亡信號通路,抑制神經膠質細胞、小腦浦肯野細胞凋亡,發(fā)揮對ASD的治療作用。
5.1.2 ?何首烏 ?何首烏是蓼科何首烏屬植物干燥塊根。歷代本草載其味苦、澀,性溫。歸肝、心、腎經,生用解毒消癰,潤腸通便,制用補肝腎,益精血,烏須發(fā),強筋骨。何首烏苷是其最主要的藥理活性成分,化學名稱為二苯乙烯苷;在該植物中的含量極高,同時藥理活性清晰。現(xiàn)代藥理學研究發(fā)現(xiàn),其在抗氧化、抑制細胞凋亡、神經保護以及改善血管功能和增強學習記憶能力等方面具有重要作用[51]。李茜茜等[52]通過細胞實驗發(fā)現(xiàn),何首烏苷預先處理的氧化損傷大鼠海馬神經元核固縮細胞的數目或核溶解成碎片明顯減少,統(tǒng)計顯示預處理組的細胞凋亡率與H2O2損傷組相比下降24%(P<0.01)。當加入BDNF/TrkB信號轉導通路阻斷劑K252a后,神經元細胞存活率大幅度下降(P<0.01),細胞骨架形態(tài)呈損傷狀態(tài)。表明何首烏苷可能通過激活BDNF/TrkB信號轉導通路及維護神經元骨架的完整,實現(xiàn)對大鼠海馬神經元氧化應激損傷的拮抗作用。
5.1.3 ?熟地黃 ?地黃是一種玄參科系植物地黃的干燥或新鮮塊根,屬草本藥物之上品。熟地黃是由地黃酒燉蒸煮炮制而來,其藥性微溫,味甘甜,有益精填髓、補血滋陰的功效。熟地黃富含氨基酸、地黃素、糖類、梓醇等多種微量元素,具有改善記憶認知、提高免疫力、抗腫瘤等多種功能。熟地黃對中樞神經系統(tǒng)具有顯著的抑制作用。據報道,從地黃中分離得到的一種環(huán)烯醚萜苷——梓醇,可減輕PC12細胞H2O2誘導的凋亡,通過抗氧化能力保護海馬CA1區(qū)神經元免于死亡,并顯著減輕認知障礙[53]。注意缺陷多動障礙(attention deficit and hyperactivity disorder, ADHD)表現(xiàn)為與年齡不相稱的注意力易分散,注意廣度縮小,不分場合的過度活動,情緒沖動并伴有認知障礙和學習困難。研究表明,ASD與ADHD兩病存在共有的基因危險座和受影響的腦部區(qū)域[54]。袁海霞等[55]發(fā)現(xiàn)熟地黃煎水灌胃4周后,ADHD模型大鼠自發(fā)活動明顯減少;與空白組相比,熟地黃組前額葉、紋狀體中BDNF、TrkB mRNA和蛋白表達水平均顯著提高(P<0.05);熟地黃可能通過增加BDNF、TrkB的表達來促進神經元生長、發(fā)育、成熟,從而起到控制ADHD多動、沖動的作用。
5.1.4 ?白芍 ?白芍是毛茛科植物芍藥的干燥根莖,味苦、酸,微寒,歸肝、脾經,具有養(yǎng)血斂陰、柔肝止痛之效。其主要化學成分包括單萜及其苷類、三萜類、黃酮類、鞣質類以及多糖類等化合物。芍藥苷及芍藥內酯苷屬于單萜及其苷類化合物,是白芍中的主要化學物質,具有抗炎、神經保護、抗氧化等藥理作用[56]。焦慮、抑郁情緒障礙是ASD患兒最常見的共患病之一[57],有研究證實ASD與重度抑郁存在遺傳風險重疊[58]。多種情緒問題嚴重影響著患兒心理健康、社會交往及家庭關系。朱映黎等[59]研究發(fā)現(xiàn),芍藥苷及芍藥內酯苷能顯著上調肝郁證模型大鼠海馬中BDNF水平,進而增加抑郁大鼠自發(fā)活動及探索行為,緩解其對陌生環(huán)境的恐懼感和緊張度。
5.2 ?中藥復方研究
中醫(yī)學古籍中沒有“孤獨癥”的相應病名。現(xiàn)代醫(yī)家根據ASD臨床表現(xiàn)將其歸于神志病范疇,并認為本病病位在心、腦,與腎、肝、脾等臟腑密切相關。病因病機為先天不足、胎毒浸淫,養(yǎng)護不當而致髓海空虛、痰蒙神竅、五臟功能失調。目前,關于中藥復方治療ASD的機制研究相對匱乏,本文擬總結中藥復方基于BDNF信號通路治療與ASD病因病機趨同的共患病的相關研究,以期為中藥復方基于異病同治理論治療ASD提供新思路。
5.2.1 ?溫膽湯 ?溫膽湯首載于唐代孫思邈的《備急千金要方》:“大病后,虛煩不得眠,此膽寒故也,宜服此溫膽湯方,法半夏、竹茹、枳實各二兩,橘皮三兩,生姜四兩,甘草片一兩。”中醫(yī)學認為痰火上擾、痰濕內阻、蒙蔽清竅則會導致神經系統(tǒng)疾病。因此,現(xiàn)代醫(yī)家將溫膽湯廣泛應用于治療兒童孤獨癥、抑郁癥、失眠癥、精神分裂癥等神經系統(tǒng)疾病。阿依奴爾·吾買爾等[60]采用加味溫膽湯配合行為教學訓練治療25例ASD患兒,治療1個月后,患兒異常生活行為較治療前減少。精神分裂癥與ASD有共同的遺傳風險因素和致病基因,是ASD常見共患病之一。高源等[61]研究發(fā)現(xiàn)溫膽湯可能通過調節(jié)BDNF信號通路因子,上調BDNF的蛋白和mRNA表達水平,改善精神分裂癥模型鼠的刻板行為,從而提高精神分裂癥認知障礙模型鼠的學習記憶、認知功能。
5.2.2 ?大補元煎 ?大補元煎源自《景岳全書》,由人參、山藥、熟地黃、杜仲、當歸、山茱萸、枸杞子和炙甘草組成,為培元固本治法的代表方。中醫(yī)學認為癡呆發(fā)病責之髓海空虛,與腎精不足所致ASD病機相似。何麗玲等[62]研究發(fā)現(xiàn),給予大補元煎能增強癡呆小鼠海馬突觸可塑性、改善突觸功能,并且機制與上調小鼠海馬中 BDNF/TrkB/CREB 信號通路相關。
5.3 ?針刺研究
目前,針灸多為治療ASD的輔助療法。針灸治療過程中辨證選穴,標本兼治,緩急兼顧,改善陰陽失衡狀態(tài),最終達到陰平陽秘。針刺頭部穴位可疏經通絡、平衡陰陽。百會穴為眾多經脈交會穴,針刺可調節(jié)經氣,增強記憶力;印堂則有明目寧心安神之功。羅彤[63]發(fā)現(xiàn)針刺百會、印堂可改善慢性應激抑郁模型大鼠的抑郁狀態(tài),提高了抑郁模型大鼠自主活動能力和空間探索能力,降低了抑郁模型大鼠快感缺失水平,其機制可能與海馬中tPA/BDNF通路有關,實驗中電針組海馬區(qū)BDNF、TrkB蛋白含量顯著高于空白組(P<0.01)。長強穴在脊柱骨的尾端,是督陽初始之處,可通任督,調腸腑。馮祥等[64]認為督脈陽虛、督脈不通與ASD發(fā)病相關。林燊[65]運用電針療法以不同時長刺激ASD模型大鼠長強穴,可改善ASD大鼠自主活動,以電針20 s為單位刺激時長(累計干預15次)能改善ASD大鼠刻板重復、興趣降低等異常行為模式;并能上調BDNF蛋白表達,下調Bcl-2蛋白表達,激活ASD大鼠海馬區(qū)p-CREB、CREB蛋白表達引起針刺響應效應。
6 展望
目前,國內外都從遺傳、環(huán)境等多方面對ASD的發(fā)病機制展開了大量的研究與探索,但是由于神經系統(tǒng)疾病發(fā)病機制的復雜性,具體病因仍不明確。現(xiàn)階段研究發(fā)現(xiàn),ASD患者外周血中BDNF水平變化,使得BDNF可能成為診斷及治療ASD的潛在方向。從BDNF信號傳導通路的異常狀態(tài)進行切入,將會成為探索ASD病因的一個新目標。ASD可能存在BDNF信號通路傳導異常,對BDNF信號傳導通路在ASD中的作用機制進行深入挖掘,旨在發(fā)現(xiàn)ASD可能存在的發(fā)病新機制,為臨床治療ASD提供新靶點。
中醫(yī)藥目前對孤獨癥核心的研究較少,且多數研究缺乏遠期療效追蹤。雖然,近年來關于中醫(yī)藥在治療ASD患兒言語、認知、社交等問題的報道越來越多,但其療效和優(yōu)勢仍難獲認同,究其原因在于:其一,中醫(yī)療效評估多基于臨床觀察及問卷調查,缺少疾病改善的生物學數據支持;其二,臨床治療ASD的中藥缺乏基礎研究、藥理機制不明,針灸推拿治療的實驗機制研究匱乏。因此,中醫(yī)藥關于ASD的研究,今后應在中醫(yī)理論基礎上,充分利用生物學、神經學、遺傳學等現(xiàn)代學科,選取接近臨床ASD的動物模型,進行嚴謹的科研設計及實驗研究,明確中醫(yī)藥治療ASD的作用機制,通過數據化的生物學評估指標證實中醫(yī)藥的切實臨床療效。
參考文獻
[1] AMERICAN PSYCHIATRIC ASSOCIATION. Diagnostic and Statistical Manual of Mental Disorders: Fifth Edition[M]. Washington: American Psychiatric Publishing, 2013: 50-58.
[2] BAXTER A J, BRUGHA T S, ERSKINE H E, et al. The epidemiology and global burden of autism spectrum disorders[J]. Psychological Medicine, 2015, 45(3): 601-613.
[3] MASI A, DEMAYO M M, GLOZIER N, et al. An overview of autism spectrum disorder, heterogeneity and treatment options[J]. Neuroscience Bulletin, 2017, 33(2): 183-193.
[4] 鄒 ?卓,劉 ?蕓,黃浩宇,等.兒童孤獨癥譜系障礙流行現(xiàn)狀和家庭干預的研究及策略[J].中國全科醫(yī)學,2020,23(8):900-907.
[5] CYNTHIA, WETMORE. Localization of brain-derived neurotrophic factor mRNA to neurons in the brain by in situ hybridization[J]. Experimental Neurology, 1990, 109(2): 141-152.
[6] COLUCCI-D'AMATO L, SPERANZA L, VOLPICELLI F. Neurotrophic factor BDNF, physiological functions and therapeutic potential in depression, neurodegeneration and brain cancer[J]. International Journal of Molecular Sciences, 2020, 21(20): 7777.
[7] HUANG E J, REICHARDT L F. Neurotrophins: Roles in neuronal development and function[J]. Annual Review of Neuroscience, 2001, 24: 677-736.
[8] LEWIN G R, BARDE Y A. Physiology of the neurotrophins[J]. Annual Review of Neuroscience, 1996, 19(1): 289-317.
[9] DAVID R, KAPLAN. Neurotrophin signal transduction in the nervous system[J]. Current Opinion in Neurobiology, 2000, 10(3): 381-391.
[10] NUMAKAWA T, ODAKA H, ADACHI N. Actions of brain-derived neurotrophin factor in the neurogenesis and neuronal function, and its involvement in the pathophysiology of brain diseases[J]. International Journal of Molecular Sciences, 2018, 19(11): 3650.
[11] CHAO M V, HEMPSTEAD B L. p75 and Trk: A two-receptor system[J]. Trends in Neurosciences, 1995, 18(7): 321-326.
[12] KOWIA■SKI P, LIETZAU G, CZUBA E, et al. BDNF: A key factor with multipotent impact on brain signaling and synaptic plasticity[J]. Cellular and Molecular Neurobiology, 2018, 38(3): 579-593.
[13] BARBOSA A G, PRATESI R, PAZ G S C, et al. Assessment of BDNF serum levels as a diagnostic marker in children with autism spectrum disorder[J]. Scientific Reports, 2020, 10(1): 17348.
[14] CASTR?魪N M, LAMPINEN K E, MIETTINEN R, et al. BDNF regulates the expression of fragile X mental retardation protein mRNA in the hippocampus[J]. Neurobiology of Disease, 2002, 11(1): 221-229.
[15] UUTELA M, LINDHOLM J, RANTAM?魧KI T, et al. Distinctive behavioral and cellular responses to fluoxetine in the mouse model for Fragile X syndrome[J]. Frontiers in Cellular Neuroscience, 2014, 8: 150.
[16] LEAH, SELBY. Major defects in neocortical GABAergic inhibitory circuits in mice lacking the fragile X mental retardation protein[J]. Neuroscience Letters, 2007, 412(3): 227-232.
[17] PIETROPAOLO S, GOUBRAN M G, JOFFRE C, et al. Dietary supplementation of omega-3 fatty acids rescues fragile X phenotypes in Fmr1-Ko mice[J]. Psychoneuroendocrinology, 2014, 49: 119-129.
[18] SUN M K, HONGPAISAN J, ALKON D L. Rescue of synaptic phenotypes and spatial memory in young fragile X mice[J]. The Journal of Pharmacology and Experimental Therapeutics, 2016, 357(2): 300-310.
[19] REIM D, SCHMEISSER M J. Neurotrophic factors in mouse models of autism spectrum disorder: Focus on BDNF and IGF-1[J]. Advances in Anatomy, Embryology, and Cell Biology, 2017, 224: 121-134.
[20] HWANG S R, KIM C Y, SHIN K M, et al. Altered expression levels of neurodevelopmental proteins in fetal brains of BTBR T+tf/J mice with autism-like behavioral characteristics[J]. Journal of Toxicology and Environmental Health Part A, 2015, 78(8): 516-523.
[21] SKOGSTRAND K, HAGEN C M, BORBYE-LORENZEN N, et al. Reduced neonatal brain-derived neurotrophic factor is associated with autism spectrum disorders[J]. Translational Psychiatry, 2019, 9(1): 252.
[22] KATOH-SEMBA R, WAKAKO R, KOMORI T, et al. Age-related changes in BDNF protein levels in human serum: Differences between autism cases and normal controls[J]. International Journal of Developmental Neuroscience, 2007, 25(6): 367-372.
[23] SAGHAZADEH A, REZAEI N. Brain-derived neurotrophic factor levels in autism: A systematic review and meta-analysis[J]. Journal of Autism and Developmental Disorders, 2017, 47(4): 1018-1029.
[24] RYLAARSDAM L, GUEMEZ-GAMBOA A. Genetic causes and modifiers of autism spectrum disorder[J]. Frontiers in Cellular Neuroscience, 2019, 13: 385.
[25] DUFFNEY L J, VALDEZ P, TREMBLAY M W, et al. Epigenetics and autism spectrum disorder: A report of an autism case with mutation in H1 linker histone HIST1H1E and literature review[J]. American Journal of Medical Genetics Part B: Neuropsychiatric Genetics, 2018, 177(4): 426-433.
[26] WONG C C, MEABURN E L, RONALD A, et al. Methylomic analysis of monozygotic twins discordant for autism spectrum disorder and related behavioural traits[J]. Molecular Psychiatry, 2014, 19(4): 495-503.
[27] DE RUBEIS S, HE X, GOLDBERG A P, et al. Synaptic, transcriptional and chromatin genes disrupted in autism[J]. Nature, 2014, 515(7526): 209-215.
[28] SAMACO R C, HOGART A, LASALLE J M. Epigenetic overlap in autism-spectrum neurodevelopmental disorders: MeCP2 deficiency causes reduced expression of UBE3A and GABRB3[J]. Human Molecular Genetics, 2005, 14(4): 483-492.
[29] KUBOTA T, MOCHIZUKI K. Epigenetic effect of environmental factors on autism spectrum disorders[J]. International Journal of Environmental Research and Public Health, 2016, 13(5): 504.
[30] CHAO H T, ZOGHBI Y, ROSENMUND C. MeCP2 controls excitatory synaptic strength by regulating glutamatergic synapse number[J]. Neuron, 2007, 56(1): 58-65.
[31] SANG H, GO. Prenatal exposure to valproic acid increases the neural progenitor cell pool and induces macrocephaly in rat brain via a mechanism involving the GSK-3β/β-catenin pathway[J]. Neuropharmacology, 2012, 63(6): 1028-1041.
[32] KO H M, JIN Y, PARK H H, et al. Dual mechanisms for the regulation of brain-derived neurotrophic factor by valproic acid in neural progenitor cells[J]. The Korean Journal of Physiology & Pharmacology, 2018, 22(6): 679-688.
[33] WOODBURY-SMITH M, SCHERER S W. Progress in the genetics of autism spectrum disorder[J]. Developmental Medicine and Child Neurology, 2018, 60(5): 445-451.
[34] MIRANDA T B, JONES P A. DNA methylation: The nuts and bolts of repression[J]. Journal of Cellular Physiology, 2007, 213(2): 384-390.
[35] MARTINOWICH K, HATTORI D, WU H, et al. DNA methylation-related chromatin remodeling in activity-dependent BDNF gene regulation[J]. Science (New York, N Y), 2003, 302(5646): 890-893.
[36] LUBIN F D, ROTH T L, SWEATT J D. Epigenetic regulation of BDNF gene transcription in the consolidation of fear memory[J]. The Journal of Neuroscience, 2008, 28(42): 10576-10586.
[37] ARPI M N T, SIMPSON T I. SFARI genes and where to find them; modelling autism spectrum disorder specific gene expression dysregulation with RNA-seq data[J]. Scientific Reports, 2022, 12(1): 10158.
[38] BACCHELLI E, CAMELI C, VIGGIANO M, et al. An integrated analysis of rare cnv and exome variation in autism spectrum disorder using the infinium psycharray[J]. Scientific Reports, 2020, 10(1): 1-13.
[39] SATTERSTROM F K, KOSMICKI J A, WANG J B, et al. Large-scale exome sequencing study implicates both developmental and functional changes in the neurobiology of autism[J]. Cell, 2020, 180(3): 568-584. e23.
[40] GONZALEZ A, MOYA-ALVARADO G, GONZALEZ-BILLAUT C, et al. Cellular and molecular mechanisms regulating neuronal growth by brain-derived neurotrophic factor[J]. Cytoskeleton, 2016, 73(10): 612-628.
[41] KWON M, FERN?魣NDEZ J R, ZEGAREK G F, et al. BDNF-promoted increases in proximal dendrites occur via CREB-dependent transcriptional regulation of cypin[J]. The Journal of Neuroscience: the Official Journal of the Society for Neuroscience, 2011, 31(26): 9735-9745.
[42] PANDYA C D, KUTIYANAWALLA A, PILLAI A. BDNF-TrkB signaling and neuroprotection in schizophrenia[J]. Asian Journal of Psychiatry, 2013, 6(1): 22-28.
[43] DEOGRACIAS R, ESPLIGUERO G, IGLESIAS T, et al. Expression of the neurotrophin receptor trkB is regulated by the cAMP/CREB pathway in neurons[J]. Molecular and Cellular Neurosciences, 2004, 26(3): 470-480.
[44] ESVALD E E, TUVIKENE J, SIRP A, et al. CREB family transcription factors are major mediators of BDNF transcriptional autoregulation in cortical neurons[J]. The Journal of Neuroscience, 2020, 40(7): 1405-1426.
[45] NUMAKAWA T, ODAKA H. Brain-derived neurotrophic factor signaling in the pathophysiology of Alzheimer's disease: Beneficial effects of flavonoids for neuroprotection[J]. International Journal of Molecular Sciences, 2021, 22(11): 5719.
[46] PORT R G, OBERMAN L M, ROBERTS T P. Revisiting the excitation/inhibition imbalance hypothesis of ASD through a clinical lens[J]. The British Journal of Radiology, 2019, 92(1101): 20180944.
[47] 楊恩璐,孫秉貴. BDNF及其下游通路與GABA能神經元發(fā)育相關性的研究進展[J].生命科學,2020,32(6):544-550.
[48] QI C C, CHEN A D, MAO H H, et al. Excitatory and inhibitory synaptic imbalance caused by brain-derived neurotrophic factor deficits during development in a valproic acid mouse model of autism[J]. Frontiers in molecular neuroscience, 2022, 15:1-19.
[49] 孫林林,喬 ?利,田振華,等.姜黃化學成分及藥理作用研究進展[J].山東中醫(yī)藥大學學報,2019,43(2):207-212.
[50] 陳淑娟,姜志梅,張士嶺,等.姜黃素對孤獨癥大鼠行為及腦源性神經營養(yǎng)因子表達的影響[J].實用兒科臨床雜志,2012,27(15):1187-1189.
[51] 王 ?浩,楊 ?健,周良云,等.何首烏化學成分與藥理作用研究進展[J].中國實驗方劑學雜志,2019,25(13):192-205.
[52] 李茜茜,李 ?飛,郎修遠,等.何首烏苷通過激活BDNF/TrkB信號通路拮抗H2O2誘導的大鼠海馬神經元氧化損傷[J].天然產物研究與開發(fā),2019,31(7):1163-1169.
[53] 陳思琦,李佳欣,吳鑫宇,等.熟地黃的藥理學研究進展[J].化學工程師,2019,33(11):46-50.
[54] BRUCHHAGE M M K, BUCCI M P, BECKER E B E. Cerebellar involvement in autism and ADHD[M]//The Cerebellum: Disorders and Treatment. Amsterdam: Elsevier, 2018: 61-72.
[55] 袁海霞,倪新強,吳正治,等.基于“腎腦相關”探討熟地黃對ADHD模型大鼠行為學的影響[J].中藥材,2018,41(8):1970-1974.
[56] 王 ?倩,李柳潼,馬永犇,等.白芍與赤芍化學成分和藥理作用比較研究及質量標志物的預測分析[J].中國新藥雜志,2021,30(12):1093-1098.
[57] 王菲菲,李 ?雪,劉 ?靖,等.孤獨癥幼兒的情緒行為問題研究[J].中國全科醫(yī)學,2019,22(18):2189-2193.
[58] MORIMOTO Y, YAMAMOTO N, KANEGAE S, et al. Genetic overlap among autism spectrum disorders and other neuropsychiatric disorders[M]//Autism Spectrum Disorders. Brisbane: Exon Publications, 2021: 67-78.
[59] 朱映黎,王林元,王成龍,等.芍藥內酯苷和芍藥苷對慢性束縛應激大鼠神經營養(yǎng)因子以及一氧化氮影響的研究[J].中國中藥雜志,2016,41(22):4240-4246.
[60] 阿依奴爾·吾買爾,劉興盛.加味溫膽湯配合教學訓練矯治孤獨癥兒童異常行為21例[J].世界最新醫(yī)學信息文摘,2015,15(48):138.
[61] 高 ?源,朱金華,張 ?媛,等.溫膽湯對精神分裂癥模型大鼠海馬組織BDNF、CaMKⅡ表達的影響[J].中藥藥理與臨床,2021,37(4):8-12.
[62] 何麗玲,龍清華,胡 ?慧,等.大補元煎通過上調BDNF/TrkB/CREB信號通路改善APP/PS1雙轉基因癡呆小鼠海馬突觸可塑性[J].中國實驗方劑學雜志,2020,26(21):1-7.
[63] 羅 ?彤.電針對CUMS抑郁模型大鼠海馬tPA/BDNF通路影響的實驗研究[D].北京:北京中醫(yī)藥大學,2020.
[64] 馮 ?祥,李 ?桃,蔣全睿,等.基于“督脈入腦”理論探討推拿干預孤獨癥譜系障礙的思路[J].湖南中醫(yī)藥大學學報,2022,42(3):401-405.
[65] 林 ?燊.電針不同刺激時長對自閉癥大鼠BDNF-CREB相關信號通路的影響[D].福州:福建中醫(yī)藥大學,2020.
〔收稿日期〕2021-12-10
〔基金項目〕湖南省科技廳重點領域研發(fā)計劃項目(2019SK2081);湖南省衛(wèi)生健康委員會科研課題(202206010043);湖南中醫(yī)藥大學校極研究生創(chuàng)新課題(2022CX157)。
〔第一作者〕吳 ?吉,女,碩士研究生,研究方向:中醫(yī)藥防治兒科疾病。
〔通信作者〕*朱沁泉,女,博士研究生,主治醫(yī)師,E-mail:121088153@qq.com;張 ?滌,男,主任醫(yī)師,E-mail:2655357548@qq.com。

