納米二氧化硅和鎘聯合暴露對人臍靜脈內皮細胞的影響*
趙 婧 焦卓亞 王 娟 劉 璐 駢玉杰 王 丹
山西醫科大學汾陽學院預防醫學教研室,山西省汾陽市 032200
環境顆粒物(Particulate matters,PM)是世界范圍內主要公共健康問題,已有越來越多的流行病學和實驗室證據證實,環境PM與心血管疾病的發生有關[1]。不同類型的污染物在環境中通常共存[2],研究表明[3],PM的有害效應是細顆粒物及其吸附的有毒污染物共同作用的結果,然而,更細的顆粒物和空氣污染物的聯合毒性仍然不清楚。納米二氧化硅(SiO2)廣泛存在于工業、醫藥和食品中[2],鎘(Cd)是一種廣泛分布的污染物[4],可能與環境中的納米SiO2共存。內皮細胞功能的體外研究常使用人臍靜脈內皮細胞(Human umbilical vein endothelial cells,HUVECs)。因此,本文旨在研究納米SiO2和Cd對HUVECs的聯合暴露效應,通過評估HUVECs氧化損傷和DNA損傷來評價其聯合作用。
1 材料與方法
1.1 材料、試劑及儀器 HUVECs株由華中科技大學同濟醫學院贈送。納米SiO2(10~20nm,純度≥99.8%,杭州萬景新材料有限公司),氯化鎘(CdCl2)(西安化學試劑廠),活性氧(ROS)試劑盒(碧云天生物技術研究所),超氧化物歧化酶(SOD)、谷胱甘肽過氧化物酶(GSH-Px)活性和丙二醛(MDA)試劑盒(南京建城),DMEM細胞培養液、胎牛血清(Gibco,USA),單細胞凝膠電泳(SCGE)試劑盒(Research Biolab,China)。所有其他化學品均屬分析級,并可在市場上買到。多功能酶標儀(BbiTeK,USA),CO2水套培養箱(Forma 3111,USA),臺式低溫離心機(eppendorf 5810R,GER),電泳儀、電泳槽(北京市六一儀器廠),熒光顯微鏡、熒光數碼顯微成像系統(OLYMPUS,Japan)。
1.2 方法
1.2.1 納米SiO2和CdCl2的配制:用無菌三蒸水制備2mg/ml納米SiO2和50mmol/L CdCl2母液,高壓滅菌,在4℃環境中保存,使用前紫外照射30min,超聲處理15min,再將納米SiO2母液和CdCl2母液用培養液稀釋。
1.2.2 細胞培養及分組:HUVECs在添加10%滅活胎牛血清、青霉素/鏈霉素的DMEM培養基中培養,在37℃含5%CO2的培養箱保存,然后收集對數生長階段的細胞,接種到96孔或24孔培養板,每孔150μl或1ml,接種密度5×104個/ml,24h后更換培養基,用PBS洗凈,然后每孔按總體積150μl或1ml添加指定的化學物質。對照組(未添加任何藥物)、納米SiO2組(添加10μg/ml的納米SiO2)、CdCl2組(添加25μmol/L的CdCl2)、聯合組(添加10μg/ml的納米SiO2和25μmol/L的CdCl2)。各組設三個復孔。以上濃度的設定都是建立在前期的預實驗基礎上的。每組均在37℃含5%CO2的培養箱中放置24h,然后用于分析。
1.2.3 ROS水平測定:24h后,取出96孔培養板,PBS洗凈,加入100μl的DCFH-DA,37℃孵育30min,棄去培養液,無血清培養液潤洗3次,再將培養板置于多功能酶標儀,對各組的DCF熒光強度進行檢測。
1.2.4 SOD、GSH-Px活性和MDA含量的測定:24h后,取出24孔培養板,用冰冷的PBS洗滌細胞,并在冰冷的RIPA裂解緩沖液中裂解30min。將裂解物按12 000r/min離心10min,收集上清液,并參照試劑盒說明書對SOD、GSH-Px活性及MDA含量進行測定。
1.2.5 DNA損傷測定: 24h后,用PBS洗凈,將10μl細胞懸液與90μl瓊脂糖混合,移至瓊脂糖包被的載玻片上,用蓋玻片遮蓋,在4℃下冷卻4min,將載玻片置于新鮮裂解液中,4℃避光2h,然后25V、300mA,電泳30min,用于DNA解鏈,載玻片用碘化丙啶(PI)染色后,再經熒光顯微鏡檢測。
1.3 統計學方法 基于析因設計實驗獲得數據采用雙因素方差分析(ANOVA)進行分析,隨后進行交互效應和不同組間差異事后檢驗。全部采用SAS8.2軟件包進行統計分析。臨界值設為P<0.05。
先通過雙因素方差分析得到F值和P值確定相互作用類型,然后比較因素A和B的聯合效應(EA×B)和單獨效應(EA或EB),相互作用類型判斷標準如下:(1)相加效應:F<5,P>0.05,且EA×B>EA+EB;(2)協同效應:F>5,P<0.05,且EA×B>EA+EB;(3)拮抗作用:F>5,P<0.05,且EA×B 2.1 納米SiO2和Cd對細胞ROS生成的影響 納米SiO2組未觀察到ROS的顯著變化(見表1);與對照組相比,Cd暴露組或納米SiO2和Cd聯合暴露組的ROS生成增加,聯合暴露組的升高幅度更大。析因分析顯示,納米SiO2和Cd對細胞ROS生成有協同作用(F=107.896,P<0.01)。結果表明,納米SiO2的暴露使Cd的細胞毒性增強。 表1 納米SiO2和Cd對HUVECs ROS生成的影響 2.2 納米SiO2和Cd對細胞SOD和GSH-Px活性的影響 SOD和GSH-Px是細胞內主要的抗氧化酶,其活性體現了細胞的酶促抗氧化能力。暴露于納米SiO2的細胞中觀察到SOD活性無顯著變化(見表2),然而,與對照組相比,暴露于Cd以及納米SiO2與Cd聯合暴露的細胞SOD活性顯著降低,與單獨暴露于Cd的細胞相比,在暴露于Cd和納米SiO2的細胞中觀察到更顯著的SOD活性降低。同樣,在暴露于Cd或納米SiO2與Cd組合的細胞中,GSH-Px活性顯著降低,在暴露于納米SiO2與Cd組合的細胞中觀察到最高的降低。結果表明,納米SiO2與Cd的聯合作用使得HUVECs的酶促抗氧化能力明顯下降。析因分析表明,納米SiO2與Cd相加作用導致SOD活性下降(F=1.956,P>0.05),納米SiO2與Cd協同作用導致GSH-Px活性下降(F=6.35,P<0.05)。 表2 納米SiO2和Cd對HUVECs SOD和GSH-Px活性的影響 2.3 納米SiO2和Cd對細胞MDA含量的影響 暴露于納米SiO2的細胞MDA含量并未觀察到顯著變化(見表3),但與對照組相比,暴露于Cd或納米SiO2與Cd聯合暴露的細胞MDA含量有明顯增加,最高的增加是在納米SiO2與Cd聯合暴露的細胞中觀察到的。析因分析表明,納米SiO2與Cd對MDA含量的增加具有相加作用(F=0.08,P>0.05)。 表3 納米SiO2和Cd對HUVECs MDA含量的影響 2.4 納米SiO2和Cd對細胞DNA損傷的影響 與對照細胞相比,暴露于納米SiO2對細胞DNA損傷無明顯影響(見表4),但Cd或納米SiO2與Cd聯合暴露均對細胞DNA損傷有明顯誘導作用,表現為明顯升高的OLIVE尾炬。納米SiO2和Cd聯合作用對HUVECs DNA損傷更嚴重。析因分析表明,DNA損傷是由納米SiO2和Cd之間的協同作用引起的(F=12.962,P<0.01)。 表4 納米SiO2和Cd對HUVECs DNA損傷的影響 因為PM組成復雜,吸入PM的生物反應不僅取決于單個組分,還取決于其與附著組分之間的相互作用,PM及其吸附污染物的聯合暴露可能會影響污染物的單獨作用[5],因此需要對PM及其吸附的有毒污染物的聯合毒性進行判定。本研究表明,納米SiO2和Cd可通過相加或協同作用增強HUVECs氧化應激和DNA損傷。 PM可誘導細胞的氧化損傷[6]。Cd具有誘導氧化應激、DNA損傷的作用[7]。本研究顯示,適度細胞毒性濃度的Cd誘導HUVECs氧化應激和DNA損傷,如ROS生成增加、SOD、GSH-Px活性降低,MDA含量增加以及DNA尾炬值增加;僅暴露于非細胞毒性濃度的納米SiO2對細胞內氧化還原平衡沒有顯著影響,然而,納米SiO2和Cd的聯合暴露顯著增強了氧化應激和DNA損傷,表現為ROS生成和MDA含量升高幅度更大,SOD和GSH-Px活性降低幅度更大,DNA損傷更嚴重。 聯合暴露于不同的毒物組合,可產生相加作用、協同作用或拮抗作用[8]。本研究表明,納米SiO2與Cd聯合暴露對細胞ROS生成、GSH-Px活性和DNA損傷具有協同效應,對SOD活性和MDA含量具有相加效應。相關類似研究表明[9],將人肝臟細胞(HepG2)暴露于納米SiO2和砷的組合中,對ROS生成、SOD活性、DNA損傷產生相加作用,對MDA含量和GSH-Px活性產生協同作用。然而,目前尚不清楚非細胞毒性濃度的納米SiO2如何增強Cd對HUVECs的毒性,可能是由于納米SiO2促進了Cd的積累。Zhang等[10]表明,在納米TiO2存在的情況下,鯉魚體內Cd2+濃度增加了146%。Yu等[11]發現,將A549細胞暴露在納米SiO2和甲基汞混合物中,細胞內甲基汞濃度明顯高于單獨暴露于甲基汞的細胞,表明納米SiO2促進了細胞對甲基汞的攝取,這可能是暴露于納米SiO2和甲基汞組合后毒性增強的原因。一些研究報道[12],納米TiO2作為載體促進Cd內化進入人肝癌和乳腺癌細胞。Limbach等[13]認為,納米SiO2在暴露于納米SiO2和錳組合的細胞中起到“特洛伊木馬”的作用,這可能解釋了吸附在納米SiO2上的有毒分子更容易進入細胞的原因。由于Cd的理化性質與吸附在PM上的典型空氣污染物錳、汞相似,因此有理由推測,更多的Cd可能通過納米SiO2的細胞內化作用進入細胞,納米SiO2可能起到載體或“特洛伊木馬”的作用,這可能促進了Cd在HUVECs中的積累,導致氧化應激和DNA損傷的增加。納米SiO2在細胞質、細胞核等的定位,除了增加細胞對Cd的攝取,還可能誘發細胞、亞細胞結構或功能的紊亂[14],誘導產生ROS和后續的氧化應激可能是導致納米SiO2誘導毒性的分子機制[15-16],所以,接下來我們要繼續探究納米SiO2細胞內分布的是怎樣的。本研究顯示,非細胞毒性濃度的納米SiO2不影響細胞內的氧化還原平衡,然而,納米SiO2對細胞的潛在干擾可能使細胞對Cd的易感性增加。 綜上所述,非細胞毒性濃度的納米SiO2和細胞毒性濃度的Cd共同作用于HUVECs,可增強細胞氧化應激和DNA損傷,其細胞毒性作用是通過納米SiO2和Cd的相加或協同作用實現的。納米SiO2作為載體的特殊理化特性,促進了Cd在HUVECs中的積聚,從而加劇Cd誘導的氧化應激和DNA損傷。更好地了解UFPs和空氣污染物的聯合毒性及其潛在毒性機制,有助于闡明暴露于PM的健康影響。2 結果
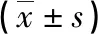


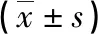
3 討論

