可溶性T細胞免疫球蛋白黏蛋白3、淋巴細胞激活基因3表達水平與子宮內膜癌疾病轉歸的相關性*
張瑞紅 張海濤
山東省成武縣人民醫院 1 婦產科 2 病理科 274200
我國子宮內膜癌發病率約為14%,5年生存率約為20%,且呈年輕化趨勢,由于早期臨床癥狀不明顯導致大部分患者確診時已發展至晚期[1-2]。目前以手術治療為主,由于局部復發、轉移導致疾病轉歸不一,因而尋找預測子宮內膜癌疾病轉歸的潛在標志物有助于改善患者預后。可溶性T細胞免疫球蛋白黏蛋白3(sTim-3)屬于免疫抑制分子,可負向調節Th1細胞增殖,抑制腫瘤相關免疫反應,其高表達與多種惡性腫瘤不良預后有關[3]。淋巴細胞激活基因3(LAG-3)屬于免疫球蛋白超家族成員,可抑制T細胞增殖、活化,并可能參與宮頸鱗癌等多種腫瘤發生發展過程[4]。目前sTim-3、LAG-3與子宮內膜癌相關研究報道較少。本研究主要觀察子宮內膜癌患者血清sTim-3、LAG-3水平變化,分析其與臨床病理特征及疾病轉歸的相關性,旨在為子宮內膜癌免疫治療提供新思路。
1 資料與方法
1.1 一般資料 選取2019年2月—2021年3月于本院接受手術治療的52例子宮內膜癌患者為對象,依據術后1年疾病轉歸情況分為良好組34例、不良組18例。良好組:年齡44~65(54.31±3.26)歲,體質量指數18~26(22.35±1.16)kg/m2,是否絕經:是18例、否16例。不良組:年齡43~63(53.27±3.18)歲,體質量指數18~28(23.01±1.38)kg/m2,是否絕經:是10例、否8例。兩組一般資料比較無明顯差異(P>0.05),具有可比性。本研究經本院倫理委員會批準。
1.2 納入與排除標準 納入標準:符合子宮內膜癌診斷標準[5],且經組織病理學檢查確診;原發性子宮內膜癌;術前經宮頸細胞學檢查顯示陽性;經陰道鏡檢查顯示無宮頸惡性病變者;接受腹腔鏡手術治療者;術前未接受放化療或激素治療者。排除標準:合并嚴重內外科合并癥者;合并其他部位惡性腫瘤者;精神障礙者;合并免疫缺陷疾病者。
1.3 方法
1.3.1 治療方法。腹腔鏡手術治療:陰道內留置舉宮器建立人工氣腹,于患者側下腹置入第2、3套管針,同時探查腹腔,留取腹腔沖洗液(100ml)進行細胞學檢查,腹腔鏡下切除子宮雙附件、盆腔淋巴結,放置引流管,使用生理鹽水沖洗盆腹腔,腹腔鏡退出,術后予以抗生素治療。術后1年觀察疾病轉歸情況,其中患者無復發為預后良好;出現復發或死亡為預后不良。
1.3.2 采集血液樣本。分別于術前、術后1d、術后1個月采集兩組空腹靜脈血5ml,4℃條件下經3 000r/min離心(10min)留取血清,儲存于-80℃冰箱。
1.3.3 檢測血清sTim-3、LAG-3水平。采用ELISA法檢測血清sTim-3水平,上海臻科生物科技有限公司提供檢測試劑盒。采用雙抗體夾心酶聯免疫吸附試驗檢測血清LAG-3水平,杭州齊譽生物科技有限公司提供檢測試劑盒。
1.4 觀察指標 (1)分析兩組術前、術后1 d、術后1個月血清sTim-3、LAG-3水平。(2)分析術前不同臨床病理特征患者血清sTim-3、LAG-3水平,其中臨床病理特征包括腫瘤大小、臨床FIGO分期、組織學分級、分化程度、肌層浸潤深度。(3)分析血清各指標(術前)與臨床病理特征相關性及其(術后1個月)對疾病轉歸的預測價值。(4)分析各指標對疾病轉歸不良發生危險度的影響。
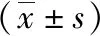
2 結果
2.1 兩組血清sTim-3、LAG-3水平比較 與術前比較,術后1d、術后1個月兩組血清sTim-3、LAG-3水平降低(P<0.05);與良好組比較,術后1d、術后1個月不良組血清sTim-3、LAG-3水平升高(P<0.05),見表1。
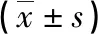
表1 兩組血清sTim-3、LAG-3水平比較
2.2 不同臨床病理特征患者血清sTim-3、LAG-3水平比較 隨著臨床FIGO分期升高、組織學分級升高、分化程度降低及發生淋巴結轉移,血清sTim-3、LAG-3水平升高(P<0.05),見表2。
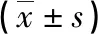
表2 不同臨床病理特征患者血清sTim-3、LAG-3水平比較
2.3 血清各指標水平與臨床病理特征相關性 血清sTim-3、LAG-3水平與臨床FIGO分期、組織學分級、淋巴結轉移呈正相關(P<0.05),而與分化程度呈負相關(P<0.05),見表3。

表3 血清各指標水平與臨床病理特征相關性
2.4 血清各指標對疾病轉歸的預測價值 以不良組18例為陽性樣本,以良好組34例為陰性樣本,繪制ROC曲線,結果顯示,術后1個月血清sTim-3、LAG-3水平聯合預測疾病轉歸不良的AUC大于單項預測(P<0.05),見表4。

表4 血清各指標對疾病轉歸的預測價值
2.5 血清各指標不同表達者疾病轉歸不良的危險度分析 以2.4結果中各指標截斷值為分界,患者分為高表達者、低表達者。sTim-3、LAG-3高表達者疾病轉歸不良的危險度分別是低表達者的1.789倍、1.737倍,見表5。

表5 血清各指標不同表達者疾病轉歸不良的危險度分析
3 討論
子宮內膜癌發病機制與抑癌基因失活、致癌基因活化、先天性/適應性免疫細胞改變有關,免疫相關因子可參與T細胞、自然殺傷細胞活化及腫瘤免疫耐受過程,同時機體內持續炎性狀態可增強腫瘤免疫原性,促使子宮內膜細胞損傷,進一步促進子宮內膜癌發生發展[6]。
Tim-3可調節免疫反應,誘導免疫耐受,介導效應T細胞凋亡,并可促進腫瘤相關巨噬細胞M2極化,阻斷自然殺傷細胞功能,還可通過白細胞介素-6(IL-6)自分泌方式,促進腫瘤細胞增殖、遷移及侵襲[7]。Tim-3配體包括半乳凝素-9(Gal-9)、癌胚抗原細胞黏附分子1(CEACAM1)等,Tim-3與配體結合可激活鈣—鈣蛋白酶—含半胱氨酸的天冬氨酸蛋白水解酶-1(caspase-1)通路,介導效應T細胞凋亡,促進腫瘤細胞免疫逃逸[8]。本研究結果顯示,術后不良組血清sTim-3水平高于良好組,表明sTim-3水平變化可反映疾病轉歸情況。本研究進一步分析發現,隨著臨床FIGO分期升高、組織學分級升高、分化程度降低及淋巴結轉移的發生,血清sTim-3水平明顯升高,表明sTim-3可能參與子宮內膜癌發展進程,并可能在一定程度上反映子宮內膜癌細胞增殖、轉移情況。其原因可能為:sTim-3可參與子宮內膜癌免疫應答過程,可能通過內源性或外源性途徑,介導腫瘤相關炎性因子生成,改變腫瘤炎性微環境,增強腫瘤細胞侵襲性,導致其逃避免疫監視。早期臨床試驗證實采用免疫抑制因子抑制劑可抑制腫瘤轉移,治療后監測免疫抑制因子水平對評價機體免疫功能及治療效果具有重要意義[9]。Chen等[10]的研究報道顯示,血清sTim-3水平升高可能作為預測術后復發的潛在指標。本研究結果顯示,血清sTim-3水平預測子宮內膜癌疾病轉歸不良的AUC為0.735,提示sTim-3對子宮內膜癌疾病轉歸不良具有一定預測價值,但仍需結合其他指標共同預測,以此提高預測效能。
LAG-3可抑制T細胞增殖及其相關細胞因子表達,負向調節T細胞功能,參與腫瘤免疫逃逸過程,并可激活一系列信號通路,抑制免疫細胞活化及分泌抗體[11]。LAG-3與腫瘤臨床病理特征相關,可在一定程度上影響腫瘤發生發展[12]。本研究結果顯示,術后不良組血清LAG-3水平高于良好組,有淋巴結轉移、較低分化程度者LAG-3水平分別高于無淋巴結轉移、較高分化程度者,且臨床FIGO分期、組織學分級越高,LAG-3水平越高,這與王聰等[13]研究結果相似。提示LAG-3高表達與子宮內膜癌發生、浸潤等一系列過程密切相關。但吳玲等[14]發現,LAG-3水平與淋巴結轉移、TNM分期呈負相關。本研究結果顯示血清LAG-3水平與臨床FIGO分期、組織學分級、淋巴結轉移呈正相關,而與分化程度呈負相關,與上述研究結果不一致[14]。原因可能為:不同類型腫瘤患者體內免疫微環境不同,選取檢測診斷方法不同,此外,LAG-3對腫瘤的作用機制可能存在雙向作用。同時本研究發現血清sTim-3、LAG-3聯合預測疾病轉歸不良的AUC大于單項預測,提示聯合檢測血清sTim-3、LAG-3水平可提高子宮內膜癌疾病轉歸的預測效能。
綜上所述,子宮內膜癌患者血清sTim-3、LAG-3水平升高,且與臨床病理特征密切相關,其聯合預測對子宮內膜癌疾病轉歸不良具有一定預測價值,可為臨床對子宮內膜癌患者轉歸結局預測提供可靠依據。

