農藥代謝物毒理學評價程序研究
石新蕾,張宏軍,陶嶺梅,劉 然,黃 嵐,劉東暉*,張麗英*
(1.中國農業大學理學院,北京100193;2.農業農村部農藥檢定所,北京100125)
農藥的使用對農業生產過程中病蟲草害的控制效果十分顯著,對保障世界糧食安全具有重要貢獻。但農藥的田間施用會使其有效成分不可避免地通過各種途徑進入環境或殘留于作物,導致農藥殘留,并在其中發生代謝、反應或降解,進而生成相應的代謝物。由于這些代謝物生成機理復雜且結構多樣,往往對其潛在風險知之甚少。因此,為了保障農藥的使用不會對人類自身和環境中的非靶標生物造成有害影響,各國監管機構在農藥登記和再評審階段中除了需要關注農藥有效成分的安全性,也會重點評估它們在作物、畜禽、加工農產品以及環境中生成的代謝物和/或轉化產物所產生的潛在風險。
1 農藥殘留物定義及代謝物定義
不同農藥的殘留物中化合物的種類和數量可能存在很大差異。農藥殘留物定義的統一為農藥及其代謝物的殘留鑒定提供了一種通用的方法。聯合國糧農組織食品法典委員會(CAC)[1]、聯合國糧農組織(FAO)/世界衛生組織(WHO)農藥殘留聯席會議(JMPR)[2]、歐洲食品安全局(EFSA)[3]等都對農藥殘留物定義進行了相關論述,但各國對如何確定殘留物定義并沒有系統規定。為了打破不同國家因標準不一所產生的技術壁壘,經濟合作與發展組織(OECD)于2009年修訂了關于農藥殘留物定義的導則[4],得到了美國、歐洲各國及日本等OECD國家的認可,作為JMPR專家用于推薦農藥殘留物定義時的指導性文件,以決定具體選擇哪些目標化合物進行風險評估,制定最大殘留限量并進行監測。根據OECD頒布的《農藥殘留物定義導則》,農藥的“殘留物定義”是指農藥管理機構對施用于可食用或可飼用作物上的農藥,在進行膳食攝入風險評估以及制定最大允許殘留限量時所明確的殘留化合物。而根據應用的目的不同,農藥殘留物定義可能不同,主要包括用于膳食風險評估的殘留物定義和用于市場監督的殘留物定義,本文主要關注前者。
在制定農藥殘留物定義過程中,最重要的是明確農藥使用后會產生何種代謝物或降解產物。主要利用同位素標記的試驗方法,了解農藥使用后在植物體內代謝、在家畜體內代謝、在魚類(代表特定的水生生物)體內代謝、在鼠體內代謝、在加工產品中的殘留特性以及在后茬作物中的代謝情況[5]。在制定膳食風險評估殘留物定義時,需要全面考慮農藥使用后所產生的降解產物或代謝物在人類膳食中暴露的潛在可能性以及其相對于母體的毒性。近年來,隨著分析方法的進步和靈敏度的提高,導致檢測出越來越多的低水平代謝物,因此,需要根據同位素標記試驗結果明確農藥使用后會產生何種代謝物,并對主要代謝物進行識別和表征,以獲得全面的代謝數據,確定是否會產生有毒理學意義的代謝物,并制定風險評估的殘留物定義。
目前,各國和國際組織對農藥代謝物定義內涵基本一致,一般包括農藥在植物、動物以及環境中的代謝物(或轉化產物),并且規定在植物和牲畜的殘留物(代謝)研究中或在限制性輪作作物研究中占總放射性殘留物(TRR)10%或以上的物質為主要代謝物;總放射性殘留物(TRR)(或環境研究中的應用劑量)中所占比例低于10%的代謝物或降解產物則為次要代謝物。
目前,從消費者所接觸到的混合物中,只有活性成分的毒理學研究較為豐富,相比之下,在大多數情況下,關于農藥代謝物的毒理學信息十分有限。因此,為了更好地保障農藥使用對人類以及環境非靶標生物的安全性,在各國批準農藥使用之前,不僅為母體化合物制訂全面的毒理學檔案,還應全面評估代謝物的毒理學負擔。
2 農藥代謝物評價程序研究
目前,關于代謝物評價的指南和資料要求相對有限,國際上僅有FAO/WHO農藥殘留聯席會議(JMPR)和EFSA制定了明確的代謝物毒理學評價程序。
2.1 JMPR對農藥代謝物的評價程序 農藥殘留聯席會議(JMPR)成立于1963年,是FAO和WHO聯合管理的三個專家咨詢機構之一,由FAO農藥殘留問題小組和WHO核心評估小組組成。WHO核心評估小組負責審查農藥毒理學數據,估算可接受每日攝入量(ADI)、急性參考劑量(ARfD)和其他毒理學標準。
JMPR采用決策樹的方式,依據暴露及毒理學資料對代謝物進行評估[6]。評價程序共分為三個模塊,17個步驟(圖1)。首先,根據已有代謝物毒理學資料判定代謝物毒性和母體的關系;然后,根據代謝物是否在大鼠/小鼠/犬的代謝中呈現,判定代謝物在母體毒性中的可能作用;最后,采用毒理學關注閾值方法(TTC)進行篩查和初步風險特征描述,判定是否需要啟動特定的毒理學測試進行進一步的風險評估。聯席會議會考慮得到的所有信息,并
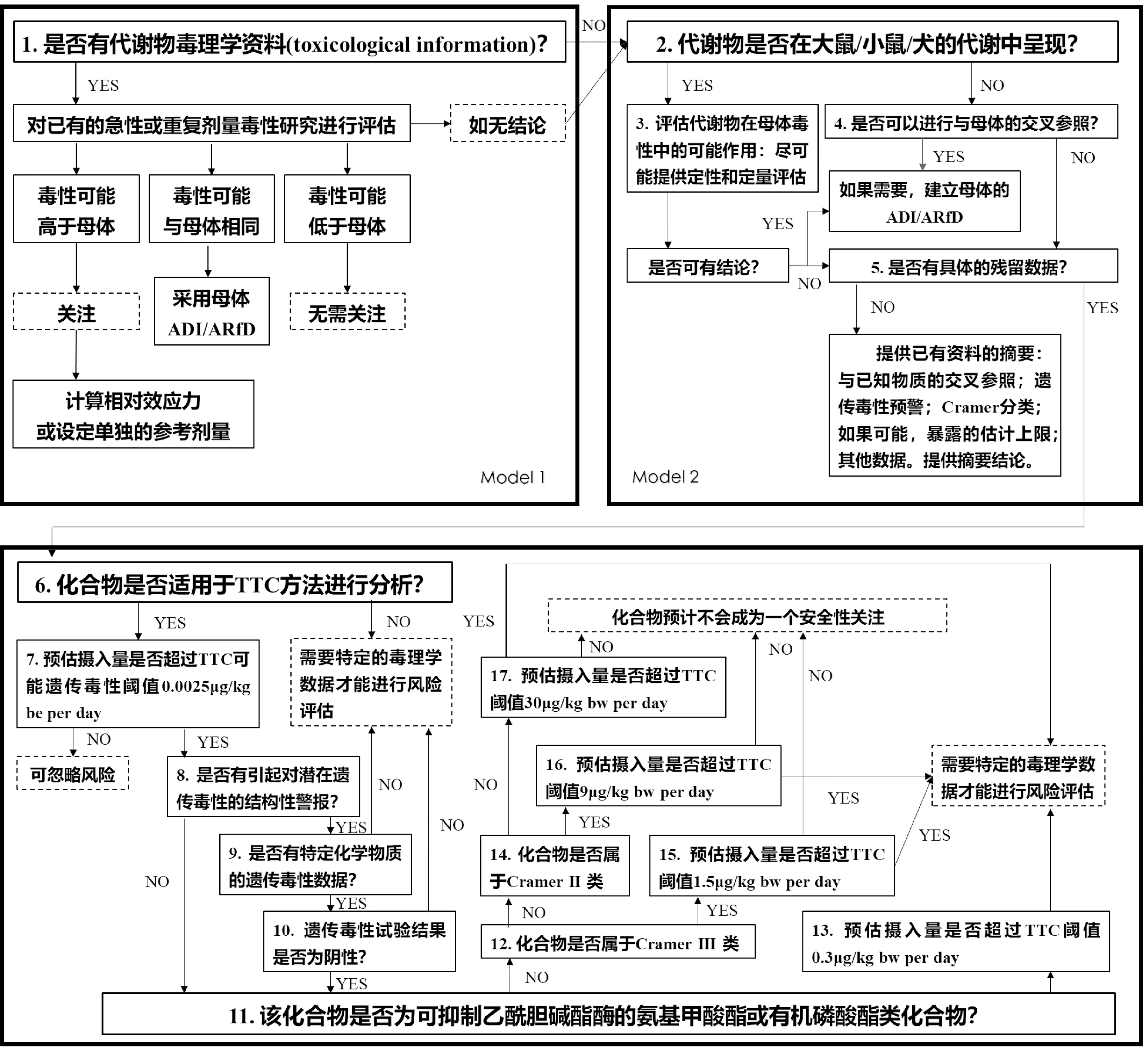
圖1 JMPR動植物代謝物/降解產物安全性評估的方案(流程圖)
對其進行科學評價。因現有資料在很大程度上各不相同,JMPR在評估時不需遵循嚴格的規則,而是根據具體情況考慮提交的信息,并在評估過程中編寫一份總結調查結果、結論和建議的評估報告,成為目前國際上很多國家在農藥登記管理及風險評估的重要參考。但需要注意的是,批準農藥的使用并不在JMPR的職責范圍內,且JMPR所評價的產品一般已在有關國家登記,故JMPR基于所提交的現有毒理學資料開展評估,評估過程主要依賴專家磋商,具有很大的靈活性。
2.2 EFSA對農藥代謝物的評價程序 歐洲食品安全局(EFSA)對農藥代謝物的毒理學評價程序主要包括三個部分,19個步驟[3](圖2)。首先,編制代謝物清單并評估遺傳毒性終點;其次,對其他毒性調控終點進行評估;最后,結合暴露來源和類型、特定暴露途徑等信息共同構成殘留物定義的基礎。該評估流程提供了所使用的科學工具和方法((定量)結構-活性關系((Q)SAR)、交叉參照(Read-across)、毒理學關注閾值(TTC)和可用數據組合(Grouping))來確定需要危害識別和表征的代謝物,且需要經驗豐富的專家深入參與,并為代謝物制定適當的測試策略。

圖2 EFSA膳食風險評估決策方案
3 農藥登記中對主要代謝物資料要求
不同國家對農藥代謝物毒理學試驗的需求不同,關于農藥代謝物評價的資料要求也各不相同。
3.1 歐盟農藥登記資料要求 歐盟主要由歐盟委員會健康與消費者保護總司(EC)負責農藥活性成分的登記注冊、歐盟殘留限量標準的制定、歐盟農藥管理政策的制定和監督執行。
根據歐盟農藥登記資料要求[7],對代謝物健康毒理學研究不作常規要求。是否需要進行補充研究應根據具體情況做出決定。如果由于代謝或其他過程的原因,植物或動物產品、土壤、地下水、露天空氣中的代謝物與用于毒理學研究的動物中的代謝物不同,或在動物中檢測到的比例較低,則應考慮與母體相比代謝物的數量和化學結構并根據具體情況進行進一步測試。
3.2 美國農藥登記資料要求 美國主要由環保局(EPA)對農藥進行監管,具體負責農藥安全性評估、登記注冊、生產、銷售、使用管理等。
根據美國農藥登記資料要求[8],對于殘留物需提供殘留信息、分析方法以及在不同動植物、水體等介質中的殘留量,雖未明確針對代謝物毒理學的專門條款,但在進行膳食風險評估中,會使用不同的工具和專家的判斷對代謝物進行證據權重評估決定,同時還會參考NAFTA QSAR指南進行逐案處理。
3.3 澳大利亞農藥登記資料要求 澳大利亞國家農藥和獸藥管理局(APVMA)負責國家農藥和獸藥登記計劃。該計劃對所有在澳大利亞使用的農藥和獸藥的生產和供應進行登記和管理。
一般來說,采用活性成分的研究可以提供母體化合物及其代謝物毒性的總體評估。但是,如果在目標植物和動物中產生的代謝物與在實驗室動物中產生的代謝物有顯著不同,則應該提供這些代謝物的毒理學研究資料。根據澳大利亞農藥登記資料要求[9],對于具有毒理學意義的代謝物,申請人需要使用兩種計算模型評估雜質的遺傳毒性潛力,并根據其計算結果決定是否對代謝物進行遺傳毒性試驗,若試驗結果呈陽性,則需要進一步確定代謝物在體細胞、生殖細胞內潛在的基因毒性。
3.4 日本農藥登記資料要求 日本農藥登記由厚生勞動省、農林水產省和環境省及內務府的食品安全委員會共同管理。厚生勞動省負責農藥毒理學資料評審、制定農藥最大殘留限量標準、進口食品農藥殘留監控;農林水產省負責農藥安全性評估、登記注冊、生產、銷售、使用管理;環境廳負責環境及水體農藥殘留資料的評審。
根據日本農藥登記資料要求[10]規定,當主要代謝物預計將在農業化學品的膳食風險評估中接受暴露評估時,視情況提交關于人類影響的試驗結果中關于急性口服毒性的試驗結果,以及遺傳毒性試驗結果中的回復突變(體外)試驗結果;若試驗結果為陽性,還需提交關于染色體畸變(體外)、微核(體內)和基因突變或DNA損傷(體內)的測試結果,并且考慮代謝物的化學結構提交其他試驗結果。
3.5 中國農藥登記資料要求 我國農業農村部負責全國農藥監督管理,農業農村部農藥檢定所負責全國農藥登記具體工作。
我國農藥毒理學評估首先需通過評價動植物代謝試驗、田間殘留試驗、飼喂試驗、加工過程和環境行為等試驗結果,確定農藥主要代謝物,然后進行毒理學試驗,實現對農藥主要代謝物的毒理學評價。根據我國農藥登記資料要求[11],申請人需要提交急性經口毒性試驗、三項致突變試驗資料、亞慢性經口毒性試驗及其他毒理學試驗資料。其中急性毒性試驗是評估受試物毒性的基礎資料,用于經口毒性分級,以便初步了解毒性特征和可能的靶器官,并為進一步毒性試驗提供劑量依據;致突變試驗組合用于檢測受試物引起的遺傳損害;90天重復經口染毒試驗可提供多次接觸受試物后引起的健康損害效應,為健康閾值的制定提供初步依據。上述試驗目的、方法和檢測指標各不相同,反映代謝物不同方面的毒理學特征,不交叉、不重復、不可替代,以便對代謝物進行全面評估。
3.6 不同國家農藥登記資料要求對比分析 對比分析歐盟、美國、澳大利亞、日本等國的農藥代謝物評估程序,認為關注內容相似,包括急性毒性、致突變性(基因突變、染色體畸變)、一般毒性(重復染毒、單次染毒),在此基礎上可能還需要關注其他毒性(如致畸、遺傳毒性等)。此外,在進行代謝物毒理學測試前,均要求比較代謝物與母體化合物毒性,判斷是否可以被母體化合物毒性數據涵蓋,并引用母體化合物的參考劑量;需要評估殘留量/暴露量,根據暴露量高低,再決定是否開展進一步的毒性測試;另外,在評估過程中要求不同程度采用TTC、QSAR、Grouping和Read-across等評估工具進行預測和評估,為是否需要開展進一步毒性測試提供依據。但具體實現方式上各有特點:歐盟、美國等對農藥代謝物毒理學評估資料并不明確,企業在申請登記時需要專業技術支持來進行逐案分析。而澳大利亞、日本等國對農藥代謝物毒理學評估資料較為明確,但在科學性上有所欠缺(未強制要求重復染毒試驗等其他試驗),不利于對農藥品種的全面科學評價,因此企業根據評價需要增加了其他一些毒理學試驗項目,如日本曹達的四唑吡氨酯增加了亞慢性經口毒性試驗、日本石原的環丙蟲酰胺增加了亞急性經口毒性試驗。我國的農藥代謝物毒理學資料要求明確,制定過程經過廣泛調研和充分討論,滿足農藥登記管理要求,符合我國現階段情況,具有科學性、適用性和可操作性,且資料要求明確有效避免了企業走彎路的情況,得到了絕大多數國內外企業的肯定,遵從度較高。
4 對中國農藥代謝物評價的思考建議
4.1 加快推進我國農藥風險評估殘留物定義的制定 隨著農藥殘留評價和檢測技術的發展,以及農藥限量標準制定過程中風險評估技術的引入,農藥殘留物定義的重要性逐漸得到重視。然而,我國目前關于農藥殘留物定義的研究不夠深入。此外,在企業申請產品登記時,一般以母體化合物作為風險評估的殘留物定義,缺少農藥在動、植物體內的代謝數據,導致登記管理部門在對農藥有效成分進行風險評估時,一般直接根據其母體的毒理學數據以及參考我國的膳食攝入數據進行評估,因此有時會低估農藥的膳食暴露風險。我國可以參考JMPR及其他發達國家或國際組織所制定的農藥殘留物定義,以加快制定我國農藥殘留物定義,解決我國目前對于殘留物定義,尤其是膳食風險評估殘留物定義標準不統一的問題[5],以保障食品及農產品安全、規范市場秩序。
4.2 優化我國農藥代謝物毒理學評價程序 我國農藥毒理學資料要求明確,具有科學性、適用性和可操作性。然而,在執行過程中僅對經過殘留和環境專業評估后提出的主要代謝物開展毒理學評價工作,需要加強對具有毒理學意義的代謝物的界定與篩選。在評審程序上,可以建立代謝物評審決策樹,明確評審流程和相應標準;建立跨學科的“代謝物評價專家組”,對登記中遇到的代謝物評價問題進行磋商討論,根據不同產品特性進行相應篩查,采取逐案分析的機制,確定需要關注的農藥代謝物。
4.3 加強QSAR等工具軟件研發和計算毒理評估技術支撐體系建設 考慮到全球毒性測試資源有限,為了盡量減少毒理學測試中實驗動物的使用,考慮新的方法來評估代謝物的風險,并且根據可用信息,使用基于結構相關化合物的毒性數據比較分析的預測模型是有必要的。因此,國際上在評估過程中均不同程度地采用TTC、QSAR、Grouping和Read-across等工具進行預測和評估,但以上預測軟件存在一定比例的假陽性和假陰性,預測結果的不確定性可能導致安全管理風險,應用尚有爭議。我國目前尚無自行研制成熟的QSAR軟件,且QSAR等軟件的開發需要足夠數量的化合物數據、專業的建模理論、嚴謹的驗證程序以及專業的技術指導,因此,我們需要組建技術團隊,依據技術需求,建立計算機科學、信息學、化學、毒理學、數學等多學科專家組成的專業技術團隊,與有關單位合作,擬定數據篩選原則,開展化合物毒理學信息收集、分析,建立基礎數據庫,在各項研究基礎上,形成系統技術文件,建設計算毒理評估技術支撐體系。
5 總結
對農藥中具有毒理學意義的主要代謝物進行評價對保障生態安全與人類健康至關重要。目前,國際上發達國家和國際組織已針對不同種類的農藥制定了其在作物中的殘留物定義以及農藥代謝物評價程序和決策,且對TTC、QSAR、Grouping和Read-across等預測工具進行了不同程度的應用。然而,我國在農藥代謝物毒理學評價研究尚不深入,需要加快推進我國農藥風險評估殘留物定義的制定和毒理學評價程序的優化,并加強QSAR等工具軟件研發和計算毒理評估技術支撐體系建設,以促進我國農藥代謝物毒理學評價,加強對農藥的風險評估,從而改善農藥所帶來的健康風險和生態安全問題。

