高鈣攝入對大鼠血管鈣化的影響
張倩蓉,劉杰,秦鈺欣,楊曉斌,郭連瑩
(1. 沈陽醫學院公共衛生學院2019級衛生檢驗與檢疫專業,遼寧 沈陽 110034;2. 公共衛生學院營養與食品教研室)
我國逐漸進入老齡化社會,老年人群糖尿病、慢性腎病等慢性疾病患病率顯著上升。最近研究表明,血管鈣化作為上述慢性疾病的病理基礎,其主要表現為動脈血管壁彈性降低、順應性降低,易導致斑塊破裂而引發血栓的形成,這可能是導致上述人群死亡的重要原因[1]。同時,隨著年齡增長,人體內鈣大量流失,老年人普遍存在骨質疏松的現象[2-3]。朱潔云等[4]的一項針對中老年人骨質疏松患病率的Meta分析,納入48篇橫斷面研究,包含68932例研究對象。Meta分析結果顯示,中國老年人骨質疏松的患病率為37.7%,且患病率隨著年齡的增長逐漸上升,嚴重影響老年人的預期壽命及生活質量,成為致死、致殘的主要原因之一。鈣劑作為基本補充劑,對于骨質疏松的防治有著重要作用。為探究上述人群在防治骨質疏松補充鈣劑時對血管鈣化的影響,本實驗在給予大鼠維生素D和尼古丁誘導模擬老年人群血管鈣化情況,通過喂飼含鈣飼料增高血鈣濃度,探討高鈣攝入是否會加重血管鈣化,為老年人群合理補充鈣制劑提供理論依據。
1 材料與方法
1.1 實驗動物 SPF級雄性2月齡Wistar大鼠30只,體重約(180±10)g,由遼寧長生生物技術股份有限公司實驗中心提供(實驗動物許可證號SCXK(遼)2020-0002)。適應性喂養1周。本研究經學校倫理委員會批準,遵守動物福利原則。
1.2 主要試劑和儀器 尼古丁、維生素D3(美國Sigma公司);磷酸氫鈣(上海試四赫維化工有限公司)。鈣測定試劑盒(中生北控生物科技股份有限公司);7170A型全自動生化分析儀(日立公司);引物設計和RT-qPCR試劑盒由大連寶生物公司提供。
1.3 實驗方法
1.3.1 動物模型制備及實驗分組 將30只大鼠隨機分成3組,其中隨機抽取20只大鼠用于制備血管鈣化模型,10只大鼠作為陰性對照組。禁食12 h后,血管鈣化模型組按照300000 IU/kg維生素D3肌肉注射和尼古丁按25 mg/kg混入2 ml花生油中進行灌胃,10 h后再灌胃1次;陰性對照組肌肉注射等量的生理鹽水和2 ml花生油灌胃。將血管鈣化模型組的20只大鼠再隨機分為2組,每組10只。其中鈣化組和陰性對照組喂飼普通基礎飼料;鈣化+2.4%鈣組,喂飼含有2.4%鈣的飼料。飼養期間自由飲水,每天稱量進食量,定期稱量體重,溫度為(22±2)℃,濕度(55±5)%,共飼養12周。
1.3.2 大鼠血清中鈣濃度測定 按照1 g/kg腹腔注射20%烏拉坦麻醉大鼠,進行腹主動脈取血。血樣在37 ℃水浴鍋中沉淀20~30 min后,經3000 r/min離心15 min取上層血清,使用全自動生化分析儀測定血清中鈣濃度。
1.3.3 大鼠血管中鈣濃度測定 處死大鼠后,采集胸腹大動脈血管,烘干稱重,按照1∶9的比例加入生理鹽水,經研磨機打碎后,再經離心機3000 r/min離心15 min取上清液,使用全自動生化分析儀測定血管中鈣濃度。
1.3.4 血管組織Von Kossa染色 采集胸主動脈一段,多聚甲醛固定后進行Von Kossa染色。血管常規石蠟包埋、切片,脫蠟、脫水后浸入5%的硝酸銀溶液中,在37 ℃溫箱中染色30 min后用蒸餾水清洗3次,用5%的硫代硫酸鈉溶液定影處理,10 min后用1%堿性品紅復染2 min,再經95%酒精脫水、透明、封片后于光鏡下觀察。通過面積大小、血管斷裂的嚴重程度來判斷鈣化程度。
1.3.5 血管組織中基質Gla蛋白(matrix Gla protein,MGP)mRNA測定 用Trizol試劑提取大鼠血管組織中總mRNA,SYBR Green qPCR法進行逆轉錄和擴增。擴增反應條件為:95 ℃ 30 s ,循環2次,95 ℃ 5 s,循環40次,60 ℃ 30 s,循環40次。MGP引物序列:上游引物5'-CGCTACG CCCTGATCTACG-3',下游引物5'-GGAATATGAA ACCAGACTCCGTAAC-3';內參照GAPDH引物序列:上游引物5'-TGGTCTACATGTTCCAGTATGA CT-3',下游引物5'-CCATTTGATGTTAGCGGGAT CTC-3'。
1.4 統計學方法 采用SPSS 26.0軟件進行統計學分析,正態分布計量資料采用均數±標準差表示,組間比較采用單因素方差分析及SNK-q檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 各組大鼠體重情況 由于受造模的影響以及大鼠自身體質原因,實驗結束時鈣化組大鼠剩8只,鈣化+2.4%鈣組大鼠剩7只。實驗結束后3組大鼠體重比較差異無統計學意義(P>0.05),見圖1。
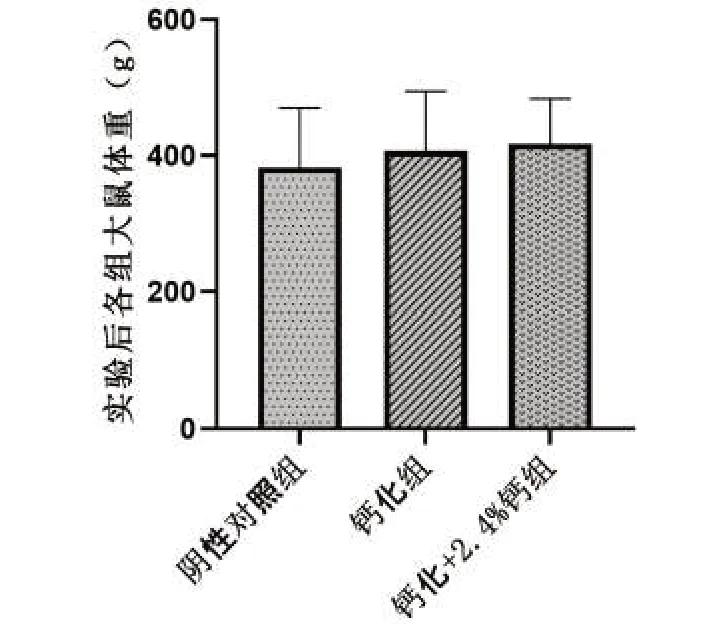
圖1 實驗結束后各組大鼠體重結果
2.2 大鼠血清和血管鈣含量測定結果 3組血清中鈣含量比較差異無統計學意義(P>0.05)。與陰性對照組比較,鈣化組和鈣化+2.4%鈣組血管鈣含量顯著升高(P<0.05),鈣化+2.4%鈣組血管鈣含量雖高于鈣化組,但差異無統計學意義(P>0.05)。見圖2。
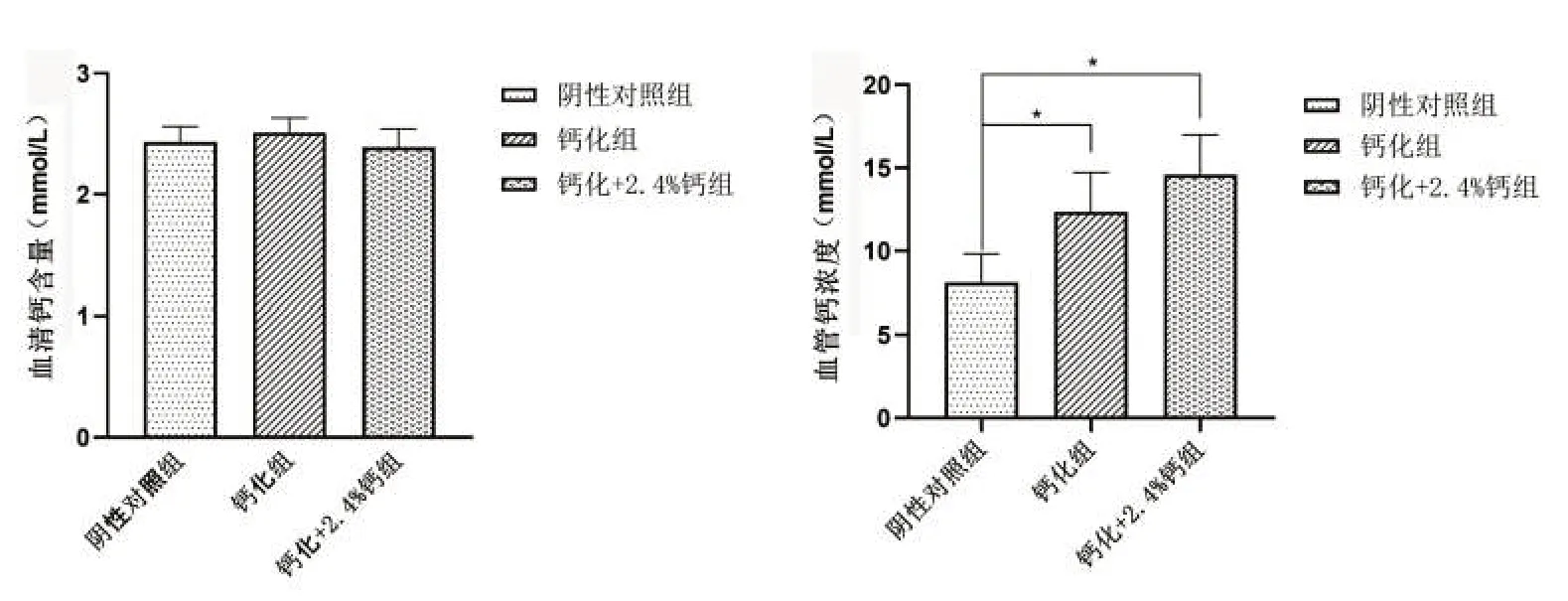
圖2 各組大鼠血清和血管鈣含量比較
2.3 大鼠胸主動脈血管Von Kossa染色結果 陰性對照組大鼠血管表面連續無明顯斷裂,無可見的斑塊,而鈣化組和鈣化+2.4%鈣組大鼠血管中不僅可見大量棕黃色斑塊,還有部分血管斷裂;與鈣化組相比,鈣化+2.4%鈣組大鼠血管中棕黃色鈣化結節明顯數量增多,面積也增大。見圖3。
2.4 大鼠胸主動脈血管MGPmRNA 表達量 鈣化組和鈣化+2.4%鈣組MGPmRNA的表達量顯著高于陰性對照組(P<0.05),鈣化組和鈣化+2.4%鈣組MGPmRNA的表達量比較差異無統計學意義(P>0.05)。見圖4。
3 討論
目前血管鈣化動物模型的制備方法有很多,如大劑量維生素D法、華法令法、基因敲除法、維生素D和尼古丁聯合法等,但各有優缺點[5]。本實驗采用了維生素D和尼古丁聯合法進行血管鈣化模型的制備,此法不但鈣化大鼠血漿鈣含量、心率、平均動脈壓無明顯影響[6],而且還可以模擬衰老、終末期腎病和糖尿病血管病變的大鼠血管鈣化模型[7]。本研究結果顯示鈣化模型組大鼠血管中鈣含量與陰性對照組比較顯著增加,血管Von Kossa染色呈現典型棕黃色鈣化結節,且與鈣化相關的MGPmRNA的表達也顯著升高[8],說明血管鈣化模型制備是成功的。
鈣是人體內含量最多的無機物,生理狀態下的主要是與磷結合存在于骨骼和牙齒中,但有研究表明如果血中鈣濃度過高,會導致鈣的異化沉積,如沉積在血管、肌肉等。王英等[9]研究表明,大鼠血管平滑肌細胞在高鈣(2.8 mmol/L)細胞培養基條件下出現鈣鹽沉積。吳勝英等[10]每天以1%(w/v)葡萄糖酸鈣飲水給予大鼠,與單純鈣化組比較,4周后血管45Ca2+沉積及堿性磷酸酶活性分別升高了38%(P<0.01)和15%(P<0.01),加重血管鈣化。但蘇克亮[11]研究結果與上述結果卻相反。蘇克亮通過建立糖尿病腎病大鼠模型,喂養高鈣飼料,結果顯示高鈣能減輕糖尿病腎病大鼠腎臟和血管組織鈣化程度。本研究鈣化+2.4%鈣組部分血管Von Kossa染色呈現出的棕黃色鈣化結節明顯比鈣化組數量增大,面積也有所增大,表明了鈣的攝入進一步加重了血管鈣化程度,但鈣化+2.4%鈣組血管中鈣的含量并沒有顯著高于鈣化組,與病理結果不一致。究其原因,其一可能是鈣的補充雖可能加重了鈣化進程,但還沒有達到顯著性水平,其二是病理結果也只是部分圖片顯示鈣補充加重了血管鈣化,而非全部圖片,所以導致病理結果與血管鈣含量結果不完全一致。另外,MGP作為一種重要的鈣化抑制蛋白,其血管中mRNA的表達往往與鈣化程度相一致,本研究中鈣化組和鈣化+2.4%鈣組MGPmRNA的表達均顯著高于陰性對照組,但二者之間差異無統計學意義,可能原因如上所述的鈣的補充雖有所加重鈣化進程,但遠還沒有達到顯著水平。
血清中的鈣含量與血管鈣化的關系還不肯定。部分研究表明血清中的鈣含量與血管鈣化程度相關[12-13],另一些研究表明血管鈣化與血鈣水平無關[14-15]。綜合目前已有研究報道認為在鈣化的初期由于機體抑制鈣化機制的存在,鈣無法大量異位沉積于血管中,所以血中鈣含量較高,而當鈣化防御機制衰竭時血中富集的鈣磷最終轉變為晶體型羥基磷灰石沉積于血管中,鈣化形成,導致血中鈣含量下降。另外機體本身也存著保持血鈣相對穩定的機制,所以血鈣水平可能無法很好地反映血管中鈣含量。Spiegel等[16]曾探討過高鈣或低鈣攝入對慢性腎病患者血中鈣平衡的影響,結果顯示即使患者每天攝入2000 mg鈣也沒有引起高鈣血癥,而在軟組織中發現了大量鈣沉積。余毅等[17]研究也發現透析患者血管鈣化的比例已很高,但血鈣還是正常的結果。本研究各組大鼠血清鈣含量接近,可能就是由于血鈣已大量沉積于血管中,也可能是機體自身的調節導致血清鈣含量無差異。
綜上所述,本實驗條件下,2.4%鈣的攝入可能會加重血管鈣化進程,確切的結論還需進一步驗證。

