牙鲆腸道益生菌的分離篩選及益生效果評價
王雪惠 王禎輝 董學旺 郝俊 耿緒云 孫金生

摘??? 要:為獲得安全有效的牙鲆益生菌,從牙鲆(Paralichthys olivaceus)腸道分離到94株菌,經溶血性、消化酶活力測試篩選出3株候選菌:Y1、Y5、I66,進行16S rDNA分子鑒定,分別為枯草芽孢桿菌(Bacillus subtilis)、解淀粉芽孢桿菌(Bacillus amyloidophilus)和蠟樣芽孢桿菌(Bacillus cereus)。經安全性檢驗后,開展為期4周的投喂試驗,分別將3株菌以1×108 CFU·g-1 添加到飼料中投喂牙鲆,為3個試驗組,同時設對照組(C),定期檢測各組魚血液先天免疫指標。結果發現,與對照組相比,試驗組魚淋巴細胞吞噬百分比顯著升高(P<0.05),血清堿性磷酸酶(AKP)和溶菌酶(LYZ)活性顯著升高(P<0.05),血清超氧化物歧化酶(SOD)活性極顯著升高(P<0.01)。投喂相應飼料4周,腹腔注射溶藻弧菌(Vibrio alginolyticus)攻毒,試驗組魚死亡延遲,累積死亡率顯著低于對照組(P<0.05)。綜上,Y1、Y5和I66是牙鲆安全有效的益生菌,能促進先天免疫,提高抗病力,具有推廣應用優勢和潛力。
關鍵詞:牙鲆;益生菌;酶活;先天免疫;抗病力
中圖分類號:S917.1???????? 文獻標識碼:A????????? DOI 編碼:10.3969/j.issn.1006-6500.2023.08.007
Isolation, Screening and Evaluation of Intestinal Probiotics from Paralichthys olivaceus
WANG Xuehui1, WANG Zhenhui2, DONG Xuewang3,? HAO Jun1,? GENG Xuyun1,? SUN Jinsheng4
(1. Tianjin Fisheries Research Institute, Tianjin 300221, China; 2. Tianjin Haifa Seafood Industrial Development Company Limited,Tianjin 300452, China; 3. Tianjin Animal Disease Prevention and Control Center, Tianjin 300402, China; 4. Tianjin Key Laboratory of Animal and Plant Resistance, College of Life Science, Tianjin Normal University, Tianjin 300387, China)
Abstract: To obtain safe and effective probiotics derived from flounder (Paralichthys olivaceus), 94 strains were collected from the intestine of flounder. 3 candidate probiotics were screened out by hemolysis and digestive enzyme activity assays. Bacillus subtilis (Y1), Bacillus amyloidophilus (Y5) and Bacillus cereus (I66) were identified by 16S rDNA molecular approach, respectively. After the safety inspection, a four-week feeding test was carried out. The 3 strains were added to the diet at 1×108 CFU·g-1, which were used as three experimental groups, and a control group (C) was set up. The blood innate immune indexes in each group were tested regularly. The results indicated that the phagocytosis percentage of lymphocytes, the activity of alkaline phosphatase (AKP) and lysozyme (LYZ) of probiotics groups were significantly higher (P<0.05) than those of the control group (C), and the serum superoxide dismutase (SOD) activity of probiotics groups was extremely significantly increased (P<0.01). After feeding corresponding diet for four weeks, each group subjects were injected to seroperitoneum with pathogenic Vibrio alginolyticus. The death of the probiotics group was delayed, and the cumulative mortality was significantly lower than that of the control group(P<0.05). In conclusion, Y1, Y5 and I66 are safe and effective probiotics for flounder, which can promote innate immunity and improve disease resistance, and have advantages and potential for popularization and application.
Key words: Paralichthys olivaceus; probiotics; enzyme activity; immunity; disease resistance
牙鲆屬鰈形目,繁殖力強,肉質鮮美,是我國重要的海水經濟品種之一。隨著集約化養殖規模的發展,由于養殖環境、養殖密度、餌料質量等因素的影響,疾病發生和流行在所難免[1],傳統的疾病治療方法以抗生素為主,但會對魚類和水生環境產生諸多不良影響,包括容易造成藥物殘留和抗性因子的傳遞,產生抗藥性病原菌等,給動物和人體健康帶來危害,還可通過細胞間遺傳物質的傳遞轉移給對人類健康有害的菌株[2]。而益生菌被視為綠色、健康、安全的抗生素替代品[3],受到研究人員和產業界的關注,益生菌是改善魚體健康的綠色添加劑,對宿主健康有積極作用且安全性更高,在魚類養殖中具有很大的潛力和前景[4-7]。益生菌的英文名“Probiotic”源于希臘語,本意是“為了生命”,聯合國糧農組織(FAO)和世界衛生組織(WHO)共同將其定義為:益生菌是一種“活的微生物,在給予足夠劑量時,對宿主的健康起有益作用”[8]。益生菌能分泌各種酶類,通過調節宿主腸道或周圍環境菌群,激活宿主免疫防御體系,或分泌拮抗物質與病原微生物競爭,從而對宿主產生有利作用[9]。Kozasa[10]1986年首次將益生菌應用到水產養殖中,此后水產益生菌的篩選和應用研究迅速發展,不論是在促進生長還是提高抗病力方面均取得良好效果[6-7,11-12],但也有使用效果不穩定的報道[13],一個重要的原因是菌株來自環境或恒溫動物。Verschuere等[14]和Ninawe等[15]學者認為,從水產動物自身或環境中分離的益生菌應用在水產養殖中效果會更佳。本研究從健康牙鲆苗種腸道分離細菌,對分離到的細菌通過潛在致病性檢驗和消化酶活性檢測篩選出候選益生菌,篩選到的候選菌株經安全性檢驗后,添加到飼料中投喂牙鲆,評價其對牙鲆苗種生長和免疫效果的影響,為自身來源益生菌的開發和應用提供數據支持。
1 材料與方法
1.1 牙鲆腸道菌的分離
試驗魚來自天津某鲆魚養殖場繁育的牙鲆苗種,健康無病,沒有投喂過抗生素或其他藥物,體長約8 cm,體質量15 g左右。用于分離牙鲆腸道菌的培養基為海水營養瓊脂(SNA)平板,具體分離方法:用50 mg·L-1魚用麻醉劑MS-222麻醉牙鲆10 min,于無菌條件下對試驗魚進行解剖,取腸道,去除內容物,用無菌生理鹽水沖洗3次,放到預冷的無菌玻璃勻漿器中,每0.1 g腸道加1 mL無菌生理鹽水勻漿,得勻漿原液。勻漿原液進行梯度稀釋,稀釋至10-5,分別取10-2、10-3、10-4、10-5 4個梯度的稀釋液0.1 mL均勻涂布于海水營養瓊脂(SNA)平板上,每個梯度做3個平行,25 ℃培養48 h以上。觀察各個平板的菌落數量、形態、顏色、大小。挑單菌落劃線純化2~3次,挑取單菌落保種備用。
1.2 牙鲆腸道菌的篩選
1.2.1 潛在致病性的檢測 將分離的腸道菌株用劃線法分別接種于血瓊脂平板(北京陸橋),25 ℃培養箱中培養24 h,根據菌落的溶血特征,篩選出不溶血的菌株。
1.2.2 產消化酶菌株的篩選 用于消化酶活性分析的培養基有酪蛋白培養基、脫脂乳培養基、淀粉培養基和油脂培養基,配制方法參照《微生物試驗》,分別用于篩選產酪蛋白酶、蛋白酶、淀粉酶,以及脂肪酶的菌株[16]。
1.2.3 產蛋白酶試驗 將分離到的不溶血菌株分別接種到海水營養肉湯中,25 ℃振蕩培養48 h,4 500 r·min-1離心20 min,留上清液用于產酶試驗。分別取受試菌上清0.1 mL加入到放置在酪蛋白培養基和脫脂乳培養基上的牛津杯中, 于25 ℃培養箱中培養24 h,觀察酪蛋白培養基上牛津杯周圍是否形成透明圈,脫脂乳培養基上牛津杯周圍是否形成溶蛋白圈,并測量透明圈和溶蛋白圈直徑,通過比較透明圈和溶蛋白圈直徑即可判斷菌株的產酶能力,透明圈和溶蛋白圈直徑越大,產酶能力越強。
1.2.4 產淀粉酶試驗 分別取受試菌上清0.1 mL加入到放置在淀粉培養基上的牛津杯中,于25 ℃培養箱中培養24 h。滴加少量碘液于培養基表面,輕輕旋轉,使碘液鋪滿整個平板。觀察并測量牛津杯周圍透明圈直徑。透明的水解圈區域顯示有酶活,通過比較水解圈直徑的數值來判斷菌株的產酶能力,透明圈直徑越大,產酶能力越強。
1.2.5 產脂肪酶試驗 將分離到不溶血的菌株用劃線法分別接種于油脂培養基上,于25 ℃培養箱中培養24 h,觀察菌落上是否有紅色斑點,有紅色斑點的是能產脂肪酶的菌株。油脂培養基中的中性紅在中性環境下呈黃色,在酸性環境下呈紅色。若菌株分泌脂肪酶,脂肪酶能將培養基中的油脂分解為脂肪酸,使中性紅變為紅色。
1.3 候選益生菌的安全性檢驗
以體質量為(22.3±2.2) g、體長為(11±1) cm、120尾的健康牙鲆苗種為試驗動物,檢驗篩選出的候選益生菌的安全性,試驗在天津市某養殖公司的養殖水箱里開展,養殖水箱與養殖車間封閉循環水系統相連,水交換量50%·h-1,養殖水溫21~ 22 ℃, 鹽度22~23,溶氧8~10 mg·L-1。試驗魚在養殖水箱里適應7 d,隨機分成4組,其中3組分別投喂添加候選益生菌的飼料,添加濃度為1×108 CFU·g-1具體方法是將細菌培養液按照體積質量比1∶40~1∶50(單位mL·g-1)拌到飼料中,另外1組為對照組,投喂牙鲆基礎飼料,連續投喂7 d,分別統計各組牙鲆苗種的成活率,并于無菌條件下解剖肝、脾、腎,用1 mL無菌生理鹽水制成組織勻漿,涂布在SNA瓊脂平板上,看是否能分離到細菌,只有沒有長出細菌,才能說明益生菌安全。
1.4 候選益生菌的鑒定
采用16S rDNA序列分析方法,對分離篩選到的3株候選益生菌進行鑒定。用細菌16S rDNA通用引物,擴增3株菌的16S rDNA片段,委托生工生物工程(上海)股份有限公司測序,序列在GenBank數據庫中進行比對(http://blast.ncbi.nlm.nih.gov/Blast.cgi)。
1.5 應用效果評價
1.5.1 應用試驗設計 經檢驗安全的3株候選益生菌,開展牙鲆應用試驗。將3株菌分別接種在海水營養肉湯中,25 ℃振蕩培養48 h,將細菌培養液按照體積質量比1∶40~1∶50(單位mL·g-1)拌到牙鲆基礎飼料中,即得濃度為1×108 CFU·g-1的益生菌飼料,基礎飼料為天津某飼料公司生產的牙鲆苗種飼料。
試驗魚為體長在9~11 cm的牙鲆健康苗種280尾,試驗條件同1.3。試驗魚在養殖水箱適應7 d,待攝食正常后,隨機分成4組:3個試驗組,1個對照組,每組隨機取20尾魚稱量體質量,計算初均質量。試驗組分別投喂添加了不同候選益生菌的飼料,對照組投喂基礎飼料,日投喂量為魚體總重量的1.5%~2%。應用試驗為期4周。
于投喂相應飼料前及投喂飼料4周后,每組隨機取20尾魚稱量體質量,計算末均質量,用于生長指標的分析。于投喂飼料后1、2、3、4周,試驗組和對照組每組隨機取5尾魚,尾靜脈采血,采用兩種方式采血:一種直接采集,用于收集血清,檢測血液酶活;另一種采集抗凝血,用≥6 μL的肝素(30 U可抗凝1 mL血)溶液潤濕的1 mL一次性注射器尾部取血200 μL,放到提前加了200 μL無菌生理鹽水和200 μL M199培養基的1.5 mL離心管中,輕輕混勻,用于檢測外周血細胞吞噬活性。
1.5.2 生長指標分析 根據試驗前、投喂飼料4周的魚體質量數據,分別計算每組初均質量、末均質量、平均增質量、增質量率、特定生長率,計算公式如下:
平均體質量=每組總質量/每組總尾數(1)
平均增質量=(末均質量-初均質量)/尾數(2)
增質量率=(末均質量-初均質量)/初均質量×100%(3)
特定生長率(%·t-1)=(ln w2-ln w1) ·t-1×100%(4)
式中,w1為初均質量,w2為末均質量,t為飼養時間。
1.5.3 細胞吞噬活性測定 取用于檢測外周血細胞吞噬活性的血—生理鹽水—培養基混合液100 μL,加入70 μL無菌生理鹽水和30 μL滅活的金黃色葡萄球菌懸液,混勻,25 ℃,200 r·min孵育30 min。取孵育好的血-菌混合液涂片,每個樣品涂片3張。用劉氏A液染色30 s,再加劉氏B液染色90~120 s,水洗,干燥,鏡檢。分別記錄100個細胞中參與吞噬的細胞個數(吞噬百分率PP)和每個細胞吞噬細菌的個數(吞噬指數PI)。
吞噬百分率(PP)=(100個細胞中參與吞噬的細胞數/100)×100%(5)
吞噬指數(PI)=被吞噬的細菌數/吞噬細菌的細胞數(6)
1.5.4 血液酶活的測定 抽取的血液樣品4 ℃過夜,3 000 r·min-1離心10 min,取血清。用南京建成試劑盒檢測堿性磷酸酶(AKP)、酸性磷酸酶(ACP)、超氧化物歧化酶(SOD)和溶菌酶(LYZ)活性,24 h內測定完畢,依據試劑盒說明進行酶活力計算。
1.6 攻毒試驗
投喂相應飼料4周后,3個試驗組和1個對照組各取20尾魚,每組設2個平行組,用本實驗室保存的牙鲆致病菌——溶藻弧菌(3×107 CFU·mL-1)攻毒,腹腔注射50 μL·尾-1,每天記錄各組的死亡數,統計2周時間,計算累計死亡率。
1.7 數據統計
數據分析采用單因素方差分析(One—Way ANOVA),并進行t檢驗,與對照組比較,P<0.05為差異顯著,P<0.01為差異極顯著。
2 結果與分析
2.1 篩選到3株候選益生菌
從健康牙鲆腸道分離到94株菌,其中不完全溶血(α溶血)43株,完全溶血(β溶血)25株,不溶血(γ溶血)26株。將26株不溶血菌株進行酪蛋白酶、蛋白酶、淀粉酶、脂肪酶活性檢測,其中8株具有酪蛋白酶活性,8株具有蛋白酶活性,12株具有淀粉酶活性,6株具有脂肪酶活性,兼具3種酶活性的菌株有3株:Y1、Y5和I66。牛津杯直徑為8 mm,3株菌的酪蛋白圈直徑、溶蛋白圈直徑、淀粉酶直徑、脂肪酶活性詳見表1。這3株菌不溶血,即沒有潛在致病性,具有多種消化酶活性,傳代穩定性好,被確定為益生菌候選菌株。
2.2 候選益生菌的安全性
投喂添加3株候選益生菌飼料1周,牙鲆苗種進食與活力正常,成活率均為100%。這說明3株菌以高劑量添加到飼料中投喂牙鲆,對魚體也是安全無危害的。用SNA瓊脂均未從各組魚的肝、脾、腎分離到細菌,說明試驗過程中未發生細菌位移。細菌位移是益生菌是否具有毒性的潛在標志,益生菌應用于養殖生產前評價其是否有細菌位移的風險十分必要[17]。試驗中菌株未遷移到肝、脾或腎,是牙鲆安全的候選益生菌,可以開展養殖試驗。
2.3 候選益生菌的分子生物學鑒定
綜合溶血性、消化酶活性和安全性試驗結果,對篩選出的3株候選益生菌進行16S rDNA測序,將測得菌株的16S rDNA 序列在GenBank中進行blast序列比對,比對結果顯示,3株菌均為芽孢桿菌屬,Y1與枯草芽孢桿菌(Bacillus subtilis)、Y5與解淀粉芽孢桿菌(Bacillus amyloidophilus)、I66與蠟樣芽孢桿菌(Bacillus cereus)的同源性均達99%以上。
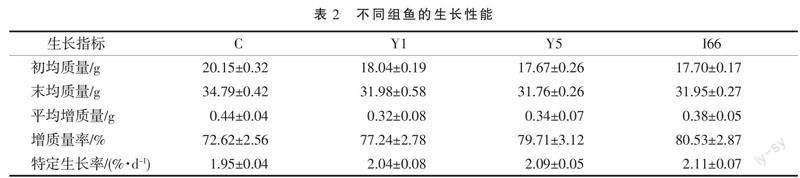
2.4 生長性能
分析了3株候選益生菌添加到飼料中投喂牙鲆4周對生長性能的影響(表2)。投喂添加候選益生菌組和投喂基礎飼料組牙鲆的末均質量、平均增質量、增質量率,以及特定生長率均未見顯著差異,說明添加的候選益生菌未能顯著促進魚體的生長,但也不會延緩魚體生長;添加候選益生菌組的增質量率和特定生長率高于對照組,雖然統計學上沒有呈現顯著性差異,但有增高的趨勢。
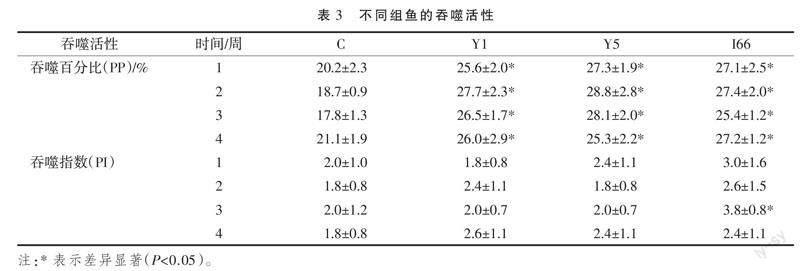
2.5 細胞吞噬活性
試驗組和對照組分別于投喂相應飼料后1、2、3、4周,尾靜脈采血,統計分析外周血細胞PP和PI,對照組4個時間點PI在(17.8±1.3)%~(21.1±1.9)%之間,P2在(1.8±0.8)~(2.0±1.2)之間。3個試驗組4個時間點血細胞PP顯著高于對照組,在(25.3±2.2)%~(28.8±2.8)%之間;投喂添加I66飼料3周時,血細胞PI顯著高于對照組,為3.8±0.8;其他試驗組血細胞PI與對照組不存在顯著性差異(表3)。
2.6 血液酶活指標
3個試驗組和1個對照組分別在投喂相應飼料1、2、3、4周時檢測血液酶活。血液AKP活性隨著魚體生長呈上升趨勢,于投喂4周時,3個試驗組AKP活性顯著高于對照組;血液ACP活性水平不隨魚體生長而發生變化,3個試驗組與對照組的ACP活力水平均一致,不存在顯著性差異;3個試驗組血液SOD活性隨著魚體生長而升高,于3周時達到最高水平,與對照組形成極顯著差異,4周時有所下降,但仍然顯著高于對照組;3個試驗組血液LYZ活性于投喂1周時即顯著升高,且與對照組一直存在顯著性差異(表4)。
2.7 攻毒試驗
為評價飼料中添加候選益生菌對牙鲆抗病力的影響,開展攻毒試驗,記錄攻毒后試驗組和對照組的死亡數,計算累計死亡率(圖1)。攻毒后2 d,對照組即開始死亡,而試驗組在攻毒10 d才開始出現死亡現象;隨著時間的推移,到攻毒14 d時,對照組累計死亡率達到50%,而各試驗組的累計死亡率在17.5%~30%范圍內,顯著低于對照組(P<0.05)。由此可見,飼料中添加Y1、Y5和I66菌均能提高牙鲆對溶藻弧菌的抵抗力,延緩發病,降低死亡率。
3 討論與結論
隨著健康養殖理念的不斷深入和對食品安全性要求的不斷提高,由抗生素導致的食品安全、生物和生態問題,特別是抗生素耐藥性菌株的出現[18-19],使抗生素的使用受到嚴格管控,亟待尋找抗生素的替代品。益生菌是一類在微生態學理論指導下,經特殊工藝制成的含活菌或者包含細菌菌體及其代謝產物的活菌制劑,對宿主具有益生作用[20]。研究表明,益生菌的益生作用主要表現在促進機體生長、提高機體免疫力、改善腸道菌群平衡等[21-22],在水產養殖中還能改善養殖水體水質,具有綠色、無污染的特點,符合水產養殖業可持續發展戰略,可以替代化學藥品和抗生素在水產養殖中使用,保護養殖對象免受疾病危害[23];但益生菌的來源、使用量和投喂期等因素會影響益生菌的免疫調節活性[24-25],導致益生菌開發的復雜性和使用效果的不穩定性等;目前水產上使用的益生菌主要來自陸生動物[4],而對人類和陸生動物安全的益生菌可能對水生動物并不安全[26-27]。研究表明,益生菌在發揮作用時存在種屬差異性和菌株特異性,宿主來源的益生菌在諸如溫度、鹽度、對生存環境的熟悉程度、對宿主的免疫條件等方面具有優勢,具有巨大的開發潛力[5,18];Carnevali等[28]發現,從魚類腸道中選擇的益生菌可能具有更強的與本地有害微生物競爭、在腸道環境中占據主導地位的能力;而不合適的益生菌會對宿主的營養物質代謝、免疫調節等產生負面影響[5,29]。由此可見,應用于水生動物的益生菌必須考慮菌種來源問題,胃腸道(GIT)和黏液是水產養殖益生菌最常見的分離來源[5,25,30-32]。因此,本研究從健康養殖牙鲆苗種腸道進行細菌分離,通過產酶試驗和安全性試驗篩選出3株牙鲆腸道固有候選益生菌,并應用于牙鲆苗種養殖試驗,避免益生菌應用時出現種屬特異性,利于候選益生菌更好的在腸道黏附或定殖,發揮促進生長或提高免疫力等益生作用。
水產養殖中,益生菌主要通過酶促消化、促進生長、增強宿主免疫力等方面發揮益生作用[33]。本研究將篩選出的兼具3種消化酶活性的候選益生菌(Y1、Y5和I66)分別添加到基礎飼料中投喂牙鲆,以期促進牙鲆對飼料營養成分的消化吸收,提高牙鲆生長速率。經過4周的養殖試驗,發現添加益生菌組牙鲆未在生長性能方面顯現優勢,但益生菌組的增質量率和特定生長率高于對照組,即使統計學上沒有顯現顯著性差異,但均有增高的趨勢。類似的結果也有報道,Sun等[34]研究了快速生長的石斑魚腸道優勢菌——短小芽孢桿菌和克勞氏芽孢桿菌分別以1.0×108 cells·g-1的濃度添加到飼料中投喂石斑魚60 d,益生菌飼養組的體質量增加和特定生長速度沒有明顯的改善,推測可能與投喂時間或投喂劑量有一定關系。
益生菌應用最大的益處之一就是調節宿主免疫[35]。本研究通過定期檢測外周血細胞吞噬活性、血液酶活(AKP、ACP、SOD、LYZ)等非特性免疫指標來評價益生菌在增強魚體免疫力方面的作用。吞噬活性出現在魚類先天免疫應答的早期,對機體抵抗細菌入侵起著重要作用;AKP和ACP是動物體內參與免疫防御的重要水解酶;SOD是機體內一種重要的抗氧化酶,主要是清除動物體液或組織中的超氧基,在防御細胞組織超氧陰離子毒性、生物分子損傷方面具有重要的作用[36];LYZ是存在于溶酶體內的水解酶,是魚類先天免疫系統重要的防御分子,是抵御病原微生物入侵的屏障[37]。目前也有不少關于益生菌調節水產動物先天免疫方面的報道,Newaj-Fyzul等[38]研究發現,枯草芽孢桿菌(Bacillus subtilis)能提高虹鱒魚的免疫反應包括白細胞數量顯著增加、呼吸爆發和吞噬活性增強等,亦能提高虹鱒對致病性嗜水氣單胞(Aeromonas hydrophila)的抵抗力;高肖微等[39]研究發現,將地衣芽孢桿菌(Bacillus licheni-formis)以不同劑量添加到飼料中投喂鯉魚,投喂20、40、60 d,均能顯著提高鯉魚SOD活性(P<0.05),投喂40、60 d,能顯著提高溶菌酶(LYZ)活性,且隨著地衣芽孢桿菌(Bacillus licheniformis)添加量的增加,鯉魚免疫機能不同程度顯著提高(P<0.05);Amoah等[40]在飼料中添加凝結芽孢桿菌(Bacillus coagulans)投喂凡納濱對蝦,發現血清溶菌酶(LYZ)、酸性磷酸酶(ACP)、超氧化物歧化酶(SOD)活力等先天免疫指標顯著提高,且對副溶血弧菌(Vibrio Parahaemolyticus)的抗感染力增強;Taoka等[41]用含有枯草芽孢桿菌(Bacillus subtilis)、嗜酸乳桿菌(Lactobacillus? acidophilus)、丁酸梭菌(Clostridium butyricum)和釀酒酵母(Saccharomyces? cerevisiae)益生菌產品添加到飼料中投喂牙鲆,牙鲆體表黏液和血漿中的溶菌酶活性均高于對照組[41]。本研究也取得類似結果,3個試驗組4個時間點血淋巴細胞PP顯著高于對照組;3個試驗組AKP、SOD和LYZ的活力顯著或極顯著的高于對照組;投喂30 d后用牙鲆致病菌進行攻毒,3個試驗組魚發病延遲,累計死亡率顯著低于對照組。以上均說明,益生菌候選菌株Y1、Y5、I66的添加,促進了牙鲆血液外周血細胞的吞噬活性,提高了牙鲆的先天免疫水平,增強了魚體的抗病力。
這3株菌經鑒定分別為:枯草芽孢桿菌(Y1)、解淀粉芽孢桿菌(Y5)和蠟樣芽孢桿菌(I66)。芽孢桿菌是水產養殖行業應用廣泛的一類益生菌,因其具有易保存、抗逆行能力強等特點,在水產養殖上有許多應用的實例[14,40,42-43]。本研究篩選出的3株菌,均有分泌消化酶的活力,以往的研究結表明,飼料中添加具有分泌消化酶活性的益生菌能補充魚體腸道消化酶不足的缺陷,促進飼料的消化吸收,提高餌料利用率,促進魚體生長,但本研究未獲得同樣的結果,僅增質量率和特定生長率有增高的趨勢,原因可能是投喂時間較短,不足以顯現顯著性差異。本試驗條件下,Y1、Y5、I66這3株菌添加到飼料中投喂牙鲆,能顯著增強牙鲆外周血細胞吞噬活性、血液堿性磷酸酶、超氧化物歧化酶和溶菌酶活性;提高牙鲆對溶藻弧菌的抵抗力,是牙鲆有效益生菌,可以在牙鲆苗種生產中應用。為了達到更好的效果,后期可以開展最佳添加劑量、最佳投喂期的優化試驗,從而確定這3株益生菌的最佳應用方案。
參考文獻:
[1] 趙志濤, 石磊, 王文娟, 等. 益生菌、益生元和合生元預防魚類弧菌病應用的研究進展[J]. 飼料研究, 2022, 45(16): 115-119.
[2] GOMEZ-GIL B, ROQUE A, TURNBULL J F. The use and selection of probiotic bacteria for use in the culture of larval aquatic organisms[J]. Aquaculture, 2000, 191(1/3): 259-270.
[3] HE T F, LONG S F, MAHFUZ S, et al. Effects of probiotics as antibiotics substitutes on growth performance, serum biochemical parameters, intestinal morphology, and barrier function of broilers[J]. Animals, 2019, 9(11): 985.
[4] IRIANTO A, AUSTIN B. Probiotics in aquaculture[J]. Journal of Fish Diseases, 2002, 25(11): 633-642.
[5] LAZADO C C, CAIPANG C M A, ESTANTE E G. Prospects of host-associated microorganisms in fish and penaeids as probiotics with immunomodulatory functions[J]. Fish & Shellfish Immunology, 2015, 45(1): 2-12.
[6] MENG D L, HAO Q, ZHANG Q S, et al. A compound of paraprobiotic and postbiotic derived from autochthonous microorganisms improved growth performance, epidermal mucus, liver and gut health and gut microbiota of common carp (Cyprinus carpio)[J]. Aquaculture, 2023, 570: 739378.
[7] SHARIFUZZAMAN S M, AUSTIN B. Influence of probiotic feeding duration on disease resistance and immune parameters in rainbow trout[J]. Fish & Shellfish Immunology, 2009, 27(3): 440-445.
[8] SANDERS M E. How do we know when something called “Probiotic” is really a probiotic? A guideline for consumers and health care professionals[J]. Functional Food Reviews, 2009, 1(1): 3-12.
[9] G?譫MEZ G D, BALC?魣ZAR J L. A review on the interactions between gut microbiota and innate immunity of fish[J]. FEMS Immunology and Medical Microbiology, 2008, 52(2): 145-154.
[10] KOZASA M. Toyocerin (Bacillus toyoi) as growth promotor for animal feeding[J]. Microbiologie Aliments Nutrition, 1986, 4(1): 121-135.
[11] 何偉聰, 董曉慧, 譚北平, 等. 益生菌對軍曹魚幼魚生長性能、消化酶和免疫酶活性的影響[J]. 動物營養學報, 2015, 27(12): 3821-3830.
[12] FERNANDES S, KERKAR S, LEITAO J, et al. Probiotic role of salt Pan bacteria in enhancing the growth of whiteleg shrimp, Litopenaeus vannamei[J]. Probiotics and Antimicrobial Proteins, 2019, 11(4): 1309-1323.
[13] NIKOSKELAINEN S, OUWEHAND A C, BYLUND G, et al. Immune enhancement in rainbow trout (Oncorhynchus mykiss) by potential probiotic bacteria (Lactobacillus rhamnosus)[J]. Fish & Shellfish Immunology, 2003, 15(5): 443-452.
[14] VERSCHUERE L, ROMBAUT G, SORGELOOS P, et al. Probiotic bacteria as biological control agents in aquaculture[J]. Microbiology and Molecular Biology Reviews, 2000, 64(4): 655-671.
[15] NINAWE A S, SELVIN J. Probiotics in shrimp aquaculture: avenues and challenges[J]. Critical Reviews in Microbiology, 2009, 35(1): 43-66.
[16] 沈萍, 陳向東. 微生物學實驗[M]. 5版. 北京: 高等教育出版社, 2018: 216-217.
[17] STEFFEN E K, BERG R D. Relationship between cecal population levels of indigenous bacteria and translocation to the mesenteric lymph nodes[J]. Infection and Immunity, 1983, 39(3): 1252-1259.
[18] ZORRIEHZAHRA M J, DELSHAD S T, ADEL M, et al. Probiotics as beneficial microbes in aquaculture: an update on their multiple modes of action: a review[J]. Veterinary Quarterly, 2016, 36(4): 228-241.
[19] SCHWARZ S, KEHRENBERG C, WALSH T R. Use of antimicrobial agents in veterinary medicine and food animal production[J]. International Journal of Antimicrobial Agents, 2001, 17(6): 431-437.
[20] MARTEAU P R. Probiotics in clinical conditions[J]. Clinical Reviews in Allergy & Immunology, 2002, 22(3): 255-273.
[21] FAO, WHO. Health and nutritional properties of probiotics in food including powder milk with live lactic acid bacteria[R]. Córdoba: FAO, 2001.
[22] JAVADI A, KHATIBI S A. Effect of commercial probiotic (Protexin R) on growth, survival and microbial quality of shrimp (Litopenaeus vannamei)[J]. Nutrition and Food Science, 2017, 47(2): 204-216.
[23] BANDYOPADHYAY P, MISHRA S, SARKAR B, et al. Dietary Saccharomyces cerevisiae boosts growth and immunity of IMC Labeo rohita (Ham.) juveniles[J]. Indian Journal of Microbiology, 2015, 55(1): 81-87.
[24] DAWOOD MAO, KOSHIO S, ISHIKAWA M, et al. Interaction effects of dietary supplementation of heat-killed Lactobacillus plantarum and β-glucan on growth performance, digestibility and immune response of juvenile red sea bream, Pagrus major[J]. Fish & Shellfish Immunology, 2015, 45(1): 33-42.
[25] HAI N V. Research findings from the use of probiotics in tilapia aquaculture: a review[J]. Fish & Shellfish Immunology, 2015, 45(2): 592-597.
[26] WANG A R, RAN C, WANG Y B, et al. Use of probiotics in aquaculture of China-a review of the past decade[J]. Fish & Shellfish Immunology, 2019, 86: 734-755.
[27] RAN C. Isolation and characterization of Bacillus spp. as potential probiotics for channel catfish, Ictalurus punctatus[D]. Auburn: Auburn University, 2013.
[28] ZORRIEHZAHRA M J, DELSHAD S T, ADEL M, et al. Probiotics as beneficial microbes in aquaculture: an update on their multiple modes of action: a review[J]. Veterinary Quarterly, 2016, 36(4): 228-241.
[28] CARNEVALI O, ZAMPONI M C, SULPIZIO R, et al. Administration of probiotic strain to improve sea bream wellness during development[J]. Aquaculture International, 2004, 12(4): 377-386.
[29] BURR G, GATLIN D III, RICKE S. Microbial ecology of the gastrointestinal tract of fish and the potential application of prebiotics and probiotics in finfish aquaculture[J]. Journal of the World Aquaculture Society, 2005, 36(4): 425-436.
[30] HAI N V. The use of probiotics in aquaculture[J]. Journal of Applied Microbiology, 2015, 119(4): 917-935.
[31] WU Z Q, JIANG C, LING F, et al. Effects of dietary supplementation of intestinal autochthonous bacteria on the innate immunity and disease resistance of grass carp (Ctenopharyngodon idellus)[J]. Aquaculture, 2015, 438: 105-114.
[32] TAPIA-PANIAGUA S T, D?魱AZ-ROSALES P, LE?N-RUBIO JM, et al. Use of the probiotic Shewanella putrefaciens Pdp11 on the culture of Senegalese sole (Solea senegalensis, Kaup 1858) and gilthead seabream (Sparus aurata L.)[J]. Aquaculture International, 2012, 20(6): 1025-1039.
[33] GIRI S S, SUKUMARAN V, OVIYA M. Potential probiotic Lactobacillus plantarum VSG3 improves the growth, immunity, and disease resistance of tropical freshwater fish, Labeo rohita[J]. Fish & Shellfish Immunology, 2013, 34(2): 660-666.
[34] SUN Y Z, YANG H L, MA R L, et al. Probiotic applications of two dominant gut Bacillus strains with antagonistic activity improved the growth performance and immune responses of grouper Epinephelus coioides[J]. Fish & Shellfish Immunology, 2010, 29(5): 803-809.
[35] NAYAK S K. Probiotics and immunity: a fish perspective[J]. Fish & Shellfish Immunology, 2010, 29(1): 2-14.
[36] 李敬璽, 劉繼蘭, 王選年, 等. 超氧化物歧化酶研究和應用進展[J]. 動物醫學進展, 2007, 28(7): 70-75.
[37] SAURABH S, SAHOO P K. Lysozyme: an important defence molecule of fish innate immune system[J]. Aquaculture Research, 2008, 39(3): 223-239.
[38] NEWAJ-FYZUL A, ADESIYUN A A, MUTANI A, et al. Bacillus subtilis AB1 controls Aeromonas infection in rainbow trout(Oncorhynchus mykiss, Walbaum)[J]. Journal of Applied Microbiology, 2007, 103(5): 1699-1706.
[39] 高肖微, 齊遵利, 張秀文. 飼料中添加地衣芽孢桿菌對鯉魚生長性能及非特異性免疫功能的影響[J]. 飼料工業, 2016, 37(8): 16-19.
[40] AMOAH K, HUANG Q C, TAN B P, et al. Dietary supplementation of probiotic Bacillus coagulans ATCC 7050, improves the growth performance, intestinal morphology, microflora, immune response, and disease confrontation of Pacific white shrimp, Litopenaeus vannamei[J]. Fish & Shellfish Immunology, 2019, 87: 796-808.
[41] TAOKA Y, MAEDA H, JO J Y, et al. Growth, stress tolerance and non-specific immune response of Japanese flounder Paralichthys olivaceus to probiotics in a closed recirculating system[J]. Fisheries Science, 2006, 72(2): 310-321.
[42] HONG H A, DUC L H, CUTTING S M. The use of bacterial spore formers as probiotics[J]. FEMS Microbiology Reviews, 2005, 29(4): 813-835.
[43] SELIM K M, REDA R M. Improvement of immunity and disease resistance in the Nile tilapia, Oreochromis niloticus, by dietary supplementation with Bacillus amyloliquefaciens[J]. Fish & Shellfish Immunology, 2015, 44(2): 496-503.
收稿日期:2023-04-12
基金項目:天津科技大學省部共建食品營養與安全國家重點實驗室開放課題資助項目(SKLFNS-KF-202106);國家重點研發計劃資助(2020YFD0900400)
作者簡介:王雪惠(1979—),女,山東煙臺人,高級工程師,碩士,主要從事魚類病害及免疫防治技術研究。
通訊作者簡介:孫金生(1965—),男,天津人,研究員,博士,主要從事水產動物疾病控制等方面研究。

