鈦白粉副產硫酸亞鐵除雜工藝綜述
馬 航,查坐統,2,顧小玉,萬邦隆,2
(1.云南云天化股份有限公司 研發中心,云南 昆明 650228;2.西安交通大學,陜西 西安 710049)
0 引言
新型儲能材料作為替代能源已成為社會關注和研究的熱點。鋰電池具備優異的電化學性能,因其具有電容量大、充放電性能好、記憶效應較小、使用壽命長等優點,在動力電池和儲能材料領域,占據重要地位。其中,成本低、結構穩定以及安全性好的磷酸鐵鋰作為應用前景較好的鋰電池正極材料而逐漸受到重視,市場前景廣闊[1]。
磷酸鐵被認為是精細化工所需的最重要材料之一,在多個領域都得到了廣泛應用,如電池電極[2]、催化劑、陶瓷[3]、農業蟲害防治[4]等,現階段磷酸鐵應用最多的是用作制備鋰離子電池正極材料的原料[5]。目前已報道關于磷酸鐵制備的方法有:液相沉淀法、水熱法[6]、溶膠-凝膠法和自定義模板法[7]等,其中主流工藝為液相沉淀法,各方法主要以鐵源(如鐵粉、硫酸亞鐵、硝酸鐵等)和磷源(如磷酸銨、磷酸鈉、磷酸等)為原料在一定條件下合成磷酸鐵[8]。應用于鋰電池正極材料的磷酸鐵制備需要的條件更加嚴格,其中對產品的結晶水、鐵磷比、粒徑、雜質含量等都有著極其嚴格的要求,其性能強弱和上述幾項指標密切相關[9]。因此,其對制備工藝和原料的要求也更加嚴格。
目前我國主要以硫酸法生產鈦白粉,每生產鈦白粉1 t副產硫酸亞鐵3.5~4.0 t[10]。鈦白粉副產硫酸亞鐵是一種價格低廉的含鐵化合物,以此為鐵源可以生產多種附加值較高的含鐵化學品,具有較好的經濟效應和環境友好性。2018 年之前,受制于磷酸鐵低迷的市場行情,硫酸亞鐵一度被當作廢品處置,浪費資源且嚴重污染環境。近年來,隨著磷酸鐵市場行情好轉和需求量增加,硫酸亞鐵開始逐漸作為重要的原料受到越來越多磷酸鐵生產企業的青睞。使用鈦白粉副產物硫酸亞鐵來制備磷酸鐵鋰電池正極材料,既可以減少生產所需原材料的成本,又可以為硫酸亞鐵提供再次利用的價值。但因其含有鈦、鎂、錳、鋁等多種雜質,會直接影響制備電池級磷酸鐵產品的質量,因此在其作為合成磷酸鐵的原料之前,需對其進行除雜處理。
1 鈦白粉副產硫酸亞鐵的凈化除雜
目前,國內外對鈦白粉加工過程中產生的副產品硫酸亞鐵去除雜質方法的研究成果有很多。水解法是借助水解反應的方法去除硫酸亞鐵溶液里的鋁和鈦等雜質;化學沉淀法是加入帶有特殊離子的試劑,如硫化鈉、硫化鋇等生成沉淀除雜;重結晶法是將所需產物溶于水后,通過多次快速降溫,根據各種雜質中相關物質溶解程度的差異性,達到把多種雜質的離子去除的目的;膠體沉淀吸附法是通過調節溶液,生成膠體,通過膠體吸附金屬離子,再過濾分離從而除去雜質離子,比如加入磷酸、氨水或者鐵粉等pH 調節劑;絮凝共沉法是在相關的溶液中形成一種新的沉淀物,然后添加一種絮凝劑,并利用其絮凝作用將雜質中不需要的離子去除。
1.1 水解法
水解法主要是用于去除硫酸亞鐵溶液里面的鈦元素雜質。酸解過程中生成的硫酸氧鈦作為鈦白粉副產物中主要雜質鈦,在一定溫度下水解可生成不溶于水的沉淀,反應如式(1):
孟素芬[11]用水溶解適量副產硫酸亞鐵,加硫化鈉除錳后過濾去除固體濾渣,在一定的溫度、時間和pH 條件下,對濾液做水解處理,會出現沉淀。研究結果表明,此方法對濾液中鋁離子和鈦離子的去除率分別為95.5%和95.7%,而對濾液中Mn的去除率只有28.4%。說明用水解法可以將硫酸亞鐵中的鋁、鈦離子去除效果理想,但對Mg、Mn離子的去除效果并不明顯。由于硫酸亞鐵會被大氣中的氣體氧化,生成氫氧化鐵,過濾過程易發生堵塞,導致操作比較困難,因此需要控制過程中的氧化問題[12]。
1.2 化學沉淀法
化學沉淀法是將鈦白粉副產物中的雜質金屬離子以沉淀的方法析出,從而降低溶液中雜質離子濃度,經過濾得到凈化的硫酸亞鐵溶液。硫化物、液體螯合樹脂等均可以用作沉淀劑,促進生成金屬離子沉淀。主要的反應機制如下:
由溶度積原理可知,溶液中物質AmBn達到溶解和沉淀平衡時的Qi,稱為溶解平衡常數Ksp。在加入沉淀劑A或者B后,Qi會隨之正比例增大,通過將沉淀劑添加到溶液中,使沉積劑與雜質金屬發生反應生成一種沉淀,從而使化學反應過程逐漸趨向于沉淀生成方向進行。當溶液中物質的Qi>Ksp時會生成沉淀,以沉淀的方式去除溶液中的雜質。鈦白粉的副產品硫酸亞鐵中存在大量鈦、錳、鋁等的硫酸鹽,可以用硫化鈉、硫化鋇等對其進行硫化,從而生成沉淀。
孟素芬[11]將硫酸亞鐵溶于水中,再添加一定量的硫化鈉溶液進行雜質的去除,過濾后,對濾液中的雜質含量進行測定,研究結果表明,鋁離子的去除率為42.5%,錳離子的去除率為92.4%,鈦離子的去除率為20.3%。表明硫化鈉可有效去除硫酸亞鐵中的金屬錳,但對鈦和鋁的析出作用不明顯。
1.3 重結晶法
重結晶法根據不同物質的溶解度差異,對硫酸亞鐵溶液進行降溫結晶,從而有效分離鈦、錳、鋁等雜質元素,硫酸亞鐵重結晶提純工藝流程見圖1。
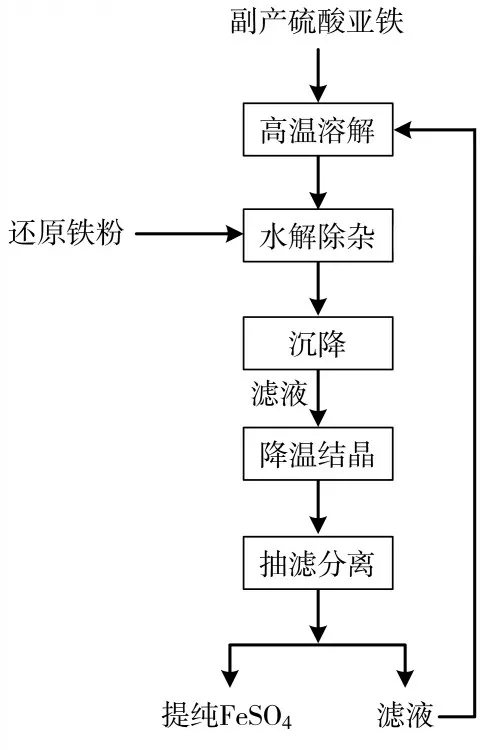
圖1 副產硫酸亞鐵重結晶提純工藝流程[13]
張克宇[13]對結晶中的副產品硫酸亞鐵的殘余物質進行研究,并分析影響其提純的相關因素,如結晶次數、攪拌轉速、結晶物pH 值等。經低溫結晶精制試驗,得到了最好的提純條件,即溫度10 ℃左右、3 次結晶、pH 值2、攪拌轉速300 r/min。用該方法純化后的硫酸亞鐵產品,硫酸亞鐵質量分數可以高達99.45%,雜質含量很低。
1.4 膠體沉淀吸附法
膠體沉淀吸附法是使溶液產生相應的膠體,主要利用膠體的吸附作用把溶液中的雜質吸附在一起,并通過過濾除去雜質的方法。由法揚斯規則可知,在達到一定的pH 值時,磷酸亞鐵會很難溶解,從而形成膠體,磷酸亞鐵凝膠體對膠體中的成分有很好的吸附作用,從而產生不能溶解的離子。對于磷酸亞鐵溶膠,形成溶膠中的Fe2+和PO43-,很容易被Fe3(PO4)2膠體吸附。從擴散雙電層理論可以看出,Fe3(PO4)2溶膠會在一定程度上吸附高電荷的Mn2+、Al3+和Ti4+等離子,從而達到去除這些雜質的目的。將磷酸添加到硫酸亞鐵溶液中,使其pH 值達到1~2,這時磷酸亞鐵溶解性降低,可以生成Fe3(PO4)2膠體。磷酸亞鐵溶膠能有效地吸附高帶電的金屬離子,使其被吸附在膠體上,再通過過濾法分離出純凈的硫酸亞鐵溶液[14]。上述方法對Ti4+的去除率高,鐵含量損失小,在低pH 條件下避免了Fe2+的氧化,未引入其他金屬雜質,工藝穩定簡單,反應周期短,適用于工業化生產。
1.5 絮凝共沉法
絮凝共沉法是將鈦白粉副產物硫酸亞鐵加水溶解除去不溶物后,加入硫化鋇溶液,升溫生成沉淀后加入絮凝劑,過濾后即可得到凈化后的硫酸亞鐵溶液。程文敢[15]在通過副產硫酸亞鐵制取氧化鐵紅時,硫酸鐵的精制采用了絮凝沉淀法,首先向硫酸亞鐵溶液中加入適量的硫化鋇溶液,升溫,并在反應過程中保持攪拌,大部分的金屬雜質被轉變成硫化物沉淀,而鈦也被水解成偏鈦酸,經過過濾分離得到凈化的硫酸亞鐵溶液。張兆麟等[16]對鈦白粉副產品提純技術進行了改良,先將鐵屑添加到溶液中還原三價鐵,然后在其中添加硫化鋇和絮凝劑,使之形成一種新的沉淀,經過過濾,便可以得到凈化的硫酸亞鐵溶液。
2 結論
從鈦白粉生產副產物硫酸亞鐵除雜工藝可知,化學沉淀法適用于除去錳離子,水解法則對鋁、鈦雜質離子去除效果較佳,因此使用單一水解法或沉淀法并不能完全去除硫酸亞鐵中的雜質離子。若是采用化學沉淀法和水解法共同除去錳、鈦、鋁雜質,除雜工藝流程較為復雜;而重結晶法在工藝上對溫度要求較高,同時結晶次數對產品的收率影響較明顯,由于存在母液雜質離子富集,產品收率還需進一步提高;絮凝共沉法需要通過加入氯化鋇或硫化鋇,引入了新的金屬雜質離子,并且要嚴格控制pH,操作較為復雜,不利于工業生產;而膠體沉淀吸附法實驗控制因素很多,如反應的具體時間、溫度、攪拌轉速等,但此方法能避免二價鐵離子的氧化問題,工藝穩定,且未引入其他金屬雜質,工藝流程簡單,反應周期短,因此是最適用于工業化生產的除雜方法。

