基于治療胃腸感染性腹瀉的藿香正氣系列制劑再評價研究
李玉婷?楊放?劉濤?雷陽?譚瑤琳

摘要:目的 對藿香正氣系列制劑的內(nèi)在質(zhì)量差異進行評價,為其臨床應用提供參考。方法 利用網(wǎng)絡藥理學、分子對接技術(shù)對藿香正氣系列制劑針對胃腸感染性腹瀉的活性成分進行篩選,以中度值較大的活性成分漢黃芩素以及藿香正氣系列制劑中的指標性成分和厚樸酚、厚樸酚等3種活性成分為度量指標,采用HPLC法,在檢測波長277? nm,體積流量1.0? mL/min,柱溫30℃,進樣量10 μL下,以乙腈:0.6%磷酸=45:55(V/V)為流動相進行檢測,采用體外抑菌試驗對評價結(jié)果進行驗證。結(jié)果? ? 相同生藥量下,不同劑型的含量存在差異,本實驗下藿香正氣水對大腸埃希菌、金黃色葡萄球菌有抑制作用。結(jié)論 藿香正氣系列制劑存在一定的內(nèi)在質(zhì)量差異,其說明書中標示功能主治完全一致的合理性有待進一步研究。
關(guān)鍵詞:藿香正氣系列制劑;網(wǎng)絡藥理學;分子對接;胃腸感染性腹瀉
中圖分類號:R961.1文獻標志碼:A
Reevaluation of Huoxiang Zhengqi series preparations for gastrointestinal infectious diarrhea
Li Yu -ting1, Yang Fang2, Liu Tao1, Lei Yang1, and Tan Yao-lin3
(1? College of Food and Bioengineering, Chengdu University, Chengdu 610106; 2 Sichuan Provincial Key Laboratory of New Drug Pilot Test, Chengdu Tianhe Integrated Traditional Chinese and Western Medicine Technology Conservation Co., Ltd., Chengdu 610106; 3 School of Pharmacy, Guangxi University of Traditional Chinese Medicine, Nanning 530200)
Abstract Objective The internal quality differences of Huoxiang Zhengqi series preparations were evaluated to provide a reference for clinical application. Methods The active components of Huoxiang Zhengqi series preparations for gastrointestinal infectious diarrhea were screened by network pharmacology and molecular docking technology. The active components of wogonin with moderate value, the index components of Huoxiang Zhengqi series preparations, magnolol, and honokiol were used as measurement indexes. HPLC method was used to detect the active components of Huoxiang Zhengqi series preparations under the conditions of the detection wavelength of 277 nm, the volume flow rate of 1.0 mL/min, column temperature of 30℃, and the injection volume of 10 μL. The mobile phase was acetonitrile : 0.6 % phosphoric acid = 45 : 55(V/V). The results were verified by in vitro antibacterial test. Results? ? Under the same dosage, the content of different dosage forms was different. In this experiment, Huoxiang Zhengqi water had inhibitory effects on Escherichia coli and Staphylococcus aureus. Conclusion There are some internal quality differences in Huoxiang Zhengqi series preparations, and the phenomenon of completely consistent functional indications in the instructions needs further study.
Key words? ? Huoxiang Zhengqi series preparations; Network pharmacology; Molecular docking; Gastrointestinal infectious diarrhea
胃腸感染性腹瀉主要是由于胃腸道被病毒、細菌、真菌等病原體感染而導致,臨床癥狀多表現(xiàn)為糞便異常、嘔吐、腹痛等癥狀,目前多以具有抑菌、抗病毒作用的中成藥進行治療,其具有較好的療效;部分細菌、病毒會引起機體出現(xiàn)炎癥,因此還需要通過中成藥相應的抗炎作用減輕炎癥[1]。藿香正氣處方中,以藿香化濕,以紫蘇、白芷解表,以蒼術(shù)、厚樸、大腹皮健脾燥濕,以茯苓、陳皮和胃清心,配伍后可使?jié)駵孟改c調(diào)和[2-3]。實驗研究表明藿香正氣系列制劑在抗炎方面表現(xiàn)出了優(yōu)異的藥理活性,且對各種致病性真菌、細菌有抑制作用[4-6]。藿香正氣系列制劑是由藿香正氣散在現(xiàn)代制藥技術(shù)上演變而來,主要包括膠囊劑、片劑、顆粒劑、水劑和口服液等近10種劑型,在臨床上普遍應用于治療腸胃型感冒、急性胃腸炎等疾病,具有改善胃腸功能、有效促進腸動力、保護腸胃屏障功能和鎮(zhèn)靜的作用,在《中國藥典》2020版一部等相關(guān)標準中,其所標示的主治功能均為解表化濕,理氣和中;主要用于外感風寒、內(nèi)傷濕滯或夏傷暑濕所致感冒[7-13]。不同劑型的藿香正氣制劑其處方雖然相同,但生產(chǎn)工藝參數(shù)甚至制備方法及工藝路線完全不同,如藿香正氣水醇提的藥材為蒼術(shù)、陳皮、厚樸、白芷等4味,提取工藝為滲漉法。并以40%~50%的乙醇作為成藥的溶媒,而藿香正氣口服液僅將厚樸一味藥材進行醇提,提取工藝為回流法,且以水為成藥的溶媒,顯然,兩者由于制備工藝不同,其所含物質(zhì)基礎有異,因此臨床上治療效果可能有異,其標示的功能主治完全一致的合理性有待再評價。
由于中成藥具有多成分、多靶點和多通路的特點,網(wǎng)絡藥理學與分子對接技術(shù)主要利用網(wǎng)絡對中成藥的多成分進行分析并通過多種途徑對相關(guān)信號通路進行調(diào)節(jié);同時組成多成分-多靶點-多途徑網(wǎng)絡。網(wǎng)絡藥理學以及分子對接技術(shù)主要利用分子生物學將中成藥中的有效成分與靶點基因相聯(lián)系,從而提高藥物療效,降低不良反應,還可用其進行老藥新用的研究。因此本研究利用網(wǎng)絡藥理學篩選藿香正氣系列制劑處方藥材中針對胃腸感染性腹瀉的抗炎、抑菌潛在活性成分,根據(jù)文獻及網(wǎng)絡藥理學評價方法指南的要求[14]。本文利用分子對接技術(shù)對篩選出的活性成分進行再驗證,篩選得到漢黃芩素,并根據(jù)文獻報道將和厚樸酚及厚樸酚作為臨床上治療感染性腹瀉的指標性成分,用以評價不同劑型的藿香正氣制劑在治療胃腸感染性腹瀉方面的物質(zhì)基礎差異,再以大腸埃希菌和金黃色葡萄球菌為例,研究藿香正氣系列制劑的體外抑菌活性,對篩選結(jié)果進行驗證[15],以期為其臨床使用提供參考。
1 儀器與試劑
PS-40型超聲波清洗器(深圳得康清洗設備有限公司);DH系列電熱恒溫培養(yǎng)箱(西安禾普生物科技有限公司);BS-6KH 型電子天平(上海友聲衡器公司);FA2004電子分析天平(上海良平儀器儀表有限公司);Ichrom5100高效液相色譜儀(大連依利特)。
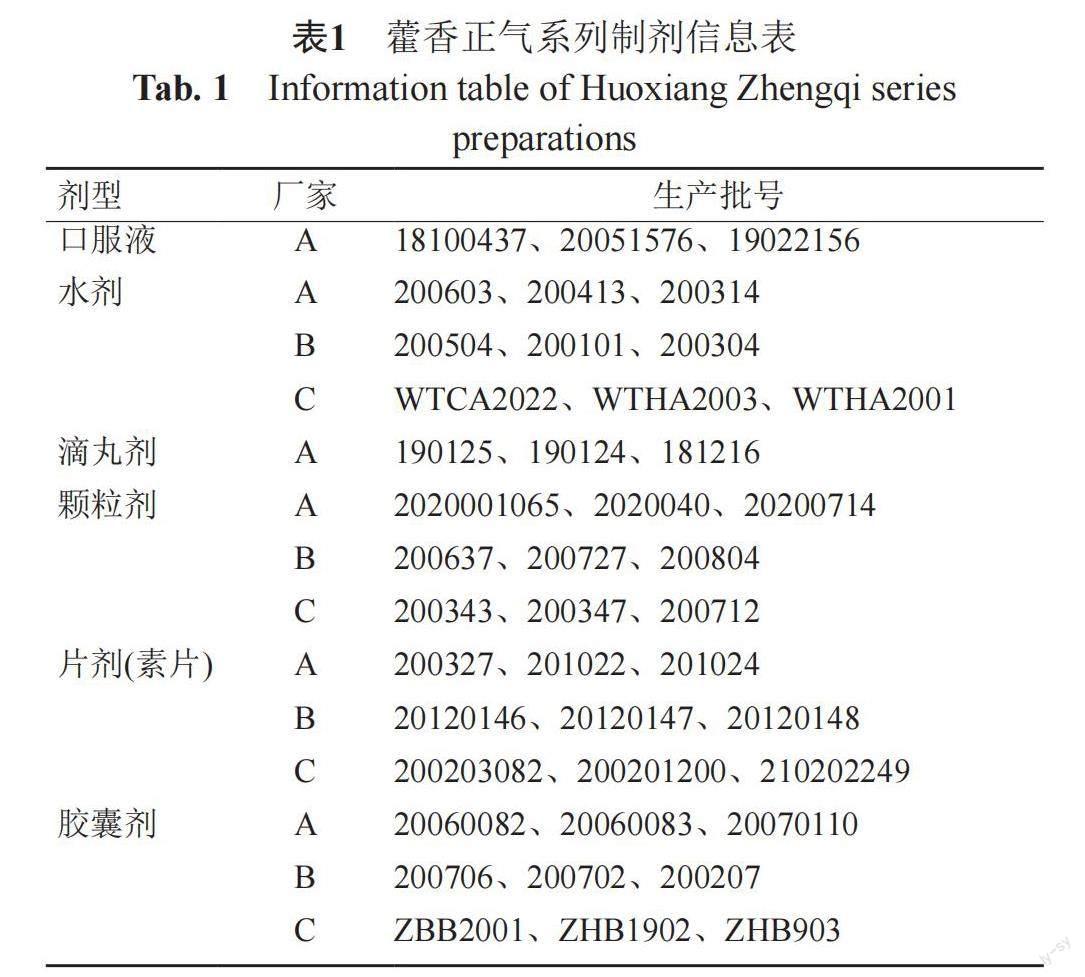
厚樸酚對照品(批號:wkq1012107質(zhì)量分數(shù)≥98%)、和厚樸酚對照品(批號:wkq21012507質(zhì)量分數(shù)≥98%)、漢黃芩素對照品(批號:wkq20030204質(zhì)量分數(shù)≥98%)等購買自四川省維克奇生物科技有限公司;藿香正氣系列制劑收集情況見表1;甲醇(批號:2021012002)、磷酸(批號:201910001)、乙腈(批號 20210104)、氯化鈉(批號:2015042401)、瓊脂粉(批號:2020092701)等購自成都市科隆化學品有限公司;蛋白胨(批號:20180928)購自北京奧博星生物技術(shù)有限公司;牛肉膏(批號:20160303)購自北京雙旋微生物培養(yǎng)基制品廠、水為蒸餾水。
2 方法
2.1 網(wǎng)絡藥理學、分子對接研究
2.1.1 藥物有效活性成分及靶標篩選
本文通過TCMSP(http://lsp.nwu.edu.cn/tcmsp.php)數(shù)據(jù)庫網(wǎng)站對藿香正氣系列制劑的10味中藥材進行檢索,本文篩選滿足口服生物利用度(oral bioavailability,OB)≥30%及類藥性(drug-likeness,DL)≥0.18的中藥成分;得到相應的靶標蛋白。借助 Uniprot(https://www.uniprot.org/)數(shù)據(jù)庫查詢相關(guān)靶標蛋白對應的基因名簡稱,利用GeneCards(http://www.genecards.org/)網(wǎng)絡數(shù)據(jù)庫對炎癥(inflammatory)、抑菌(antibacterial)進行檢索,得到疾病基因,利用Venny(http://bioinfogp.cnb.csic.es/tools/venny/)網(wǎng)絡數(shù)據(jù)庫,將藥物靶標基因和疾病基因?qū)霐?shù)據(jù)庫中進行整合,得到相應交集基因及韋恩圖。將整合后的交集基因?qū)隨TRING(http://string-db.org/cgi/input.pl)網(wǎng)絡數(shù)據(jù)庫中進行GO分析,設置物種選擇為“Homo sapiens”(人類),并選擇最低蛋白相互作用閾值為“highest confidence”(最高置信度)0.9,默認其余參數(shù),得到PPI網(wǎng)絡,再將交集基因?qū)隓AVID(https://david.ncifcrf.gov/home.jsp)網(wǎng)絡數(shù)據(jù)庫中,選擇“OFFICIAL GENE SYMBOL”和“Homo sapiens”,并清除所有默認選項進行KEGG富集分析。并用Prism軟件進行GO分析柱狀圖的構(gòu)建,利用Omishare(http://www.omicshare.com/tools/index.php/)網(wǎng)絡數(shù)據(jù)庫設定閾值P<0.05,選取前20個信號通路進行高級氣泡可視化分析,得到KEGG分析高級氣泡圖。
將不重復的通路基因?qū)隨TRING(http://string-db.org/cgi/input.pl)網(wǎng)絡數(shù)據(jù)庫,選擇網(wǎng)絡復雜程度為0.900進行PPI網(wǎng)絡構(gòu)建,借助Cytoscape3.7.2軟件將PPI數(shù)據(jù)中的成分-靶標文件和靶標-通路文件導入進行網(wǎng)絡拓撲學分析,將得到的數(shù)據(jù)進行可視化分析,得到成分-靶標-通路網(wǎng)絡,利用Microsoft Excel軟件對網(wǎng)絡拓撲數(shù)據(jù)進行處理以得到各個節(jié)點的中心度值(degree),以中心度值的中位數(shù)11為節(jié)點從大到小篩選關(guān)鍵核心基因,大于中位數(shù)兩倍為關(guān)鍵節(jié)點,得出排名靠前的藥物活性成分。
2.1.2 關(guān)鍵化合物-靶點分子對接
利用PDB數(shù)據(jù)庫(https://www.rcsb.org/)下載關(guān)鍵基因的蛋白受體,運用Discovery Studio 2020軟件移除蛋白受體中的配體和水分子;從PubChem(https://pubchem.ncbi.nlm.nih.gov/)數(shù)據(jù)庫中下載網(wǎng)絡藥理學篩選出的有效活性成分的2D結(jié)構(gòu)文件。利用Discovery Studio 2020軟件將蛋白受體與2D結(jié)構(gòu)結(jié)合,并顯示蛋白受體與配體相連的氫鍵得到優(yōu)化的2D結(jié)構(gòu),利用PyRx軟件上傳已經(jīng)去掉水分子加上氫的蛋白文件,將其進行格式轉(zhuǎn)化,再上傳2D結(jié)構(gòu)格式文件使其能量最小化后,進行對接;借助PyMOL軟件導入2D結(jié)構(gòu)選擇顯示蛋白受體與化合物配體間的氫鍵,修改繪制成3D對接圖,最后利用Microsoft Office PowerPoint軟件進行3D對接圖的調(diào)整。
2.2 含量測定方法
2.2.1 含量測定色譜條件
色譜柱為Supersil C18柱(250 mm×4.6 mm,5 μm),以乙腈-0.6%磷酸水溶液(45:55)(V/V)為流動相,進樣量10 μL,體積流量為1.0 mL/min,在277 nm檢測波長下測定,柱溫為30℃,理論塔板數(shù)以各定量成分峰計算均大于3000。
2.2.2 對照品溶液制備
稱取漢黃芩素、和厚樸酚以及厚樸酚對照品適量,精密稱定,用甲醇分別配制成漢黃芩素1.1558 μg/mL、和厚樸酚8.8 μg/mL、厚樸酚0.0111 mg/mL的對照品溶液,待用。
2.2.3 供試品溶液制備
(1)藿香正氣口服液供試品溶液的制備:精密量取藿香正氣口服液10 mL于25 mL容量瓶中,用甲醇定容至刻度,超聲提取(30℃、300 W、50 Hz)30 min,放冷,濾過,取濾液用 0.45 μm 微孔濾膜濾過,取續(xù)濾液,即得。
(2)藿香正氣水供試品溶液的制備:同“2.2.3(1)”。
(3)藿香正氣滴丸供試品溶液的制備:將藿香正氣滴丸研碎,取相同生藥量細粉,精密稱定,置于具塞錐形瓶中,精密量取25 mL分析甲醇,稱定重量,超聲提取(30℃、300 W、50 Hz)30 min,放冷,再稱定重量,用分析甲醇補足減失的重量,搖勻;濾過,濾液用0.45 μm 微孔濾膜濾過,取續(xù)濾液,即得。
(4)藿香正氣顆粒、藿香正氣片劑供試品溶液的制備:將藿香正氣顆粒、片劑研碎,取相同生藥量細粉,同“2.2.3(3)”項下藿香正氣滴丸供試品溶液制備方法自“置于具塞錐形瓶……”起,同法操作。
(5)藿香正氣膠囊供試品溶液的制備:取相同生藥量藿香正氣膠囊內(nèi)容物,同“2.2.3(3)”項下藿香正氣滴丸供試品溶液制備方法自“置于具塞錐形瓶……”起,同法操作。
2.2.4 方法學考察
(1)系統(tǒng)適用性試驗:精密移取“2.2.2”項下對照品溶液、藿香正氣水供試品溶液各10 μL,按“2.2.1”項下色譜條件測定。含量測定結(jié)果表明,供試品溶液的出峰位置與對照品溶液的出峰位置的相對保留時間對應一致,分離度均大于1.5。
(2)系統(tǒng)方法學考察:本文含量測定方法已經(jīng)方法學考察,儀器精密度試驗、線性條件考察、樣品穩(wěn)定性試驗、供試品重復性試驗及加樣回收試驗均符合相關(guān)要求,限于篇幅,將另文發(fā)表。
2.2.5 樣品測定
“2.2.3”項下制備的供試品溶液按照“2.2.1”項下的高效液相含量測定色譜條件進行測定。 相關(guān)高效液相含量測定色譜圖,見圖1~3。
2.3 抑菌藥效實驗
2.3.1 固體培養(yǎng)基制備及菌懸液制備
稱取牛肉膏1.2 g,蛋白胨4 g,NaCl 2 g,瓊脂粉8 g左右,加入400 mL純化水,在電熱套上邊攪拌邊加熱,使其完全溶解,在121℃高壓滅菌30 min后備用。在超凈工作臺無菌操作下,挑取適量大腸埃希菌、金黃色葡萄球菌于固體培養(yǎng)基中在37℃恒溫培養(yǎng)箱中倒置培養(yǎng)24 h左右。待細菌培養(yǎng)好后,在超凈工作臺無菌條件下,挑取適量已培養(yǎng)好的大腸埃希菌、金黃色葡萄球菌于裝有適量無菌水的試管中與麥氏比濁管對比制成1×106~107? CFU/mL的菌液,振蕩搖勻后備用。
2.3.2 抑菌供試品溶液的制備
(1)藿香正氣口服液、藿香正氣水直接使用。
(2)藿香正氣滴丸供試品溶液的制備:將藿香正氣滴丸研碎,取相同生藥量細粉,精密稱定,分別置于具塞錐形瓶中,精密量取10 mL純化水,超聲提取(30℃、300 W、50 Hz)30 min,搖勻;濾過,取續(xù)濾液,即得。
(3)藿香正氣顆粒、片劑供試品溶液的制備:將藿香正氣顆粒、片劑分別研碎,取相同生藥量細粉,同“2.3.2(2)”項下藿香正氣滴丸供試品溶液制備方法自“分別置于具塞錐形瓶……”起,同法操作。
(4)藿香正氣膠囊供試品溶液的制備:取相同生藥量藿香正氣膠囊內(nèi)容物,同“2.2.3(3)”項下藿香正氣滴丸供試品溶液制備方法自“分別置于具塞錐形瓶……”起,同法操作。
2.3.3 抑菌活性的測定
固體培養(yǎng)基高壓滅菌后,在超凈工作臺無菌條件下進行倒平板操作,待固體培養(yǎng)基冷卻凝固后,精密量取1 mL已制備好的大腸埃希菌、金黃色葡萄球菌菌液于培養(yǎng)基表面涂布均勻,將牛津杯按照順序放置在固體培養(yǎng)基上,在牛津杯中加入80 μL的供試品溶液,采用0.0068 mg/mL阿莫西林溶液作陽性對照,45%乙醇作為藿香正氣水的陰性對照、純化水作其他制劑陰性對照,確定其抑菌效果。
3 結(jié)果與分析
3.1 網(wǎng)絡藥理學預測結(jié)果
3.1.1 藥物有效活性成分及靶標篩選
通過TCMSP網(wǎng)絡數(shù)據(jù)庫檢索組成藿香正氣系列制劑的10味中藥材,并設置口服生物利用度OB≥30%且類藥性DL≥0.18篩選出6種中藥材的有效活性化合物成分。繼續(xù)借助Uniprot網(wǎng)絡數(shù)據(jù)庫檢索得到130個靶標簡稱,合并相同靶標簡稱得到117個不同成分靶標。通過GeneCards(https://www.genecards.org/)網(wǎng)絡數(shù)據(jù)庫查詢炎癥(inflammatory)、抑菌(antibacterial)兩個方面的疾病基因,并進行整合得到共539個疾病基因相關(guān)靶點。通過Venny網(wǎng)絡數(shù)據(jù)庫,將117個成分靶點與539個疾病基因靶點相整合得到藿香正氣系列制劑對炎癥、抑菌的潛在作用靶點39個,如圖4所示。
經(jīng)KEGG分析得圖5~7中顯示富集的主要條目有細胞過程的陽性調(diào)節(jié)(positive regulation of cellular process),細胞對化學刺激的相應(cellular response to chemical stimulus);在細胞組成中作用的靶點主要在細胞質(zhì)(cytoplasmic part),細胞器的管腔(intracellular organelle lumen)等區(qū)域。KEGG分析篩選得到203條信號通路,選擇P值較小的前20個信號通路進行高級氣泡可視化分析,得到KEGG分析高級氣泡圖,見圖8。圖中相關(guān)靶點主要富集在癌癥通路(pathways in cancer)、乙型肝炎(hepatitis B)、腫瘤信號通路(TNF signaling pathway)等相關(guān)的信號通路上。
通過STRING網(wǎng)絡數(shù)據(jù)庫有效活性成分的基因與交集基因整合得到通路-基因的PPI網(wǎng)絡。借助Cytoscape3.7.2軟件對網(wǎng)絡拓撲數(shù)據(jù)進行可視化分析,得到成分-靶標-通路網(wǎng)絡如圖9以及網(wǎng)絡拓撲學參數(shù)。以網(wǎng)絡拓撲學參數(shù)中心度值(degree)的中位數(shù)11為節(jié)點從大到小篩選關(guān)鍵核心基因,大于中位數(shù)為重要節(jié)點,大于中位數(shù)兩倍為關(guān)鍵節(jié)點,得到Degree排名為漢黃芩素(MOL000173)為關(guān)鍵節(jié)點、表兒茶素(MOL000073)及β-谷甾醇(MOL000358)為重要節(jié)點。
3.1.3 分子對接結(jié)果
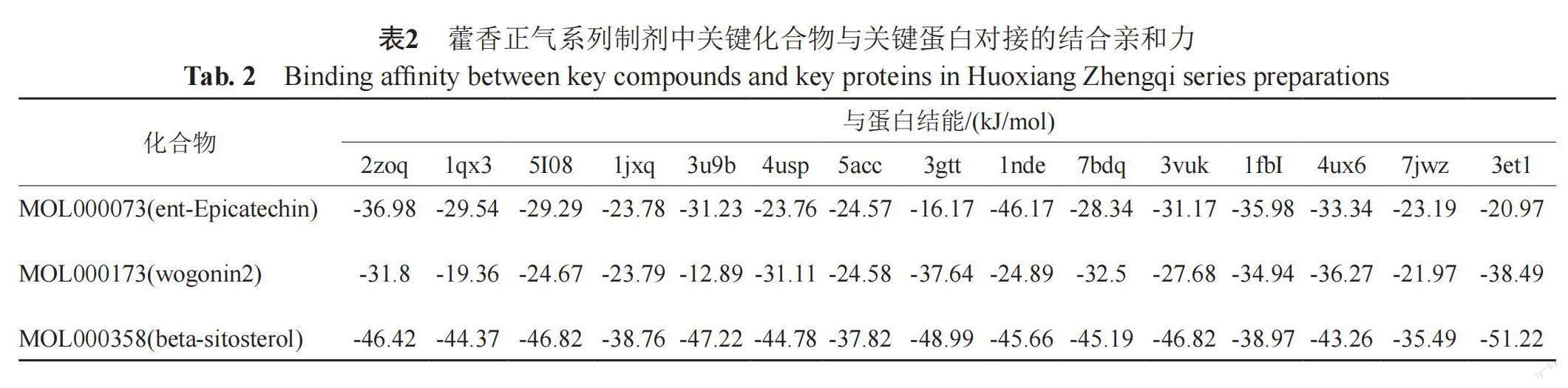
當配體與受體結(jié)合的構(gòu)象穩(wěn)定時能量越低時,配體與受體自發(fā)結(jié)合的阻力越小,發(fā)生的作用可能性越大。分子對接3D結(jié)構(gòu)圖顯示,將藿香正氣系列制劑通過網(wǎng)絡藥理學篩選出的活性成分漢黃芩素(wogonin2)、表兒茶素(ent-Epicatechin)、β-谷甾醇(beta-sitosterol)與關(guān)鍵靶標基因進行分子對接,關(guān)鍵化合物與關(guān)鍵蛋白對接的結(jié)合親和力均在數(shù)值-10以下,見表2;其中3D分子對接圖,見圖10。據(jù)圖可知,藿香正氣系列制劑針對胃腸感染性腹瀉抑菌、抗炎的治療效果最佳的有效活性成分為漢黃芩素。3.2 含量測定結(jié)果?根據(jù)篩選結(jié)果及相關(guān)文獻,選擇漢黃芩素、和厚樸酚及厚樸酚作為指標,對不同劑型的藿香正氣制劑進行評價,并在相同生藥量下,推測不同劑型的藿香正氣制劑針對胃腸感染性腹瀉的臨床使用效果,在生藥量相同的情況下不同劑型不同廠家不同批次間的含量測定結(jié)果,如表3及圖11所示。結(jié)果表明,片劑、膠囊劑、滴丸與藿香正氣口服液均呈極顯著差異(P<0.01);水劑、顆粒劑與藿香正氣口服液也有明顯差異;相同廠家相同劑型不同批次間含量也存在差異。
3.3 藿香正氣系列制劑對大腸埃希菌、金黃色葡萄球菌的抑菌作用
在大腸埃希菌、金黃色葡萄球菌的平板中加入供試品溶液、陰性對照品溶液及陽性對照品溶液,觀察藿香正氣系列制劑的抑菌作用,并測量其抑菌圈面積大小(每皿兩個平行樣品)。實驗結(jié)果表明藿香正氣水對大腸埃希菌、金黃色葡萄球菌均有抑制作用,其他制劑對大腸埃希菌、金黃色葡萄球菌均未見明顯抑菌作用;不同廠家生產(chǎn)的藿香正氣水對不同菌種的抑制作用不同,且相同廠家不同批次間的抑菌作用也存在差異,結(jié)果見表4及圖12~17。
4 討論
藿香正氣系列制劑在臨床上普遍應用于治療腸胃型感冒、胃腸感染性腹瀉、急性胃腸炎等消化系統(tǒng)的疾病以及呼吸內(nèi)科、皮膚科、兒科疾病,在《新型冠狀病毒肺炎診療方案(試行第四版)》至試行第八版均將藿香正氣系列制劑作為新型冠狀病毒醫(yī)學觀察臨床表現(xiàn)為乏力伴有腸胃不適患者的推薦用藥。本研究及相關(guān)文獻表明,藿香正氣系列制劑其物質(zhì)基礎、成分含量、制備工藝不同;且相關(guān)文獻表明系列制劑的適應癥有所不同[16-22];因此說明書中標治的主治功能完全一致的合理性還有待評價。
本研究主要利用了系統(tǒng)的網(wǎng)絡藥理學篩選出藿香正氣系列制劑針對胃腸感染性腹瀉對炎癥、抑菌作用的活性成分,分析結(jié)果的靶點主要是漢黃芩素(MOL000173)、表兒茶素(MOL000073)、β-谷甾醇(MOL000358);然而利用分子對接技術(shù)對3種活性成分進行與關(guān)鍵靶標基因進行3D分子對接,結(jié)果表明僅有漢黃芩素對治療胃腸感染性腹瀉的抗炎、抑菌作用有效;相關(guān)標準將厚樸酚、和厚樸酚以及橙皮苷作為制劑的指標性成分,但由于漢黃芩素和橙皮苷均為黃酮類化合物,其化學結(jié)構(gòu)相似,均具有抗炎抑菌等藥理作用[23-24]。因此本文僅選用漢黃芩素、和厚樸酚及厚樸酚作為度量治療感染性腹瀉抗炎、抑菌的理論指標,并輔以抑菌作用實驗對含量測定結(jié)果進行驗證。
本文研究結(jié)果表明在基于網(wǎng)絡藥理學以及分子對接技術(shù)研究的基礎上,不同藿香正氣系列制劑具有不同的物質(zhì)究基礎;在指標性成分的測定基礎上,不同劑型、不同廠家、不同批次的藿香正氣系列制劑間3種活性成分存在差異。部分文獻表明漢黃芩素因其本身所帶有的酚羥基較多且在溶液中不穩(wěn)定, 采用乙醇可使?jié)h黃芩素充分溶出,和厚樸酚及厚樸酚在乙醇濃度為40%~60%之間時的厚樸總酚得率較大;而藿香正氣水多味藥材采用乙醇浸提,且以40%~50%的乙醇為溶媒[25];含量測定結(jié)果中也表明藿香正氣水中3種成分度量指標較其他劑型數(shù)值更大,抑菌藥效學實驗結(jié)果表明在本實驗條件下藿香正氣系列制劑中只有藿香正氣水對大腸埃希菌、金黃色葡萄球菌表現(xiàn)出明顯抑制作用,其他制劑均未表現(xiàn)出明顯抑菌作用,與含量測定結(jié)果有一定關(guān)聯(lián)性。本研究于一定程度上揭示藿香正氣系列制劑說明書上標示主治功能相同的現(xiàn)象可能不合理,研究結(jié)果為藿香正氣系列制劑在臨床上針對不同病癥的用藥選擇提供參考。
參 考 文 獻
葉青艷, 陳建杰, 周華, 等. 感染性腹瀉的中醫(yī)治療進展[J]. 遼寧中醫(yī)雜志, 2014, 41(12): 2730-2732.
付麗娜, 張啟堂, 龐榕. 藿香正氣四種制劑的藥效學和毒理學研究[J]. 廣東化工, 2014, 41(14): 35-37.
張慧, 李詩暢, 肖洪彬. 藿香正氣類制劑的臨床應用研究概況[J]. 湖南中醫(yī)雜志, 2018, 34(3): 203-205.
錢星文, 何雁, 羅曉健, 等. 高效液相色譜法測定藿香正氣制劑中橙皮苷的含量[J]. 江西中醫(yī)學院學報, 2005, 17(3): 38-39.
王澤想, 盧丹, 張鵬, 等. 藿香正氣方的化學成分與藥理作用及質(zhì)量標志物的預測分析[J]. 中國醫(yī)藥科學, 2019, 9(21): 28-34.
羅黎霞. 藿香正氣水(液、丸)中脂溶性成分的測定及比較[J]. 中華中醫(yī)藥學刊, 2011, 29(12): 2789-2792.
張慧敏, 任虹, 何瑤, 等. 藿香正氣制劑中厚樸不同提取工藝對胃腸活動的影響研究[J]. 中藥與臨床, 2014, 5(6): 30-32.
尚曙玉, 張啟堂, 李曉光, 等. 藿香正氣不同制劑對動物小腸運動的影響[J]. 中國醫(yī)藥導報, 2012, 9(6): 96-98.
黃慶芳, 龔夢鵑, 陳艷芬, 等. 藿香正氣口服液對濕困脾胃證大鼠腸屏障功能的作用研究[J]. 中國中藥雜志, 2020, 45(9): 2144-2150.
劉瑤, 盧素宏, 林華景. 藿香正氣口服液對DSS誘導結(jié)腸炎小鼠腸黏膜屏障的保護作用及機制研究[J]. 中藥新藥與臨床藥理, 2021, 32(4): 473-478.
曹苗苗, 門鵬, 溫劍, 等. 藿香正氣口服制劑治療胃腸功能紊亂的循證評價[J]. 中國醫(yī)院用藥評價與分析, 2021, 21(05): 600-602.
曹爽, 孫超越, 張楠, 等. 針藥結(jié)合治療腹瀉型腸易激綜合征70例[J]. 光明中醫(yī), 2011, 26(12): 2488-2489.
劉海燕. 藿香正氣系列制劑在皮膚科的臨床應用[J]. 世界最新醫(yī)學信息文摘, 2016, 16(84): 164-165.
牛明, 張斯琴, 張博, 等. 《網(wǎng)絡藥理學評價方法指南》解讀[J]. 中草藥, 2021, 52(14): 4119-4129.
Wu B H, Wang G W, Xin L, et al. Network pharmacology-based therapeutic mechanism of Kuanxiong aerosol for angina pectoris[J]. J Ethnopharmacol, 2020, 261: 113079.
Gao D, Wu S N,? Zhang C E, et al. Exploration in the mechanism of rhubarb for the treatment of hyperviscosity syndrome based on network pharmacology[J]. J Ethnopharmacol, 2020, 261: 113078.
鄧燕君, 劉博文, 賀楨翔, 等. 基于網(wǎng)絡藥理學和分子對接法探索藿香正氣口服液預防新型冠狀病毒肺炎(COVID-19)活性化合物研究[J]. 中草藥, 2020, 51(5): 1113-1122.
王金榜, 梁保麗, 孫樹椿. 新型冠狀病毒(COVID-19)感染性肺炎現(xiàn)代中醫(yī)診療建議方案與探討[J]. 世界中醫(yī)藥, 2020, 15(1): 35-46.
汪海英. 藿香正氣丸(水、液等制劑)在消化系統(tǒng)疾病臨床應用的藥理研究[J]. 大家健康(學術(shù)版), 2014, 8(4): 243-244.
張洪坤. 中藥藿香正氣水抑菌藥效物質(zhì)及其質(zhì)量控制研究[D]. 廣東藥學院, 2013.
鐘林江, 楊俊莉, 奉梅, 等. 基于數(shù)據(jù)挖掘的金蓮花系列制劑治療上呼吸道感染的作用機制[J]. 成都大學學報(自然科學版), 2021, 40(1): 1-7.
胡一冰, 羅虹, 潘春暉, 等. 基于光譜法的六味地黃系列制劑質(zhì)量再評價研究[J]. 成都大學學報(自然科學版), 2020, 39(4): 368-373.
方靈芝, 吳雪松, 張玥. 高效液相色譜-電霧式檢測器法同時測定小兒解感片中7種黃酮類成分的含量[J]. 中國醫(yī)院藥學雜志, 2019, 39(23): 2402-2406.
李文娟, 潘馨, 陳曉蘭, 等. 黃芩中漢黃芩素的提取制備[J]. 亞太傳統(tǒng)醫(yī)藥, 2014, 10(9): 33-35.
徐洲, 李旭, 郭軍偉, 等. 響應面優(yōu)化超聲輔助醇堿法提取厚樸總酚的工藝條件[J]. 四川農(nóng)業(yè)大學學報, 2013, 31(1): 93-98.

