陽極泥中銻測定方法研究
關國軍,陳永紅,蘆新根,洪 博,葛仲義
(1.長春黃金研究院有限公司; 2.國家金銀及制品質量檢驗檢測中心(長春))
金屬銻是陽極泥重要的組成部分。目前,相關標準與文獻對于礦石中銻的測定方法主要有氫化物發生—原子熒光光譜法(銻品位0.010 %~0.40 %)、火焰原子吸收光譜法(銻品位0.40 %~10 %)、硫酸鈰滴定法[1]3種。高品位銻采用硫酸鈰滴定法測定,但砷、銻、鉍之間發生的復雜化學反應影響銻的測定;含碳過高的樣品在溶解過程中沒有有效除碳,影響后續滴定;銻易水解,影響樣品溶解與滴定;滴定過程中甲基橙指示劑的顏色突變不明顯,影響滴定終點的判定。因此,本文對硫酸鈰滴定法測定陽極泥中銻進行了優化實驗研究,確定了最佳測定條件,取得了滿意結果。
1 實驗部分
1.1 試 劑
硝酸、硫酸、磷酸、鹽酸、尿素、硫酸鉀、過氧化氫、酒石酸。
硝酸-酒石酸混酸:稱取10 g酒石酸溶于100 mL(1+3)硝酸中,混勻,備用。
(1+1)鹽酸:取50 mL蒸餾水,加入50 mL鹽酸,混勻。
甲基橙(5 g/L):稱取0.5 g甲基橙溶于70 mL水中,用水稀釋至100 mL。
亞甲基藍(5 g/L):稱取0.5 g亞甲基藍溶于50 mL無水乙醇中,用水稀釋至100 mL。
硫酸鈰標準滴定溶液(0.1 mol/L):稱取40.50 g四水硫酸鈰,置于1 000 mL燒杯中,加入30 mL硫酸,攪拌均勻,在電熱板上加熱至糊狀,并冒硫酸白煙約20 min,取下冷卻,加入140 mL硫酸,再緩慢加入400 mL水,攪拌溶解至澄清,冷卻。移入1 000 mL容量瓶中,用水稀釋至刻度,混勻,備用。放置3~4 d后,采用 GB/T 7739.10—2007 《金精礦化學分析方法 第10部分:銻量的測定》,用純銻標定。
砷銻鉍溶液:稱取5.000 0 g銻粒、5.000 0 g砷粒、5.000 0 g鉍粒,加入40 mL王水,250 ℃溶解,待全部溶解后用20 %鹽酸定容至1 000 mL容量瓶中備用。移取該溶液10 mL,當稱樣量為0.200 0 g時,砷、銻、鉍品位均為25 %。
銻溶液:稱取5.000 0 g銻粒,加入40 mL王水,250 ℃溶解,待全部溶解后用20 %鹽酸定容至1 000 mL容量瓶中,備用。移取該溶液10 mL,當稱樣量為0.200 0 g時,銻品位為25 %。
1.2 實驗方法
稱取0.200 0~0.300 0 g樣品于250 mL錐形瓶,用少量水潤濕[2],加入2~3 g硫酸鉀、50 mL水、3 mL過氧化氫、2 mL硝酸-酒石酸混酸,輕輕搖動后加入15 mL硫酸,在電熱板上將水蒸干(每隔10 min輕輕晃動),蒸干水分后加蓋表面皿,冒硫酸白煙計時再溶解15 min,取下冷卻。如果樣品含碳高,冒硫酸白煙時逐滴加入硝酸,直至樣品溶解完全,取下冷卻,加入1 g尿素,繼續加熱至溶液呈淡黃色,并冒硫酸白煙5 min,取下冷卻。加入7 cm2濾紙(約1/16直徑為12.5 cm濾紙),繼續加熱,直至溶液的暗紅色消失,取下冷卻至室溫。緩慢加入40 mL水、40 mL(1+1)鹽酸,加熱至微沸(85 ℃左右),取下加入10 mL磷酸、1滴甲基橙指示劑(5 g/L),用硫酸鈰標準滴定溶液滴定,臨近終點,再將溶液加熱至85 ℃左右,取下,加入2滴亞甲基藍指示劑(5 g/L),繼續用硫酸鈰標準滴定溶液滴定至紅色消失,突變為亮藍色為終點。
銻計算公式為:
式中:w(Sb)為銻質量分數(%);c為硫酸鈰標準滴定溶液濃度(mol/L);V為滴定試液消耗硫酸鈰標準滴定溶液的體積(mL);V0為滴定空白消耗硫酸鈰標準滴定溶液的體積(mL);m為樣品質量(g);121.76為銻摩爾質量(g/mol)。
2 結果與討論
2.1 過氧化氫用量
分別移取10 mL砷銻鉍溶液,在樣品溶解過程中分別加入不同量過氧化氫,并與不加入過氧化氫進行對比,實驗結果見表1。
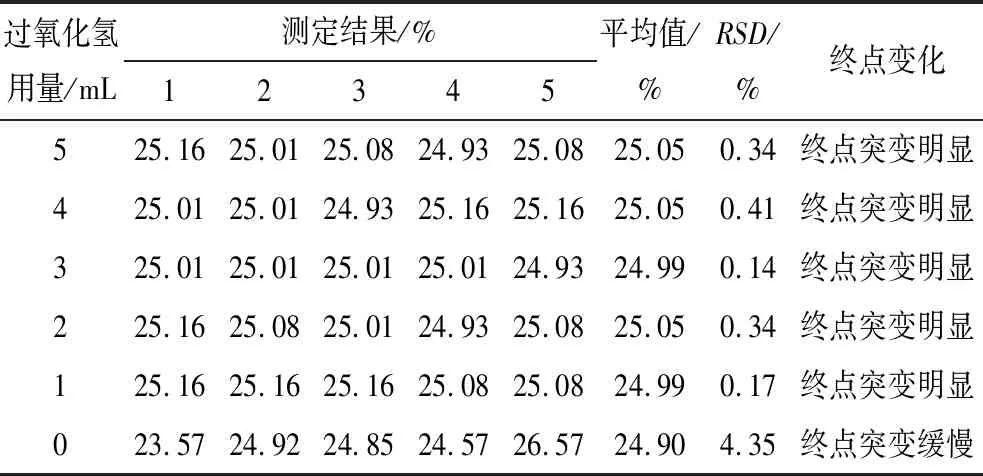
表1 過氧化氫用量對實驗結果的影響
從表1可以看出:加入過氧化氫對樣品進行預處理可以有效降低測定結果的相對標準偏差,原因是樣品中砷、銻、鉍含量高時,它們會發生一系列復雜的化學反應,影響銻的分析結果。例如:As(Ⅴ)與Sb(Ⅴ)可形成一系列不同組成與結構的砷銻酸,砷銻酸可與As(Ⅲ)、Sb(Ⅲ)、Bi(Ⅲ)進一步反應生成即使在酸性溶液中溶解度也很小的砷銻酸鹽。過氧化氫具有強氧化性,尤其在酸性溶液中其氧化性要顯著強于硫酸,利用過氧化氫的這一特性,破壞砷銻酸或砷銻酸鹽,實現Sb(Ⅲ)完全被氧化為Sb(Ⅴ)。過氧化氫用量為3 mL時,測定結果理想且滴定終點突變明顯。綜上所述,為了消除樣品中砷、銻、鉍之間復雜的化學反應,選擇在樣品溶解過程中加入3 mL過氧化氫。
2.2 硝酸-酒石酸混酸用量
銻易水解,樣品溶解過程中經常會出現銻水解現象,程度不一且不可控,對實驗影響較大,因此選擇加入硝酸-酒石酸混酸抑制銻的水解[3]。分別移取10 mL銻溶液,控制加入不同量硝酸-酒石酸混酸及不加入硝酸-酒石酸,實驗結果見表2。
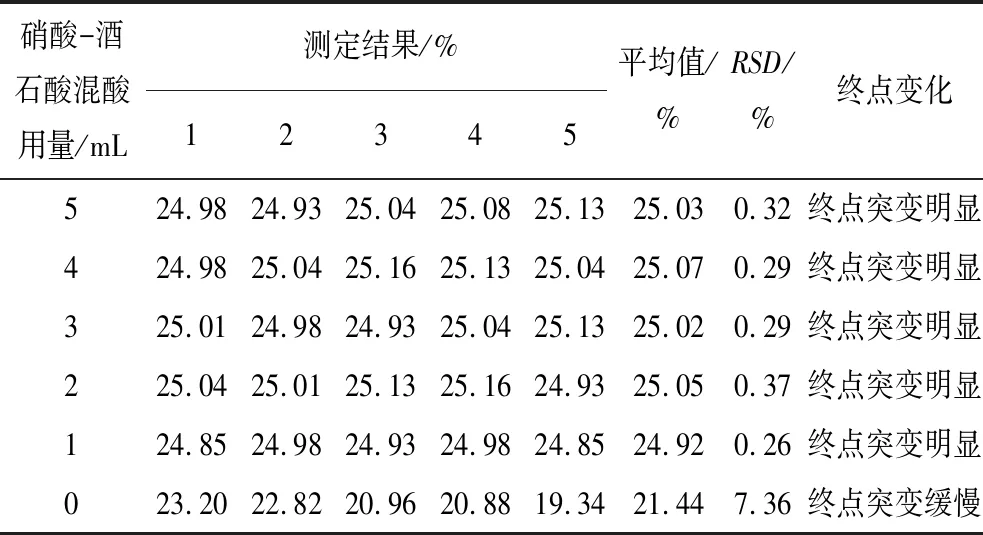
表2 硝酸-酒石酸混酸用量對實驗結果的影響
從表2可以看出:當不加入硝酸-酒石酸混酸時,會出現銻水解現象,導致測定結果偏低。當加入硝酸-酒石酸混酸后,測定結果接近真值,且數據集中,相對標準偏差較低。實驗過程中發現,當硝酸-酒石酸混酸用量過大時,樣品溶解過程中會出現迸濺且溶解時間較長。綜合考慮,選擇樣品溶解過程中加入2 mL硝酸-酒石酸混酸。
2.3 高碳處理方法
當樣品中含碳過高時,樣品處理不好會出現測定結果偏低的現象。實驗選用3個高碳陽極泥樣品,分別采用原子吸收光譜法和ICP法進行測定,平均值分別為12.36 %、25.47 %、49.89 %。實驗采用3種方案處理:方案1,在樣品冒硫酸白煙前加入5 mL硝酸;方案2,在樣品冒硫酸白煙時逐滴加入硝酸;方案3,不加硝酸。實驗結果見表3。
從表3可以看出:采用提前加入硝酸與不加硝酸處理樣品時,測定結果都偏低且離散,這是由于樣品含碳過高,樣品溶解不完全。當冒硫酸白煙時逐滴加入硝酸,此時硝酸的強氧化性會完全溶解樣品,測定結果更接近真值。綜上所述,如果樣品含碳高時,采用冒硫酸白煙時逐滴加入硝酸的方式處理樣品。
采用硝酸除去碳后,考察了硝酸對實驗是否有影響。移取10 mL銻溶液,分別加入不同量尿素及不加入尿素進行實驗,結果見表4。
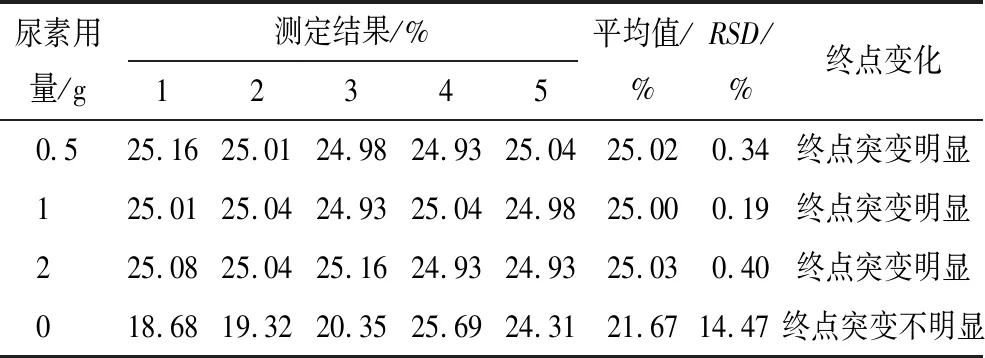
表4 尿素除硝酸實驗結果
從表4可以看出:當溶液中有硝酸存在時,對滴定終點有影響;這是因為硝酸具有強氧化性,在此氧化還原反應中生成的既有氧化性又有還原性的亞硝酸根離子對硫酸鈰滴定銻的氧化還原反應有影響。尿素可以與硝酸生成穩定的鹽類,達到除去硝酸的目的,且不影響滴定終點。故采用硝酸處理高碳陽極泥樣品后,需要加入1~2 g尿素除去硝酸。
2.4 指示劑
相關標準與方法中硫酸鈰法滴定銻的指示劑為甲基橙,終點顏色變化為紅色消失,但在實驗過程中發現,對于復雜樣品終點突變不明顯[4]。實驗采用甲基橙-亞甲基藍雙指示劑,終點顏色突變明顯。分別選用5.00 mL、10.00 mL、15.00 mL、20.00 mL銻溶液,以及3個陽極泥樣品(ICP法測定銻品位分別為18.88 %、23.31 %、30.56 %),考察甲基橙-亞甲基藍雙指示劑的影響,結果見表5、表6。
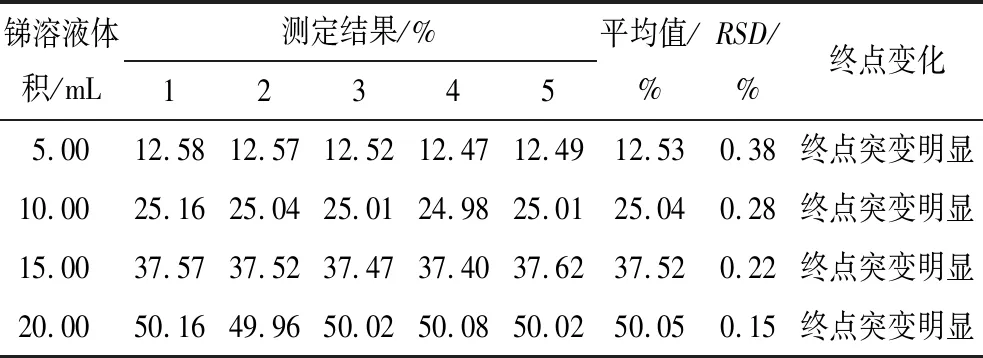
表5 銻溶液考察指示劑的實驗結果
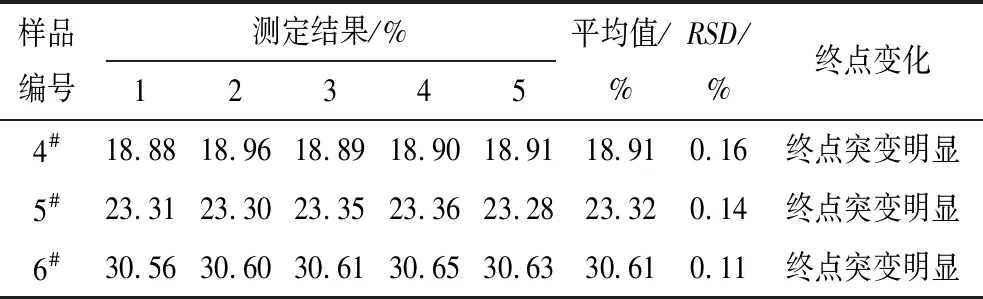
表6 陽極泥樣品考察指示劑的實驗結果
從表5、表6可以看出:對于銻溶液和復雜陽極泥樣品,甲基橙-亞甲基藍雙指示劑顯色明顯,且準確度和精密度均達到滿意效果,故采用甲基橙-亞甲基藍雙指示劑。
2.5 滴定溫度
硫酸鈰法滴定銻時,滴定溫度應嚴格控制在80 ℃~90 ℃,但隨著滴定時間的延長和硫酸鈰加入量的逐漸增大,造成滴定溫度不好控制[5]。實驗過程中監測溫度發現:煮沸時溫度為98 ℃~100 ℃;硫酸鈰用量為10 mL時溫度為92 ℃,15 mL時溫度為88 ℃,20 mL時溫度為80 ℃。當滴定硫酸鈰用量大于20 mL時,不能保證滴定溫度在要求內。移取20 mL銻溶液,進行滴定溫度考察,實驗結果見表7。
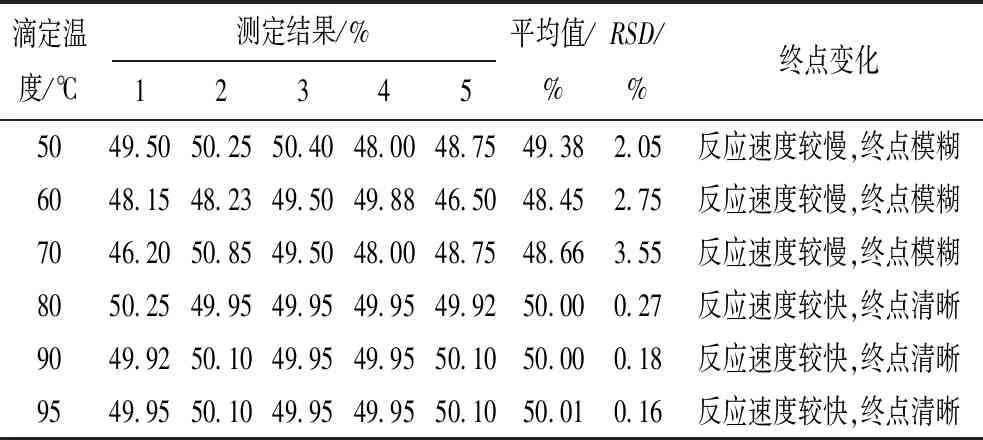
表7 滴定溫度對實驗結果的影響
從表7可以看出:當滴定溫度低于80 ℃時,反應速度較慢,終點顏色變化不明顯,有延遲,測定結果偏高,且相對標準偏差較大。滴定溫度為80 ℃~95 ℃時,反應速度較快,終點顏色變化明顯,測定結果基本一致,相對標準偏差為0.16 %~0.27 %。因此,采用硫酸鈰滴定銻的過程中,當臨近終點時,需要將溶液進行二次加熱,加熱至85 ℃左右,保持滴定溫度在80 ℃~95 ℃。
2.6 酸 度
硫酸鈰滴定銻的氧化還原反應必須在鹽酸介質中進行,考察了滴定過程中鹽酸加入量對實驗的影響。分別移取10 mL銻溶液,加入不同量(1+1)鹽酸,結果見表8。

表8 鹽酸加入量對實驗結果的影響
從表8可以看出:當(1+1)鹽酸加入量小于40 mL時,由于酸度過低,導致部分銻水解,造成測定結果偏低,相對標準偏差較大,且終點突變不明顯。當(1+1)鹽酸加入量為40~50 mL時,測定結果穩定,接近真值,且終點清晰。當(1+1)鹽酸加入量為60 mL時,由于酸度過高,造成測定結果偏低,且相對標準偏差偏高。綜上所述,當(1+1)鹽酸加入量控制在40~50 mL時,可得到滿意結果,但考慮到滴定過程的可操作性,確定(1+1)鹽酸加入量為40 mL。
2.7 磷酸加入量
加入磷酸的作用主要是掩蔽Fe3+,因為Fe3+會消耗硫酸鈰,造成結果偏高[6]。分別移取10 mL銻溶液,考察磷酸加入量為5 mL、10 mL、12 mL對測定結果的影響,見表9。
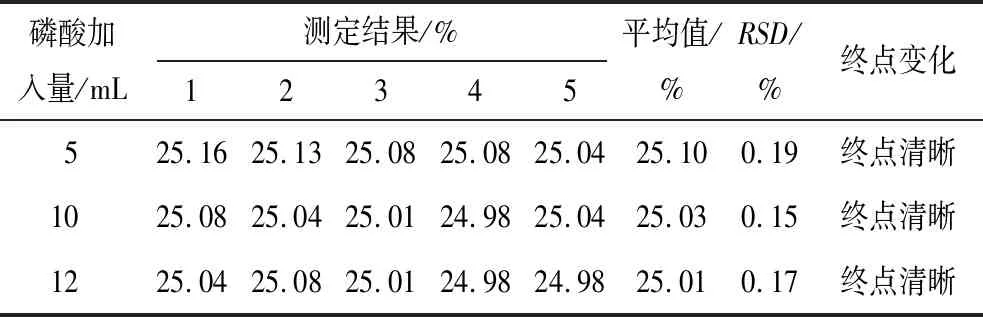
表9 磷酸加入量對實驗結果的影響
從表9可以看出:磷酸加入量對測定結果的影響很小。考慮實驗的可操作性,磷酸加入量確定為10 mL。
2.8 還原劑濾紙加入量
濾紙在實驗過程中作為還原劑,將Sb(Ⅴ)還原為Sb(Ⅲ)。分別移取10 mL銻溶液,考察還原劑濾紙加入量對銻測定結果的影響,見表10。
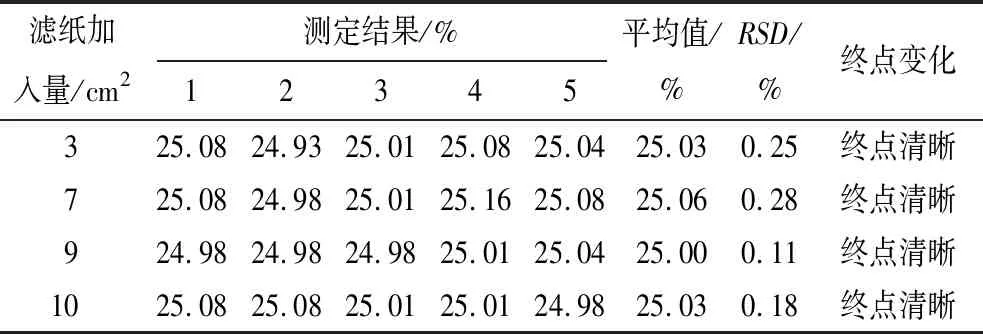
表10 還原劑濾紙加入量對實驗結果的影響
從表10可以看出:不同濾紙加入量對滴定終點無明顯影響,且測定結果的精密度都符合要求,但濾紙加入量過高會造成還原時間過長,拖慢實驗速度。故濾紙加入量確定為7 cm2(約1/16直徑為12.5 cm濾紙)。
2.9 發煙時間
發煙過程為硫酸將低價離子氧化為高價離子的過程,在該實驗中體現為將Sb(Ⅲ)氧化為Sb(Ⅴ)。移取10 mL銻溶液,考察不同發煙時間的影響,結果見表11。
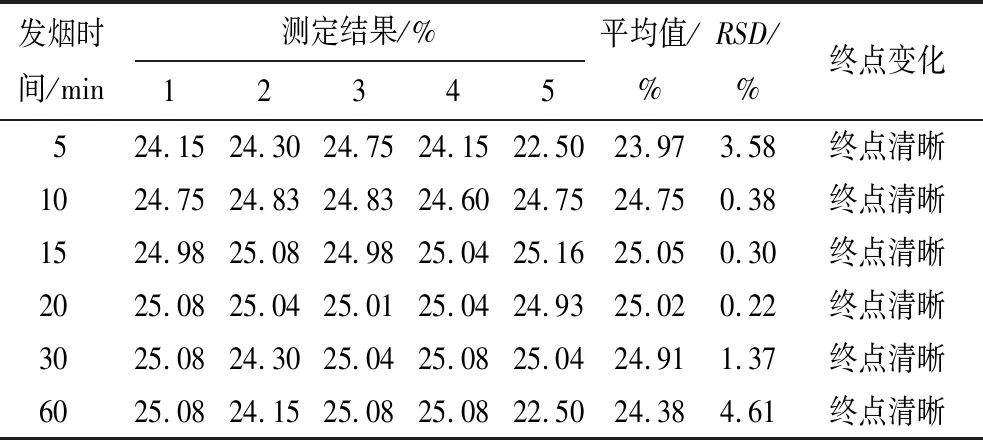
表11 發煙時間對實驗結果的影響
從表11可以看出:當發煙時間過短時,樣品中的Sb(Ⅲ)不能完全氧化為Sb(Ⅴ),因此造成測定結果偏低;當發煙時間過長時,硫酸除起到氧化作用,還會進一步分解為大量的二氧化硫,從而增大體系的還原氣氛,影響后續濾紙的還原,造成測定結果的相對標準偏差增大。故選擇發煙時間為15 min。
2.10 加標回收率實驗
移取5 mL、10 mL、20 mL銻溶液,編號為1*、2*、3*,分別加入不同量銻粒,測定加標回收率,結果見表12。
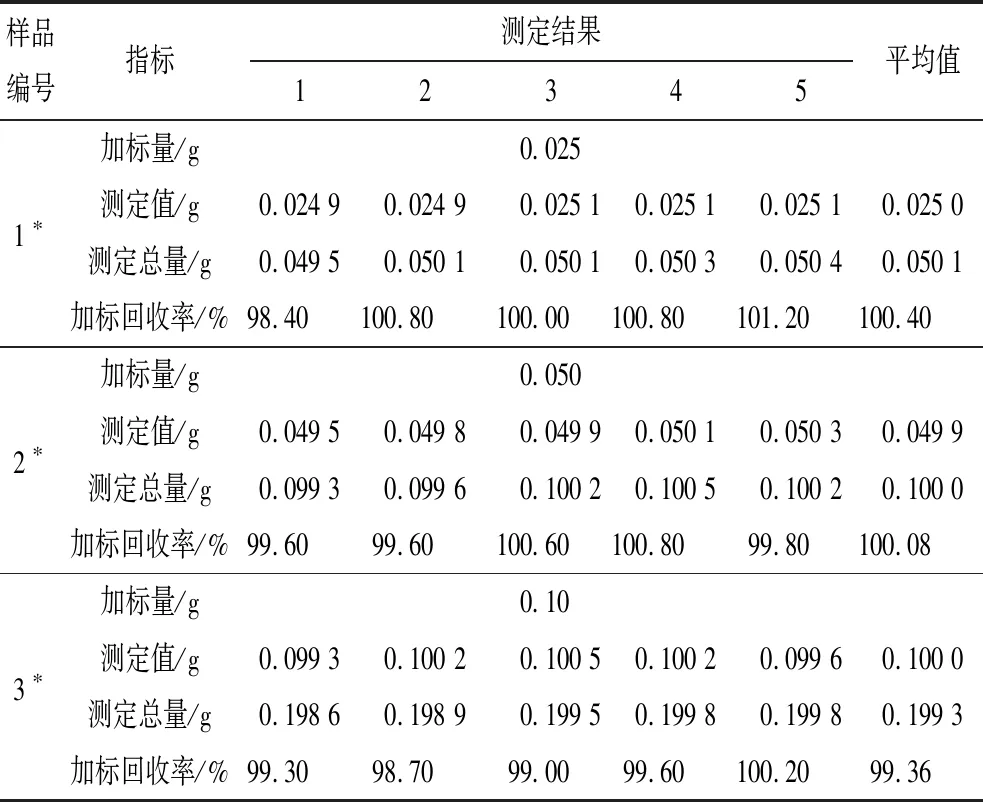
表12 加標回收率實驗結果
從表12可以看出,加入標準物質回收率為98.40 %~101.20 %,方法準確度良好,滿足分析要求。
2.11 方法的精密度
選用5 mL、10 mL、20 mL銻溶液進行方法的精密度驗證實驗,結果見表13。
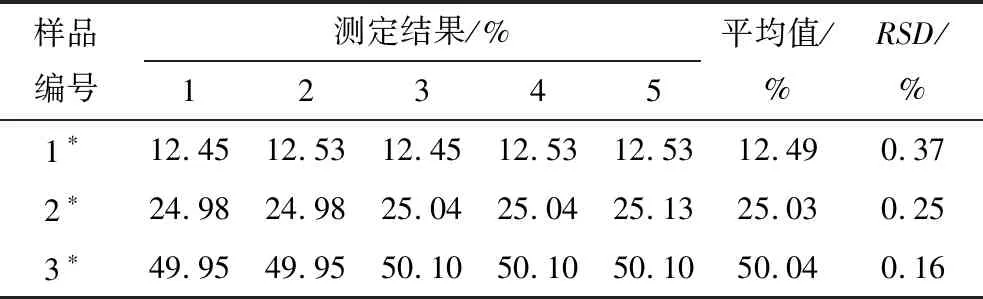
表13 方法的精密度實驗結果
從表13可以看出,3個樣品測定結果的相對標準偏差為0.16 %~0.37 %,精密度良好,滿足分析要求。
3 結 語
實驗確定了硫酸鈰滴定法測定陽極泥中銻的最佳條件為:過氧化氫3 mL,硝酸-酒石酸混酸2 mL,甲基橙-亞甲基藍雙指示劑,滴定溫度控制在80 ℃~95 ℃,(1+1)鹽酸40 mL,磷酸10 mL,濾紙7 cm2(約1/16直徑為12.5 cm濾紙),發煙時間15 min。當樣品含碳過高時,在冒硫酸白煙時逐滴加入硝酸,之后加入1~2 g尿素除去硝酸。研究建立的方法準確度和精密度良好,適合陽極泥中銻的準確測定。

