肝硬化門靜脈血栓形成的危險因素分析
胡宜濤,張 帆
云南省第三人民醫院消化內科,云南 昆明 650000
門靜脈血栓(PVT)形成是一般人群中一種相對少見的疾病,但在肝硬化患者中PVT 是一種常見的并發癥,發病率為0.6%到26%[1],PVT也發生于其他疾病,如遺傳性血小板減少癥、腹部感染或腸道疾病。急性PVT 可導致腸系膜缺血,甚至是嚴重的不良后果,如腸壞死等。慢性PVT 可導致門靜脈阻塞,從而導致繼發性門靜脈高壓[2]。有研究[3]表明,肝硬化PVT 的發病機制可能是多因素共同作用的結果,主要包括門靜脈血流量改變、血管壁的高凝性及血管壁損壞。同時也有研究[4]指出,門靜脈內徑、脾臟厚度、糖尿病、肥胖、凝血酶原時間(PT)、纖維蛋白原、D-二聚體、抗凝血酶Ⅲ(AT-Ⅲ)、血紅蛋白、脾切除史、硬化劑注射史、靜脈曲張程度、MELD 評分、Child-Pugh 評分等均可能與肝硬化患者PVT 的發生有關。本研究通過分析肝硬化合并PVT 的危險因素,并對肝硬化合并這些危險因素的患者進行跟蹤隨訪,從而明確肝硬化PVT 發生的危險因素,可更好地指導臨床,預防肝硬化PVT的發生。
1 資料與方法
1.1 一般資料
回顧性分析2017 年1 月—2018 年12 月在云南省第三人民醫院消化內科就診并診斷為肝硬化患者的臨床資料。入組患者共206 例,以是否發生PVT 分為PVT 組和對照組,其中PVT 組90例,對照組116例。收集患者的一般資料,包括性別、年齡、側支循環、硬化劑治療、脾切除、飲酒、高血壓、腹腔積液、Child-Pugh 評分。收集患者的實驗室檢查,包括紅細胞(RBC)、白細胞(WBC)、血紅蛋白(Hb)、血小板(PLT)、谷丙轉氨酶(ALT)、谷草轉氨酶(AST)、PT、活化部分凝血酶原時間(APTT)、D-二聚體。收集患者的影像學檢查結果,包括門靜脈主干直徑、脾臟厚度。
1.2 選取標準
納入標準:(1)年齡為18~85歲。(2)患者病史、臨床表現、實驗室及影像學檢查(腹部超聲、門靜脈超聲、腹部CT、MRI等)符合肝硬化的診斷標準。(3)入院后完善門靜脈超聲或腹部增強CT 或CTA 提示有或無PVT。(4)患者資料完整。(5)患者均知情同意本研究。排除標準:(1)年齡<18歲或>85歲。(2)合并惡性腫瘤。(3)肝移植患者。(4)近期有服用抗凝藥物史。(5)其他原因導致PVT。本次研究共隨訪患者86 人,隨訪過程中至少每3個月復查1 次門靜脈超聲或腹部增強CT 或CTA,以發現PVT為隨訪終點。
1.3 統計學方法
采用SPSS 20.0 軟件進行統計分析。正態分布的計量資料以均數±標準差(±s)表示,組間參數比較采用獨立樣本t檢驗,組內參數比較重復測量方差分析。計數資料以例數和百分比(%)表示,比較采用χ2檢驗或Fisher 確切概率法,非正態分布計量資料以中位數(M)和四分位數間距(IQR)表示,組間比較采用秩和檢驗,等級資料比較采取秩和檢驗。采用多因素logistic 回歸分析危險因素分析。用ROC曲線進行預測價值分析,患者的隨訪結果采用生存分析進行比較。以P<0.05為差異有統計學意義。
2 結果
2.1 兩組患者的一般資料情況
單因素分析顯示,肝硬化PVT 的發生與患者的性別、年齡、側支循環、是否行硬化劑治療、是否行脾切除治療、飲酒、高血壓、是否有腹腔積液比較,差異無統計學意義(P>0.05),見表1。
2.2 兩組患者的檢查情況
單因素分析顯示,肝硬化PVT 的發生與患者的PT、D-二聚體、門靜脈主干直徑有關,差異有統計學意義(P<0.05)。與RBC、WBC、Hb、PLT、Child-Pugh 評分、ALT、AST、APTT、脾臟厚度無關,差異無統計學意義(P>0.05),見表2。
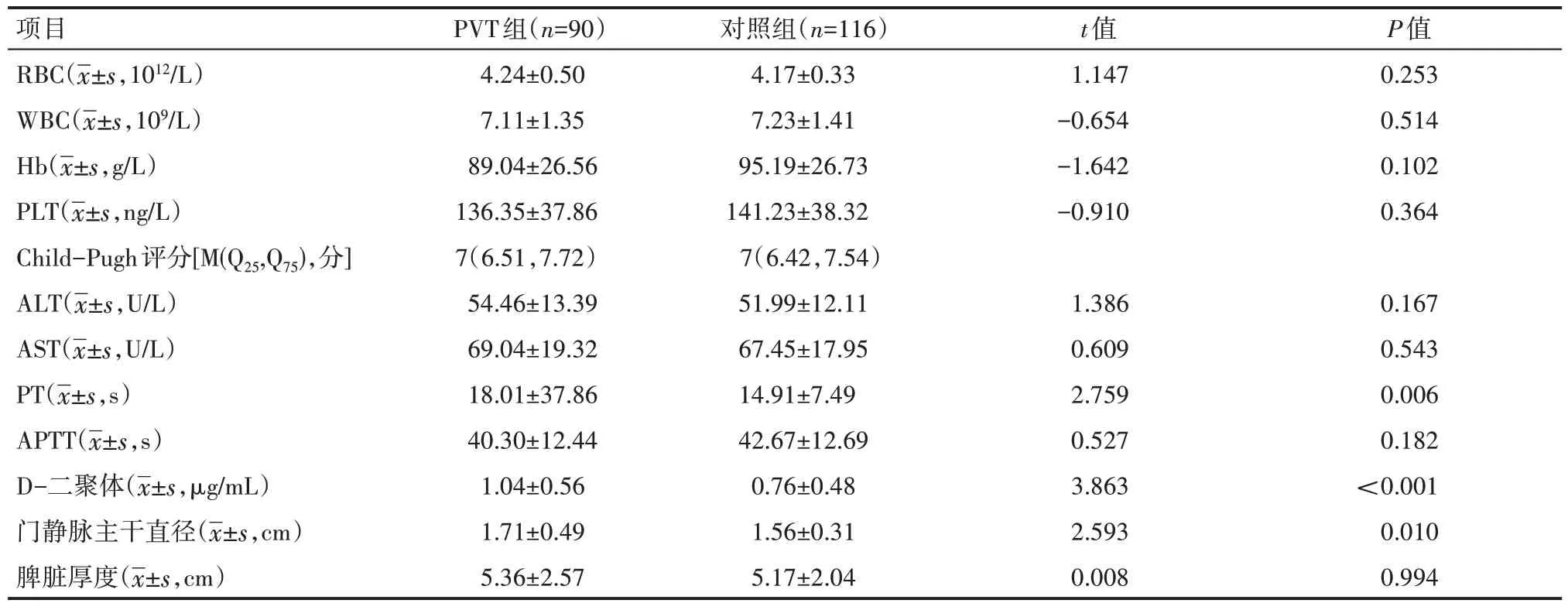
表2 兩組患者的檢查情況
2.3 肝硬化PVT形成的多因素logistic回歸分析結果
以是否發生PVT 為因變量,將上述單因素分析P<0.2的變量(Hb、ALT、PT、APTT、D-二聚體、門靜脈主干直徑)納入模型,進行多因素logistic 回歸分析,結果發現D-二聚體、門靜脈主干直徑、PT 是肝硬化PVT 形成的危險因素,其OR及95%CI分別為(OR=3.115,95%CI:
1.713~5.663,P<0.001)、(OR=2.643, 95%CI: 1.238~5.646,P=0.012)、(OR=1.044,95%CI:1.005~1.058,P=0.026),見表3。

表3 肝硬化PVT形成的多因素logistic回歸分析結果
2.4 PT、D-二聚體、門靜脈主干直徑單項檢測及3 項指標聯合檢測對肝硬化PVT的診斷效能情況
PT、D-二聚體、門靜脈主干直徑單項檢測診斷肝硬化PVT 診斷的ROC 曲線AUC 分別為:0.66、0.68、0.73,三項指標聯合檢測ROC曲線AUC為0.82,以約登指數最大值為診斷閾值,其敏感度為0.61,特異度為0.92,見圖1。
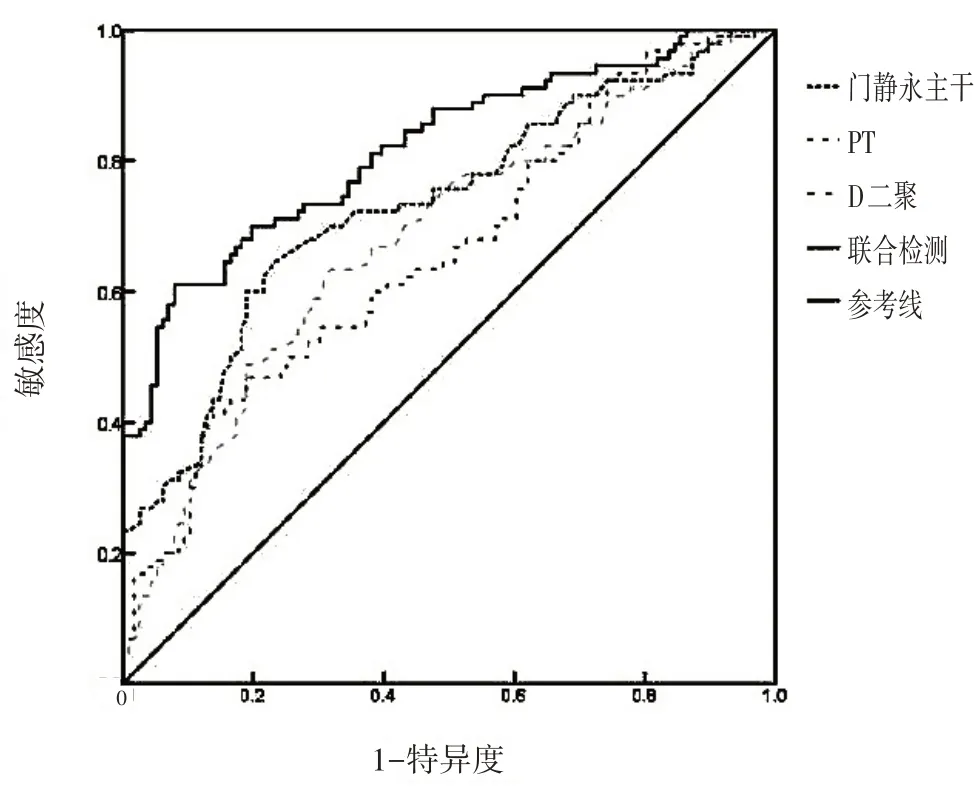
圖1 PT、D-二聚體、門靜脈主干直徑指標單獨檢測與聯合檢測診斷肝硬化PVT的ROC曲線
2.5 PT、D-二聚體、門靜脈主干直徑與肝硬化發生PVT關系情況
為了更進一步明確三項指標與肝硬化PVT 形成的關系,對在樣本醫院診斷為肝硬化的患者進行了隨訪,隨訪患者共86 人,診斷肝硬化時一項指標為陽性者共36 人,隨訪過程中發生PVT 共17人;兩項指標為陽性者共28人,隨訪過程中發生PVT 共19 人;3 項指標為陽性者共15 人,隨訪過程中形成PVT 共11 人;3 項指標均陰者共7 人,隨訪過程中形成PVT 共1 人;診斷肝硬化時各個指標不同表達狀態與后期PVT 的發生,差異有統計學意義(P<0.05)。診斷肝硬化時3 項指標均陽性的患者后期發生PVT的概率明顯高于3項指標均陰性的患者,見圖2。
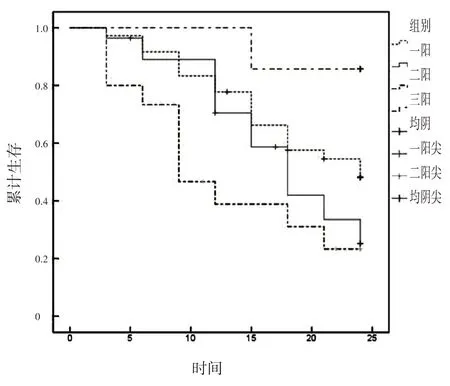
圖2 PT、D-二聚體、門靜脈主干直徑與肝硬化發生PVT關系情況
3 討論
肝硬化,特別是在肝硬化失代償階段,機體的凝血功能發生了復雜的改變,促凝物質的抗凝物質的改變,最終導致了出血或血栓形成[5]。有研究[6]表明,肝硬化患者發生PVT 的風險是非肝硬化患者的兩倍,PVT 在肝硬化患者中的發生機制目前尚未明確,PVT 的發生是一個涉及先天遺傳的和后天獲得的多因素共同作用的結果[7]。肝硬化和門靜脈高血壓引起的肝臟結構紊亂,門靜脈血流減緩,血管壁損傷,從而誘導高凝,在PVT 的發生過程中起著至關重要的作用[8]。因此,肝硬化不再被認為是一種血栓發生概率很小的疾病。
對肝硬化患者,腹部手術是導致局部血管損傷的最常見原因。在我國,脾切除術是一種處理門脈高壓并發癥常用的手術方法,有研究[9]表明,脾切除使PVT 發生的概率增加了10倍。但在本研究中,我們并沒有發現脾切除與PVT 的發生有明顯關系,這可能是因為入組的患者中行脾切除的患者過少。D-二聚體是一種纖維蛋白降解產物,通過增加纖維蛋白的形成和纖維蛋白的溶解而升高[10]。D-二聚體檢測已被廣泛應用于靜脈血栓栓塞的診斷,預測靜脈血栓栓塞的發生和復發,指導患者使用抗凝血藥物的持續時間。有研究[11]表明,D-二聚體作為內源性纖維蛋白解的標記物可以在PVT 患者中被檢測到,并可以預測疾病進展和預后。本研究證實了這一點,PVT組患者中D-二聚體明顯高于對照組。有研究[12]表明,在肝硬化的進程中,門靜脈的擴張是持續發展的,門靜脈的不斷擴張會引起血管內皮細胞的損傷,內皮細胞的損傷是血栓形成的關鍵因素之一。DONG[13]的研究表明,隨證門脈直徑的增加,PVT 發生的風險也在增加,門靜脈直徑>12.5 mm 對預測PVT 的發生有很高的敏感性。本研究同樣證實了隨著門靜脈直徑的增加,肝硬化PVT 發生的概率明顯增加,這可能是因為血管壁的損傷和門靜脈直徑增加導致門靜脈內血液流速降低所致。肖春桃等[4]的研究指出門靜脈內徑、脾臟厚度、糖尿病、肥胖、PT、纖維蛋白原、D-二聚體、AT-Ⅲ、血紅蛋白、脾切除史、硬化劑注射史、靜脈曲張程度、MELD 評分、Child-Pugh 評分等均可能與肝硬化患者PVT 的發生有關。本研究同樣把凝血酶原時間納入研究,通過多因素logistic 分析顯示,PT 是肝硬化PVT 發生的危險因素。
為了更好地評價PT、D-二聚體、門靜脈主干直徑對肝硬化PVT 形成的預測作用,本研究有對3 個指標進行了ROC 曲線分析,結果顯示三者聯合檢測對肝硬化PVT的發生具有一定的預測價值,其敏感度為0.61,特異度為0.92。為了更進一步地明確3 項指標與肝硬化PVT 形成的關系,本研究對診斷肝硬化時患者3 項指標不同表達狀態進行了生存分析,結果顯示診斷肝硬化時各個指標不同表達狀態與后期PVT 的發生有統計學意義,診斷肝硬化時3 項指標均陽性的患者后期發生PVT 的概率明顯高于3 項指標均陰性的患者。
本研究初步對肝硬化PVT 發生的危險因素進行了分析,發現PT、D-二聚體、門靜脈主干直徑是PVT 發生的危險因素,三者聯合檢測對PVT 的發生有一定的預測價值。本研究為單中心研究,入組樣本量有限,在后續的研究中我們會納入更多的患者,更全面的對PVT 發生的臨床因素進行分析,更好的服務臨床。

