火焰原子吸收分光光度法測定鋰含量的不確定度評定*
朱禮兵 龔 明 蘭書元 胡江峰 李紅妮
(1 江西省建筑衛生陶瓷質量監督檢驗中心 江西 高安 300800)
(2 江西建陶產業技術研究有限公司 江西 高安 330800)
鋰與人們的日常生活息息相關,小到筆記本電腦、手機、耳機,大到航空航天等產品都離不開鋰。鋰化物在陶瓷工業中應用廣泛,鋰質陶瓷相比于傳統陶瓷具有更加優異的耐急冷急熱性能。氧化鋰能降低釉面磚坯體的燒成溫度、提高坯體的機械強度、降低坯體的吸水率、減小坯體的熱膨脹系數等;氧化鋰具有極強的助熔作用,能有效降低釉料及微晶玻璃的始熔溫度、熔化溫度,降低釉料及微晶玻璃的粘度等[1]。
不確定度是與測量結果相關聯的數據,它表征了可以合理地賦予被測量的量值分散程度。測量不確定度的大小,可以說在一定程度上反映出實驗室的測量能力水平。筆者結合實際工作經驗,對原子吸收光譜法測定鋰含量的不確定度進行了研究,建立了鋰含量計算的數學模型,分析了測量不確定度的主要來源。根據GB/T 14506.15-2010硅酸鹽巖石化學分析方法第15部分:鋰量測定,參照化學分析中不確定度的評估指南方法,對影響鋰含量合成不確定度的測量重復性、鋰標準溶液、標準溶液稀釋、待測樣品溶液中鋰濃度和樣品質量稱量等不確定度分量進行了評定。
1 實驗
1.1 主要儀器
電子天平,型號BSA224S;火焰原子吸收分光光度計,北京瑞利分析儀器有限公司,型號WFX-210。
1.2 主要試劑
1000μg/m L鋰元素標準溶液(GSB 04-1734-2004;國家有色金屬及電子材料分析測試中心)、用水為超純水、氫氟酸、濃硫酸、鉀鹽溶液。
1.3 試驗方法
將待測樣品在(105±5)℃烘箱中預干燥2~4 h,置于干燥器中冷卻至室溫。稱取(0.500 0±0.000 1)g樣品,放入聚四氟乙烯坩堝中,用水濕潤,加入1 m L濃硫酸(1+1),10~15 m L氫氟酸,置于電熱板(350~380℃)上加熱分解,消解完全,取下冷卻,移入盛有鉀鹽溶液的50 m L 容量瓶中,加水稀釋至刻度處,并搖勻備用。與校準溶液系列同時測量。必要時對定容好的樣品溶液進行適當的稀釋,確保待測樣品溶液中鋰含量在標準曲線范圍內[2]。
2 數學模型
計算的結果以質量分數w(Li)計,數值以μg/g來表示:
式中:f——樣品溶液稀釋倍數,未稀釋時,f取1;C——從校準曲線上測定的待測樣品溶液中鋰的濃度,μg/m L;V——樣品溶液的體積,m L;m——稱量樣品的質量,g。分析結果表示到小數點后第一位。
3 不確定度的主要來源
根據實際測量過程,并結合數學模型進行分析,鋰含量測量不確定度主要來源于測量重復性、鋰標準溶液、標準溶液稀釋、待測樣品溶液中鋰濃度、樣品質量稱量[3]。
4 不確定度各分量的評定
4.1 測量重復性引入的不確定度Urel(S)
在相同實驗條件下獨立重復測量待測樣品溶液共10次,測量結果見表1。根據試樣測定結果,可計算樣品鋰濃度的平均值w 和標準偏差S[4]。

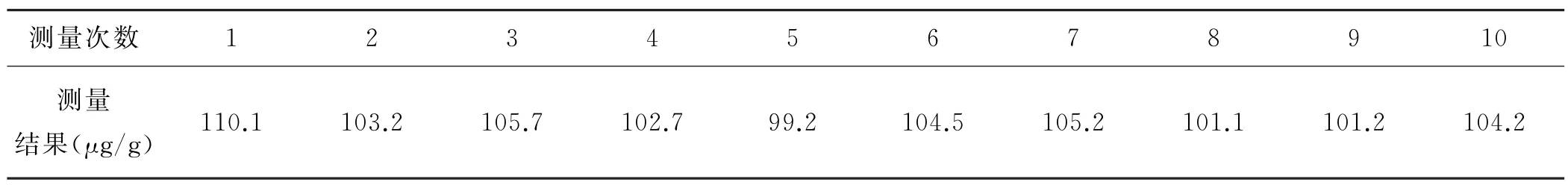
表1 測量結果
4.2 鋰標準溶液的不確定度Urel(標)
本次測量采用的鋰標準溶液為國家有色金屬及電子材料分析測試中心的1 000μg/m L,其相對擴展不確定度(k=2)為0.7%,其相對標準不確定度Urel(標)=0.7%/2=0.35%
4.3 標準溶液配制稀釋過程引入的不確定度Urel(稀釋)
用1 m L 移液管分取1 000μg/m L 的鋰標液,并用100 m L容量瓶定容,稀釋為10μg/m L,將其作為工作溶液,配置濃度為0、0.5μg/m L、1μg/m L、1.5 μg/m L、2μg/m L、2.5μg/m L 的標準溶液。因分取溶液與配制各標準溶液在同一時刻、同一溫度,故不考慮溫差帶來的不確定度;由于配制標準溶液的過程各溶液稀釋在同體積的容量瓶中,故可認為各容量瓶的體積誤差、稀釋重復性的不確定度包含在工作曲線變動中,不需要再進行評定。根據表2和表3計算配制工作溶液和各標準溶液產生的相對標準不確定度。
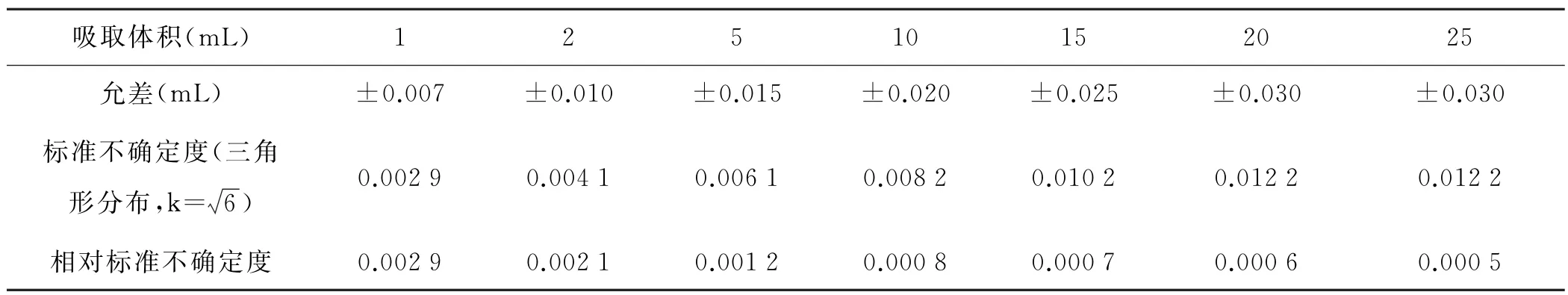
表2 吸取體積相對標準不確定度

表3 定容體積相對標準不確定度
4.4 待測樣品溶液中鋰濃度的不確定度Urel(C)[5]
待測樣品溶液中鋰濃度是根據標準曲線獲得的,所以鋰濃度的不確定度應也根據標準曲線回歸方程進行評定。一般工作曲線回歸方程可表示為A=b·C+a,其中A 為樣品溶液吸光度值,C 為待測樣品鋰元素濃度(μg/m L),b為斜率,a為截距。鋰濃度計算公式為C=(A-a)/b。


(2)配制各標準溶液產生的相對標準不確定度:

分別對6種濃度的鋰標準溶液進行3次測定,得到相應的吸光度值,采用最小二乘法進行擬合,得到標準曲線的線性回歸方程,測定原始數據見表4。根據表4數據分別計算出斜率b、截距a、線性相關系數r和相關指數R2,得到標準曲線的回歸方程為A=0.091 7·C+0.000 7,r=0.999 2,R2=0.998 3,鋰標準溶液的標準曲線見圖1。由標準曲線擬合引入的待測樣品溶液中鋰濃度的標準不確定度U(C)計算公式:

圖1 鋰標準溶液的標準曲線

表4 6種鋰標準溶液的測定結果
其中:p——待測樣品溶液測試次數,取10;
n——各鋰標準溶液測試次數,取18;
C——待測樣品溶液鋰濃度,取1.037μg/m L(樣品溶液稀釋了100倍);
Ci——各鋰標準溶液測試時的鋰濃度。
所以,待測樣品溶液中鋰濃度的相對標準不確定度:
Urel(C)=U(C)/C=0.015 2/1.037=1.47%
4.5 樣品質量稱量的不確定度Urel(m)




5 合成不確定度
由于不確定度各分量互不相關,相互獨立,因此合成相對標準不確定度:

6 擴展不確定度
采用置信概率為95%(k=2)時,則擴展不確定度U=k×U(w)=2×1.88=3.76μg/g。所以,此樣品鋰含量測試結果為w=(103.7±3.8)μg/g(k=2)。
7 結果分析
通過對火焰原子吸收分光光度法測定鋰含量不確定度的分析,鋰含量不確定度核算表見表5,不確定度分量排序圖見圖2,其結果表明:

圖2 鋰含量不確定度分量排序圖
(1)樣品溶液中鋰濃度和測量重復性引入的不確定度分量對合成不確定度影響最大,其次是鋰標準溶液和標準溶液稀釋引入的不確定度,而樣品質量稱量幾乎對不確定度無影響。
(2)樣品溶液中鋰濃度引入的不確定度是根據標準曲線的回歸方程進行評定的,可通過合理設計鋰標準溶液濃度梯度和范圍,使樣品溶液濃度在標準曲線的中間位置;同時適當增加標準曲線點數和測量次數,來提高標準曲線的可靠性和相關性。而對于測量重復性引入的不確定度,則需要適當增加平行測定的次數。
(3)對于標準溶液引入的不確定度,需要合理選擇標準物質來控制,盡量選擇權威機構提供的,有準確定值和較小不確定度的有證標準物質。
(4)在日常試驗中,注意儀器設備的維護保養,使其保持最佳狀態;并且加強對人員的技能培訓和實操訓練,也是降低測量不確定度的有效途徑。

