抑乳調經顆粒對奧氮平在大鼠體內藥動學的影響 Δ
鄭暉暉,周龍玥,趙博欣,王春霞 (南方醫科大學南方醫院藥學部,廣州 510080)
精神分裂癥是一種慢性精神障礙,屬于重性精神疾病,嚴重影響患者的正常生活。精神障礙的發病機制較為復雜,且病程較長,患者需要長期服藥控制病情[1]。然而長期服用抗精神病藥物,會導致患者出現糖脂代謝異常、體重增加、泌乳素異常升高等副作用,進而給患者帶來更大的危害[2]。
奧氮平(olanzapine,OLZ)是一種二苯丁基哌啶類藥物,該藥不僅對精神分裂癥有較好的治療效果,還能改善患者認知功能[3]。臨床實踐發現,服用OLZ后,患者的泌乳素水平在1~2 周內迅速上升,并達到峰值,而長期服藥后泌乳素水平會逐漸穩定甚至出現下降,但仍明顯高于正常值,最終導致高泌乳素血癥[4—5]。抑乳調經顆粒(Yiru tiaojing granules,YRTJ)是南方醫科大學南方醫院的院內制劑(粵藥制字Z07022807),經過近20年臨床研究證實,其治療高泌乳素血癥療效較好[6]。該方以張仲景《傷寒論》的芍藥甘草湯(白芍、甘草)為基礎,加用巴戟天和仙茅而成。方中巴戟天歸腎、肝二經,可補腎壯陽,兼養精血,為君藥;仙茅補腎脾之陽,強肝健筋散寒,助巴戟天溫補腎肝,為臣藥;白芍入肝、脾二經,甘草味甘性平、調和諸藥,兩者共為佐使藥。本課題組前期研究發現,YRTJ可以治療由OLZ引起的高泌乳素血癥,但YRTJ 是否會影響OLZ 的藥動學過程尚不清楚。為此,本研究采用液相色譜-質譜(liquid chromatographymass spectroscopy,LC-MS)技術測定了大鼠血漿中OLZ濃度,考察了YRTJ對OLZ在大鼠體內藥動學的影響,旨在為臨床合理用藥提供依據。
1 材料
1.1 主要儀器
本研究所用主要儀器包括Agilent 1260 液相色譜-G6460 三重四極桿質譜聯用儀(美國Agilent 公司)、XW-80A 型旋渦混合器(海門市其林貝爾儀器制造有限公司)、Milli-Q 超純水純化系統(美國Millipore 公司)、5810R型高速冷凍離心機(德國Eppendorf公司)。
1.2 主要藥品與試劑
OLZ 對照品(批號O830525,純度≥98%)購自上海麥克林生化科技股份有限公司;奧氮平-d3 對照品(內標,批號B71387,純度≥98%)購自上海源葉生物科技有限公司;YRTJ(批號20220413,規格10 g/袋)由南方醫科大學南方醫院藥學部提供;肝素鈉溶液(批號M052787)購自北京邁瑞達科技有限公司。
1.3 動物
SD大鼠24只,雌性,6~8周齡,體重180~200 g,購自珠海百試通生物科技有限公司[動物質量合格證明號:44822700014688;實驗動物生產許可證號:SCXK(粵)2020-0051]。所有大鼠于標準環境下適應性飼養1周。動物實驗符合南方醫科大學南方醫院實驗動物倫理委員會的有關規定及要求(倫理證號:NFYY-2022-0316)。
2 方法與結果
2.1 色譜與質譜條件
2.1.1 色譜條件
以Agilent Poroshell EC-C18(50 mm×3.0 mm,2.7 μm)為色譜柱;以0.1%甲酸的乙腈溶液(A)-5 mmol/L甲酸銨溶液(B)為流動相進行梯度洗脫(0~0.5 min,95%B;0.5~1.7 min,50%B;1.7~2.5 min,5%B;2.5~5 min,95%B);流速為0.5 mL/min;進樣量為5 μL。
2.1.2 質譜條件
采用電噴霧正離子源,掃描方式為多反應監測(multiple reaction monitoring,MRM);毛細管電壓為4 000 V;噴霧氣壓力為40 psi;干燥氣體流速為10 L/min;干燥氣體溫度為340 ℃。用于定量分析的離子對(m/z)分別為313→256.1(OLZ)、316.1→87.2(內標)。
2.2 溶液的制備
2.2.1 對照品溶液的制備
精密稱取OLZ 對照品2.5 mg,加入甲醇溶解,并定容至25 mL 容量瓶中,制成質量濃度為0.1 mg/mL 的OLZ 溶液。取上述OLZ 溶液,加入甲醇稀釋,制成質量濃度為500 μg/mL 的OLZ 儲備液;臨用時,用甲醇稀釋成所需質量濃度的對照品溶液。
2.2.2 內標溶液的制備
精密稱取內標對照品2.5 mg,加入乙腈溶解,并定容至25 mL容量瓶中,制成質量濃度為0.1 mg/mL 的內標儲備液。取上述內標儲備液,加入甲醇稀釋,制成質量濃度為250 ng/mL的內標溶液。
2.3 血漿樣品的處理
取血漿樣品50 μL,置于1.5 mL 的EP 管內,加入“2.2.2”項下內標溶液100 μL,快速旋渦振蕩1 min,以14 000 r/min離心15 min,取5 μL上清液進樣分析。
2.4 方法學考察
2.4.1 專屬性考察
分別取不同來源的大鼠空白血漿、空白血漿+OLZ(質量濃度為500 ng/mL)、大鼠單次給藥后1 h的血漿樣品各50 μL,分別按“2.3”項下方法處理(其中空白血漿不加內標溶液),再按“2.1”項下條件進樣分析,記錄色譜圖。如圖1所示,OLZ及內標在分析物保留時間處均無雜質干擾,空白血漿中的內源性物質不干擾OLZ及內標的測定,表明本方法專屬性較好。

圖1 空白血漿、空白血漿+OLZ、大鼠給藥后血漿樣品的MRM色譜圖
2.4.2 線性關系及定量下限考察
取大鼠空白血漿,加入“2.2.1”項下對照品溶液,制成OLZ 質量濃度分別為5、50、150、300、500、750、1 000 ng/mL 的質控樣品,按“2.3”項下方法處理后,再按“2.1”項下條件進樣分析,記錄峰面積。以OLZ質量濃度為橫坐標(x)、OLZ 與內標峰面積比值為縱坐標(y),采用加權最小二乘法作回歸分析。結果顯示,OLZ的回歸方程為y=0.006x(R2=0.993 2),表明OLZ在5~1 000 ng/mL范圍內呈良好的線性關系。定量下限為5 ng/mL。
2.4.3 基質效應與提取回收率考察
將不同來源的大鼠空白血漿,按“2.3”項下方法處理后,加入“2.2.1”項下對照品溶液,制成低、中、高質量濃度(10、500、750 ng/mL)的樣品,每個質量濃度樣品平行制備6 份,再按“2.1”項下條件進樣分析,記錄峰面積為A。分別制備OLZ和內標質量濃度與前者一致的標準溶液,按“2.1”項下條件進樣分析,記錄峰面積為B。按“2.4.2”項下方法制備OLZ 質量濃度與前者一致的質控樣品,每個質量濃度樣品平行制備6 份,按“2.3”項下方法處理后,再按“2.1”項下條件進樣分析,記錄峰面積為C。按以下公式計算基質效應和提取回收率:基質效應(%)=A/B×100%,提取回收率(%)=C/A×100%。結果見表1。由表1 可知,低、中、高質量濃度樣品的基質效應為70.56%~82.43%,RSD 不超過3.52%(n=6);OLZ 的平均提取回收率為86.71%~93.65%、RSD 不超過2.79%(n=6),內標的平均回收率為91.56%、RSD 為1.57%(n=6),均符合生物樣品定量分析方法要求。
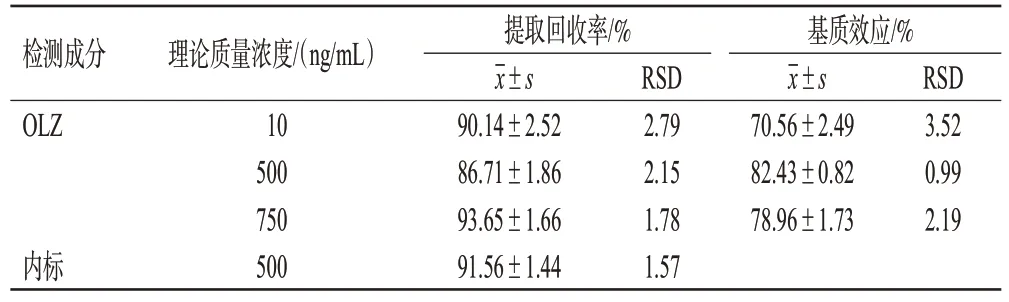
表1 基質效應與提取回收率結果
2.4.4 精密度與準確度考察
按“2.4.3”項下方法制備OLZ 質量濃度分別為5、10、500、750 ng/mL(定量下限及低、中、高質量濃度)的質控樣品,按“2.3”項下方法處理后,再按“2.1”項下條件進樣分析。每個分析批平行操作5 個樣品,連續操作3個分析批,再根據同批隨行回歸方程計算OLZ的實際質量濃度,考察批內、批間精密度。將實際質量濃度與理論質量濃度進行比較,以相對誤差(relative error,RE)考察準確度,結果見表2。由表2 可見,OLZ 的批內、批間RSD 均不超過7.69%,RE 為-3.11%~3.05%,均符合生物樣品定量分析方法要求。
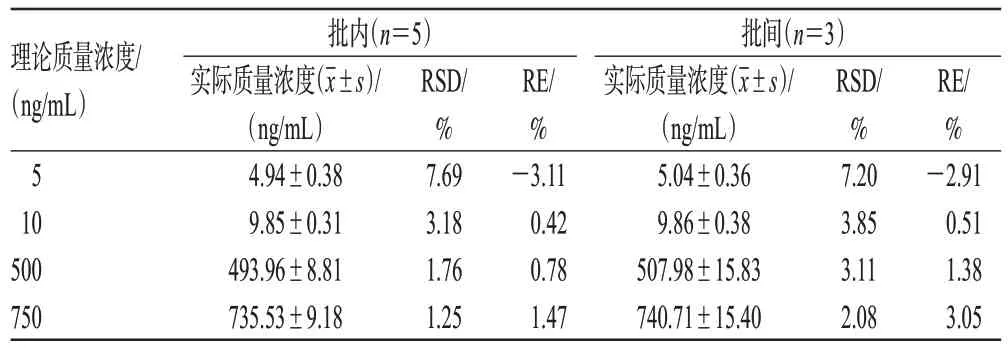
表2 精密度與準確度考察結果
2.4.5 穩定性考察
按“2.4.3”項下方法制備OLZ 質量濃度分別為10、500、750 ng/mL(低、中、高質量濃度)的質控樣品,每個質量濃度樣品平行制備6份,考察室溫(25 ℃)放置8 h、凍融(-80 ℃~室溫)循環3 次、4 ℃冰箱中存放24 h、-80 ℃冷凍1個月的穩定性。結果顯示,各樣品在上述條件下的RSD均不超過8.62%(n=6),表明樣品穩定性良好。
2.5 藥動學實驗
2.5.1 給藥劑量的確定
根據現有的研究及美國FDA藥量轉換原則,大鼠灌胃OLZ 劑量一般為2~20 mg/kg,但由于10 mg/kg 以上的劑量會使大鼠出現明顯的鎮靜效果,且根據本課題組前期研究結果,故將大鼠灌胃OLZ 的劑量設定為5 mg/kg[7]。YRTJ 臨床使用中按每人每天2 次、每次1 袋、每袋10 g 計,參照FDA 藥量轉換原則及本課題組前期藥理毒理學研究結果,將大鼠灌胃YRTJ 的劑量設定為0.972 g/kg。
2.5.2 單劑量給藥實驗
將SD 大鼠隨機分為A 組和B 組,每組6 只,給藥前所有大鼠禁食12 h,自由飲水。A 組大鼠灌胃OLZ(5 mg/kg);B 組大鼠先灌胃OLZ(5 mg/kg),1 min 后再灌胃YRTJ(0.972 g/kg)。分別在給藥前及給藥后5、15、30 min和1、2、3、6、8、12、24 h于大鼠眼眶靜脈叢采血約0.2 mL,置于肝素化的EP管中,于4 ℃、3 000 r/min離心10 min,取上層血漿,保存于-20 ℃冰箱中,待測。
2.5.3 多劑量給藥實驗
將SD大鼠隨機分為C組和D組,每組6只。C組大鼠灌胃OLZ(5 mg/kg);D組大鼠先灌胃OLZ(5 mg/kg),1 min 后再灌胃YRTJ(0.972 g/kg)。兩組均每天給藥1次,連續給藥14 d。其余操作同“2.5.2”,給藥后采血時間為末次給藥后。
2.5.4 數據處理
取不同時間點的血漿樣品,按“2.3”項下方法處理后,再按“2.1”項下條件進樣分析,記錄峰面積,根據隨行的回歸方程計算OLZ濃度。采用GraphPad Prism 9.0軟件進行數據分析并作圖,數據以±s表示,以獨立樣本t檢驗進行組間比較,檢驗水準α=0.05。采用DAS 2.0軟件,選擇合適的數學模型擬合,計算藥動學參數。藥-時曲線見圖2,藥動學參數見表3。由表3 可知,在單劑量給藥中,與A 組比較,B 組大鼠24 h 內的藥-時曲線下面積(area under the concentration-time curve within 24 h,AUC0-24h)、AUC0-∞、峰濃度(maximum concentration,cmax)均顯著降低(P<0.05),24 h 內的平均滯留時間(mean resident time within 24 h,MRT0-24h)、MRT0-∞、表觀清除率(apparent clearance,CLz/F)均顯著延長(P<0.05);在多劑量給藥中,C 組與D 組大鼠的藥動學參數比較,差異均無統計學意義(P>0.05)。
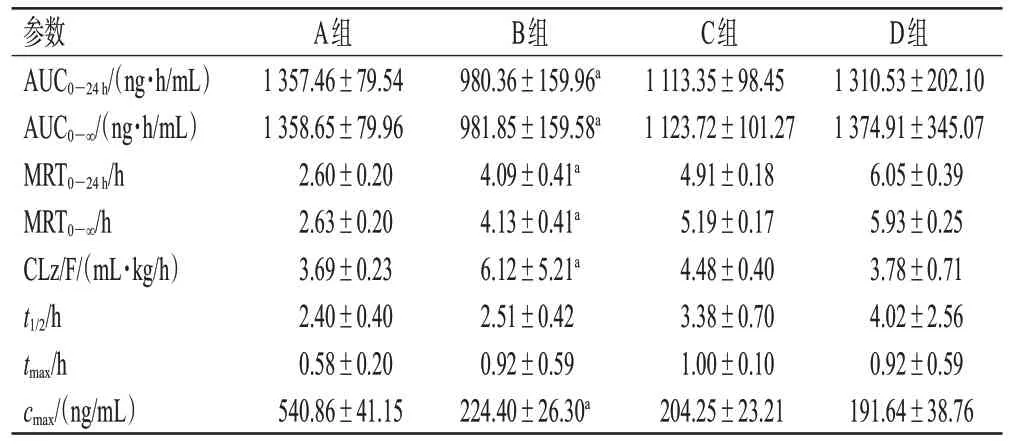
表3 大鼠體內OLA的藥動學參數(n=6)
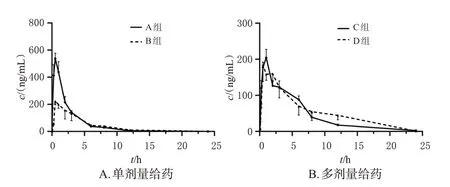
圖2 各組大鼠的藥-時曲線圖(n=6)
3 討論
人們在日常生活中通常會同時或先后序貫服用兩種及以上藥物。一方面是出于治療需要,另一方面是為了增加療效,減少藥物毒副作用。但是服用兩種及以上藥物容易引起藥物之間的相互作用,而導致其中一種或多種藥物的藥效或毒性發生改變[8]。其中,體內藥動學的改變是最常見的原因,藥物之間通過影響其體內的吸收、分布、代謝、排泄,從而導致血藥濃度發生改變,進而影響藥物療效,甚至產生毒副作用[9—10]。近年來,中西藥聯用已經成為一種常見的疾病治療手段。合理的中西藥聯用可以增強藥物療效、減少藥物不良反應,反之則會影響藥物療效。由于中藥成分復雜,可能存在多種相互反應,從而影響化學藥的療效。因此,藥動學研究成為了探討中西藥相互作用的一個重要手段。
本研究初步探討了YRTJ對OLZ在大鼠體內藥動學的影響,結果顯示,各組大鼠OLZ的tmax均小于2 h,這與文獻報道一致[11]。在單劑量給藥中,與單用OLZ 比較,OLZ 與YRTJ 聯用后OLZ 的AUC0-24h、AUC0-∞、cmax均顯著降低,MRT0-24h、MRT0-∞、CLz/F 均顯著延長,說明YRTJ 可能會降低OLZ 的吸收;但在多劑量給藥中,YRTJ對OLZ在大鼠體內的藥動學參數無明顯影響。
單劑量給藥與多劑量給藥的藥動學參數結果存在差異,其原因可能是中藥含有多種成分。中藥復方制劑的化學成分復雜,在與其他化學藥聯用時,可能其中的有效單體成分會影響化學藥在體內的吸收、分布、代謝和排泄。當單劑量給藥時,YRTJ 對OLZ 的藥動學過程可能產生了直接作用,從而導致了較大的藥動學差異;而多劑量給藥時,YRTJ 對OLZ 的藥動學過程可能是一個長期多方面的調節,從而導致藥動學參數差異不大。
對于OLZ 來說,單次給藥的大鼠模型存在許多缺陷,一是僅單次給藥容易造成體內血藥濃度的大幅度波動[12];二是對于精神病患者來說,需要長期服用抗精神病藥物治療,單次給藥無法模擬臨床上的穩態濃度[13]。以上結果提示,多劑量給藥更為合理。
綜上所述,單次聯用YRTJ 會抑制OLZ 在大鼠體內的吸收,長期聯用YRTJ 對OLZ 的藥動學過程無明顯影響。

