阿米卡星在老年腎功能不全患者中生理藥動學模型的建立與應用 Δ
李喬希 ,管宴萍 ,夏 晨 ,吳莉莉 ,王 妍 (.佛山市第一人民醫院藥學部,廣東 佛山 58000;.中山大學藥學院臨床藥理研究所,廣州 50030)
阿米卡星是一種氨基糖苷類抗菌藥物,在臨床上被廣泛用于治療由革蘭氏陰性病原菌引起的細菌感染,對銅綠假單胞菌等常見多藥耐藥菌也有較好的抗菌效果[1]。阿米卡星作為一種濃度依賴性抗菌藥物,其體內抗菌效果取決于藥動學-藥效學指標,即血藥峰濃度(cmax)與最小抑菌濃度(MIC)之比[2]。腎毒性是阿米卡星最常見的嚴重不良反應之一,這與其在腎小管中出現飽和性蓄積有關[3],通常認為穩態谷濃度<4 μg/mL有利于降低其腎毒性的發生風險[2]。因此,每日1次的給藥方案有助于增強阿米卡星的抗菌效果,減少腎毒性的發生[4]。
阿米卡星的體內藥動學過程具有較大的個體間差異,易受患者年齡、體重、腎功能水平等多種因素影響[1],同時由于阿米卡星的治療窗較窄且不良反應較嚴重,所以開展精準用藥以保證其臨床療效和避免毒性反應發生就顯得非常重要。阿米卡星在體內主要經腎排泄,腎功能水平是影響阿米卡星體內暴露的最主要因素,因此根據血肌酐水平調整阿米卡星給藥方案較為常見。老年人因身體機能衰退和免疫功能低下,是住院患者中抗菌藥物使用最廣泛的特殊人群之一。由于受衰老和基礎疾病等因素影響,老年人的解剖學和生理學特征與中青年人存在一定差異,因此有必要根據藥物在老年患者體內的藥動學過程來調整給藥方案[5]。
生理藥動學(physiologically-based pharmacokinetic,PBPK)模型是一種以人體的解剖學和生理學特征為基礎,結合藥物的理化性質和生物化學過程建立的一種用于描述和模擬藥物體內藥動學過程的數學模型[6]。近年來,PBPK 模型已被廣泛用于藥物研發和臨床應用的各個領域,特別是預測藥物在特殊人群體內的藥動學過程方面。采用PBPK 模型模擬的方法,根據已有臨床研究數據,對部分關鍵解剖學和生理學參數進行調整,能預測未報道的特殊人群用藥后的體內暴露情況[6],可為臨床精準用藥提供有效信息和安全保障。基于此,本研究建立了阿米卡星在老年腎功能不全患者體內的PBPK模型,估算其暴露情況,從有效性和安全性兩方面對模擬的給藥方案進行評價,旨在為阿米卡星在老年腎功能不全患者中的臨床合理用藥提供參考。
1 材料
1.1 軟件工具
使用PK-SIM?軟件(version 11,Bayer Technology Services)實現PBPK 模型的構建、擬合和模擬。使用Graph Grabber 軟件(version 2.0.2,Steven Benbow)獲取已發表文獻中的藥時曲線等數據。使用PkanalixTM軟件(version 2021R2,Lixoft)的非房室模型功能計算文獻數據或模擬數據的藥動學參數。使用R語言軟件(version 4.1.2)及相關軟件包實現圖像的制作、編輯及用單因素方差分析結合事后檢驗進行多組數據間的統計比較。
1.2 資料來源
檢索DrugBank數據庫以獲取阿米卡星的理化性質參數。以“阿米卡星”“藥動學”“老年”“腎功能不全”“amikacin”“pharmacokinetic”“elderly”“renal impairment”為中英文關鍵詞,檢索PubMed、Google scholar、Web of Science、中國知網等學術引擎,獲取成人體內藥動學特性參數以及模型驗證所需的臨床藥動學數據。排除人口學資料欠缺、給藥方案模糊、藥時曲線缺失、給藥方案重復的研究,將收集到并應用于模型建立和驗證的臨床藥動學研究整理匯總(表1)。
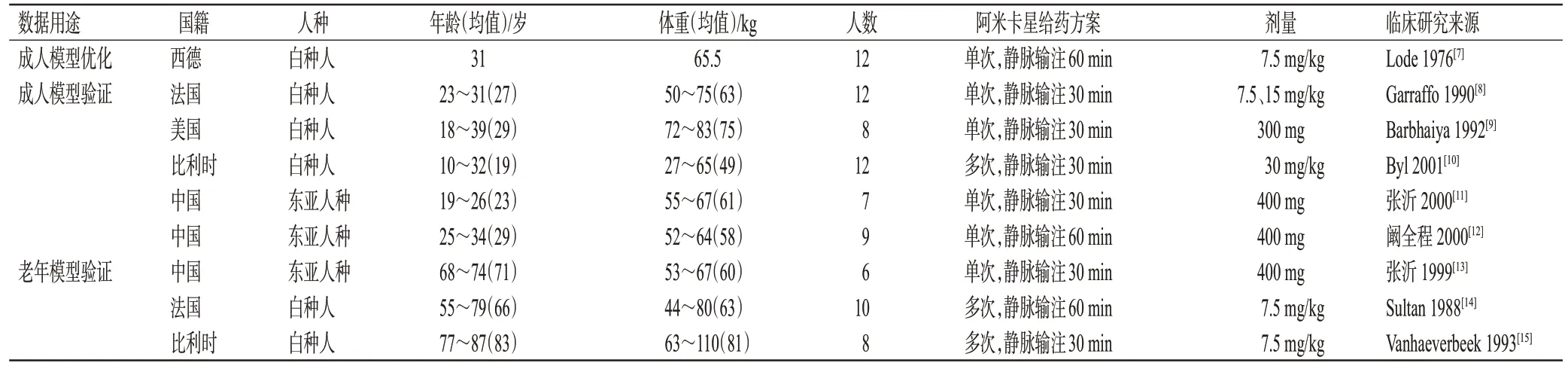
表1 阿米卡星PBPK模型建立與驗證中使用的臨床藥動學研究
2 方法
2.1 PBPK模型研究流程
首先,輸入阿米卡星理化性質參數(如脂水分配系數)和體內藥動學特性參數(如腎小球濾過比例),建立靜脈輸注阿米卡星在成人體內的PBPK模型并根據臨床研究數據進行參數優化。其次,固定理化性質參數和藥動學特性參數設置,將成人模型外推至老年腎功能正常和腎功能不全患者。將模擬得到的數據與真實臨床研究數據進行比較,對模型預測性能進行驗證。最后,使用最終模型模擬老年不同程度腎功能不全患者靜脈輸注阿米卡星臨床常用劑量后的血藥濃度數據,對安全性和有效性進行評估。
2.2 成人PBPK模型建立與驗證
根據查詢資料所得的理化性質參數和藥動學特性參數初始值(表2),建立阿米卡星的“化合物”模塊。使用PK-SIM?軟件內置的成人模型描述阿米卡星在成人體內的分布情況,該模型包含18 個組織器官形成的隔室,隔室之間由動靜脈血液循環連接,組織分配系數和細胞膜滲透性使用默認的“PK-SIM standard”算法計算。由于阿米卡星在健康人體內主要經腎小球濾過消除,剩余約10%通過非腎途徑消除[7],故使用腎小球濾過模型(公式1)和非腎的全身清除模型組合描述阿米卡星的體內消除過程(公式2):
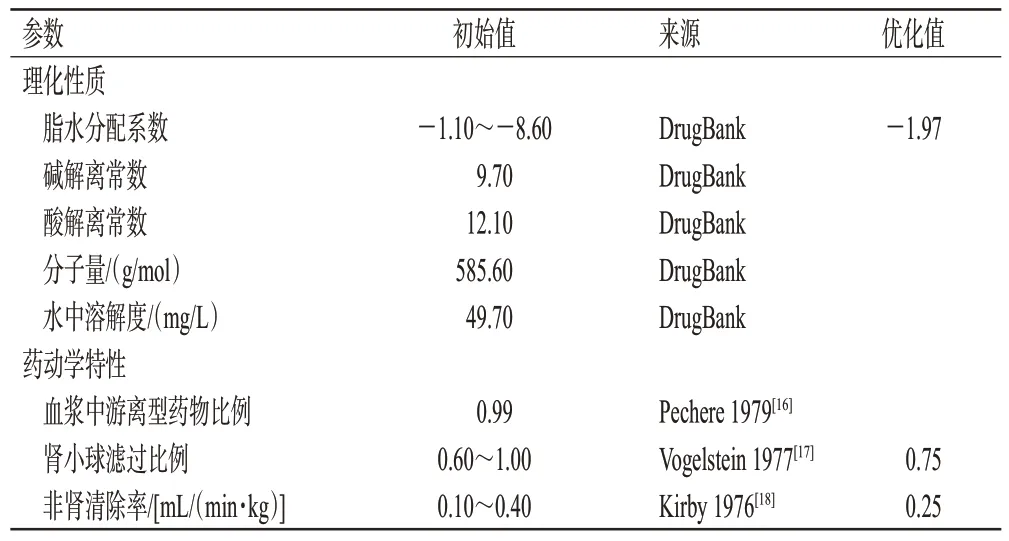
表2 阿米卡星PBPK模型建立中化合物相關參數
其中,GFR為腎小球濾過率;fu為血漿中游離型藥物比例;fGFR為腎小球濾過比例,該值用以量化藥物在腎小管重吸收或主動分泌對濾過性清除的影響;CLrenal為腎清除率;CLnon-renal為非腎清除率;CLtotal為總清除率。
在“人口模型構建”模塊中輸入表1中成人藥動學研究的人口學資料信息,建立成人個體和群體模型。根據成人藥動學研究的給藥方案,模擬生成血藥濃度數據,并對表2中的部分參數進行擬合優化,得到阿米卡星在成人體內的PBPK模型。
將模擬給藥個體模型的血藥濃度預測值(Cpre)與觀測值(Cobs)進行比較,生成擬合優度圖,Cpre與Cobs誤差應在2 倍范圍以內[19]。按公式3 計算相對殘差,以評估模型的準確性,若相對殘差絕對值<30%,說明模型預測準確性較好[20]。同時,比較各模擬場合下藥動學參數的預測值(Ppre)與觀測值(Pobs)的一致性,按公式4計算平均折疊誤差(mean fold error,MFE),以評估模型的預測性能,若0.5<MFE<2,則說明模型預測性能良好[21]。
2.3 老年患者模型的外推與驗證
通過PK-SIM?軟件中內置的年齡相關性算法調整解剖學和生理學參數,輸入表1中老年患者藥動學研究的人口學資料信息,建立老年患者個體和群體模型。隨后,輸入優化后的成人模型化合物相關參數,外推生成阿米卡星在老年患者體內的PBPK 模型,使用老年腎功能正常患者[13]、老年腎功能不全患者[15]及重癥監護室(ICU)老年患者[14]的臨床藥動學數據對模型進行驗證。
2.4 老年腎功能不全患者給藥方案評價
將“人口模型構建”模塊中的疾病狀態由“健康”更改為“慢性腎病(chronic kidney disease,CKD)”,GFR 范圍設置為60~89(CKD2 期)、45~59(CKD3a期)、30~44(CKD3b 期)、15~29(CKD4 期),單位為mL/(min·1.73 m2),建立老年輕度至重度腎功能不全患者群體模型(年齡65~85歲,數量200人,男女各50%)。模擬靜脈輸注阿米卡星治療革蘭氏陰性菌感染情況下患者的穩態血藥濃度。給藥劑量為5、7.5、10、15、20 mg/kg,給藥間隔為24、36、48 h,輸注時間為30 min。對給藥后60 min的cmax和下一次給藥前的谷濃度進行統計分析[2]。以cmax/MIC≥8作為抗菌效果的藥效指標,穩態谷濃度<4 μg/mL 作為避免腎毒性風險的安全指標[1—2]。計算各模擬場合下的目標達成率(probability of target attainment,PTA),預期目標為PTA≥90%。
3 結果
3.1 阿米卡星成人PBPK模型
根據一項成人的臨床藥動學研究[7]建立個體模型,并利用靜脈輸注阿米卡星后的藥時曲線和尿藥排泄數據,對脂水分配系數、fGFR、CLnon-renal進行擬合優化,優化后的參數值見表2,擬合的藥時曲線見圖1。由圖1 可知,建立的阿米卡星成人PBPK模型可較好地對觀測數據進行擬合,且能較準確地描述阿米卡星在成人體內的藥動學過程。本次擬合中cmax和從0 到無窮大時間的藥時曲線下面積(area under the concentration-time curve within infinite time,AUC0-∞)的MFE分別為0.83和0.92。
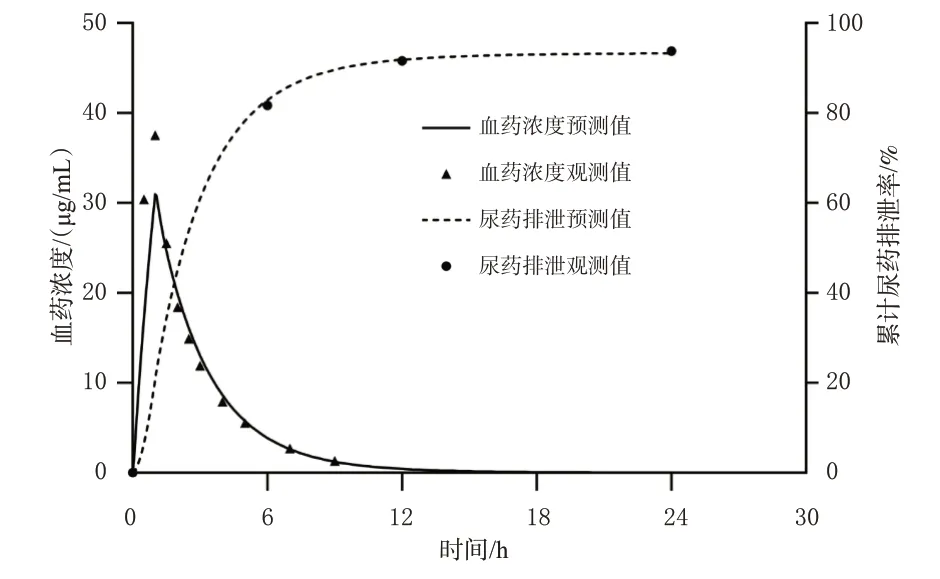
圖1 單次靜脈輸注7.5 mg/kg 阿米卡星后藥時曲線和尿藥排泄率的預測值與觀測值
隨后,根據6 項成人臨床藥動學研究中的數據[8—12],分別建立對應的個體和群體模型,通過外部數據驗證的方式對模型預測性能進行評估。結果顯示,56個觀測值中位于預測值90%置信區間的比例>80%(圖2);約95%的預測值位于觀測值2 倍誤差范圍內(圖3A);僅6個濃度點相對殘差超過±50%,位于±30%區間的濃度點比例>80%,相對殘差絕對值均數為25%(圖3B)。所有參數的MFE 均在>0.5~<2 范圍內(表3)。以上結果說明,模型具有較好的預測性能,可以較準確地預測不同給藥方案下阿米卡星的血藥濃度數據。
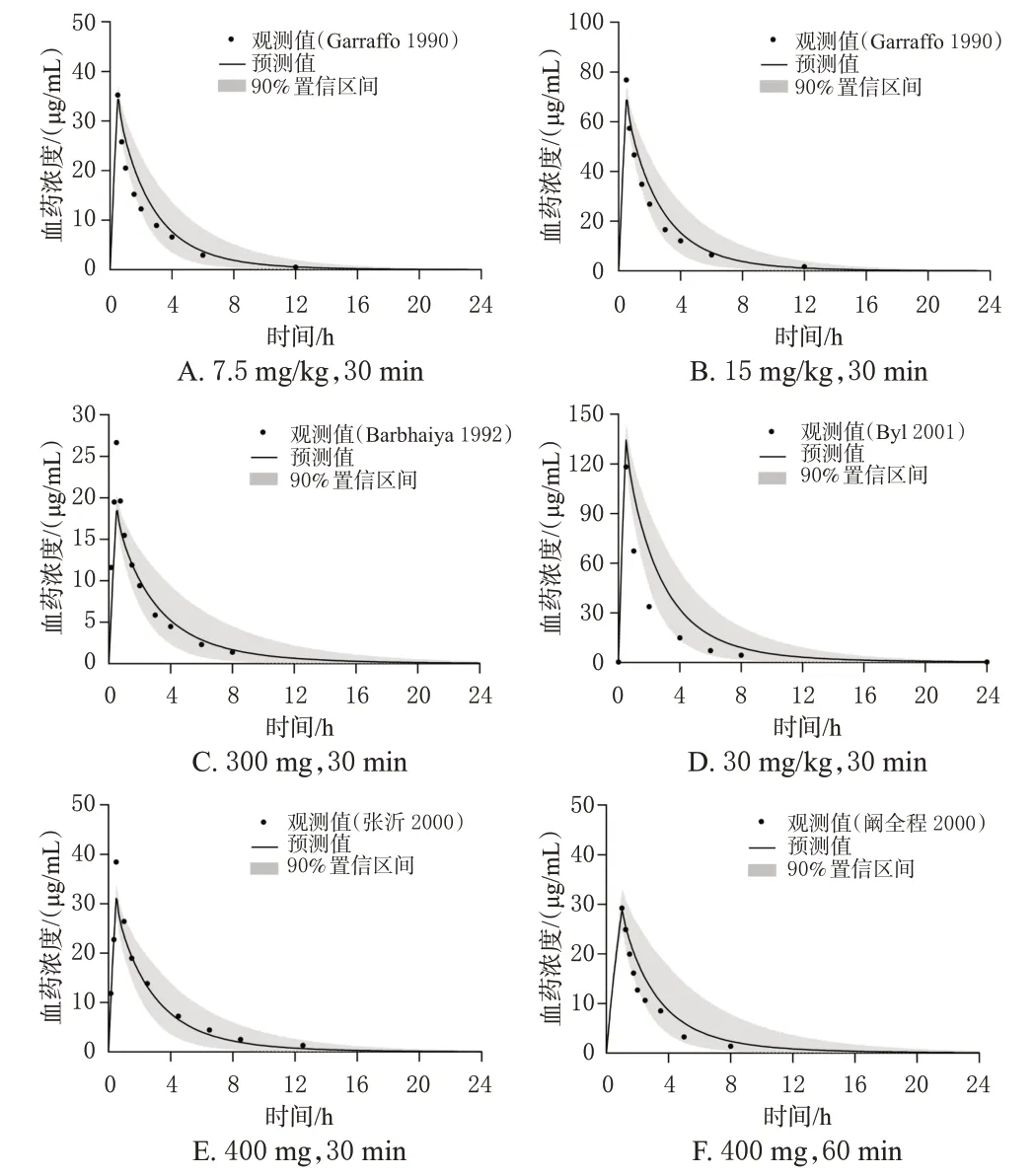
圖2 成人靜脈輸注不同劑量阿米卡星后藥時曲線觀測值、預測值及預測值的90%置信區間
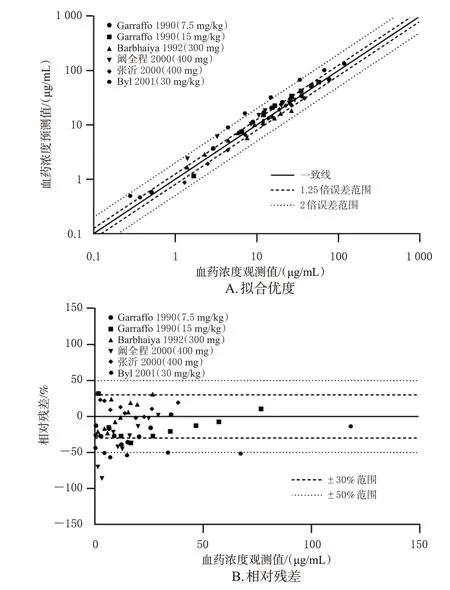
圖3 成人PBPK模型驗證中的擬合優度和相對殘差
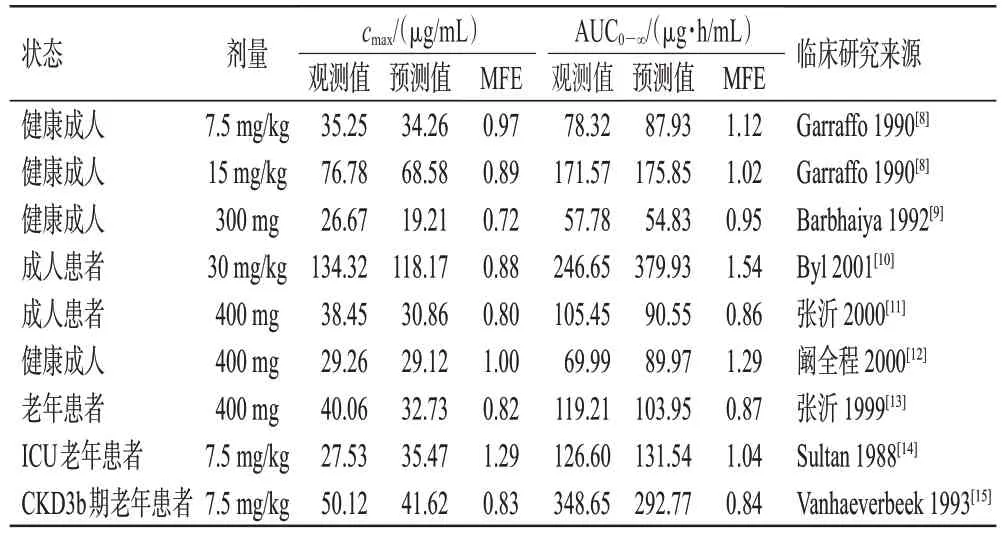
表3 PBPK模型驗證中的藥動學參數預測值與觀測值
3.2 阿米卡星老年患者PBPK模型
在驗證的成人PBPK 模型基礎上,通過軟件內置的年齡算法對解剖學和生理學參數進行調整,建立老年患者PBPK 模型并使用3 項老年患者臨床藥動學研究[13—15]進行驗證(圖4)。3 項模擬中cmax和AUC0-∞預測值與觀測值比較的MFE 均在>0.5~<2 范圍內(表3),說明模型外推至老年患者具有較好的適用性,能合理預測老年腎功能不全患者給藥后的體內暴露。
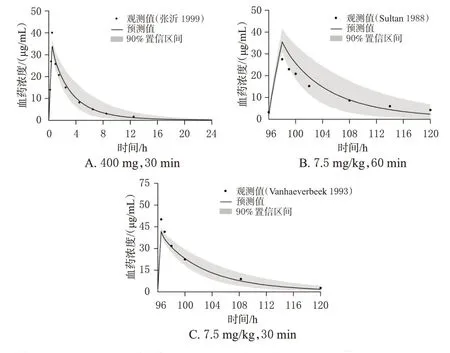
圖4 老年腎功能不全患者靜脈輸注不同劑量阿米卡星后藥時曲線觀測值、預測值及預測值的90%置信區間
3.3 老年腎功能不全患者給藥方案評價
每日給予不同劑量阿米卡星達穩態后,不同CKD分期老年患者的平均藥時曲線顯示,腎功能不全對穩態谷濃度的影響明顯大于對cmax的影響。其中,當阿米卡星為標準劑量(15 mg/kg)時,CKD4期患者相較于CKD2期患者的cmax比值為1.12(P<0.000 1),穩態谷濃度比值為21.05(P<0.000 1)。結果見圖5。

圖5 老年不同程度腎功能不全患者靜脈輸注15 mg/kg阿米卡星后的平均藥時曲線
各模擬情況下,不同CKD 分期老年患者穩態谷濃度<4 μg/mL 的PTA 見表4。由表4 可知,CKD2、CKD3a、CKD3b 期老年患者給藥劑量為5~15 mg/kg時,可每24 h 給藥1 次;CKD4 期老年患者給藥劑量為7.5~15 mg/kg時,給藥間隔應延長至36 h。當使用超過說明書劑量(≥20 mg/kg)時,CKD3b期老年患者的給藥間隔需延長至36 h,CKD4期老年患者應延長至48 h。
老年CKD 患者在不同模擬情況下,cmax/MIC≥8 的PTA見表5。以銅綠假單胞菌為例,對于MIC≤2 μg/mL的敏感菌,阿米卡星5 mg/kg每24 h給藥1次即可在所有人群中達到PTA≥90%。當MIC 增至4 μg/mL 時,GFR<45 mL/min 的患者可使用阿米卡星7.5 mg/kg,GFR≥45 mL/min的患者需使用10 mg/kg。當MIC增至8 μg/mL 時,GFR<45 mL/min 的患者可使用阿米卡星15 mg/kg,GFR≥45 mL/min 的患者需使用20 mg/kg(略超過說明書最大劑量)。當MIC增至16 μg/mL時(接近折點),所有模擬場合均無法達成cmax/MIC≥8。

表5 阿米卡星各模擬情況下不同CKD 分期老年患者cmax/MIC≥8的PTA
綜合以上結果,在有藥敏試驗結果作為依據時,推薦老年腎功能不全患者給藥方案見表6。

表6 根據藥敏試驗結果推薦的老年腎功能不全患者阿米卡星的給藥方案
4 討論
約三分之二的老年人會出現不同程度的生理或病理性腎功能減退,這使得主要經腎排泄的藥物在體內消除延長,而部分藥物的腎毒性還可能使腎功能進一步受損,例如阿米卡星等氨基糖苷類抗菌藥物。權衡利弊后,若老年患者必須使用阿米卡星,需在保證治療效果的同時避免腎毒性發生。PBPK模型與模擬技術的發展為特殊人群精準用藥提供了新的思路和工具,可根據已有臨床研究數據對成人的藥動學模型進行合理外推,在未進行研究或研究不充分的情況下獲得特殊人群給藥后的體內暴露情況,為其給藥方案的制定提供了依據。
阿米卡星幾乎不與血漿蛋白結合,可在腎小球處被動濾過,在腎小管處不發生主動分泌,但存在一定的重吸收。盡管以原型經腎排泄是阿米卡星的主要消除方式,但仍有一定比例通過非腎途徑從體內消除[17]。該非腎消除機制尚不明確,但在老年腎功能不全患者中可觀察到非腎消除比例增加[15]。若按照說明書中推薦的根據血肌酐水平進行劑量調整,將忽略非腎消除部分的影響,可能會低估腎功能不全患者的藥物清除速率,導致調整后的藥物體內暴露不足。因此,本研究采用腎小球濾過模型與非腎的全身清除模型相結合來描述阿米卡星的消除過程,同時利用尿藥排泄數據對關鍵參數fGFR、CLnon-renal進行優化,較已發表的同類模型中采用固定清除率的方式更為合理[22]。本研究的不足之處在于,觀察到部分驗證中存在低估cmax預測值的傾向,這或許與未知的體內分布過程相關,有待進一步探討。
本研究中,模擬的腎功能不全對阿米卡星穩態谷濃度的影響較為顯著,而對cmax影響較小,這與以往研究結果相似[22]。在根據腎功能調整給藥方案時,需首要考慮避免藥物體內蓄積引發腎毒性。本研究結果顯示,GFR>45 mL/min 的老年腎功能不全患者,在各模擬給藥方案下,因谷濃度蓄積引起腎毒性的風險較低,與以往研究報道相似[23]。而對于CKD4 期老年患者,不削減每次給藥劑量,延長給藥間隔至36~48 h更有利于保持cmax/MIC≥8,且可避免谷濃度蓄積引起腎毒性的發生風險。老年人是ICU中的主要病患人群,受血管內皮功能紊亂、腎功能減退和大量輸液等因素影響,ICU 老年患者常出現體液超載。阿米卡星cmax水平主要由表觀分布容積(Vd)決定,由于阿米卡星具有極強的親水性,ICU患者細胞外液增加可導致阿米卡星的Vd增加,引起cmax降低[24]。本研究在驗證中同樣發現,ICU 老年患者的血藥濃度觀測值低于對應的模擬預測值[14],預測值為觀測值的1.29倍(表3)。一項針對阿米卡星在危重癥患者中的藥動學研究發現[25],即便在25 mg/kg 的高劑量下,仍有25%~33%的患者未能達到cmax/MIC≥8(cmax>60~64 μg/mL)。近年來,國際上關于阿米卡星中高劑量用于ICU患者和老年患者的報道不斷增加[26]。出于對腎毒性的擔憂,高于15 mg/kg 的給藥方案在國內應用較少[27]。本研究前期對阿米卡星20~30 mg/kg 劑量范圍進行了模擬。從安全性角度考慮,在應用阿米卡星超說明書劑量時,CKD3b 期患者可將給藥間隔至少延長至36 h,CKD4 期患者至少延長至48 h。從有效性角度考慮,當ICU老年患者必須使用阿米卡星時,為避免Vd增加導致的暴露不足風險,本研究建議在表6推薦劑量的基礎上加量25%~50%,以確保cmax/MIC≥8,然后再根據血藥濃度監測進行個體化調整[26]。
綜上,本研究較為完整地建立并驗證了阿米卡星在老年腎功能不全患者中的PBPK 模型,可為經腎排泄藥物PBPK模型的研究和應用提供思路。建立的PBPK模型經臨床藥動學數據驗證,通過合理外推后實現了在老年腎功能不全患者體內的暴露情況模擬,并從有效性和安全性兩方面對臨床常見給藥方案進行了評估和推薦,能夠為阿米卡星在老年腎功能不全患者中的合理用藥提供參考。

