尼妥珠單抗聯(lián)合放化療治療局部晚期宮頸癌的療效及對相關(guān)腫瘤因子水平和免疫功能的影響
朱海藝,周麗妃,張玉蘭
(海南醫(yī)學(xué)院第二附屬醫(yī)院腫瘤內(nèi)科,海南 海口 570311)
宮頸癌是女性最為常見的一種惡性腫瘤,局部晚期患者預(yù)后不佳[1]。對于局部晚期宮頸癌(locally advanced cervical cancer,LACC),同步放化療仍是標準治療方案,但由于放化療抵抗等因素,臨床療效受限,需積極探索新的有效治療手段。約85%的宮頸癌患者存在與其預(yù)后密切相關(guān)的表皮生長因子受體(epidermal growth factor receptor,EGFR)表達[2],基于EGFR的靶向治療為宮頸癌治療帶來新思路。尼妥珠單抗作為一種針對EGFR的人源化單克隆抗體,能夠阻斷EGFR介導(dǎo)的信號傳導(dǎo)通路,進而發(fā)揮抗腫瘤作用[3]。尼妥珠單抗在局部晚期非小細胞肺癌、頭頸部鱗狀細胞癌、食管癌等多種惡性腫瘤的治療中有著確切療效[4-6],但目前關(guān)于其在LACC治療中的應(yīng)用尚缺乏足夠的臨床數(shù)據(jù)。為此,本研究擬探討尼妥珠單抗聯(lián)合放化療治療LACC的療效。
1 資料與方法
1.1 一般資料
選取2020年1月至2021年12月海南醫(yī)學(xué)院第二附屬醫(yī)院收治的90例LACC患者作為研究對象。納入標準:(1)經(jīng)病理活檢證實為宮頸癌,FIGO分期屬于II B-Ⅲ期;(2)無遠處轉(zhuǎn)移;(3)美國東部腫瘤協(xié)作組(east-ern cooperative oncology group,ECOG)評分為0~2分;(4)預(yù)計生存期不少于3個月;(5)年齡≥18歲。排除標準:(1)合并重要臟器(如心肺腎)功能不全者;(2)合并其他惡性腫瘤者;(3)合并嚴重血液系統(tǒng)疾病者;(4)對放化療無法耐受者;(5)處于妊娠或哺乳期;(6)合并免疫系統(tǒng)疾病者。按照治療方式不同將患者分為對照組(n=45)與觀察組(n=45)。本研究獲倫理委員會審批通過,患者均簽署知情同意書。兩組患者一般資料比較,差異均無統(tǒng)計學(xué)意義。見表1。
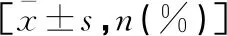
表1 兩組患者一般資料比較
1.2 治療方法
對照組予以同期放化療治療。放療采用體外照射+內(nèi)照射。外照射總劑量48~60 Gy,照射22~25次,5次/周;內(nèi)照射5次,每次10~15 Gy。化療采用TP方案:順鉑+紫杉醇,前者第1~3天,50 mg/m2,后者135 mg/m2,治療28 d。觀察組聯(lián)合尼妥珠單抗,放化療前,尼妥珠單抗400 mg溶于250 mL 0.9%氯化鈉溶液后,靜脈滴注時間>1 h,1次/周,共6周。
1.3 觀察指標
(1)臨床療效:治療后兩個月,進行療效評價,使用實體瘤療效標準[7],包括完全緩解(CR)、部分緩解(PR)、疾病穩(wěn)定(SD)、疾病進展(PD),計算客觀緩解率(ORR)和腫瘤控制率(DCR),其中ORR=(CR例數(shù)+PR例數(shù))/總例數(shù)×100%,DCR=(CR+PR+SD)/每組總例數(shù)×100%。(2)生活質(zhì)量:于治療前和治療后兩個月,采用癌癥患者生命質(zhì)量測定量表體系之宮頸癌量表(QLICP-CEV2.0)[8]評定患者生存質(zhì)量,分值越高表明生存質(zhì)量越好。(3)腫瘤標志物:于治療前和治療后兩個月,采集患者空腹靜脈血5 mL,經(jīng)3 500 r/min離心取生層血清待檢。采用酶聯(lián)免疫吸附法測定血清鱗狀細胞癌抗原(squamous cell carcinoma antigen,SCC)、糖鏈抗原125(carbohydrate antigen 125,CA125)水平,腫瘤特異性生長因子(tumor specific growth factor,TSGF)經(jīng)電化學(xué)發(fā)光法獲得。(4)免疫功能:于治療前和治療后(放化療后兩個月),采集外周血標本,采用流式細胞儀(美國BD公司)進行T淋巴細胞亞群(CD4+T細胞、CD8+T細胞)的檢測。(5)安全性:參照美國腫瘤放射治療協(xié)作組織常見不良反應(yīng)事件評價標準[9]進行不良反應(yīng)評價與記錄,分為I-Ⅳ級。
1.4 統(tǒng)計學(xué)分析

2 結(jié)果
2.1 兩組患者臨床療效比較
觀察組ORR高于對照組(86.67%vs.66.67%,P<0.05)。兩組DCR比較,差異無統(tǒng)計學(xué)意義(P>0.05)。見表2。

表2 兩組臨床療效比較 [n(%)]
2.2 兩組生存質(zhì)量評分比較
治療后,兩組QLICP-CEV2.0評分均增高(P<0.05),且觀察組高于對照組(P<0.05)。見表3。
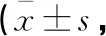
表3 兩組QLICP-CEV2.0評分比較分)
2.3 兩組腫瘤標志物比較
治療后,兩組SCC、CA125、TSGF均降低(P<0.05),且觀察組低于對照組(P<0.05)。見表4。

表4 兩組腫瘤標志物比較
2.4 兩組免疫功能指標比較
治療后,兩組CD4+T細胞均降低(P<0.05),但觀察組高于對照組(P<0.05);兩組CD8+T細胞水平比較,差異無統(tǒng)計學(xué)意義(P>0.05)。見表5。

表5 兩組免疫功能指標比較
2.5 兩組不良反應(yīng)比較
兩組不良反應(yīng)均屬于I-II級,未見Ⅲ-Ⅳ級不良反應(yīng),差異無統(tǒng)計學(xué)意義(P>0.05)。見表6。

表6 兩組不良反應(yīng)比較[n(%)]
3 討論
同步放化療是LACC的標準治療方法,但仍存在部分患者由于對放化療敏感性差,加上化療耐藥的問題,可能會導(dǎo)致治療效果差。血管內(nèi)皮細胞生長因子可作為宮頸癌靶向治療的理想靶標[10]。但目前關(guān)于宮頸癌的靶向治療研究,多針對復(fù)發(fā)、轉(zhuǎn)移性宮頸癌[11],LACC的靶向治療仍缺乏足夠的臨床數(shù)據(jù)。
EGFR高表達與腫瘤進展和不良預(yù)后密切相關(guān),在宮頸癌中的高表達率約85%[12],是宮頸癌治療的理想靶標。尼妥珠單抗是全球第一個以EGFR為靶點的單抗藥物,也是我國第一個批準上市的功能性單抗藥物,其能與EGFR細胞外特定區(qū)域結(jié)合,導(dǎo)致EGFR構(gòu)象發(fā)生變化,進而影響其與表皮細胞生長因子及轉(zhuǎn)化生長因子α結(jié)合,阻斷EGFR介導(dǎo)的信號向細胞內(nèi)傳導(dǎo),發(fā)揮抗腫瘤效應(yīng)。此外,尼妥珠單抗具有放化療增敏作用,增強放化療效果[13]。同時,尼妥珠單抗的親和力適度,不良反應(yīng)少[14]。在體外實驗和很多實體瘤治療中,尼妥珠單抗已表現(xiàn)出能夠增強抗腫瘤免疫力,發(fā)揮著強大的抗腫瘤活性和理想的組織特異性,獲得了良好治療療效,且耐受性良好[4-6]。
Cao等[15]研究顯示,對LACC患者實施尼妥珠單抗+放化療治療,患者ORR顯著提升(88.4%vs.67.4%);Chen等[16]發(fā)現(xiàn),尼妥珠單抗聯(lián)合放化療治療LACC能夠明顯提高ORR(87.0%vs.73.3%)。本研究顯示,觀察組ORR為86.67,高于對照組的66.67%,表明尼妥珠單抗聯(lián)合放化療治療LACC能夠提高近期療效,與既往報道[15-16]一致。本研究中,治療后,觀察組QLICP-CEV2.0評分高于對照組,表明尼妥珠單抗的應(yīng)用有助于改善患者生存質(zhì)量。
SCC、CA125及TSGF是由腫瘤細胞合成、分泌,反映腫瘤存在及生長的物質(zhì),其與腫瘤生長、發(fā)展、復(fù)發(fā)及轉(zhuǎn)移等密切相關(guān)[17-18]。SCC是鱗狀細胞癌患者組織分泌的糖蛋白;CA125作為常見的腫瘤標志物,對宮頸癌的診斷、預(yù)后判斷有重要價值;TSGF是能夠反映腫瘤早期增殖、浸潤和轉(zhuǎn)移的腫瘤標志物,與宮頸癌的發(fā)生發(fā)展、預(yù)后緊密關(guān)聯(lián)[19-20]。本研究結(jié)果顯示,尼妥珠單抗聯(lián)合放化療能夠明顯降低血清SCC、CA125、TSGF水平,這從分子水平進一步驗證了尼妥珠單抗的治療價值。
腫瘤細胞的增殖可導(dǎo)致患者免疫力低下,而機體免疫差可使得患者感染風險增高,進而影響化療效果,甚至導(dǎo)致部分患者不得不終止治療[21]。T淋巴細胞亞群在細胞免疫過程中有著重要作用,其中CD4+T細胞為輔助性T細胞表面分子,能夠通過輔助或調(diào)控其他類型淋巴細胞來產(chǎn)生免疫調(diào)節(jié)作用,發(fā)揮抗腫瘤作用;CD8+T細胞主要是細胞毒性T細胞表面分子,其在外周血的表達水平與腫瘤的預(yù)后相關(guān)。本研究中,治療后,兩組CD4+T細胞下調(diào),但觀察組比對照組高,這提示尼妥珠單抗能夠改善LACC放化療患者免疫功能,這可能與尼妥珠單抗增強抗腫瘤免疫力的作用有關(guān)[22]。機體抗腫瘤免疫主要依靠CD8+CTL介導(dǎo)的細胞免疫為主,本研究中,觀察組治療后CD8+T細胞水平低于對照組,可能是因為CD8+T細胞參加抗腫瘤消耗更多所致。本研究還表明,尼妥珠單抗安全性較高,未加重不良反應(yīng)。
綜上,尼妥珠單抗聯(lián)合放化療治療LACC,不僅使臨床療效提高,還可改善血清腫瘤因子水平及免疫功能,且不增加不良反應(yīng)。

