鱗翅目昆蟲性別決定機制研究進展
萬 倩, 劉萬學, 呂志創, 郭建洋, 黃 聰, 嚴 盈, 楊念婉,3*
(1. 中國農業科學院植物保護研究所,植物病蟲害綜合治理全國重點實驗室,北京 100193;2. 德國吉森大學昆蟲生物技術研究所,植物保護昆蟲生物技術系,吉森 35394;3. 中國農業科學院西部農業研究中心,昌吉 831100)
自然界中,生物的性別決定機制復雜多樣,大體可分為遺傳性別決定(genotypic sex determination, GSD)和環境性別決定(environmental sex determination, ESD)兩大類[1]。昆蟲作為動物界中最大的一個類群,其性別決定機制一直是研究熱點。對不同昆蟲性別決定通路和關鍵基因功能的探究,既能揭示昆蟲物種分化的關系,也能為基于基因編輯技術的昆蟲不育技術(sterile insect technique, SIT)提供理論和實踐基礎[2]。昆蟲的性別決定機制復雜多樣,性別決定關鍵基因對個體雌雄性別分化的調控表現為級聯反應。主要的表達模式為早期胚胎中性別決定初始信號調控關鍵靶基因進行雌雄差異性表達,關鍵靶基因表達產物在其他因子的幫助下作用于級聯反應底層的雙性基因doublesex(dsx),使dsx產生雌雄特異性剪接產物,從而調控下游雌雄性別偏向基因的表達,最終實現昆蟲的性別分化;而缺乏性別決定初始信號的則為默認的表達模式,最后個體呈現出與之相反的性別分化[3]。
鱗翅目Lepidoptera是昆蟲綱Insecta中僅次于鞘翅目Coleoptera的第二大目,包括蛾類和蝶類。鱗翅目昆蟲大多為植食性,許多成蟲能傳粉,在生態系統中發揮著重要作用;一些物種還在人類社會生產中發揮著經濟價值,如家蠶Bombyxmori和柞蠶Antheraeapernyi的應用推動了絲綢業的發展。也有不少鱗翅目昆蟲為農業重大害蟲,如草地貪夜蛾Spodopterafrugiperda、蘋果蠹蛾Cydiapomonella、棉鈴蟲Helicoverpaarmigera、草地螟Loxostegesticticalis等。鱗翅目昆蟲繁殖方式以兩性生殖為主,不同于哺乳動物以及其他昆蟲的XY/XX性染色體系統,鱗翅目大多為ZW/ZZ系統,雌性為染色體異配型即ZW型,雄性為ZZ型[4]。因此,鱗翅目昆蟲所特有的W染色體使其性別決定機制不同于其他昆蟲。在ZW/ZZ系統中,位于W染色體的性別決定初始信號沉默Z染色體上的雄性化關鍵基因Masc,然后位于常染色體上的dsx基因被雌性特異性剪接,實現雌蟲分化;而雄蟲中無W染色體,Masc基因正常表達并調控dsx基因的雄性特異性剪接,促進雄性偏向基因的表達,完成雄性發育。本文對鱗翅目昆蟲性別決定機制的研究以及性別決定機制在鱗翅目昆蟲種群遺傳調控中的應用進行綜述,以期為鱗翅目重要經濟昆蟲的性別篩選和防治有性繁殖的重大害蟲的種群遺傳防控技術提供理論基礎。
1 鱗翅目昆蟲性染色體研究進展
鱗翅目昆蟲性染色體系統多為ZW/ZZ型,雌性為ZW型,雄性為ZZ型(表1)[5-23]。少部分缺失W染色體,雌性表現為Z0型,雄性ZZ型,歸為Z0/ZZ系統,如蓑蛾科Psychidae的Proutiabetulina、Taleporiatubulosa和Diplodomalaichartingella的雌蟲均缺失W染色體[16]。還有部分鱗翅目昆蟲表現出截然不同的性染色體系統,如小蔗桿草螟Diatraeasaccharalis雌蟲減數分裂產生了三價體WZ1Z2,雄蟲則表現為Z1Z1Z2Z2[18]。在小粉蝶屬Leptidea中還發現了W1-3Z1-3/Z1-3Z1-3、W1-3Z1-4/Z1-4Z1-4和W1-3Z1-6/Z1-6Z1-6等性染色體系統的存在[5-6]。
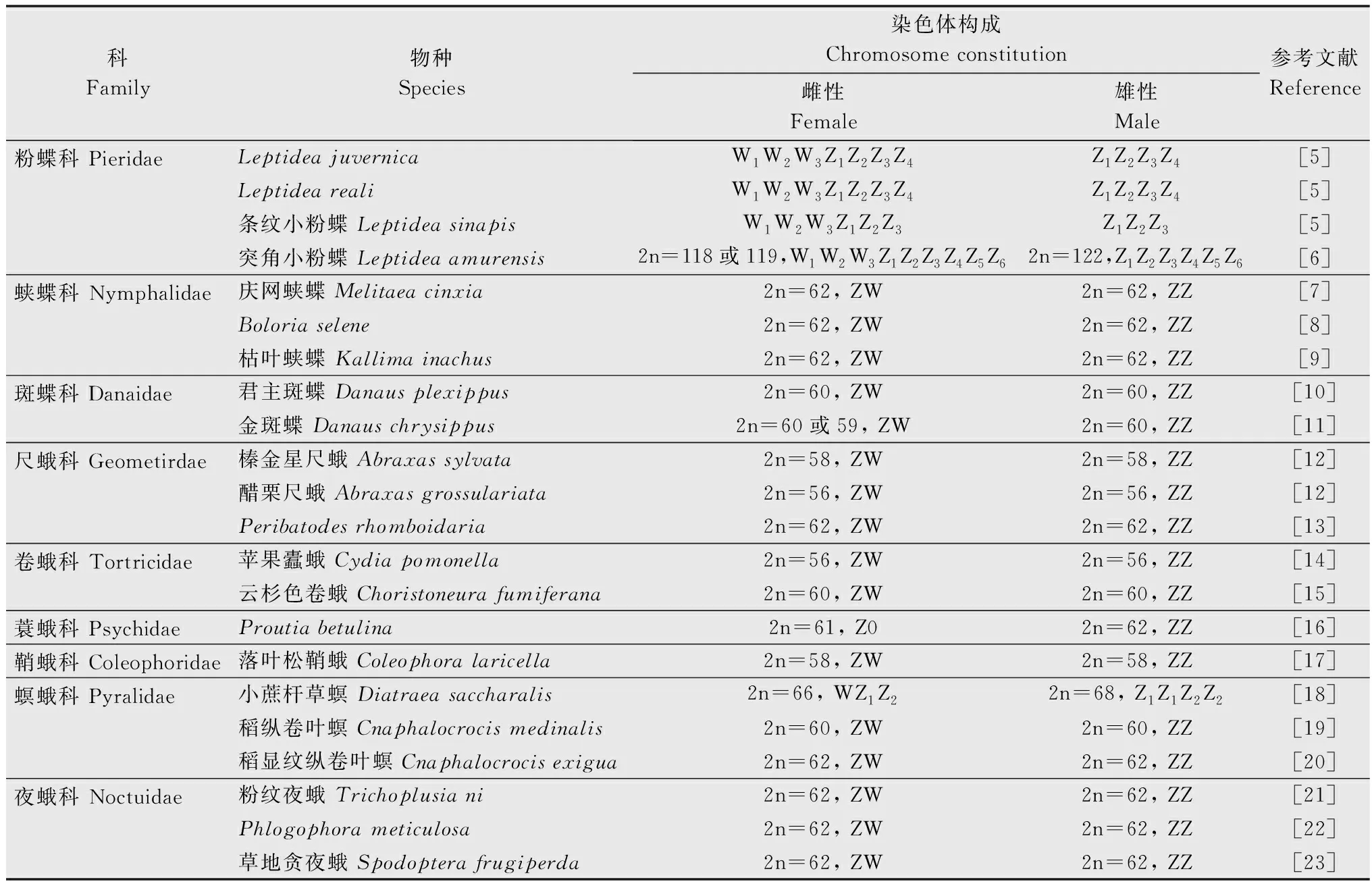
表1 鱗翅目昆蟲性染色體研究進展Table 1 Research progress on sex chromosomes in lepidopteran insects
一般認為鱗翅目ZW/ZZ系統是從古老的Z0/ZZ系統中演化而來。對鱗翅目和毛翅目進行系統發育分析發現,雌性異配型性別染色體系統至少存在1.8億年,而W染色體約0.9億~1億年前才出現,存在于更為高級的物種中,且正在快速進化,Z染色體則較為保守[4,24-26]。最初對W染色體上基因的研究發現,W染色體存在很多雌性特異的重復序列,未發現能編碼蛋白質的基因。如利用W染色體來源的細菌人工染色體(W chromosome-derived bacterial artificial chromosome,W-BAC)作為探針進行基因組原位雜交(genomic in situ hybridization,GISH),或利用高通量測序技術等對家蠶、地中海粉螟Ephestiakuehniella、蘋果蠹蛾W染色體進行研究,發現W染色體上存在大量的功能性轉座元件(transposable elements, TEs)和其他重復序列[14,27-28]。近年來,隨著對鱗翅目染色體研究的深入,陸續在一些鱗翅目昆蟲W染色體上發現了能編碼蛋白的基因,如Deng等[29]在棉鈴蟲中發現了第一個鱗翅目昆蟲W染色體上特異性編碼蛋白的基因GUW1。在水稻常發害蟲稻縱卷葉螟Cnaphalocrocismedinalis的W染色體上則發現了755個編碼蛋白的基因,但只有5%是能鑒定的蛋白[19]。
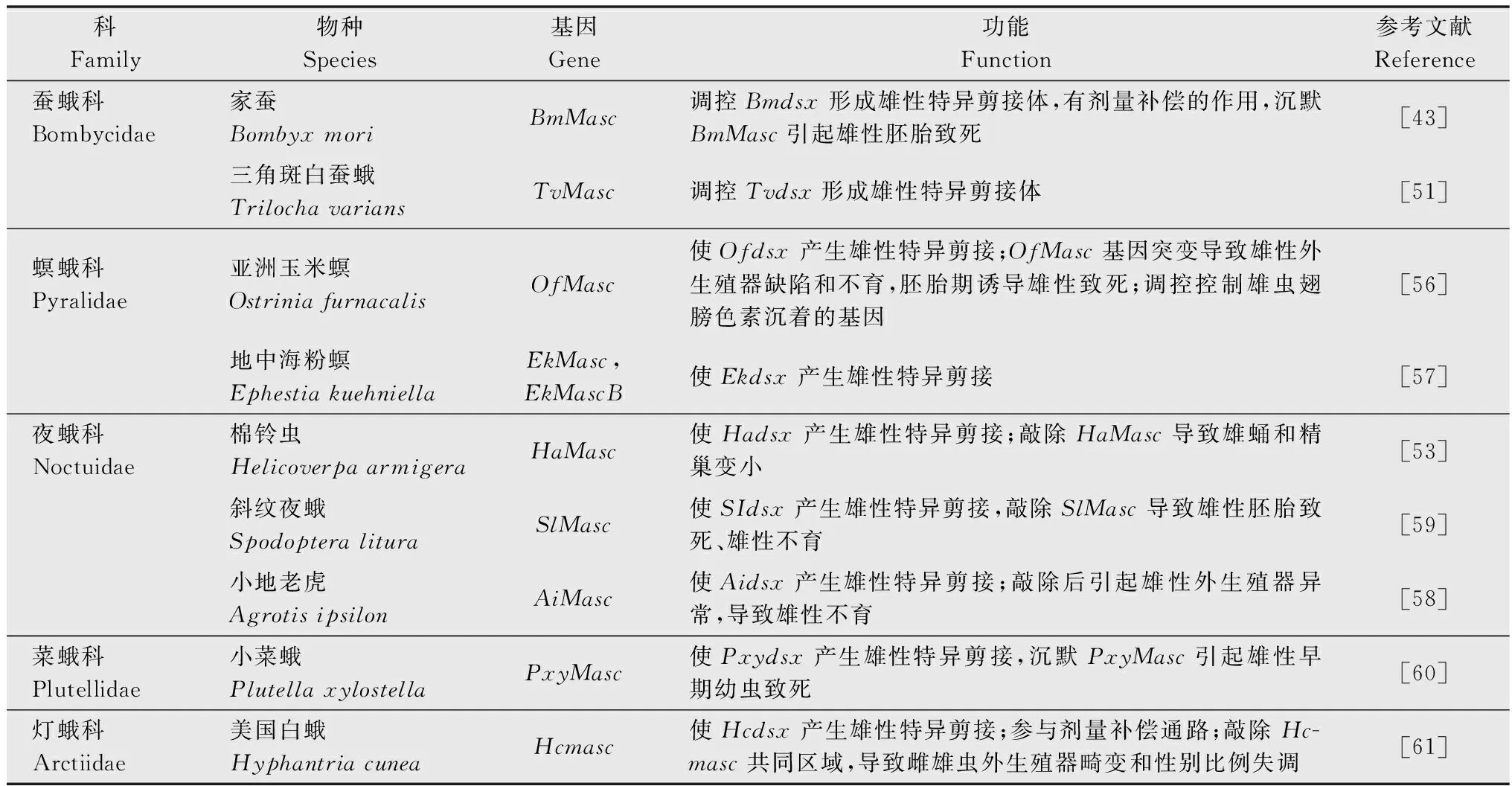
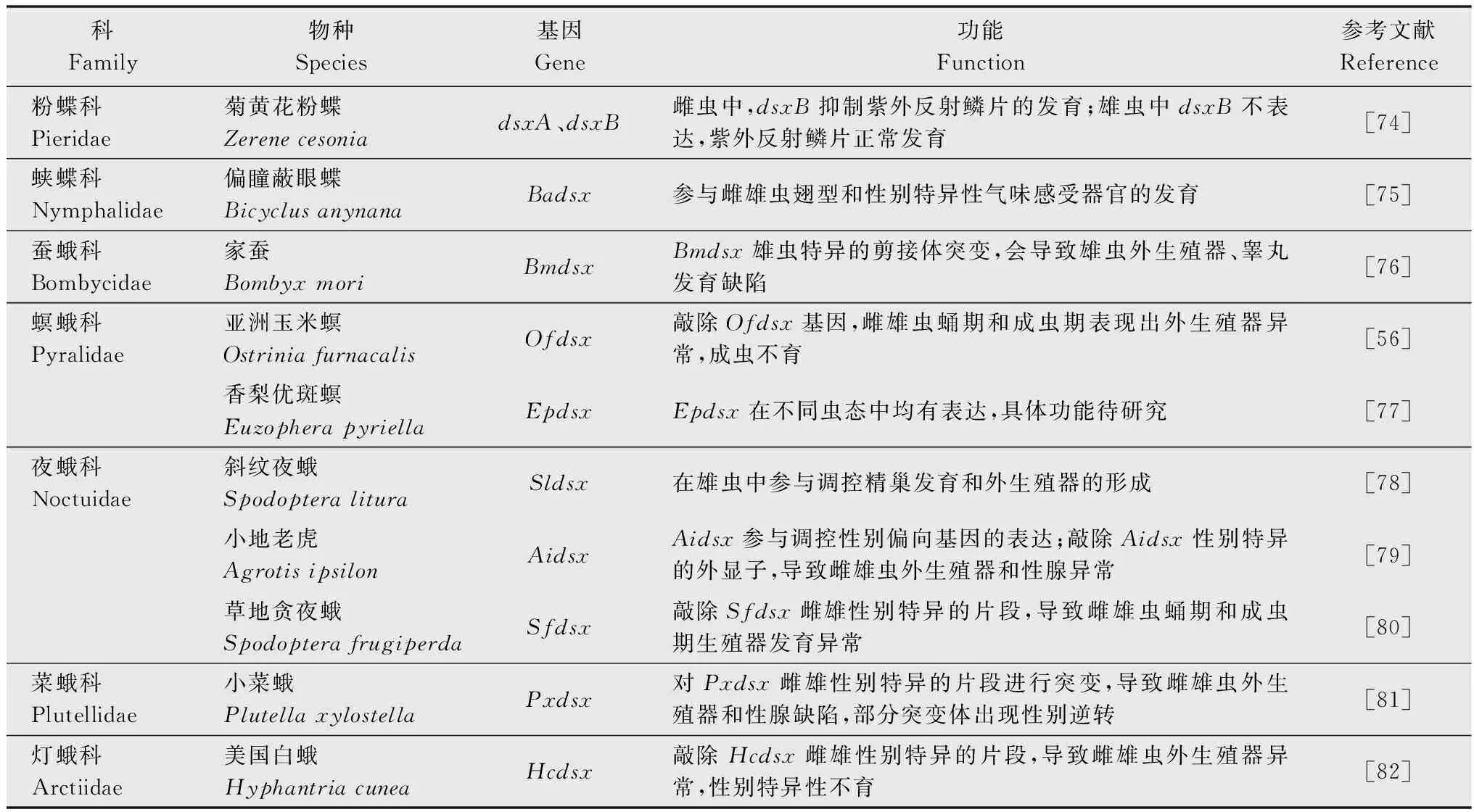
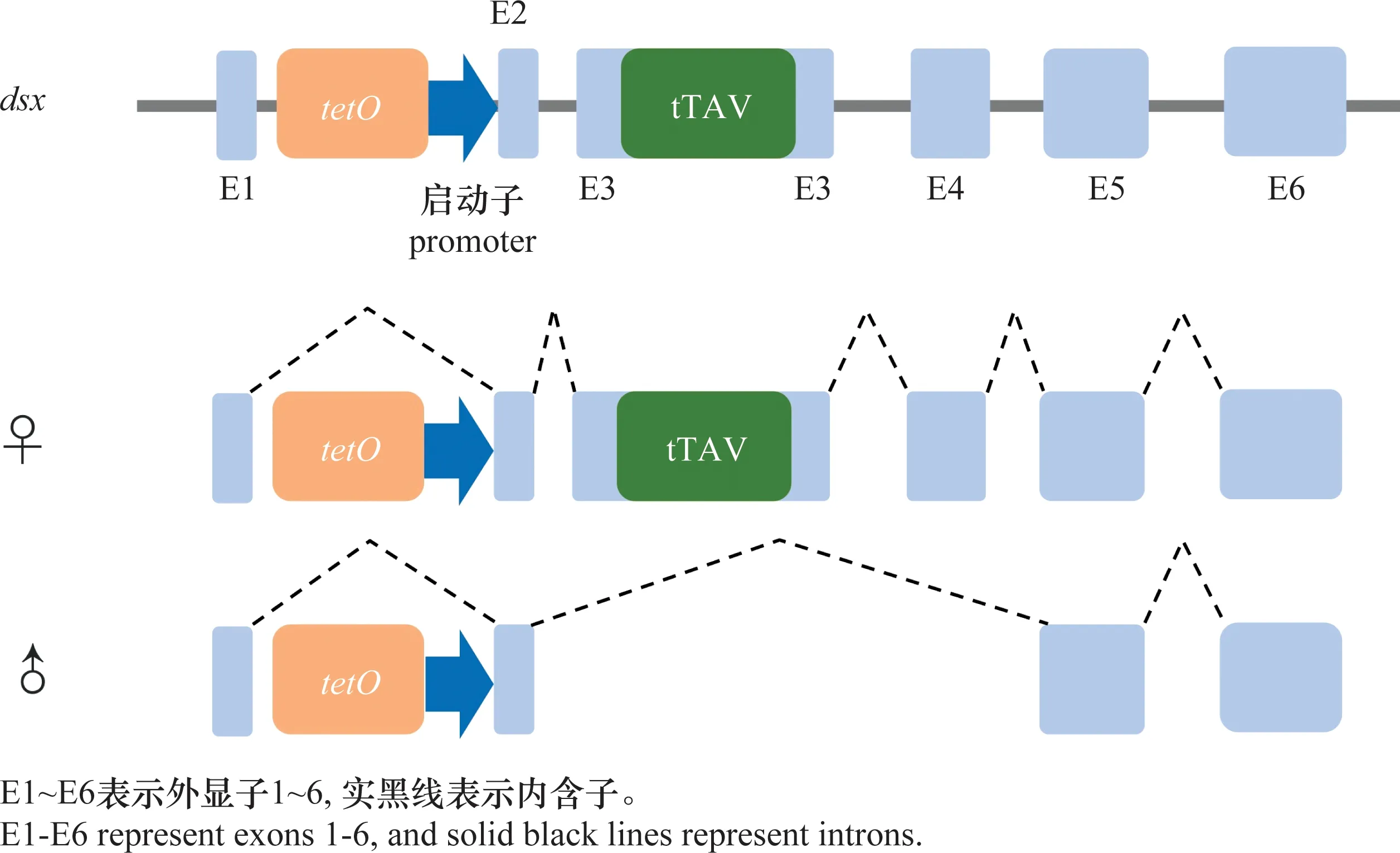
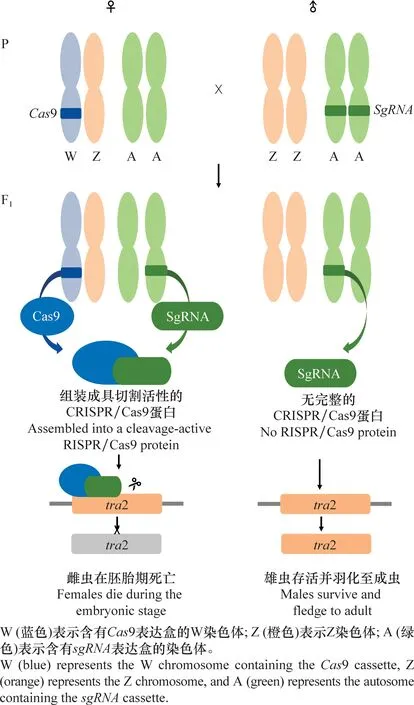
不同于W染色體,鱗翅目昆蟲Z染色體上富含能編碼蛋白質的基因,如家蠶的Z染色體上有編碼肌動蛋白的基因[30]。同時,Z染色體上還有與雄性分化有關的基因,如條紋小粉蝶LeptideasinapisZ染色體上富集了大量雄性偏向表達的基因[31]。在煙草天蛾Manducasexta和君主斑蝶Danausplexippus的Z染色體中也發現了大量的精子蛋白基因[32]。在具有XY/XX性別決定系統的生物中,兩性的X染色體數量不同,但X染色體連鎖基因在2種性別中卻有著相等或近乎相等的表達量,這種能平衡性染色體連鎖基因的遺傳效應叫做劑量補償效應(dosage compensation)[33-34]。對鱗翅目昆蟲性染色體劑量補償的研究發現,Z染色體的劑量補償機制在鱗翅目中普遍存在[35]。利用RNA-seq技術對蘋果蠹蛾Z染色體的劑量補償模式進行分析發現,Z染色體連鎖基因在兩性中的表達水平相當,且低于二倍體常染色體基因的表達水平,即Z≈ZZ 昆蟲性別決定表現為級聯反應。在鱗翅目昆蟲ZW/ZZ性別決定系統中,位于W染色體的性別決定初始信號沉默Z染色體上的雄性化關鍵基因Masc,促使dsx基因形成雌性特異性剪接體,進而調控一系列雌性偏向基因的表達,實現雌蟲分化;而雄蟲為ZZ型,缺失W染色體上的性別決定初始信號,因此Masc基因正常表達并產生Masc蛋白,調控dsx基因形成雄性特異性剪接體,進而促進雄性分化[41-47](圖1)。 在鱗翅目ZW/ZZ系統中,W染色體常與雌性的性別分化有關。利用GISH、比較基因組雜交(comparative genomic hybridization, CGH)和熒光原位雜交(fluorescence in situ hybridization, FISH)這3種方法對蘋果蠹蛾3種輻射突變異常的W染色體進行詳細的細胞遺傳學分析,并與野生型雌蟲進行比較,發現其W染色體上存在雌性決定因子的獨特序列[48]。目前,鱗翅目昆蟲中已鑒定出的性別決定初始信號僅有家蠶中和小菜蛾Plutellaxylostella中的Fem。在雌蟲早期胚胎中,位于W染色體的Fem轉錄生成小沉默RNA(small silencing RNA, ssRNA),沉默雄性化基因Masc,實現雌性的性別分化。ssRNA是一類長度約20~30 nt的小RNA,能與Argonaute蛋白結合后使靶基因的表達降低,主要分為microRNA (miRNA)、small interfering RNA (siRNA) 和 Piwi-interacting RNA (piRNA)三類[49]。Fem是piRNA的前體,最終產生一個長29 nt且3′端被2′-O-甲基化修飾的piRNA。然后該FempiRNA與靶標基因Masc第9外顯子上的特異性序列相互作用,沉默Masc,實現家蠶雌性的發育[43]。在小菜蛾中,Pxyfem能產生多個ssRNA,并在雌蟲胚胎期對PxyMasc轉錄本外顯子5進行剪切,以沉默PxyMasc基因的表達[50]。在與家蠶親緣關系較近的三角斑白蠶蛾Trilochavarians中也發現了Fem的直系同源基因,但進一步研究發現FempiRNA并不參與三角斑白蠶蛾的性別決定級聯反應;在與家蠶親緣關系較遠的蔗莖禾草螟Chilosacchariphagus中,則沒有找到Fem的同源基因[51-52]。棉鈴蟲W染色體上的蛋白質編碼基因GUW1可能是其主要的性別決定初始信號,能抑制雌蟲中HaMasc的表達,調控雌性分化,然而該猜想還需要試驗進行驗證[29,53]。雖然鱗翅目昆蟲的W染色體常與性別有關,但W染色體并不總是對性別決定起主導作用。如利用樗蠶蛾Samiacynthia的2個亞種S.cynthiapryeri(WZ/ZZ)和S.cynthiawalkeri(neo-Wneo-Z/neo-Zneo-Z)進行正反交試驗,發現F2代中存在無W染色體和 neo-W染色體的雌蟲以及攜帶W染色體或neo-W染色體的雄蟲,進一步研究發現W染色體和neo-W染色體的存在與否對卵的孵化率并沒有影響,表明W染色體對樗蠶蛾這2個亞種的性別決定和生殖能力不起作用[54]。隨后通過人工合成的多倍體試驗,發現樗蠶蛾的性別是由Z染色體數量與常染色體數量的比值所決定[55]。 Masc基因能調控下游基因dsx形成雄性特異性剪接體,實現雄性性別分化。Masc基因最初在家蠶Z染色體上發現,由10個外顯子組成,編碼一種鋅指蛋白Masc,在雌蟲中被FempiRNA沉默,促使Bmdsx形成雌性特異剪接體。同時還發現Masc蛋白在胚胎期會抑制雄蟲Z染色體上基因的表達,具劑量補償的作用[43]。目前,在地中海粉螟、棉鈴蟲、亞洲玉米螟Ostriniafurnacalis、小地老虎Agrotisipsilon、三角斑白蠶蛾、小菜蛾、斜紋夜蛾Spodopteralitura、美國白蛾Hyphantriacunea等鱗翅目昆蟲中均發現了Masc蛋白,敲除Masc后,雄蟲的外生殖器、精巢等出現異常,生長發育和生殖能力受到了負面影響;在部分物種的雄蟲突變體中,甚至出現了胚胎或早期幼蟲致死的現象(表2),表明Masc基因在雄蟲正常生長發育中起著重要作用[43,51,53,56-61]。 表2 鱗翅目昆蟲Masc基因研究進展Table 2 Research progresses in Masc gene in lepidopteran insects Masc蛋白由588~658個氨基酸組成,具4個典型的結構,2個串聯的CCCH型鋅指結構域(CCCH-type zinc finger domains, ZFs),1個核定位信號和1個高度保守的含11個氨基酸的區域[58,62-63]。目前已發現的Masc蛋白幾乎都有2個串聯的ZFs,但有研究表明ZFs對于鱗翅目昆蟲雄性化和劑量補償不是必須的。利用CRISPR/Cas9技術敲除家蠶Masc基因的ZFs后,發現突變后的雄性胚胎正常生長,無任何表型缺陷[62]。在對地中海粉螟的研究中發現,EkMasc和EkMascB兩個基因只在雄性早期胚胎中表達,編碼類似的Masc蛋白,調控Ekdsx形成雄性特異剪接體,但在這兩個Masc蛋白中未發現ZFs[57]。雖然目前對ZFs的功能并不清楚,但Masc蛋白C端(210~288個氨基酸)富含脯氨酸的區域、第301和304位高度保守的2個半胱氨酸殘基Cys,都是調控雄性化和劑量補償的關鍵區域[57,62,64]。 不同昆蟲的性別決定初始信號不同,但性別決定級聯反應下游的基因dsx在雙翅目、膜翅目、鞘翅目、直翅目、鱗翅目等昆蟲中均有發現且保守性較高[65]。dsx基因受上游基因的調控,形成雌雄性別特異的剪接體,進一步調控下游性別偏向基因的表達,最終實現雌雄性別分化,是性別決定與性別分化的中間樞紐。dsx編碼的DSX蛋白,N端一般都有一個DNA結合結構域(OD1),中間有一個蛋白寡聚結構域(OD2)以及C末端有一個性別特異的氨基酸序列[66-67]。 研究發現,黑腹果蠅雌蟲中,dsx在上游基因tra/tra2的調控下形成雌性特異剪接體,促進雌性相關基因的表達,最終完成雌性的性別分化[68]。在家蠶中鑒定出了一個與黑腹果蠅dsx同源的基因Bmdsx,其受到Z染色體上Masc基因的調控。Bmdsx有6個外顯子,雄性早期胚胎中,Bmdsx轉錄成不含外顯子3和4的雄性特異BmdsxMmRNA,編碼蛋白BmDSXM,激活雄蟲中信息素結合蛋白(pheromone-binding protein, PBP)基因高表達,促進雄性生殖器的發育;而雌性特異BmdsxFmRNA則包含外顯子3和(或)4,編碼BmDSXF蛋白,正向調控雌蟲中表達的卵黃蛋白原(vitellogenin,Vg)基因和雌性特異六聚體儲存蛋白1(storage protein 1, Sp1)基因[69-73]。對其他鱗翅目昆蟲的dsx進行研究,發現dsx都在上游基因的調控下形成性別特異的剪接體,從而促進性別偏向基因的表達,實現性別分化(表3)[56,74-82]。 表3 鱗翅目昆蟲dsx基因研究進展Table 3 Research progresses in dsx gene in lepidopteran insects 目前在不少鱗翅目昆蟲中都發現了dsx的可變剪接,雄蟲大多只有一種剪接體,而雌蟲中卻有多種形式的剪接體。先后在家蠶中發現了BmdsxF1、BmdsxF2和BmdsxF3等3種雌性特異剪接體,產生的3種蛋白均能調控Vg、Sp1等在雌蟲中上調表達[69,83-84]。在小地老虎和小菜蛾中,dsx分別有6種和3種雌性特異的剪接體[76,78]。但對美國白蛾的研究發現,雄蛹中至少包含了3種dsx的剪接體,不同于其他物種dsx只有一種雄性特異剪接體的情況[82]。dsx除了能通過可變剪接調控雌雄性別分化外,還發現存在基因復制調控雌雄二型的分化。如Rodriguez-Caro等[74]在菊黃花粉蝶Zerenecesonia中發現了dsx的直系同源基因dsxA及其復制產生的旁系同源基因dsxB,dsxA在雄性翅中表達,dsxB在雌性翅中表達,從而調控翅膀雌雄二型的發育。這項研究的發現,表明dsx在控制昆蟲性別分化中的功能多樣。 昆蟲遺傳調控技術是通過對昆蟲的基因進行整合,讓靶標基因調控昆蟲的生長發育,從而導致害蟲種群衰退甚至滅亡。鑒于dsx基因的保守性,目前在鱗翅目昆蟲中,dsx是昆蟲遺傳調控中常用的可遺傳性別決定靶標基因[85]。其中基于dsx可變剪接構建的昆蟲不育技術(SIT)和釋放攜帶雌性特異顯性致死基因昆蟲技術(female-specific release of insects carrying dominant lethal, fsRIDL),已在家蠶、斜紋夜蛾、小菜蛾等昆蟲中進行研究。 SIT是指通過物理、化學處理或遺傳不育獲得不育雄蟲,然后將大量的不育雄蟲釋放到野外與野生型雌蟲進行交配,導致雌蟲不育或產生的后代不育,從而達到減少害蟲種群數量的目的。以草地貪夜蛾Sfdsx基因外顯子2、4和5為靶標分別設計構建突變體,其中外顯子2是雌雄蟲dsx剪接體共有的區域,外顯子4是dsx雌蟲剪接體特有的,而外顯子5是dsx雄蟲剪接體所特有的(圖2);讓這3種突變體分別與野生型的雌雄蟲配對,發現與野生型相比,這3種突變體繁殖力顯著下降。野生型雌蟲與雄蟲突變體(即突變外顯子5)交配后,其產卵量下降率達91%,卵的孵化率為0[80]。在美國白蛾中,利用dsx外顯子的特異性,敲除Hcdsx外顯子3和5后,分別獲得了雌蟲和雄蟲的不育突變體(圖2),發現敲除外顯子3的雄蟲生殖能力不受影響,讓該雄蟲突變體與野生型雌蟲進行雜交,顯示這種突變能在子代中繼續遺傳給下一代,且當子代雌性個體獲得純合的遺傳突變時表現為不育[61]。雖然鱗翅目昆蟲dsx的突變能產生雌雄性別特異的不育成蟲,但還有待進行后續的田間試驗。 圖2 草地貪夜蛾和美國白蛾基于dsx可變剪接構建的突變位點示例圖Fig.2 Constructed mutation sites based on dsx variable splicing in Spodoptera frugiperda and Hyphantria cunea fsRIDL通過將致死基因與某些能進行性別特異剪接的基因或性別特異性啟動子相結合,使致死基因能在雌蟲中特異性表達,而同樣攜帶致死基因的雄蟲則正常生長發育。當攜帶致死基因的雄蟲釋放到田間與野生型雌蟲進行交配后,致死基因能在后代中順利表達,并導致子代雌蟲死亡,最終達到消滅害蟲種群的目的[86-87]。目前,鱗翅目中常見的fsRIDL系統是基于dsx可變剪接構建的四環素調控系統(Tet-off)。Tet-off有調節元件(tTAV)和反應元件(tetO)兩部分,正常情況下,tTAV與tetO相結合,增強tetO下游基因的表達,形成一個正向反饋循環系統;當四環素或四環素類似物等解毒劑存在時,解毒劑與tetO結合,tTAV的表達被抑制[86]。根據鱗翅目昆蟲雌雄蟲dsx的剪接形式不同,將調節元件tTAV插入雌性特異剪接體所特有的外顯子3中,而反應元件tetO則插入到雌雄蟲dsx剪接體所共有的外顯子2中(圖3)。當飼料中有解毒劑時,解毒劑與tetO結合,使得tTAV的轉錄停止,雌蟲生長發育正常;但停止提供解毒劑時,雌蟲中tTAV與tetO正常結合, tTAV蛋白不斷積累造成對細胞的毒害,最終導致雌蟲在幼蟲期就死亡。而雄蟲中dsx的可變剪接不包含調節元件tTAV,因此有無解毒劑都不會激活tetO下游基因的表達,雄蟲均能正常生長發育。基于dsx可變剪接構建的fsRIDL已在棉紅鈴蟲Pectinophoragossypiella、家蠶以及小菜蛾中成功實現[88-89]。在溫室中引入Tet-off篩選出來的小菜蛾雄成蟲,發現轉基因雄成蟲競爭野生雌蛾進行交配的能力比野生雄蟲強,最終成功導致野生種群數量下降,同時發現釋放該轉基因雄成蟲還能延緩Bt抗性在小菜蛾自然種群中的擴散,具較好的種群控制作用[90]。 圖3 基于dsx基因性別特異性可變剪接與Tet-off系統相結合的fsRIDL結構示例圖Fig.3 Schematic representation of fsRIDL of Tet-off system constructs based on dsx female- and male-specific variable splicing 不少研究人員在雙翅目、鞘翅目和膜翅目昆蟲的性別決定通路中都發現tra和tra2基因參與調控dsx基因的可變剪接,在家蠶中也發現tra2的同源基因Bmtra2參與調控Bmdsx,且敲除Bmtra2后,導致雌雄蟲在胚胎期死亡[91]。基于Bmtra2基因這一性質,研究人員利用類轉錄激活因子效應物核酸酶(transcription activator-like effector nuclease, TALEN)技術介導同源重組,將Cas9基因轉入家蠶W染色體中,構建了雌性特異表達Cas9的品系;以 PiggyBac轉座子的方式將sgRNA(靶標Bmtra2)整合到雄蟲染色體中,構建了雄性特異表達sgRNA的品系。2種品系雜交產生的子代中,雌蟲Cas9和sgRNA同時表達時,Bmtra2被敲除,在胚胎期死亡;而雄胚胎中無Cas9的表達,成功存活(圖4)[92]。這為基于基因組編輯工具對昆蟲性染色體實施基因定點整合、實現蠶業早期篩選大量雄蠶以及鱗翅目害蟲遺傳調控技術提供了理論與實踐依據。 圖4 通過CRISPR/Cas9技術進行家蠶W染色體連鎖靶基因整合操作示例圖Fig.4 Diagram of target gene integration operation linked to the W chromosome of silkworms by CRISPR/Cas9 technology 傳統的SIT有輻射不育、化學不育、胞質不親和性染色體易位等,研究較多的是輻射不育[93]。但輻射不育的突變體常產生較大的適合度代價,競爭交配能力弱,難以持續有效地控制害蟲的數量;當有新蟲源加入種群,依然有大暴發的可能性,需要多次大量釋放才能達到預期效果[94]。近年來,隨著對昆蟲性別決定機制的不斷研究,性別決定途徑已經并將繼續成為昆蟲種群調控技術的重要組成部分,對性別決定和性別分化相關基因的研究將促進SIT的發展。如對岡比亞按蚊Anophelesgambiae的dsx基因進行雌性特異的突變,導致雌性純合突變體完全不育,但并不會影響雄蟲的繁殖能力[95]。對dsx雌雄蟲特異的剪接體進行基因編輯獲得雌性或雄性不育的成蟲,已在埃及伊蚊Aedesaegypt、橘小食蠅Bactroceradorsalis、草地貪夜蛾、美國白蛾等多種昆蟲中成功應用[61,80,96-97]。除了dsx基因,還有對性別分化相關基因的研究,如利用CRISPR/Cas9技術對地中海實蠅Ceratitiscapitata的tra2基因的ts2位點進行點突變,獲得的純合tra2ts2突變體成功實現了由雌蟲到雄蟲的性別轉換[98]。同樣地,利用CRISPR/Cas9基因組編輯技術敲除斜紋夜蛾雄蟲分化基因Ser2導致了雄蟲不育,而雌蟲生殖功能正常。將構建的雄蟲不育品系與野生型雌蟲進行雜交后,只有少數卵能孵化。研究者進一步檢測Ser2突變體雄蟲不育表型的可遺傳性,發現在斜紋夜蛾中,雄性不育表型能在后代中穩定遺傳[59]。除了利用CRISPR直接敲除關鍵基因,實現雌蟲的性別逆轉或雄蟲不育,基于CRISPR的精確引導SIT技術(precision guided SIT, pgSIT)則通過同時破壞雄蟲生殖能力和雌蟲生存能力所必需的基因,確保所有存活的F1代都是不育的雄蟲,以達到直接釋放基因編輯過的卵就能抑制種群的效果,是一種更實用的SIT新技術[99]。該技術已在果蠅和埃及伊蚊中應用,果蠅中同時敲除βTub、sxl基因成功導致100%的雄性不育和雌性致死;埃及伊蚊中同時敲除βTub、myo-fem基因成功導致雄性不育和雌性無飛行能力,無飛行能力的雌蟲存活率和繁殖力均明顯降低。模擬pgSIT,基于Wolbachia的不相容昆蟲技術(incompatible insect technique,IIT)、RIDL和fsRIDL技術對種群密度進行控制,發現直接釋放pgSIT處理的埃及伊蚊卵抑制種群的效果最好,表現出強大的應用潛力[99-100]。目前在家蠶、香梨優斑螟Euzopherapyriella中已發現tra2的同源基因[77,101]。Ser2基因已被證實在家蠶、小菜蛾的雄性生殖和不育中發揮重要作用[102]。因此未來繼續對鱗翅目dsx、tra2和Ser2等性別分化相關基因的功能進行研究,將會豐富SIT的潛在靶基因,為pgSIT等技術在鱗翅目昆蟲中的應用奠定理論基礎。 性別決定初始信號在不同昆蟲中表現出多樣性和專一性,家蠶中以Fem為雌蟲分化的初始信號,果蠅以XSE的表達量作為調控性別的初始信號,意大利蜜蜂Apismellifera則以Csd基因的純合/雜合作為信號[43,103-104]。對性別決定初始信號進行敲入或敲除,能實現雌雄蟲完全的性別逆轉。如Nix基因是埃及伊蚊雄蟲的性別決定初始信號,研究人員構建Nix轉基因雌蟲品系,成功實現了雌蟲100%轉化為可育的雄蟲,且該性別逆轉獲得的雄蟲能繼續穩定地產生后代。同時有模擬顯示,釋放這種含性別轉化純合基因的雄蟲能實現種群的自我維持,會比SIT更有效地抑制害蟲種群[105-107]。然而家蠶雄蟲中表達Fem時,并未出現從雄性到雌性的性別逆轉突變體,推測家蠶中可能還存在另一種主要的性別決定初始信號[108]。因此未來繼續對鱗翅目性別決定初始信號進行研究,實現從雌性到雄性的完全性別逆轉,或將降低實現雌雄蟲分離和害蟲防控的成本。2 鱗翅目昆蟲性別決定機制研究進展
2.1 鱗翅目性別決定初始信號研究進展
2.2 鱗翅目昆蟲Masc基因研究進展
2.3 鱗翅目昆蟲dsx基因研究進展
3 鱗翅目性別決定機制在昆蟲遺傳調控中的應用
3.1 基于dsx可變剪接構建的昆蟲不育技術(SIT)研究進展
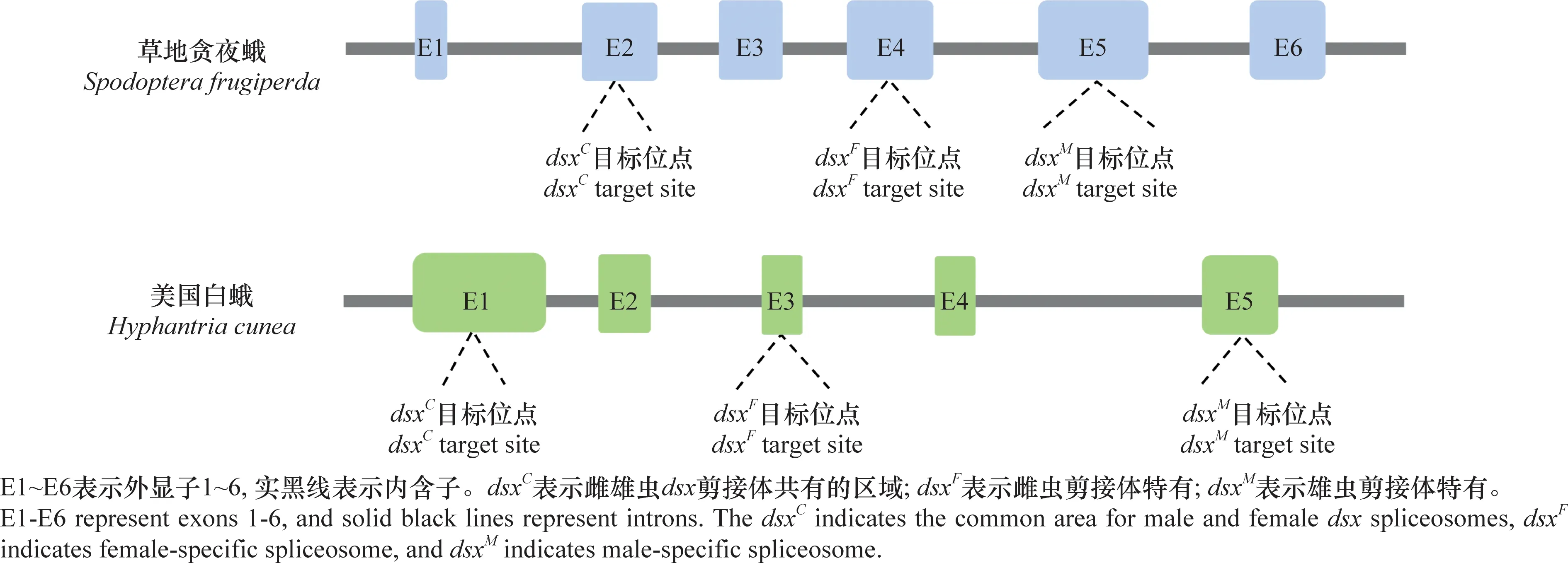
3.2 基于dsx可變剪接構建的釋放攜帶雌性特異顯性致死基因昆蟲技術(fsRIDL)研究進展
3.3 其他性別相關基因在鱗翅目性別篩選中的應用
4 展望

