ADC類藥物治療乳腺癌療效與安全性的Meta分析Δ
徐吟雪,張蕾,喬熙雯,沈曉嵐,沈倩,張學會 (南京醫科大學附屬江蘇盛澤醫院藥學部,江蘇 蘇州 215228)
根據2020年全球癌癥統計,乳腺癌在女性惡性腫瘤中占據首位,且死亡率位居女性惡性腫瘤第二位[1]。抗體藥物偶聯物(antibody-drug conjugate,ADC)是一類由抗體、連接頭和細胞毒性藥物組成的靶向生物藥,此類藥物以單抗為載體,可將小分子細胞毒性藥物靶向、高效地運輸至目標腫瘤細胞內而發揮抗腫瘤的作用,目前主要用于治療乳腺癌[2],代表藥物有恩美曲妥珠單抗(trastuzumab emtansine,T-DM1)、德曲妥珠單抗(trastuzumab deruxtecan,T-Dxd)和戈沙妥珠單抗(sacituzumab govitecan,SG)。《美國國立綜合癌癥網絡乳腺癌臨床實踐指南 v3.2022》推薦T-DM1和T-Dxd為人表皮生長因子受體-2(human epidermal growth factor receptor 2,HER2)陽性復發轉移性乳腺癌患者的二線用藥,且T-Dxd為首選方案[3]。《中國臨床腫瘤學會(CSCO)乳腺癌診療指南(2023)》中,對于曲妥珠單抗治療失敗的HER2陽性晚期乳腺癌患者,T-DM1為Ⅰ級推薦,T-Dxd為Ⅱ級推薦;對于紫杉類藥物治療失敗的三陰性乳腺癌(triple-negative breast cancer,TNBC)晚期患者,SG為Ⅱ級推薦[4]。有研究顯示,在曲妥珠單抗治療失敗后,T-Dxd較T-DM1更能顯著改善患者的無進展生存期(progression-free survival,PFS),疾病進展或死亡風險比(hazard ratio,HR)降低了72%[5]。ASCENT研究結果顯示,在既往多線耐藥的難治性TNBC患者中,與單藥化療(如卡培他濱、艾立布林等)相比,SG降低了患者59%的疾病進展風險以及52%的死亡風險[6—7]。雖然已有一些新的關于ADC類藥物的臨床研究數據公布,但其療效和安全性尚不明確,因此有必要對ADC類藥物治療乳腺癌的療效與安全性進行評價。為此,本研究采用Meta分析的方法評價了ADC類藥物治療乳腺癌的療效和安全性,以期為臨床用藥提供循證依據。
1 資料與方法
1.1 納入與排除標準
1.1.1 研究類型
本研究納入文獻類型為國內外公開發表的隨機對照試驗(randomized controlled trial,RCT);語種限定為中文或英文。
1.1.2 研究對象
本研究納入的患者均經組織病理學診斷為乳腺癌。
1.1.3 干預措施
試驗組患者給予T-DM1、T-Dxd或SG;對照組患者給予化療藥物(如卡培他濱、吉西他濱、艾立布林等)或其他抗腫瘤藥物(如曲妥珠單抗、多西他賽、拉帕替尼、紫杉醇等)。
1.1.4 結局指標
本研究的結局指標包括:(1)PFS;(2)總生存期(overall survival,OS);(3)客觀緩解率(objective response rate,ORR);(4)臨床獲益率(clinical benefit rate,CBR);(5)3/4級不良反應(adverse drug reactions,ADR)發生率。
1.1.5 排除標準
本研究的排除標準包括:(1)評論、個案報道、綜述、系統性評價文獻;(2)無法獲取全文、數據不全的文獻;(3)無法提取結局指標的文獻。
1.2 文獻檢索策略
計算機檢索PubMed、the Cochrane Llibrary、Embase、Web of Science、中國知網、萬方數據庫、維普網,英文檢索詞為“breast neoplasm”“breast cancer”“sacituzumab govitecan”“SG”“trodelvy”“trastuzumab emtansine”“TDM1”“trastuzumab deruxtecan”“T-Dxd”;中文檢索詞為“乳腺腫瘤”“乳腺癌”“戈沙妥珠單抗”“恩美曲妥珠單抗”“德曲妥珠單抗”。采用主題詞和自由詞相結合的方式檢索,檢索時限均為建庫起至2023年4月。
1.3 文獻篩選與資料提取
由2名研究者獨立按納入與排除標準篩選文獻,如遇分歧則通過討論或由第三方解決。提取數據包括:第一作者及發表年份、樣本量、干預措施、結局指標等。
1.4 文獻質量評價
采用Cochrane系統評價員手冊推薦的5.1.0偏倚風險評估工具進行質量評價,具體包括:隨機分配方法、是否實施分配隱藏、對患者和研究者采用盲法、對結果測量者采用盲法、結果數據完整性、選擇性報告結果和其他偏倚來源。每個條目分為“高偏倚”“低偏倚”“不清楚”[8]。
1.5 統計學方法
采用RevMan 5.4.1軟件進行Meta分析。PFS、OS以HR及其95%置信區間(confidence interval,CI)表示,ORR和CBR及3/4級ADR發生率以比值比(odds ratio,OR)及其95%CI表示。采用χ2檢驗分析各研究間的異質性,若P>0.1,I2<50%,表明各研究間無統計學異質性,采用固定效應模型分析;反之,則采用隨機效應模型分析。若結果存在臨床異質性,則進行亞組分析;若結果無臨床異質性,則進行敏感性分析。檢驗水準α=0.05。
2 結果
2.1 文獻篩選結果與納入研究基本信息
初檢共檢索到6 067篇文獻,經閱讀題目、摘要及全文后,最終納入文獻8篇[9—16],共計5 577例患者,其中試驗組2 988例,對照組2 589例。結果見圖1、表1。
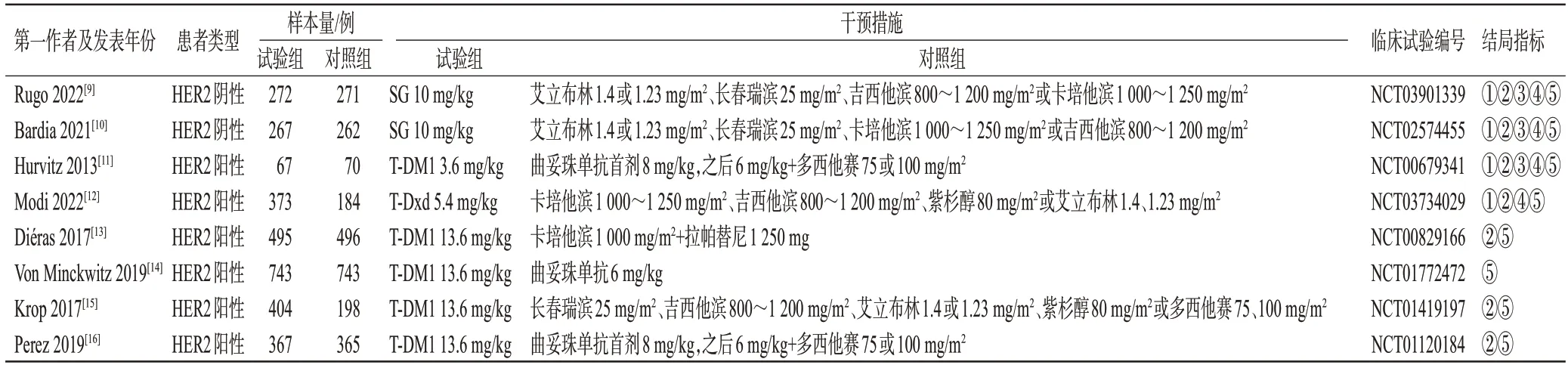
表1 納入研究的基本信息
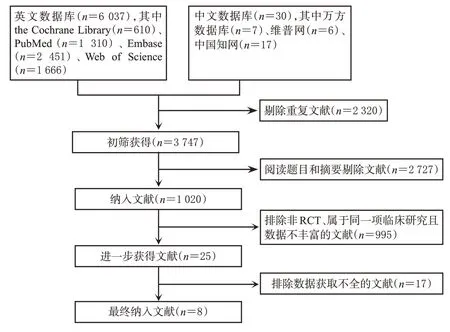
圖1 文獻篩選流程圖
2.2 納入文獻的質量評價結果
8項研究均為RCT[9—16];所有研究均為合理產生分配序列,均不清楚分配隱藏;4項研究對研究者和受試者均采用盲法[9—10,12,15],6項研究在結局評估時使用盲法[9—10,12—13,15—16];所有研究結局數據完整,均未選擇性報告結果,均不清楚是否存在其他偏倚來源。結果見圖2、圖3。
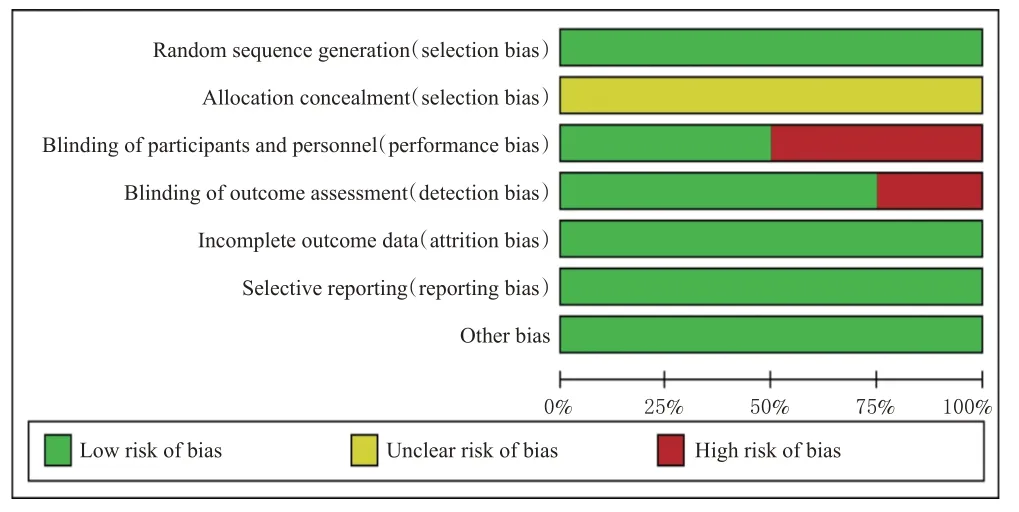
圖2 偏倚風險條形圖
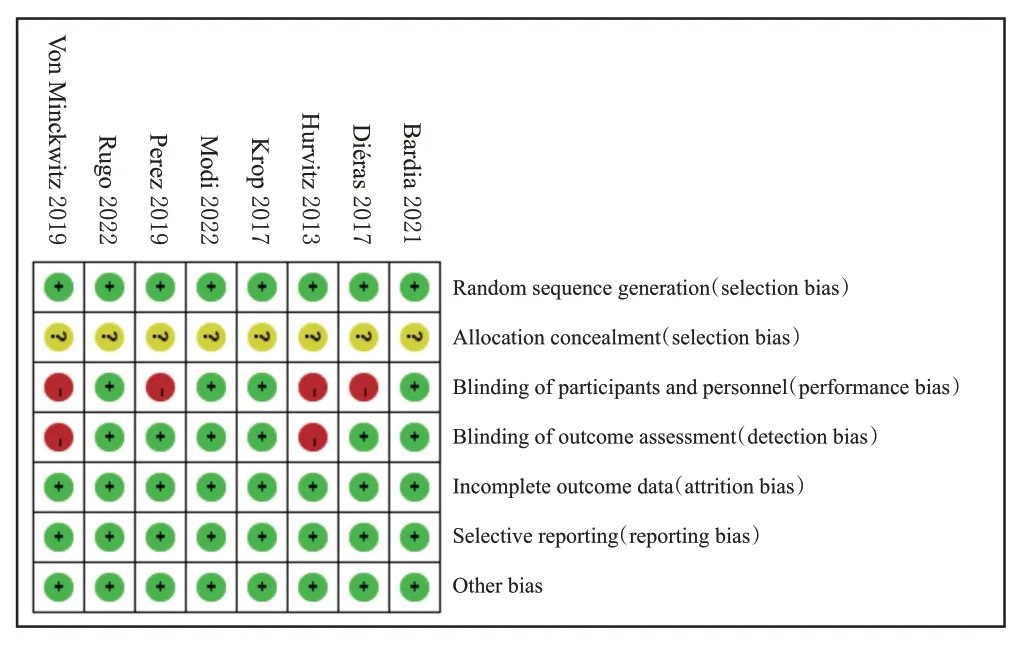
圖3 偏倚風險圖
2.3 Meta分析結果
2.3.1 PFS
4項研究報道了PFS[9—12],各研究間有統計學異質性(P=0.05,I2=61%),采用隨機效應模型。結果顯示,試驗組患者的PFS顯著長于對照組[HR=0.76,95%CI(0.69,0.83),P<0.000 01],詳見圖4。
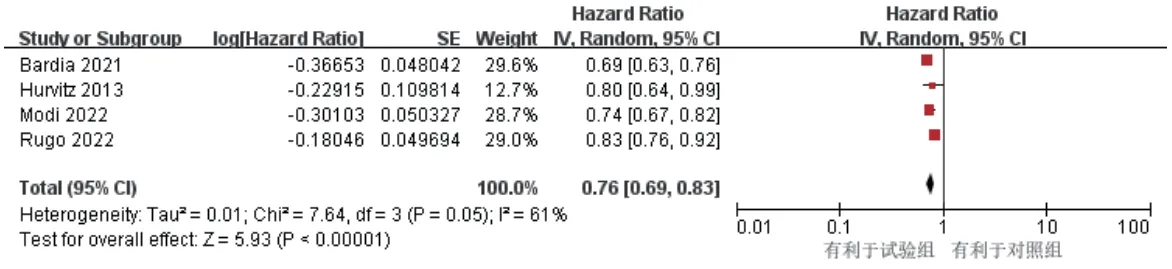
圖4 PFS的Meta分析森林圖
按HER2表達的不同進行亞組分析。結果顯示,試驗組HER2陽性患者[HR=0.75,95%CI(0.69,0.82),P<0.000 01]、HER2陰性患者的PFS[HR=0.76,95%CI(0.63,0.91),P=0.003]均顯著長于對照組,詳見表2。
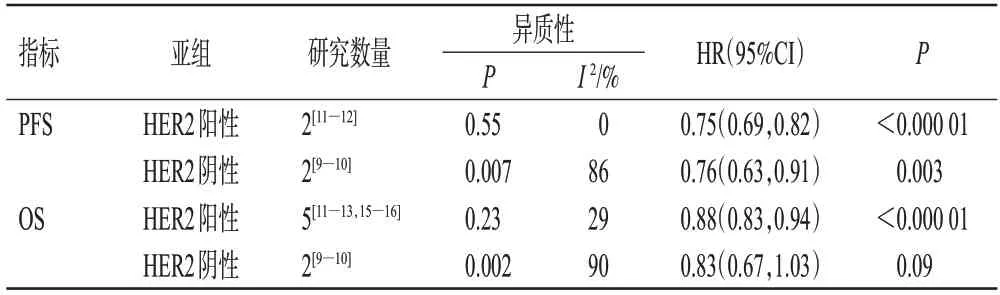
表2 兩組患者PFS和OS的亞組分析結果
2.3.2 OS
7項研究報道了OS[9—13,15—16],各研究間有統計學異質性(P=0.005,I2=68%),采用隨機效應模型。結果顯示,試驗組患者的OS顯著長于對照組[HR=0.87,95%CI(0.81,0.93),P<0.000 1],詳見圖5。
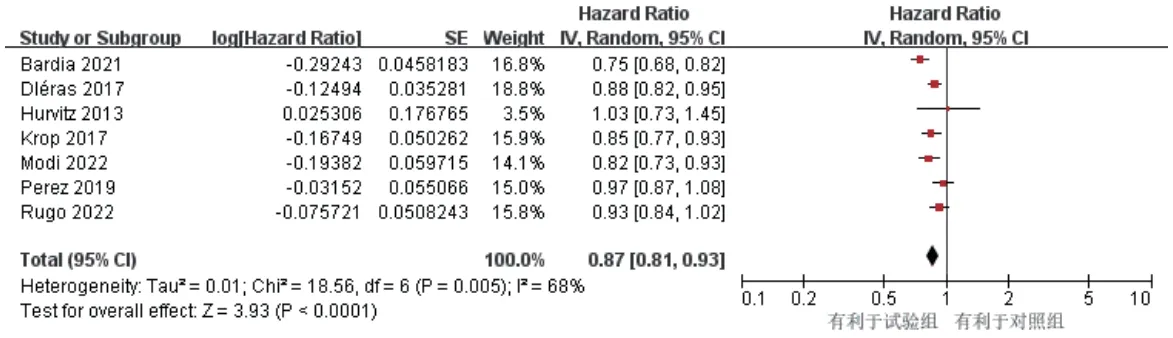
圖5 OS的Meta分析森林圖
按HER2表達的不同進行亞組分析。結果顯示,試驗組HER2陽性患者的OS[HR=0.88,95%CI(0.83,0.94),P<0.000 01]顯著長于對照組;兩組HER2陰性患者的OS[HR=0.83,95%CI(0.67,1.03),P=0.09]比較,差異無統計學意義,詳見表2。
2.3.3 ORR
3項研究報道了ORR[9—11],各研究間有統計學異質性(P<0.000 01,I2=94%),采用隨機效應模型。結果顯示,兩組患者的ORR比較,差異無統計學意義[OR=2.34,95%CI(0.59,9.33),P=0.23],詳見圖6。
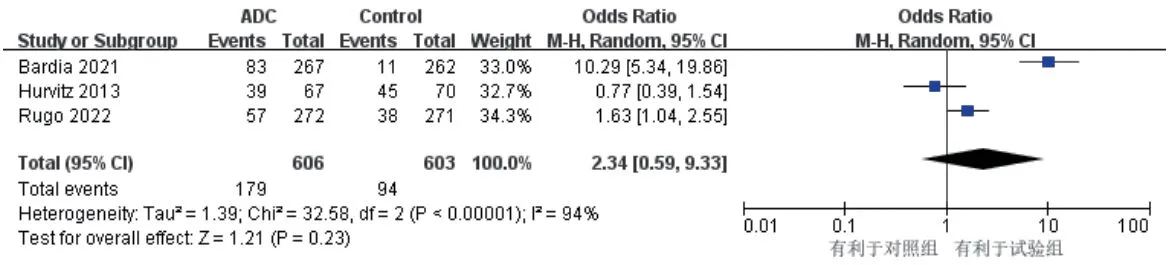
圖6 ORR的Meta分析森林圖
2.3.4 CBR
4項研究報道了CBR[9—12],各研究間有統計學異質性(P<0.000 01,I2=92%),采用隨機效應模型。結果顯示,試驗組患者的CBR顯著高于對照組[OR=2.70,95%CI(1.15,6.33),P=0.02],詳見圖7。
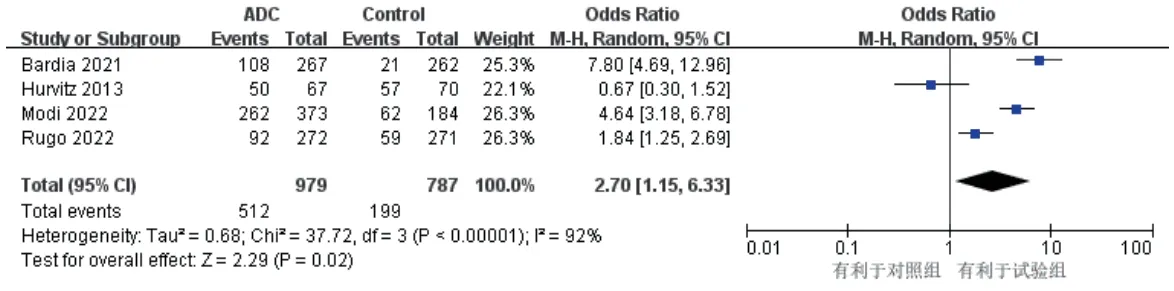
圖7 CBR的Meta分析森林圖
2.3.5 3/4級ADR發生率
試驗組患者的貧血、天冬氨酸轉氨酶升高發生率均顯著高于對照組(P<0.05);兩組患者的中性粒細胞減少、白細胞減少、腹瀉、嘔吐發生率比較,差異均無統計學意義(P>0.05)。結果見表3。
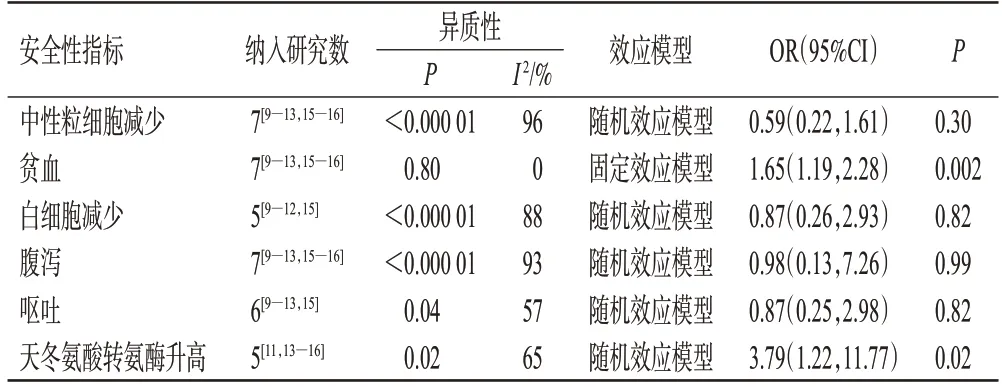
表3 兩組患者3/4級ADR發生率的Meta分析結果
2.4 敏感性分析
以PFS、OS、ORR為指標,逐一剔除各項研究后,所得結果異質性改變較明顯,但結果無統計學意義上的改變,表明上述結果穩健。以CBR為指標,逐一剔除各項研究后,所得結果差異無統計學意義,表明CBR的Meta分析結果易因研究數量變化而改變,缺乏穩健性,結果需謹慎對待。
3 討論
T-DM1是我國第一個獲批的ADC類藥物,用于治療HER2陽性乳腺癌患者。T-Dxd是T-DM1后的新一代ADC類藥物,具有毒性低、復發率低、療效好、安全性可靠等特點[17]。SG是由SN-38(伊立替康的活性代謝產物)通過可水解連接頭與滋養層細胞表面抗原2(trophoblast cell surface antigen 2,Trop-2)偶聯形成的[18],作為一種抗Trop-2的新型ADC類藥物,SG為晚期TNBC患者帶來了更多治療選擇。
EMILIA試驗結果顯示,與拉帕替尼聯合卡培他濱相比,T-DM1能顯著延長HER2陽性晚期乳腺癌患者的OS和PFS,同時也得到了更好的ORR和中位緩解持續時間(duration of overall response,DOR)[19]。另有研究表明,T-Dxd用于HER2低表達轉移性乳腺癌患者的中位DOR和中位PFS分別為10.4、11.1個月[20]。此外,一項Ⅰ/Ⅱ期試驗(IMMU-132-01)也證實,SG用于晚期TNBC的療效顯著[21]。本研究結果顯示,與對照組比較,試驗組患者的PFS、OS顯著延長,CBR顯著升高,這表明ADC類藥物在治療乳腺癌方面效果顯著,能顯著延長患者生存時間和改善預后,提示當乳腺癌患者使用其他化療藥物療效欠佳時,可以根據情況選擇ADC類藥物。
本研究中,兩組患者的ORR比較,差異無統計學意義,表明ADC類藥物在減小腫瘤體積方面無顯著優勢,提示ADC類藥物可能更適用于輔助治療原發腫瘤體積較小的患者[22]。有文獻報道,HER2陽性患者可在TDM1和T-Dxd治療中獲益[12—13],而HER2陰性患者使用SG獲益更多[10]。本研究的亞組分析結果顯示,試驗組HER2陽性患者的PFS、OS均顯著長于對照組;試驗組HER2陰性患者的PFS顯著長于對照組,但兩組HER2陰性患者的OS比較,差異無統計學意義。由于納入HER2陰性亞組的研究僅2篇,且這2篇文獻都是SG的相關研究,因此,造成兩組HER2陰性患者在OS指標上無顯著性差異的原因可能是本研究納入的SG相關研究和患者數量較少。
本研究結果還顯示,試驗組患者貧血發生率顯著高于對照組。貧血的發生可能與ADC類藥物所載藥物相關,表現出與細胞毒化療藥物相似的骨髓抑制,從而造成血液系統不良反應[23]。T-DM1、T-Dxd和SG屬于不同化學結構的ADC類藥物,其載藥量也不盡相同,因此其誘導產生的血液系統不良反應也有所區別,臨床使用時應針對不同ADC類藥物引起的血液系統不良反應選擇不同的干預措施。此外,試驗組患者天冬氨酸轉氨酶升高發生率顯著高于對照組,這與Zhang等[24]的研究結果一致。ADC類藥物與嚴重的肝毒性密切相關,以TDM1為例,當其被肝臟分解代謝后,其中的微管蛋白抑制劑被釋放到肝細胞中,從而破壞肝臟的微管網絡,導致細胞有絲分裂和凋亡停止[25]。因此,使用ADC類藥物時應注意潛在的肝毒性,密切監測患者的肝功能,如果患者肝功能出現異常,應盡快干預。敏感性分析結果顯示,以PFS、OS、ORR為指標時,所得結果較穩健;以CBR為指標時,所得結果缺乏穩健性。
綜上所述,ADC類藥物用于乳腺癌的療效顯著,但會增加貧血和天冬氨酸轉氨酶升高的發生風險。本研究的局限性為:(1)納入的文獻較少,無法進行發表偏倚分析;(2)納入的部分研究缺少患者臨床病理分期的相關信息;(3)納入文獻的異質性較大,可能與樣本量較小、不同組間使用的對照藥物不同有關。故本研究所得結論尚需大樣本、高質量的RCT進一步驗證。

