人臍帶間充質干細胞在脊髓損傷修復中的研究進展
李永超, 馮曉飛, 蘇啟航, 譚 軍, 李立鈞
(同濟大學附屬東方醫院脊柱外科,上海 200120)
脊髓損傷(spinal cord injury, SCI)發病率和致殘率高,給患者家庭和社會帶來了沉重的負擔,其治療和康復現已成為醫學研究的一大難點[1-2]。臨床上,治療SCI的常見方法包括藥物、手術和康復鍛煉,但只能部分改善癥狀,很難從根本上恢復損傷的脊髓。大多數SCI患者仍然失去神經功能,部分原因是脊髓自身再生能力非常有限[1,3]。因此,迫切需要一種新穎、有效的SCI治療方法,以挽救喪失的脊髓功能[4]。
近年來,干細胞移植技術的進步和對SCI病理生理學機制的深入研究,給SCI患者帶來了新的希望[5-8]。目前,已發現多種可用于修復SCI的種子干細胞,見表1[5]。在眾多干細胞中,人臍帶間充質干細胞(human umbilical cord mesenchymal stem cells, hUC-MSCs)移植可能是修復損傷脊髓極具吸引力的治療選擇之一[9-11]。hUC-MSCs具有取材方便、易于運輸、低免疫原性、無倫理爭議、無成瘤性、快速增殖和多向分化等優點[12]。臨床前動物研究已證實hUC-MSCs修復SCI的巨大潛力,但臨床轉化并不順利[6,13-14]。其臨床最佳移植途徑、劑量、時間窗,以及hUC-MSCs脊髓修復機制、臨床安全性和有效性等仍需進一步探索。本文就hUC-MSCs治療SCI的最新研究進展進行綜述。
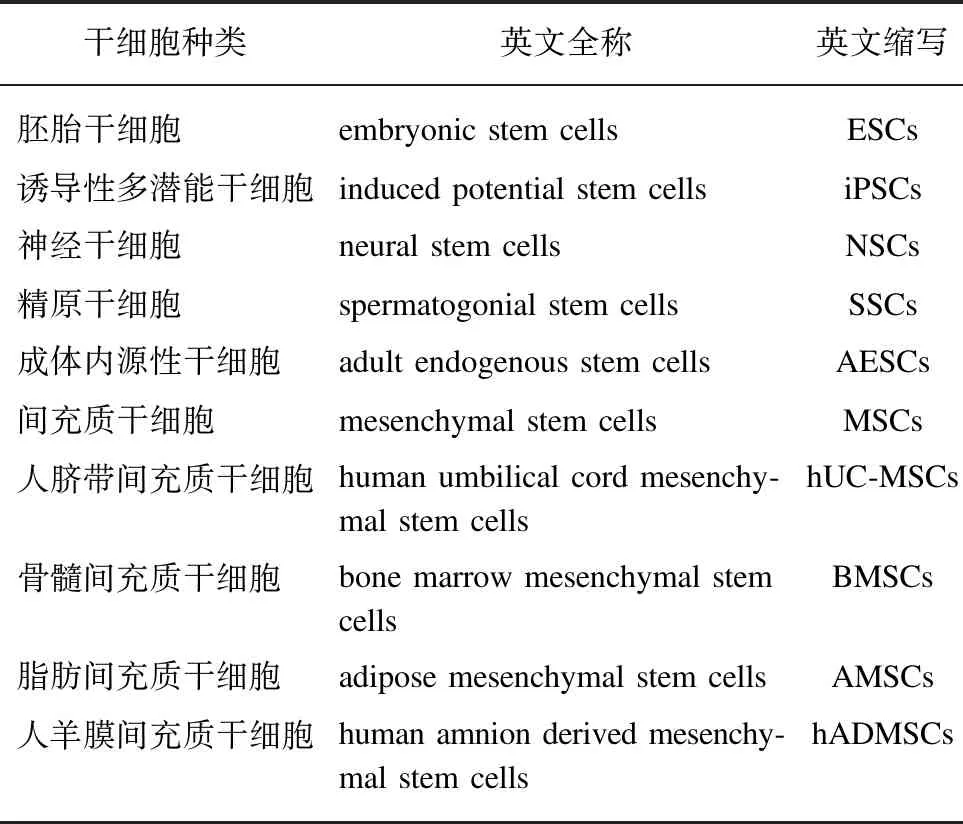
表1 用于修復SCI的干細胞分類
1 SCI的病理生理和分子病理機制
損傷脊髓神經功能的恢復與不同病理生理時期密切相關[1]。SCI急性期(2周內)以免疫炎癥反應為主;亞急性期(2周-2個月)表現為神經元壞死及神經抑制因子表達升高;慢性期(>2個月)表現為軸突變性、空洞和膠質瘢痕形成,導致神經功能永久喪失[1,10]。在分子病理機制層面,SCI也可分為原發性脊髓損傷和繼發性脊髓損傷[9,15]。繼發性脊髓損傷包括炎性反應、神經細胞死亡和微環境失衡等在內的一系列復雜的病理反應[9]。在繼發性脊髓損傷中,微環境失衡是限制脊髓修復的關鍵因素[9]。目前,針對SCI后不同分子病理特點和病理生理時期,通過抗炎、神經營養和免疫調節等作用,以改善失衡的脊髓微環境是治療SCI的關鍵[9-10,15]。
2 hUC-MSCs的生物學特性
臍帶具有來源廣泛,取材方便無創等優點,其動靜脈之間含有特殊的胚胎黏液樣結締組織(沃頓膠),而從中分離得到的基質細胞即為hUC-MSCs[16-17]。hUC-MSCs表達具有干細胞特性的標志,且具有自我更新、大量增殖和多向分化潛能,其誘導培養能向神經元細胞、骨細胞等多種成體細胞分化[12,16]。hUC-MSCs除了具有向神經細胞分化的潛能,也有很強的自分泌與旁分泌功能[18]。此外,hUC-MSCs很少表達人類白細胞Ⅰ類抗原、缺乏人類白細胞DR抗原和共刺激分子CD40和CD80,且擁有較低的免疫原性和良好的移植后受體耐受性[19]。
3 hUC-MSCs對SCI的神經修復機制
目前,hUC-MSCs對SCI的詳細神經修復機制尚未完全的闡明,可大致概括為3個方面[10,14,20-25]。
(1) 通過分泌各種因子保護神經元,促進殘存神經元軸突的再生和突觸形成,并促使損傷脊髓局部的血管再生。Xie等[14]大鼠SCI動物模型發現,移植hUC-MSCs可分泌神經生長因子,維持細胞在高活性氧微環境中的活力,使損傷脊髓得到有效恢復。此外,Xiao等[21]通過體外研究證實hUC-MSCs分泌的外泌體可通過miR-29b-3p/PTEN軸激活PI3K/AKT通路減少SCI神經元的凋亡。與此同時,Cao等[26]研究發現,在亞急性SCI大鼠模型中,hUCMSCs有效劑量移植可促進γ-氨基丁酸A型(γ-aminobutyric acid A, GABAA)受體表達的部分恢復,提示GABAA受體可能是SCI的治療靶點。
(2) 改善損傷脊髓局部微環境,減輕炎癥反應,并減少脊髓空洞、膠質瘢痕的形成和瘢痕的屏障阻礙作用。Liu等[22]研究發現大鼠SCI造模后血清中促炎細胞因子IL-1β、IFN-γ、IL-6和TNF-α升高。而鞘內注射hUC-MSCs治療3、7 d后,IFN-γ、IL-6和TNF-α呈明顯下降趨勢。Zhu等[27]研究發現hUC-MSCs移植治療小鼠急性脊髓損傷可促進運動功能的恢復,且與對小膠質細胞的抑制作用密切相關。他們認為hUC-MSCs移植治療急性SCI的效果取決于其對神經損傷后炎癥反應的抑制能力。此外,Li等[23]發現hUC-MSCs可能通過抑制Ⅰ型膠原蛋白、Ⅲ型膠原蛋白、FGF 2、p-p38、TRPV1、TLR4和p-NF-κB的表達,在急性SCI后膀胱功能重建中發揮關鍵作用。
(3) 可多向分化為神經元和少突膠質細胞,促進軸突再生、髓鞘化和重建神經環路。Cao等[25]發現hUC-MSCs移植通過調節損傷脊髓的繼發性免疫炎癥反應和PTBP-1表達,調節瘢痕形成和神經元再生,促進SCI小鼠功能恢復。
此外,hUC-MSCs還可釋放含有大量生物活性分子的微泡和外泌體,刺激神經軸突再生、抑制瘢痕形成,同時加速血管再生和重建,發揮抗炎、抗凋亡作用,促進脊髓損傷的恢復[17,20]。Kang等[24]發現來自hUC-MSCs的外泌體可通過激活Wnt信號通路,降低小鼠小膠質細胞和星形膠質細胞的激活,抑制了神經元的凋亡,增強SCI小鼠的運動功能。
4 hUC-MSCs治療SCI的最佳移植途徑、劑量和時機
目前,hUC-MSCs的移植途徑主要有鞘內注射、損傷局部注射和靜脈輸注。損傷局部注射可將hUC-MSCs直接注射至損傷脊髓周圍,但也有導致脊髓二次損傷和出血風險。而靜脈輸注簡單易行,風險相對較小,但多數hUC-MSCs遷移到肺、脾臟和腎臟,很少遷移至脊髓損傷部位。蛛網膜下腔鞘內注射可避免上述問題,簡便易行,損傷小,且hUC-MSCs可從蛛網膜下腔遷移至脊髓損傷部位,保障足夠的細胞數量[20]。有研究發現,鞘內遞送后細胞植入和組織保存明顯更好,并且蛛網膜下腔鞘內注射降低了宿主免疫反應。相較于其他細胞輸送方法,鞘內注射能更好地恢復脊髓功能[28]。2022年,Liu等[22]發現相比靜脈注射,鞘內注射hUC-MSCs對SCI大鼠具有劑量依賴的神經保護作用,可減少移植所需的細胞數量,是治療需要控制炎性細胞因子或組織修復的SCI的更合適的方法。Lu等[10]基于動物研究的系統綜述和Meta分析發現局部hUC-MSCs移植(鞘內注射或損傷局部注射)的治療效果明顯優于靜脈移植。Chen等[29]通過Meta分析發現鞘內注射移植入路對脊髓損傷患者的神經功能改善最大。因此,微創蛛網膜下腔鞘內注射被認為是最安全、最有效的hUC-MSCs輸送方法[1]。
hUC-MSCs的移植劑量決定了到達損傷部位的有效干細胞的數量,且與SCI的修復密切相關。與骨髓間充質干細胞相比,hUC-MSCs體積更小,在宿主環境中更具移動性,更容易通過體內的各種屏障,更小的體積可以容納更多的細胞。因此,hUC-MSCs的劑量依賴效應更為明顯。然而,過大的移植劑量可能導致細胞團的形成,導致器官和組織栓塞,從而影響干細胞的功能。反之,過低劑量的干細胞不能充分發揮修復作用,因為沒有足夠劑量的干細胞到達損傷部位。為了保證足夠的干細胞發揮修復作用,必須增加干細胞的移植劑量[10]。Cao等[26]研究發現,在亞急性SCI大鼠模型中,1×106hUC-MSCs/kg的劑量(而不是0.25×106hUC-MSCs/kg的較低劑量)與4×106hUC-MSCs/kg一樣有效地改善功能恢復。因此,他們認為鞘內植入1×106hUC-MSCs/kg是治療亞急性脊髓損傷的替代方法。有研究表明,過高劑量的細胞移植可引發強烈的炎癥反應,從而降低干細胞的修復效果[12]。最近,Lu等[10]基于動物研究的系統綜述和Meta分析發現無論何種移植途徑和時機,都得到了相同的結果,即高劑量≥1×106hUC-MSCs移植優于低劑量<1×106hUC-MSCs移植。此外,由于鞘內注射的hUC-MSCs生存時間有限,相同劑量的hUC-MSCs移植后,重復移植的效果明顯優于單次移植。因此,多次重復注射hUC-MSCs可能是提高干細胞修復效果的一種潛在策略,值得未來繼續探索[10]。
hUC-MSCs在體內容易受損傷脊髓局部微環境的影響,因此選擇最佳的移植時機非常重要。hUC-MSCs移植過早會導致細胞壞死,過晚容易受膠質瘢痕影響,阻礙神經纖維再生[10]。此外,hUC-MSCs可分泌多種因子,更早期移植利于消除或減輕繼發性脊髓損傷。Lu等[10]基于動物研究的Meta分析發現亞急性hUC-MSCs移植的治療效果明顯優于急、慢性移植。因此,他們認為SCI亞急性期(2周-2個月)移植是hUC-MSCs的最佳移植時機。也有研究發現,hUC-MSCs的最佳移植時機是損傷后3-4周內,既可避免脊髓損傷急性期炎性因子對hUC-MSCs的損害,也可避免慢性期膠質瘢痕形成對軸突再生的阻礙[20]。因此,hUC-MSCs的最佳移植時機仍需進一步探索,尤其需開展臨床研究以驗證最佳的移植時機。
5 hUC-MSCs移植治療SCI的臨床安全性和有效性
雖然多項動物研究支持hUC-MSCs移植修復損傷的脊髓,但臨床應用卻取得了不一致的結果[6,13-14]。Dai等[30]將自體hUC-MSCs直接移植到SCI部位,發現18例患者中僅有8例感覺和運動功能輕度恢復,干細胞移植可能引起發熱、頭痛、神經性疼痛等不良反應。Oh等[31]的三期臨床試驗也顯示,在接受干細胞移植的16例患者中,只有2例患者神經功能略有改善。但在Yao等[32]的研究中,25例外傷性脊髓損傷(損傷時間>6個月)患者通過靜脈和鞘內注射hUC-MSCs后隨訪1年,可發現部分患者自主神經得到恢復。Zhu等[33]研究報道了20例SCI慢性期患者經hUC-MSCs移植后,13例改善了運動和括約肌功能,且5例從完全轉化為不完全SCI。而劉靜等[20]長期隨訪研究采用hUC-MSCs蛛網膜下腔注射治療35例SCI患者,輸注劑量為每次1×106cells/kg,1周1次,1療程4次,共完成46個療程。結果發現25例不完全性SCI患者有效率達88%,10例完全性SCI患者均無效。最后,她們認為hUC-MSCs鞘內注射治療安全可靠,且能改善大多數脊髓不完全性損傷患者的神經功能,多療程治療有可能使患者療效得到進一步提高。上述臨床研究結果差異較大,主要原因是未采用一致的hUC-MSCs移植途徑、劑量和時機。2022年,石堯等[6]開展的一項hUC-MSCs治療SCI有效性與安全性的Meta分析,共納入6篇隨機對照試驗和4篇隊列研究,結果發現hUC-MSCs治療SCI安全有效,患者的感覺和運動功能以及日常生活能力可得到顯著改善,不良反應較少。他們認為具有高等級證據支持hUC-MSCs治療SCI,值得在臨床中進行更大規模研究。但值得注意的是,該Meta分析所納入研究的hUC-MSCs移植途徑、劑量和時機存在著不同,可能會對結論產生一定的影響。
6 展 望
目前,大量的基礎實驗和臨床研究發現hUC-MSCs移植是治療SCI的一個有前景的治療方法,但仍存在一些問題亟待解決: (1) 受損脊髓局部炎性環境可導致所移植的hUC-MSCs大量死亡,并影響其發揮正常功能。因此,采用綜合治療方法如聯合應用水凝膠或納米材料支架,以最大發揮hUC-MSCs的生物活力。Chen等[34]發現3D打印的膠原蛋白/絲素蛋白攜帶hUC-MSCs分泌蛋白質組支架可以通過橋接脊髓損傷來部分重建脊髓損傷后的神經回路,從而改善神經功能障礙,這表明植入攜帶MSCs分泌蛋白質組的3D打印膠原蛋白/絲素蛋白支架有可能成為一種新的、更安全的脊髓損傷修復治療方法。(2) 需進一步闡明hUC-MSCs的生物學特點,采用小分子活性肽、生長因子等新方法以更好誘導hUC-MSCs向神經細胞分化。(3) 急需建立臨床級、標準化的hUC-MSCs體系,助于同質化地開展基礎實驗和臨床研究。(4) 目前,僅局限臨床研究應用hUC-MSCs移植治療SCI患者,進一步仍需開展大樣本的隨機對照臨床研究,以驗證hUC-MSCs最佳的移植途徑、劑量和時機[2]。

