改性硅藻土負載磷鉬酸銨復合吸附劑的制備及其吸附Cs+研究
郭雪琴,鄧小川,朱朝梁,扶 鑫,王瑞瑞,馬婉霞,樊 潔,左方濤,卿彬菊
(1.中國科學院青海鹽湖研究所,中國科學院鹽湖資源綜合高效利用重點實驗室,青海西寧 810008;2.青海省鹽湖資源開發工程技術研究中心,青海西寧 810008;3.中國科學院大學,北京 100049;4.杭州水處理技術研究開發中心有限公司,浙江杭州 310012)
銫(Cs)由于其活潑的化學性質和獨特的光電效應,在特種玻璃、催化劑、生物醫藥等傳統領域及銫原子鐘、離子推進劑火箭、光敏電子元件等高新技術領域有著十分廣泛的應用前景[1-4]。隨著鹽湖提鉀、提鋰工業的快速發展,鹽湖鹵水中稀散元素的提取也受到廣泛關注。中國鹽湖數量多,液態礦銫資源豐富,且部分鹽湖原鹵中銫含量達到工業開采品位以上[5]。相較于美國、智利、以色列等國家,中國鹽湖資源開發產品較為單一,而鹽湖鹵水中含有大量未被開發利用的有用成分,因而造成了資源浪費[6]。開展鹽湖鹵水中分離提銫工藝的研究有利于資源與環境的可持續發展及鹽湖資源的綜合利用。
現階段已開發了多種從溶液相分離提銫的方法,其中吸附法因選擇性高、適用于低濃度目標離子的分離,在溶液相分離Cs+方面表現出一定的優勢[7-8]。鹽湖鹵水中Cs+含量低,且含有大量高濃度金屬元素(如Li+、Na+、K+、Ca2+、Mg2+等),使得吸附法選擇性分離Cs+較為困難。因此,制備選擇性強、吸附容量大的吸附劑成為吸附法的關鍵。
硅藻土(Diatomite,De)是一種天然多級孔無機材料,但其存在可用活性位較少、比表面積小等缺點。基于此,研究者使用有機表面活性劑或無機表面涂層對硅藻土表面進行改性,以提高硅藻土表面活性和比表面積。改性硅藻土已廣泛應用于水處理領域[9-13],但對Cs+的吸附能力并不理想。磷鉬酸銨[AMP,分子式為(NH4)3PMo12O40·xH2O]由于其獨特的Keggin骨架及NH4+(3.31 ?)和Cs+(3.29 ?)水合離子半徑相近,對Cs+吸附有較高的選擇性和吸附量。大量研究表明,AMP 對Cs+的吸附機理是以NH4+和Cs+之間的離子交換為主,如式(1)所示[14-18]。因此,本研究以具有高Cs+吸附選擇性的AMP為吸附劑主體材料,將其分散負載到改性硅藻土表面制備復合吸附劑,并用于Cs+吸附性能研究。
1 實驗部分
1.1 實驗試劑和儀器
試劑:硅藻土(白色)、氯化鋁(AlCl3·6H2O)、氯化銫(CsCl)、十二烷基苯磺酸鈉(SDBS)、尿素、氯化銨(NH4Cl)、磷鉬酸[H3P(Mo3O10)4·xH2O]、鹽酸,均為分析純;氨水,質量分數為25%。
儀器:高壓反應釜;X'Pert Pro 型X 射線衍射儀(XRD);SU8010 型場發射掃描電子顯微鏡(FESEM);NEXUS 型傅里葉變換紅外光譜儀(FT-IR);AAnalyst 800 型原子吸收光譜儀(AAS);930 Compact IC Flex型離子色譜儀;Avio 20型電感耦合等離子體發射光譜儀(ICP-OES)。
1.2 γ-Al2O3/De-AMP復合吸附劑的制備
1)取10 g 硅藻土置于三口燒瓶中,加入一定量質量分數為5%的鹽酸,加熱至100 ℃后攪拌1 h,自然冷卻至室溫后真空抽濾,用去離子水洗滌至濾液呈中性,干燥備用。
2)取4 g 預處理的硅藻土置于燒杯中,加入80 mL去離子水攪拌至分散均勻;稱取5.79 g氯化鋁晶體加入到上述懸濁液中,強力攪拌90 min;稱取0.18 g SDBS 作為模板劑,加入到懸濁液中,攪拌3 h后用氨水調節pH 至4;加入4.32 g 尿素,繼續攪拌30 min;將上述懸濁液轉入反應釜中,加熱至180 ℃后反應5 h;自然冷卻至室溫后離心分離,用去離子水和乙醇洗滌樣品至濾液顯中性,真空干燥后得到改性硅藻土γ-AlOOH/De。將制備的γ-AlOOH/De在500 ℃下煅燒3 h后得到γ-Al2O3/De。
3)稱取1 g制得的γ-Al2O3/De置于燒杯中,加入15 mL NH4Cl溶液(1 mol/L),室溫下磁力攪拌8 h;取25 mL 磷鉬酸溶液(0.02 mol/L),緩慢滴加至混合液中,繼續攪拌12 h;反應生成的AMP 晶體分散沉淀在改性硅藻土表面;固液分離后用去離子水將固樣洗滌數次,然后在80 ℃下干燥12 h 以上,最終制得復合吸附劑γ-Al2O3/De-AMP。
1.3 材料表征
采用X射線衍射儀對所制備吸附劑物相結構進行分析;采用場發射掃描電子顯微鏡觀察分析吸附劑表面形貌;采用傅里葉變換紅外光譜儀對制備的復合吸附劑表面官能團進行分析;采用原子吸收光譜儀測定吸附前后溶液中Cs+濃度;采用離子色譜儀測定吸附前后溶液相中的NH4+;采用ICP-OES 測定吸附前后Cs+以外的離子含量。
1.4 吸附實驗
為了研究吸附劑γ-Al2O3/De-AMP 對Cs+的吸附性能,考察了吸附時間、Cs+初始濃度、溶液pH 及干擾離子對吸附過程的影響。制得的復合吸附劑對Cs+的吸附容量(qe)和吸附率(R)的計算公式如下:
式中:qe為吸附平衡時的吸附容量,mg/g;ρ0和ρe分別為溶液中初始和吸附平衡時的Cs+質量濃度,ρt為吸附時間t時的Cs+質量濃度,mg/L;V為溶液體積,mL;m為吸附劑用量,mg。
為了探究γ-Al2O3/De-AMP 對Cs+的吸附過程,分別用準一級和準二級吸附動力學模型對吸附數據進行擬合分析。相關模型方程如下:
式中:qt為吸附時間為t時的吸附容量,mg/g;t為吸附時間,min;k1、k2分別為準一級、準二級吸附速率常數。
采用Langmuir 和Freundlich 兩種吸附等溫模型對吸附數據進行擬合,以探究吸附質與吸附劑之間的相互作用。其中,Langmuir 吸附等溫模型是吸附質在吸附劑表面的單層吸附模型;Freundlich吸附等溫模型是吸附劑的吸附能分布不均的多層吸附模型。相關模型方程如下:
式中:qm為以吸附等溫線性模型計算的理論吸附容量,mg/g;KL是特定溫度下Langmuir 常數;KF、n分別為與吸附容量和吸附強度有關的Freundlich常數。
1.5 脫附實驗
稱取一定量吸附飽和后的吸附劑置入離心管中,以一定比例的H2O、KCl、NH4Cl、NH4NO3為脫附劑進行脫附實驗研究。脫附率(D)計算公式如下:
式中:ρ2為脫附液中Cs+質量濃度,mg/L;V2為脫附劑用量,mL;m2為脫附時吸附劑(吸附Cs+后)用量,mg。
2 結果與討論
2.1 材料表征
2.1.1 樣品XRD分析
圖1 為De、改性硅藻土γ-AlOOH/De、煅燒后改性硅藻土γ-Al2O3/De及復合吸附劑γ-Al2O3/De-AMP的XRD譜圖。由圖1可知,De樣品的X射線衍射峰表現出典型的晶態SiO2衍射峰,這主要是因為本研究選擇了SiO2含量較高的優質硅藻土。γ-AlOOH/De的XRD譜圖中出現了新衍射峰,對應于γ-AlOOH的標準卡片(PDF#21-1307)的晶面衍射峰。γ-AlOOH/De 經500 ℃煅燒后,γ-AlOOH 的衍射峰消失,此時改性硅藻土表面γ-AlOOH 轉變成γ-Al2O3晶體[13,19]。在γ-Al2O3/De上負載AMP后,樣品在10.72°、13.13°、15.16°、18.63°、24.11°、32.53°、39.35°處出現新的衍射峰,分別對應于(110)(111)(200)(211)(310)(411)(510)晶 面 衍 射 峰,與(NH4)3PO4(MoO3)12·4H2O 標準卡片(PDF#09-0412)相符,說明制備的樣品中含有AMP。

圖1 De、γ-AlOOH/De、γ-Al2O3/De和γ-Al2O3/De-AMP的XRD譜圖Fig.1 XRD patterns of De,γ-AlOOH/De,γ-Al2O3/De and γ-Al2O3/De-AMP
2.1.2 樣品SEM分析
圖2為De、γ-AlOOH/De、γ-Al2O3/De及γ-Al2O3/De-AMP 的SEM 圖。從圖2a 可以看出,本實驗所選De為直徑在30~40 μm的圓盤狀De,且該De經過1 200 ℃煅燒后表面部分孔道被堵塞,這也是本研究所選De 比表面積(見表1)遠小于文獻報道[13]的主要原因。從圖2b 可以看出,經氯化鋁改性后De 表面生成結構豐富的納米片層晶體。從圖2c 可以看出,γ-AlOOH/De經500 ℃煅燒后表面束狀結構未發生顯著變化,但片層輪廓模糊。從圖2d 可以看出,負載AMP對改性硅藻土表面片層結構無顯著影響,AMP 球形顆粒均勻負載在γ-Al2O3/De 表面,有利于AMP與Cs+的充分接觸,提高吸附量。

表1 De、γ-AlOOH/De、γ-Al2O3/De和γ-Al2O3/De-AMP的比表面積、平均介孔孔徑及孔容積Table 1 Specific surface area,average mesoporous pore size and pore volume of De,γ-AlOOH/De,γ-Al2O3/De and γ-Al2O3/De-AMP

圖2 De(a)、γ-AlOOH/De(b)、γ-Al2O3/De(c)、γ-Al2O3/De-AMP(d)的SEM圖Fig.2 SEM images of De(a),γ-AlOOH/De(b),γ-Al2O3/De(c)and γ-Al2O3/De-AMP(d)
2.1.3 樣品FT-IR分析
圖3為De、γ-AlOOH/De、γ-Al2O3/De及γ-Al2O3/De-AMP 的FT-IR 譜圖。由圖3 可知,γ-AlOOH/De樣品在3 102 cm-1處出現對應于Al—O—H伸縮振動帶的吸收峰,經過500 ℃煅燒處理后樣品中Al—O—H伸縮振動峰消失,結合圖1 中改性硅藻土的XRD 譜圖分析,可推測硅藻土改性成功,且在煅燒后形成穩定性較強的γ-Al2O3。樣品γ-Al2O3/De-AMP在1 405 cm-1處出現對應于NH4+振動帶的吸收峰,分別在1 060、961、866 cm-1處出現對應于P—O、Mo—O、Mo—O—Mo 振動帶的吸收峰[15]。結合γ-Al2O3/De-AMP 的SEM 圖和XRD 譜圖分析,可推斷成功制備了復合吸附劑γ-Al2O3/De-AMP。

圖3 De、γ-AlOOH/De、γ-Al2O3/De和γ-Al2O3/De-AMP的FT-IR譜圖Fig.3 FT-IR spectra of De,γ-AlOOH/De,γ-Al2O3/De and γ-Al2O3/De-AMP
2.1.4 比表面積及孔結構分析
圖4為De、γ-AlOOH/De、γ-Al2O3/De及γ-Al2O3/De-AMP 的N2吸附-脫附曲線,表1 為相應材料的比表面積、平均介孔孔徑及孔容。根據國際理論與應用化學聯合會(IUPAC)的分類方法可知,圖4中4種樣品的N2吸附-脫附曲線均屬于Ⅱ型等溫線;在p/p0>0.4 區域出現H3 型遲滯回線,表明孔結構不規整;在p/p0>0.9 區域吸附曲線陡增,且沒有出現吸附飽和平臺,說明樣品中含有大孔結構。這些現象均與樣品的SEM 圖中所觀察到的多級孔結構對應。由表1 可知,由于納米γ-AlOOH、γ-Al2O3中束狀片層結構的存在,改性硅藻土的平均介孔孔徑減小,比表面積增大;此外,γ-AlOOH 經煅燒后轉變成γ-Al2O3,片層結構表面變得粗糙[13]。因此,煅燒后的改性硅藻土比表面積更大,同時較大的比表面積有利于AMP的均勻分散。

圖4 De、γ-AlOOH/De、γ-Al2O3/De和γ-Al2O3/De-AMP的N2吸附-脫附曲線Fig.4 N2 adsorption-desorption curves of De,γ-AlOOH/De,γ-Al2O3/De and γ-Al2O3/De-AMP
2.2 吸附實驗
2.2.1 吸附時間對γ-Al2O3/De-AMP 吸附性能的影響及吸附動力學擬合
在吸附溫度為25 ℃、Cs+初始濃度為5 mmol/L條件下,考察了吸附時間對γ-Al2O3/De-AMP吸附性能的影響,結果見圖5。由圖5可知,在前15 min內γ-Al2O3/De-AMP 對Cs+的吸附量明顯增加;在15 min時Cs+吸附量達到74.30 mg/g,基本達到吸附平衡狀態;15 min后吸附量增速降低,主要是因為隨著吸附過程的進行,吸附劑表面可用吸附位點數量減少。

圖5 吸附時間對γ-Al2O3/De-AMP的Cs+吸附量的影響Fig 5 Effect of adsorption time on Cs+ adsorption capacity of γ-Al2O3/De-AMP
圖6為γ-Al2O3/De-AMP吸附Cs+的準一級、準二級動力學模型擬合曲線,表2為γ-Al2O3/De-AMP 對Cs+的吸附動力學擬合參數。結合圖6 和表2 可知,γ-Al2O3/De-AMP 對Cs+的吸附過程更符合準二級動力學模型,說明γ-Al2O3/De-AMP對Cs+的吸附以化學吸附為主。

表2 γ-Al2O3/De-AMP對Cs+的吸附動力學擬合參數Table 2 Linear fitting constants of adsorption kinetic parameters on Cs+ of γ-Al2O3/De-AMP

圖6 γ-Al2O3/De-AMP對Cs+的吸附動力學線性擬合曲線Fig.6 Linear fitting curves of adsorption kinetic of Cs+ by γ-Al2O3/De-AMP
2.2.2 Cs+初始濃度對γ-Al2O3/De-AMP 吸附性能的影響及吸附等溫模型研究
在其他吸附條件保持不變的情況下,探究Cs+初始濃度對γ-Al2O3/De-AMP吸附性能的影響,結果見圖7。由圖7 可知,在Cs+初始濃度為0.1~5 mmol/L時,γ-Al2O3/De-AMP 對Cs+的吸附量隨初始濃度的增大顯著增加;當Cs+初始濃度達到5 mmol/L 時,吸附量可達到79.41 mg/g,這主要是因為該階段的Cs+初始濃度較低,γ-Al2O3/De-AMP 表面還有大量未被占用的吸附位點;在Cs+初始濃度大于5 mmol/L以后,其吸附量增速變緩并趨于平衡。

圖7 Cs+初始濃度對γ-Al2O3/De-AMP吸附Cs+量的影響Fig.7 Effect of Cs+ initial concentration on Cs+ adsorption capacity of γ-Al2O3/De-AMP
圖8 為25 ℃下γ-Al2O3/De-AMP 對Cs+的Langmuir和Freundlich吸附等溫線性模型擬合曲線,表3為對應的吸附等溫模型擬合參數。結合圖8 和表3可知,γ-Al2O3/De-AMP 對Cs+的吸附過程與Langmuir吸附等溫模型更吻合,說明γ-Al2O3/De-AMP對Cs+的吸附是吸附劑表面單層吸附。

表3 γ-Al2O3/De-AMP對Cs+的吸附等溫模型擬合參數Table 3 Adsorption isotherm model parameters on Cs+ of γ-Al2O3/De-AMP

圖8 γ-Al2O3/De-AMP對Cs+的吸附等溫線性模型擬合曲線Fig.8 Linear fitting curves of adsorption isothermal model of γ-Al2O3/De-AMP
2.2.3 pH對γ-Al2O3/De-AMP吸附性能的影響
鹽湖鹵水因其水化學類型不同而表現出不同的酸堿度,因此有必要對γ-Al2O3/De-AMP 的pH 適用范圍進行探究。利用一定濃度的HCl和NaOH 溶液調節CsCl 溶液pH 為2~11,開展γ-Al2O3/De-AMP 對Cs+吸附實驗,結果見圖9。由圖9 可知,當溶液pH為2 時,γ-Al2O3/De-AMP 對Cs+的吸附量較低,主要是因為此時溶液中H+與Cs+存在競爭吸附;當溶液pH 為3~9 時,吸附量無顯著變化;當pH 調至11時,γ-Al2O3/De-AMP 對Cs+的吸附量最高。由此說明,γ-Al2O3/De-AMP 吸附Cs+時可適用的pH 范圍較寬。

圖9 pH對γ-Al2O3/De-AMP吸附Cs+性能的影響Fig.9 Effect of pH on Cs+ adsorption properties of γ-Al2O3/De-AMP
2.2.4 干擾離子的影響及γ-Al2O3/De-AMP 在模擬鹵水中的應用
為了探究γ-Al2O3/De-AMP 對Cs+的吸附選擇性,分別配制了Cs+與干擾離子(Li+、Na+、K+、Ca2+、Mg2+)共存的簡單二元體系和1#、2#模擬鹵水復雜體系溶液,進行Cs+吸附實驗,結果如圖10 所示。圖10a 為干擾離子存在的情況下,γ-Al2O3/De-AMP對Cs+的吸附量。由圖10a 可知,干擾離子共存對γ-Al2O3/De-AMP 的Cs+吸附量無顯著影響,仍保持較高的吸附量。圖10b 為模擬鹵水中γ-Al2O3/De-AMP 對Cs+的吸附率。由圖10b 可知,γ-Al2O3/De-AMP 在兩種模擬鹵水中對Cs+的吸附率均保持在95%以上,說明γ-Al2O3/De-AMP有較高的吸附選擇性,這對γ-Al2O3/De-AMP在實際鹵水中的應用提供了一定參考。

圖10 γ-Al2O3/De-AMP對Cs+的吸附選擇性Fig.10 Adsorption selectivity of γ-Al2O3/De-AMP for Cs+
2.3 脫附及循環實驗
為了進一步探究所制備吸附劑γ-Al2O3/De-AMP 的循環使用性能,本研究以H2O 及1 mol/L 的KCl、NH4Cl、NH4NO3溶液為脫附劑進行脫附實驗,結果如圖11a 所示。由圖11a 可知,脫附劑為NH4Cl、NH4NO3時Cs+的脫附率較高,但并不理想。故本研究考慮通過調整NH4NO3濃度來提高Cs+脫附率,結果如圖11b 所示。由圖11b 可知,隨著NH4NO3濃度的增加,Cs+脫附率顯著增加,當NH4NO3濃度增加至5 mol/L 時,Cs+脫附率最高可達88.23%。由于NH4NO3濃度在大于3 mol/L 以后脫附率增量不顯著,故后續實驗選擇以3 mol/L NH4NO3為脫附劑。以3 mol/L 的NH4NO3為脫附劑時脫附時間對Cs+脫附率的影響結果如圖11c 所示。由圖11c 可知,γ-Al2O3/De-AMP對Cs+的脫附速率極快,可在30 min內快速達到脫附平衡。圖11d 為以3 mol/L 的NH4NO3溶液為脫附劑時γ-Al2O3/De-AMP 的循環使用性能。由圖11d可知,經過4次吸附-脫附循環后γ-Al2O3/De-AMP 對Cs+的吸附量仍可達到初始吸附量的74.38%,這對吸附劑在實際鹵水中的循環利用十分有利。
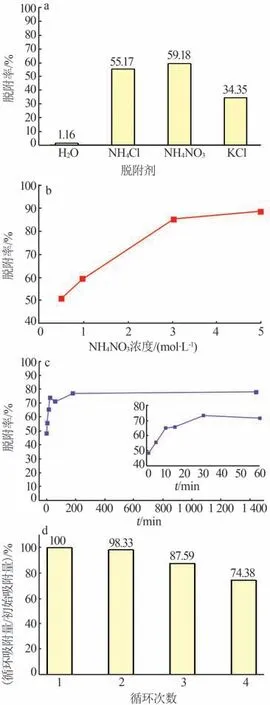
圖11 脫附及循環實驗研究Fig.11 Study on desorption and cycling experiment
2.4 吸附機理研究
為了進一步探究γ-Al2O3/De-AMP 材料結構穩定性及吸附機理,對吸附前后材料進行了SEM 和XRD 表征分析,結果如圖12 所示。由圖12a~b 可知,4次吸附-脫附循環后吸附劑表面形貌無顯著變化,改性硅藻土表面仍附著大量AMP 顆粒,僅表面片層結構略有損毀。由圖12c 可以看出,吸附前后晶體結構未發生顯著變化,僅有部分晶面衍射峰強度變弱,說明該吸附過程不會破壞γ-Al2O3/De-AMP的晶體結構。

圖12 吸附前(a)、吸附后(b)的SEM圖和吸附前后XRD譜圖(c)Fig.12 SEM images before(a) and after(b) adsorption,and XRD patterns before and after adsorption(c)
表4 為γ-Al2O3/De-AMP 吸附Cs+前后溶液相中Cs+和NH4+的濃度。由表4可知,吸附前后溶液相中Cs+和NH4+濃度近似等物質的量變化,其中Cs+濃度略高于NH4+濃度的部分可認為是γ-Al2O3/De-AMP對Cs+的物理吸附,該結果與文獻報道的反應式(1)一致,證實了γ-Al2O3/De-AMP 對Cs+的吸附是由溶液中Cs+和吸附劑中NH4+交換實現的。
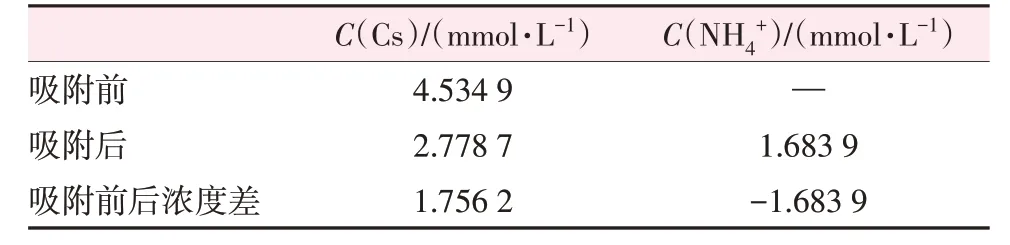
表4 γ-Al2O3/De-AMP吸附Cs+前后溶液中各離子濃度變化Table 4 Changes of ion concentration in solution before and after Cs+ adsorption by γ-Al2O3/De-AMP
2.5 與其他AMP基復合吸附劑的比較
表5 歸納了近年來以AMP 為吸附劑主體的復合吸附劑對Cs+的吸附性能。通過對比發現,本研究所制備的復合吸附劑適用的pH范圍較寬,且在吸附速率、吸附容量等方面均表現出較優的Cs+吸附性能。

表5 近年來文獻報道的AMP基復合吸附劑對Cs+的吸附性能Table 5 Cs+ adsorption properties of AMP-based adsorbents reported in recent years
3 結論
本研究通過前期條件探索制備了表面結構豐富的改性硅藻土,并將其作為載體材料,在500 ℃下煅燒后負載AMP制備了復合吸附劑γ-Al2O3/De-AMP。
1)通過SEM、XRD、FT-IR 表征手段證實了γ-Al2O3/De-AMP已成功制備。
2)通過系統的Cs+吸附實驗,得出γ-Al2O3/De-AMP可在15 min內快速達到吸附平衡;所制備的復合吸附劑在較寬的pH范圍內均適用。
3)對吸附數據進行動力學和吸附等溫模型擬合,得出吸附過程更符合準二級動力學模型和Langmuir吸附等溫模型。
4)以3 mol/L NH4NO3為脫附劑時表現出較優的吸附-脫附循環性能;且制備的吸附劑在模擬鹵水復雜體系中保持了較高的吸附率,這對其在實際鹵水中的應用推廣有非常重要的參考價值。

