甘草預防氣管插管致呼吸道損傷的有效成分篩選
張杰,丁聲雙,郭敏,薛陽,徐紫清,侯懷晶,薛建軍*
1.730050 甘肅省蘭州市,甘肅省中醫院麻醉科
2.730050 甘肅省蘭州市,甘肅省中西醫結合麻醉臨床研究中心
3.730000 甘肅省蘭州市,甘肅中醫藥大學第一臨床醫學院
4.730050 甘肅省蘭州市,甘肅省中醫院
氣管插管術是全身麻醉過程中最重要、最安全的呼吸支持方式。但由于其屬于侵入性操作,可引起多種并發癥。術后咽喉痛(POST)是全身麻醉后常見的輕微但令人不快的術后并發癥之一,發病率高達62%[1]。POST 會使患者術后的不適感增加、住院時間延長,嚴重影響了患者滿意度和術后恢復質量[2-3]。隨著全身麻醉氣管插管手術患者日趨增多和加速康復外科(ERAS)的快速發展,POST 的防治受到廣大麻醉醫師的關注。最近一項網狀Meta 分析[4]比較了6 種外用藥物預防氣管插管POST 的療效,結果發現利多卡因并不是預防POST 的最佳外用藥物,建議根據臨床經驗和患者的喜好選擇甘草甜素、皮質類固醇、非甾體抗炎藥或N-甲基-D-門冬氨酸(NMDA)受體拮抗劑用于減輕POST。目前,針對POST 的干預措施多以術前預防為主,具有一定的緩解作用,但POST發生率仍然較高[5]。因此,尋找具有療效確切且不良反應小的臨床干預方法已成為研究熱點。
甘草來源于豆科植物甘草、脹果甘草或光果甘草的干燥根和根莖[6],主要包括三萜皂苷類化合物、黃酮類化合物和多糖類化合物等[7],具有抗炎、免疫調節、抗氧化等多種功效[8],是臨床常用中藥之一。本課題組前期研究[9]發現甘草噴劑能明顯減輕大鼠氣管黏膜水腫滲出和炎性細胞浸潤,降低大鼠氣管插管后血清促炎因子腫瘤壞死因子(TNF)-α、白介素(IL)-1 的表達水平。此外,通過臨床研究發現甘草噴霧劑可減輕全身麻醉氣管插管應激反應和POST 的發生率[10],同時基于循證醫學的證據顯示甘草制劑局部應用能有效預防氣管插管后的咽喉痛[11],但目前尚無針對甘草具體有效成分防治插管后氣道損傷或POST 的研究。因此,本研究通過建立全身麻醉氣管插管大鼠模型,篩選甘草預防氣管插管致呼吸道損傷的有效成分,從中醫藥角度為防治全身麻醉氣管插管致呼吸道損傷提供新思路。
1 資料與方法
1.1 實驗動物
SPF 級Wistar 大鼠60 只,6~8 周齡,雌雄各半,體質量(200±20)g,購于甘肅中醫藥大學實驗動物中心(合格證號62001000000591)。所有動物操作獲得甘肅中醫藥大學動物實驗倫理委員會審查(倫理審批編號:2020-233),并根據國際疼痛研究協會的動物實驗指南進行。
1.2 實驗儀器與試劑
DH-140 型小動物呼吸機(深圳市瑞沃德生命科技有限公司),高速冷凍離心機(5424R,德國Eppendorf),病理切片機(RM2016,德國徠卡),組織攤片機(KD-P,鄭州博邦儀器有限公司),顯微拍照系統(ICX41,寧波舜宇光學科技有限公司),酶標儀(ELX800,美國Bio Rad 公司)。
異氟醚購自深圳市瑞沃德生命科技有限公司,丙二醛(MDA)、總抗氧化能力(T-AOC)、超氧化物歧化酶(SOD)試劑盒購于南京建成科技有限公司,TNF-α、IL-2、IL-4、IL-10、皮質醇(Cor)、腎上腺素(E)和去甲腎上腺素(NE)試劑盒購于江蘇酶免實業有限公司。
1.3 甘草提取物的制備
甘草購于甘肅數字本草檢驗中心有限公司,并經該公司鑒定為甘草根和莖。將甘草飲片粉碎,過60 目篩;稱取甘草粉末三份,每份約10.0 g,加水200 mL,超聲提取1 h,離心(3 000 r/min,5 min),取上清液,醇沉(80%乙醇、9 h),離心,取上清液,水浴濃縮至約50 mL,得總多糖(TP);加75%乙醇200 mL,超聲提取1 h,過濾,濾液用AB-8 大孔吸附樹脂純化,80%乙醇洗脫,洗脫液濃縮至約50 mL,得總黃酮;加75%乙醇200 mL,回流提取90 min,過濾,濾液用HPD-300 大孔吸附樹脂純化,50%乙醇洗脫,洗脫液濃縮至約50 mL,得總皂苷。
1.4 研究方法
1.4.1 動物分組及處理:本研究于2021年4月—2022年7月進行。將60 只SPF 級Wistar 大鼠按隨機數字表法分為6 組:對照組、氣管插管組、利多卡因組、總多糖組、總皂苷組、總黃酮組,每組10 只。除對照組外,其余五組采用1%戊巴比妥鈉麻醉,制備氣管插管模型。插管前各治療組按1 mL/100 g(按體質量計)分別經口噴入1%利多卡因、總多糖、總皂苷、總黃酮,浸潤軟腭及懸雍垂周圍組織。對照組和氣管插管組經口噴入等體積0.9%氯化鈉溶液。
1.4.2 參照文獻[8]制備氣管插管大鼠模型。模型制備:將大鼠用1%戊巴比妥鈉溶液(50 mg/kg)腹腔注射麻醉后,3~5 min 后大鼠意識消失,全身肌肉松弛。將麻醉后的大鼠仰臥固定于手術板上,把固定的大鼠同手術臺一起傾斜約45°(大鼠頭朝上),用手術鉗將大鼠舌頭小心拉出口腔,左手持大鼠喉鏡,右手持自制氣管導管(16G 血管穿刺針),趁大鼠吸氣時聲門打開瞬間將自制氣管導管插入氣道,用棉簽確認氣管導管的位置,然后連接呼吸機。參數設置:頻率80 次/min,潮氣量5~10 mL,吸呼比為1∶1.5。麻醉維持:持續吸入1.3%異氟醚,機械通氣期間觀察大鼠狀態,包括大鼠胸廓起伏頻率與程度、口唇黏膜是否紅潤、有無異動等,若發現異常,及時檢查呼吸回路。麻醉蘇醒:機械通氣2 h后停止異氟醚吸入,待大鼠完全清醒后拔除氣管導管,將其放回鼠籠待解剖。
1.4.3 蘇木精-伊紅(HE)染色:氣管導管拔除2 h 后,在1%戊巴比妥鈉深麻醉(80 mg/kg)狀態下,采集大鼠咽部黏膜組織,用4%多聚甲醛固定,觀察病理。將標本脫水,石蠟包埋,制作5 μm 厚切片,用HE 染色,并采用寧波舜宇ICX41 顯微鏡拍照系統進行觀察、拍照。
1.4.4 酶聯免疫吸附(ELISA)測定:拔除氣管導管2 h后,在1%戊巴比妥鈉深麻醉(80 mg/kg)狀態下,從腹主動脈采集血液樣本,在3 500 r/min 條件下離心10 min,收集血清并保存在-80 ℃冰箱備用。按照ELISA 試劑盒說明書檢測炎性因子(TNF-α、IL-2、IL-4、IL-10)、氧化應激指標(MDA、T-AOC、SOD)及應激激素(Cor、E、NE)水平。
1.4.5 免疫組化檢測Toll 樣受體2(TLR2)和Toll 樣受體4(TLR4)表達水平:將制備好的咽部黏膜組織石蠟切片用二甲苯脫蠟,然后依次加入高至低濃度乙醇使組織再水化,加入抗原修復液,然后用3% H2O2消除過氧化物酶,然后用牛血清密封。經一抗和二抗孵育后,進行脫蠟洗滌,抗原修復,加入DAB 顯色,脫水密封后使用顯微拍照系統觀察和拍照。通過Image-Pro Plus 6.0軟件計算各視野TLR2 和TLR4 平均光密度值(AOD),以AOD=IOD/Area(即intDen/Area)表示。
1.5 統計分析
采用SPSS 22.0 軟件(IBM 公司,阿蒙克市,美國)進行統計分析,使用GraphPad Prism 9.0 軟件作圖。計量數據以(±s)表示。當方差齊檢驗沒有呈現出顯著性(α=0.05)時,采用單因素方差分析和Tukey 事后檢驗來評估多重比較。反之,采用Dunnett's T3 進行組間分析。以P<0.05 為差異有統計學意義。
2 結果
2.1 甘草不同成分對大鼠咽部黏膜組織病理變化的影響
對照組黏膜層和黏膜下層結構完整,細胞形態結構正常,未見炎性細胞浸潤現象。氣管插管組可見黏膜脫落,黏膜下結構嚴重破壞并伴有大量炎性細胞浸潤。與氣管插管組相比,利多卡因組黏膜層及黏膜下層結構破壞較輕,可見大量炎性細胞浸潤;總多糖組和總黃酮組黏膜及黏膜下層結構相對完整,炎性細胞浸潤相對減少;總皂苷組黏膜及黏膜下層結構基本完整,細胞形態接近正常,可見散在的炎性細胞,見圖1。
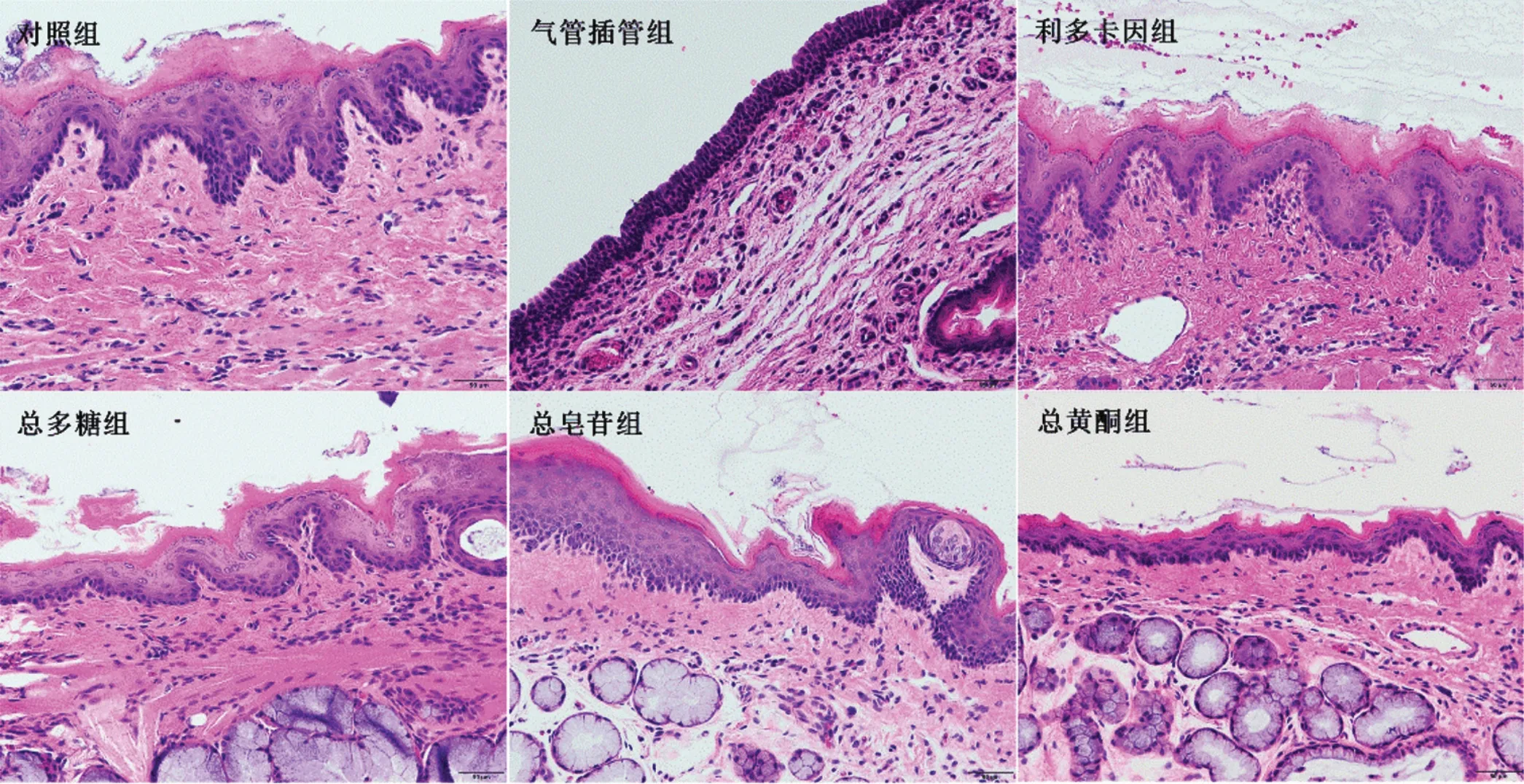
圖1 6 組大鼠咽部黏膜病理變化(HE 染色,×200)Figure 1 Pathological changes of pharyngeal mucosa among 6 groups
2.2 甘草不同成分對大鼠血清炎性因子的影響
6 組大鼠血清炎性因子TNF-α、IL-2、IL-4、IL-10 水平比較,差異有統計學意義(P<0.05)。與對照組相比,氣管插管組大鼠血清中的TNF-α、IL-2 水平升高,IL-4、IL-10 水平降低,差異有統計學意義(P<0.05)。與氣管插管組相比,總多糖組IL-4 水平升高,總皂苷組大鼠血清TNF-α 和IL-2 水平下降,IL-4 和IL-10 水平升高,差異有統計學意義(P<0.05);利多卡因組和總黃酮組大鼠血清TNF-α 水平低于氣管插管組,差異有統計學意義(P<0.05),見表1。
表1 6 組大鼠血清炎性因子的比較(±s)Table 1 Comparison of serum inflammatory factors among 6 groups
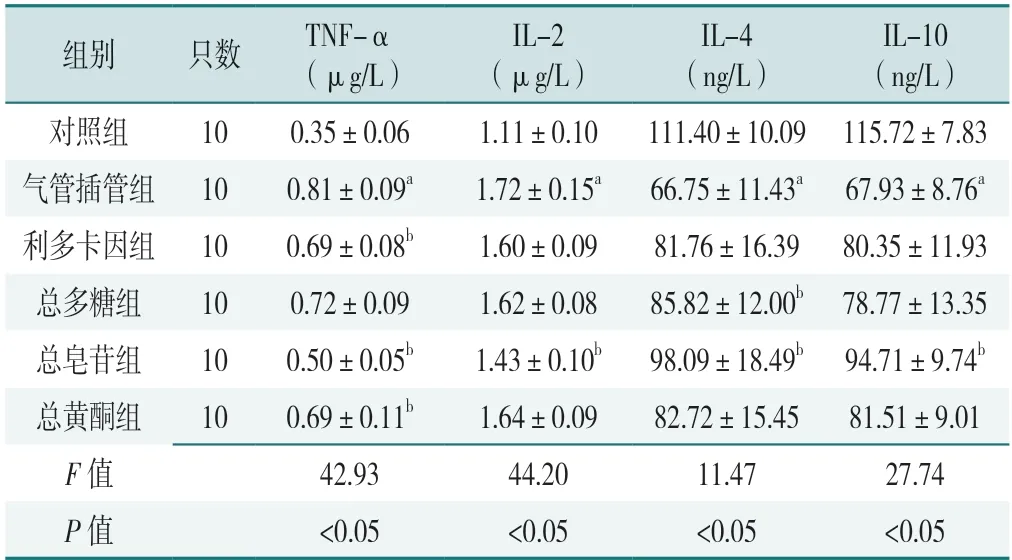
表1 6 組大鼠血清炎性因子的比較(±s)Table 1 Comparison of serum inflammatory factors among 6 groups
注:TNF-α=腫瘤壞死因子α,IL=白介素;a 表示與對照組比較P<0.05,b 表示與氣管插管組比較P<0.05。
IL-10(ng/L)對照組100.35±0.061.11±0.10111.40±10.09 115.72±7.83氣管插管組100.81±0.09a1.72±0.15a66.75±11.43a 67.93±8.76a利多卡因組100.69±0.08b1.60±0.0981.76±16.39 80.35±11.93總多糖組100.72±0.091.62±0.0885.82±12.00b 78.77±13.35總皂苷組100.50±0.05b1.43±0.10b98.09±18.49b 94.71±9.74b總黃酮組100.69±0.11b1.64±0.0982.72±15.4581.51±9.01 F 值42.9344.2011.4727.74 P 值<0.05<0.05<0.05<0.05組別只數TNF-α(μg/L)IL-2(μg/L)IL-4(ng/L)
2.3 甘草不同成分對氧化應激的影響
6 組大鼠血清氧化應激指標MDA、SOD、T-AOC水平比較,差異有統計學意義(P<0.05)。與對照組相比,氣管插管組大鼠血清中的MDA水平升高,SOD和T-AOC水平下降,差異有統計學意義(P<0.05)。利多卡因組和總多糖組大鼠血清MDA、SOD、T-AOC 水平與氣管插管組比較,差異無統計學意義(P>0.05)。與氣管插管組相比,總皂苷組和總黃酮組大鼠血清MDA 水平下降,SOD 和T-AOC 水平升高,差異有統計學意義(P<0.05),見表2。
表2 6 組大鼠血清氧化應激水平的比較(±s)Table 2 Comparison of serum oxidative stress level among 6 groups
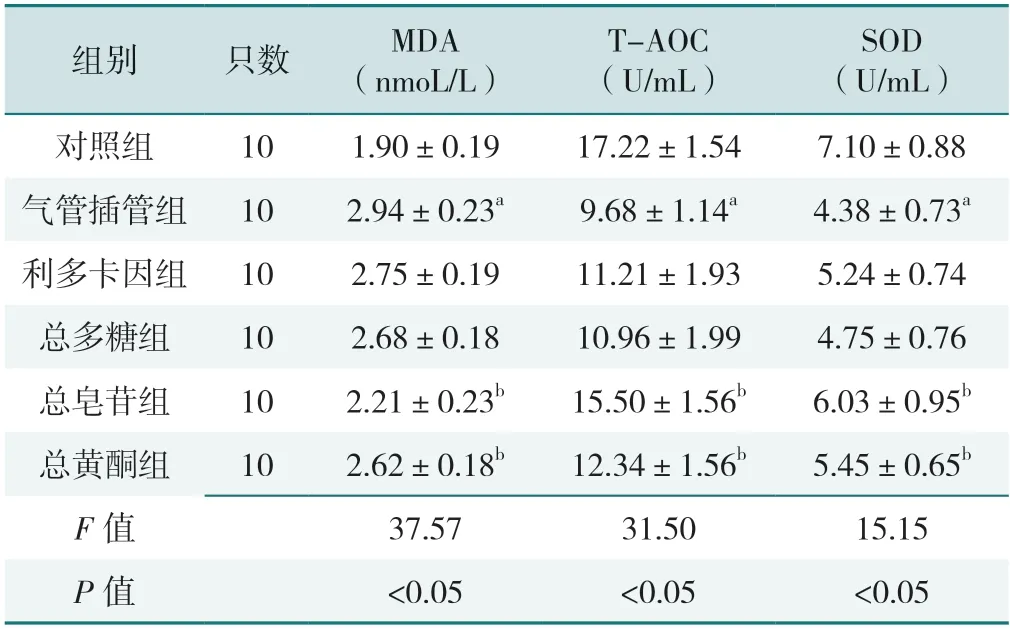
表2 6 組大鼠血清氧化應激水平的比較(±s)Table 2 Comparison of serum oxidative stress level among 6 groups
注:MDA=丙二醛,T-AOC=總抗氧化能力,SOD=超氧化物歧化酶;a 表示與對照組比較P<0.05,b 表示與氣管插管組比較P<0.05。
SOD(U/mL)對照組101.90±0.1917.22±1.547.10±0.88氣管插管組102.94±0.23a9.68±1.14a4.38±0.73a利多卡因組102.75±0.1911.21±1.935.24±0.74總多糖組102.68±0.1810.96±1.994.75±0.76總皂苷組102.21±0.23b15.50±1.56b6.03±0.95b總黃酮組102.62±0.18b12.34±1.56b5.45±0.65b F 值37.5731.5015.15 P 值<0.05<0.05<0.05組別只數MDA(nmoL/L)T-AOC(U/mL)
2.4 甘草不同成分對應激激素水平的影響
6 組大鼠血清應激激素Cor、E、NE 水平比較,差異有統計學意義(P<0.05)。氣管插管組大鼠血清Cor、E 和NE 水平高于對照組,差異有統計學意義(P<0.05)。利多卡因組和總皂苷組大鼠血清中Cor、E 和NE 水平低于氣管插管組,差異有統計學意義(P<0.05)。總多糖組和總黃酮組大鼠血清Cor、E 和NE 水平與氣管插管組比較,差異無統計學意義(P>0.05),見表3。
表3 6 組大鼠血清應激激素水平的比較(±s)Table 3 Comparison of serum stress hormone level among 6 groups
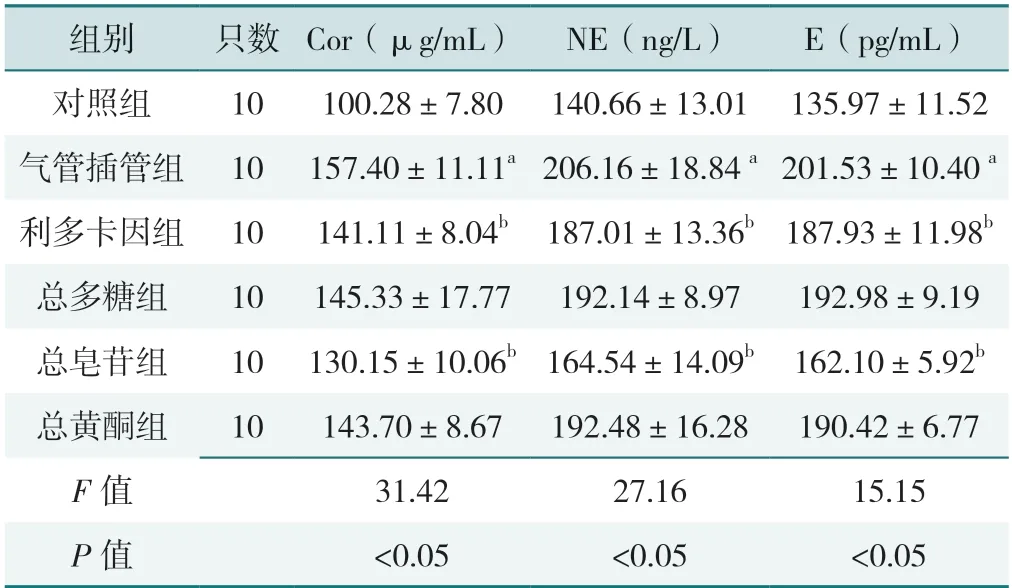
表3 6 組大鼠血清應激激素水平的比較(±s)Table 3 Comparison of serum stress hormone level among 6 groups
注:Cor=皮質醇,NE=去甲腎上腺素,E=腎上腺素;a 表示與對照組比較P<0.05,b 表示與氣管插管組比較P<0.05。
組別只數 Cor(μg/mL)NE(ng/L)E(pg/mL)對照組10100.28±7.80 140.66±13.01 135.97±11.52氣管插管組 10 157.40±11.11a 206.16±18.84 a 201.53±10.40 a利多卡因組 10141.11±8.04b 187.01±13.36b 187.93±11.98b總多糖組10 145.33±17.77 192.14±8.97 192.98±9.19總皂苷組10 130.15±10.06b 164.54±14.09b 162.10±5.92b總黃酮組10143.70±8.67 192.48±16.28 190.42±6.77 F 值31.4227.1615.15 P 值<0.05<0.05<0.05
2.5 甘草不同成分對TLR2 和TLR4 表達的影響
6 組大鼠咽部黏膜組織TLR2、TLR4 蛋白表達水平比較,差異有統計學意義(P<0.05)。氣管插管組TLR2 和TLR4 表達的AOD 高于對照組,差異有統計學意義(P<0.05)。利多卡因組、總多糖組、總皂苷組和總黃酮組大鼠咽部組織TLR2 表達的AOD 與氣管插管組相比,差異無統計學意義(P>0.05)。總皂苷組大鼠咽部組織TLR4 表達的AOD 明顯低于氣管插管組(P<0.05),而利多卡因組、總多糖組和總黃酮組大鼠咽部組織TLR4 表達的AOD 與氣管插管組相比,差異無統計學意義(P>0.05),見圖2、表4。
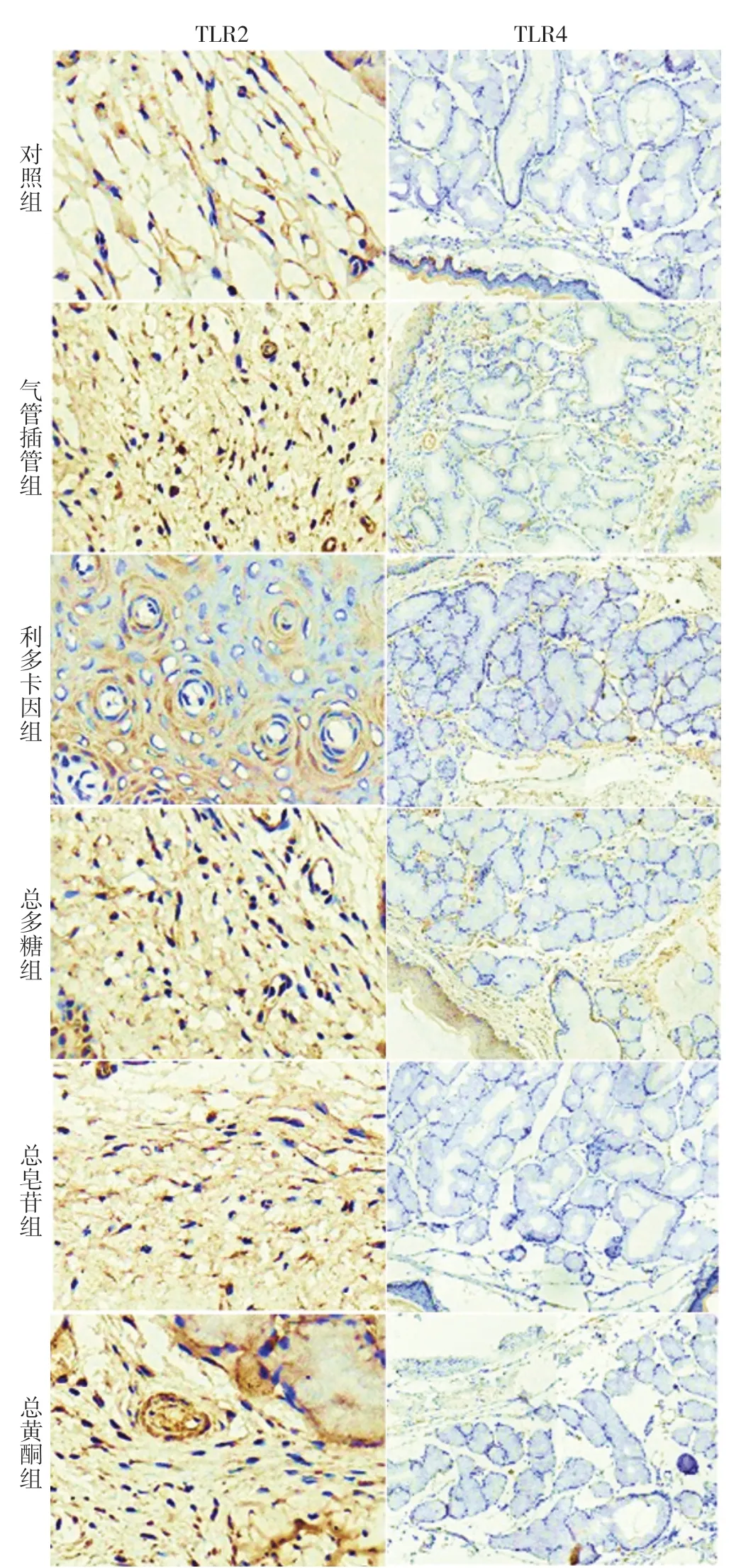
圖2 6 組大鼠咽部組織TLR2 和TLR4 表達免疫組化染色圖(×200)Figure 2 Immunohistochemical staining of TLR2 and TLR4 expression in pharyngeal tissues among 6 groups
表4 6 組大鼠咽部組織TLR2、TLR4 蛋白表達AOD 比較(±s)Table 4 Comparison of AOD expressed by TLR2 and TLR4 protein in the pharyngeal tissues among 6 groups
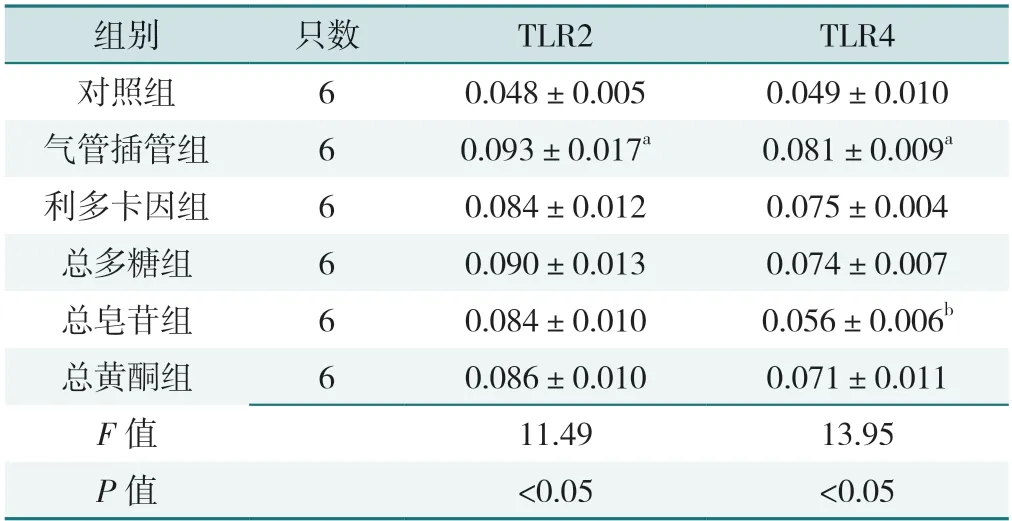
表4 6 組大鼠咽部組織TLR2、TLR4 蛋白表達AOD 比較(±s)Table 4 Comparison of AOD expressed by TLR2 and TLR4 protein in the pharyngeal tissues among 6 groups
注:TLR2=Toll 樣受體2,TLR4=Toll 樣受體4;a 表示與對照組比較P<0.05,b 表示與氣管插管組比較P<0.05。
組別只數TLR2TLR4對照組60.048±0.005 0.049±0.010氣管插管組60.093±0.017a 0.081±0.009a利多卡因組60.084±0.012 0.075±0.004總多糖組60.090±0.013 0.074±0.007總皂苷組60.084±0.010 0.056±0.006b總黃酮組60.086±0.010 0.071±0.011 F 值11.4913.95 P 值<0.05<0.05
3 討論
在接受全身麻醉的患者中,氣管內插管對于保持氣道通暢至關重要,在臨床上應用廣泛,其侵入性操作帶來的機械刺激易引起咽喉部黏膜屏障破壞,誘發機體出現炎性反應、應激反應等,從而引起咽喉部疼痛及咳嗽等呼吸道并發癥。雖然可以通過選擇直徑較小的氣管導管,使用適當的氣管導管套囊壓力[12],靜脈注射或局部應用利多卡因[13],包括利多卡因堿化氣管導管套囊,以及類固醇等抗炎藥[4]降低POST 的發生率,但上述措施均不令人滿意。此外,喉鏡的放置通常伴有嚴重的交感神經刺激,這對心血管疾病患者極為危險。目前已經設計了許多技術來減少圍術期應激反應發生的可能性,例如對喉黏膜進行局部麻醉、靜脈給予局部麻醉藥、短效阿片類藥物或β 腎上腺素能拮抗劑[14]。然而,這些方法無法有效抑制應激反應。近年來,中醫藥技術廣泛應用于氣管插管呼吸道并發癥的防治。現代藥理學研究表明,甘草具有補脾益氣、清熱解毒、抗炎、抗氧化、調節免疫等藥理作用[15-18],廣泛應用于呼吸系統疾病。
以往研究表明,氣管導管與人或豬的氣管黏膜接觸導致機械性損傷,表現為咽喉痛(人)、氣管炎、中性粒細胞活化[19-21],同時彈性蛋白酶、活性氧(ROS)、IL-1β、TNF-α 和細胞間黏附分子1 表達增加[21]。甘草的抗炎活性及其在炎癥性疾病中的應用自古以來就有記載[22]。有學者認為甘草的抗炎作用主要由皂苷類和黃酮類化合物介導[23],甘草中的三萜皂苷類化合物是其具有特異性標志的成分,其中甘草酸和甘草次酸是甘草根的主要成分[23],二者在藥理學上表現出相似的特征。KAGEYAMA 等[24]認為甘草酸的抗炎作用與糖皮質激素和鹽皮質激素相似。黃酮類化合物是甘草中僅次于三萜皂苷類的第二大化合物。甘草類黃酮顯示出良好的抗炎作用,在肺炎、肝炎、潰瘍性結腸炎、胃炎和其他炎癥性疾病中顯示出治療效果[25]。本研究發現氣管插管組大鼠咽部黏膜脫落,黏膜下層結構破壞嚴重并伴有大量炎性細胞浸潤,血清中促炎因子TNF-α 和IL-2 水平顯著升高,抗炎因子IL-4 和IL-10 水平降低。總皂苷組大鼠咽部黏膜及黏膜下層結構破壞減輕,炎性細胞浸潤減少。大鼠血清中促炎因子TNF-α 和IL-2水平下降,抗炎因子IL-4 和IL-10 水平升高。這些結果提示總皂苷對氣管插管引起的氣道損傷和炎性反應有一定的抑制作用,這一結果與梁曦等[9]研究結果一致。
甘草的抗氧化活性是其廣泛使用的主要原因之一。三萜皂苷類化合物甘草酸的抗輻射、神經保護、抑制線粒體通透性變化、防止缺血再灌注損傷及緩解肝損傷等多種活性與其清除自由基、對抗氧化應激的作用密切相關[23]。有學者將甘草的抗氧化活性歸因于黃酮類化合物[26]。MDA 是一種能間接反映機體ROS 代謝狀態和對組織的氧化損傷程度的脂質過氧化反應的中間產物[27],也是機體發生氧化應激的重要標志;SOD 作為抗氧化劑,能減少ROS 在體內的積聚,減少MDA 的產生[28],從而減輕氧化應激損傷;T-AOC 可反映機體內總體的抗氧化水平[29]。本研究發現:氣管插管組大鼠血清中MDA 水平明顯增加,SOD 和T-AOC 水平明顯下降。給予甘草提取物預處理后,發現總皂苷組和總黃酮組MDA 水平降低,SOD 和T-AOC 水平升高,表明總皂苷和總黃酮對氣管插管引起的氧化應激損傷均有一定的抑制作用,這一研究結果與王軍等[30]研究一致。
氣管插管等應激反應促使交感-腎上腺髓質和下丘腦-垂體-腎上腺皮質軸興奮為主的一系列神經內分泌反應,促使機體兒茶酚胺和糖皮質激素分泌增加[31]。因此,血漿中Cor、E 和NE 濃度能夠評估應激反應的程度。楊開銀等[10]通過臨床研究發現甘草噴霧劑能降低氣管拔管后24 h 內血清E 和NE 水平。本研究發現利多卡因組和總皂苷組大鼠血清中Cor、E 和NE 水平較氣管插管組顯著降低,表明甘草抑制氣管插管時的應激反應可能與總皂苷相關。
TLR 是參與非特異性反應的蛋白分子[32],TLR 有多重亞型,其中TLR4 被認為是無菌炎癥的主要介質[33],促進炎性因子的合成和釋放是其主要的生物學功能。有研究表明,促炎介質HMGB1 在細胞外與TLR 結合,進而激活核因子(NF)-κB 通路,誘導氧化應激反應,加劇炎性因子釋放[34],從而介導組織傷過程。本研究結果發現,氣管插管組TLR2 和TLR4 表達的AOD 高于對照組,表明氣管插管誘導的氣道損傷可以激活TLR2和TLR4 蛋白表達。總皂苷組大鼠咽部組織TLR4 表達的AOD 明顯低于氣管插管組,提示TLR4 在甘草預防全身麻醉氣管插管所致的呼吸道損傷中發揮重要作用。
綜上,本研究通過觀察甘草不同成分對大鼠氣管插管模型咽部組織病理形態學、炎性因子、氧化應激、應激激素和TLR 等相關指標的影響,分別考察甘草不同成分對氣管插管引起的氣道損傷的作用。結果表明總皂苷成分可通過減輕炎性反應、氧化應激和抑制TLR4 表達改善氣管插管大鼠呼吸道損傷,故初步確定甘草預防全身麻醉氣管插管呼吸道損傷的有效成分為總皂苷。
作者貢獻:張杰和薛建軍構思并設計了實驗,指導研究實施與修改稿件;張杰、丁聲雙、郭敏、薛陽負責實驗實施和血清學指標檢測;張杰和郭敏撰寫論文初稿。丁聲雙和徐紫清進行HE 染色和免疫組化;丁聲雙和侯懷晶統計分析數據;所有作者審閱并批準了最終稿件。
本文無利益沖突。

