基于化學(xué)鍵偶極的精氨酸分子力場(chǎng)參數(shù)的建立
劉 琦, 祝佳怡, 姜笑楠, 孫長(zhǎng)亮, 郝 強(qiáng), 王長(zhǎng)生
(1.遼寧師范大學(xué) 化學(xué)化工學(xué)院,遼寧 大連 116029; 2.沈陽(yáng)化工大學(xué) 分析測(cè)試中心,遼寧 沈陽(yáng) 110142)
在細(xì)胞代謝、信號(hào)傳導(dǎo)以及基因表達(dá)等關(guān)鍵生命過(guò)程中,精氨酸顯現(xiàn)出不可或缺的作用. 作為蛋白質(zhì)的構(gòu)建元素之一,精氨酸參與了蛋白質(zhì)的構(gòu)建,氨基酸及其衍生物的生物合成過(guò)程[1],同時(shí)也參與了尿素循環(huán)的調(diào)控[2]. 精氨酸在細(xì)胞質(zhì)和細(xì)胞核內(nèi)的生物合成過(guò)程中也具有重要的功能. 此外,精氨酸在胍基乙酸以及隨后形成的肌酸合成過(guò)程中充當(dāng)了重要的供體. 這種多重作用使得精氨酸成為維持蛋白質(zhì)結(jié)構(gòu)穩(wěn)定性和功能活性的關(guān)鍵成分. 精氨酸在染色體包裝、DNA修復(fù)以及其他細(xì)胞過(guò)程中的參與[3],使其備受生物學(xué)研究關(guān)注.
然而,精氨酸分子的復(fù)雜性遠(yuǎn)不止于其在生物學(xué)中的角色. 分子內(nèi)和分子間的相互作用很大程度上受到其胍基上電荷分布和立體構(gòu)型的影響. 這些電荷分布在精氨酸分子與其他分子之間的氫鍵、離子鍵以及范德華力等相互作用中扮演著至關(guān)重要的角色. 精確描述這些相互作用對(duì)于理解精氨酸在蛋白質(zhì)結(jié)構(gòu)的穩(wěn)定性、酶活性以及其他生物學(xué)功能方面的作用至關(guān)重要[4].
分子力場(chǎng)方法作為分子模擬和計(jì)算化學(xué)領(lǐng)域的基石,為揭示生物分子的結(jié)構(gòu)和相互作用提供了關(guān)鍵支持. 然而,現(xiàn)有的力場(chǎng)方法在涉及帶電體系的精確描述方面仍存在限制. 特別是在描述如胍基上電荷分布這類復(fù)雜氨基酸的時(shí)候,現(xiàn)行的力場(chǎng)參數(shù)無(wú)法提供令人滿意的結(jié)果. 因此,開發(fā)出適用于精氨酸分子的精準(zhǔn)力場(chǎng)參數(shù)成為當(dāng)前亟待解決的任務(wù). 通過(guò)建立一個(gè)基于化學(xué)鍵偶極的精氨酸分子力場(chǎng)參數(shù),將能夠更加準(zhǔn)確地模擬精氨酸胍基上電荷分布以及與其他分子間的相互作用,從而有助于更加深入地研究和理解生物分子中精氨酸的功能.
1 化學(xué)鍵偶極的分子力場(chǎng)方法
為了精確預(yù)測(cè)精氨酸分子,尤其是帶電氨基酸側(cè)鏈部分與水分子之間的相互作用,本文對(duì)質(zhì)子化的精氨酸側(cè)鏈與水分子組成的團(tuán)簇體在NPT系綜下進(jìn)行2 ns的分子動(dòng)力學(xué)模擬. 以軌跡中精氨酸側(cè)鏈分子及其周圍的兩個(gè)水分子組成的復(fù)合物為基礎(chǔ),在B3LYP/6-31+G(d,p)水平下進(jìn)行了結(jié)構(gòu)優(yōu)化. 以一個(gè)質(zhì)子化的精氨酸側(cè)鏈分子與兩個(gè)水分子形成的復(fù)合物為研究對(duì)象,構(gòu)建了一個(gè)包含15個(gè)穩(wěn)定三體復(fù)合物(S1~S15)的訓(xùn)練集(如圖1所示). 此外,還在考慮基組重疊誤差校正的情況下,采用MP2方法結(jié)合aug-cc-pVTZ基組,獲得了訓(xùn)練集中各構(gòu)象的二體和三體相互作用能. 二體和三體相互作用能分別由式(1)、式(2)和式(3)、式(4)計(jì)算得到.

圖1 15個(gè)由精氨酸側(cè)鏈與水形成的三聚體復(fù)合物Fig.1 15 Trimeric complexes formed by 15 arginine side chain interacting with water molecules
V2b(i,j)=E(i,j)-E(i)-E(j),
(1)
(2)
V3b(i,j,k)=E(i,j,k)-E(i,j)-E(i,k)-E(j,k)+E(i)+E(j)+E(k),
(3)
(4)
基于課題組前期的研究基礎(chǔ),本文采用了靜電作用函數(shù)、范德華作用函數(shù)和軌道作用函數(shù)構(gòu)建了一種適用于質(zhì)子化精氨酸分子的分子間相互作用勢(shì)函數(shù). 與傳統(tǒng)的力場(chǎng)方法不同,這個(gè)勢(shì)函數(shù)的靜電相互作用部分是基于可極化的化學(xué)鍵偶極矩建立的,其具體函數(shù)形式如式(5)所示:
(5)
(6)
其中,δμA-B代表了分子中A-B鍵的誘導(dǎo)偶極矩,μ0,A-B是無(wú)外部作用時(shí)A-B鍵的固有偶極矩,qind,A和qind,B分別是采用AM1方法計(jì)算得到的復(fù)合物的A-B鍵上A原子和B原子的電荷,qind,A,0和qind,B,0分別是無(wú)外部作用下分子中A-B鍵上A原子和B原子的電荷.
在前期研究工作的基礎(chǔ)上[5-8],本文對(duì)精氨酸側(cè)鏈相關(guān)參數(shù),尤其是胍基部分進(jìn)行了參數(shù)化. 表1給出了本文確定的相關(guān)參數(shù).
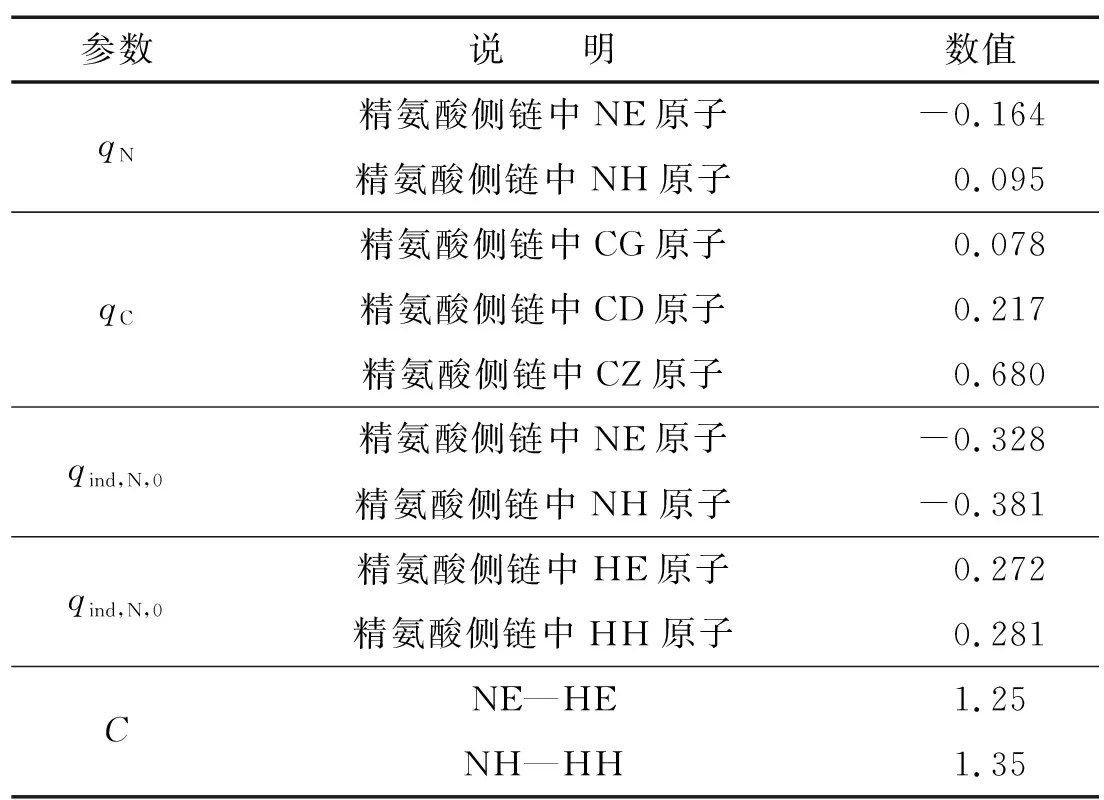
表1 本文所確定的參數(shù)Table 1 Parameters determined in this work
基于上述參數(shù),計(jì)算了訓(xùn)練集中的15種構(gòu)象的二體和三體作用能,如表2所示. 表中列出了采用MP2/aug-cc-pVTZ和本文方法計(jì)算得到的二體作用能和三體作用能的數(shù)值,以及本文方法與MP2/aug-cc-pVTZ的絕對(duì)誤差. 該結(jié)果顯示,重新擬合的參數(shù)能夠準(zhǔn)確計(jì)算這些復(fù)合物的二體和三體作用能.
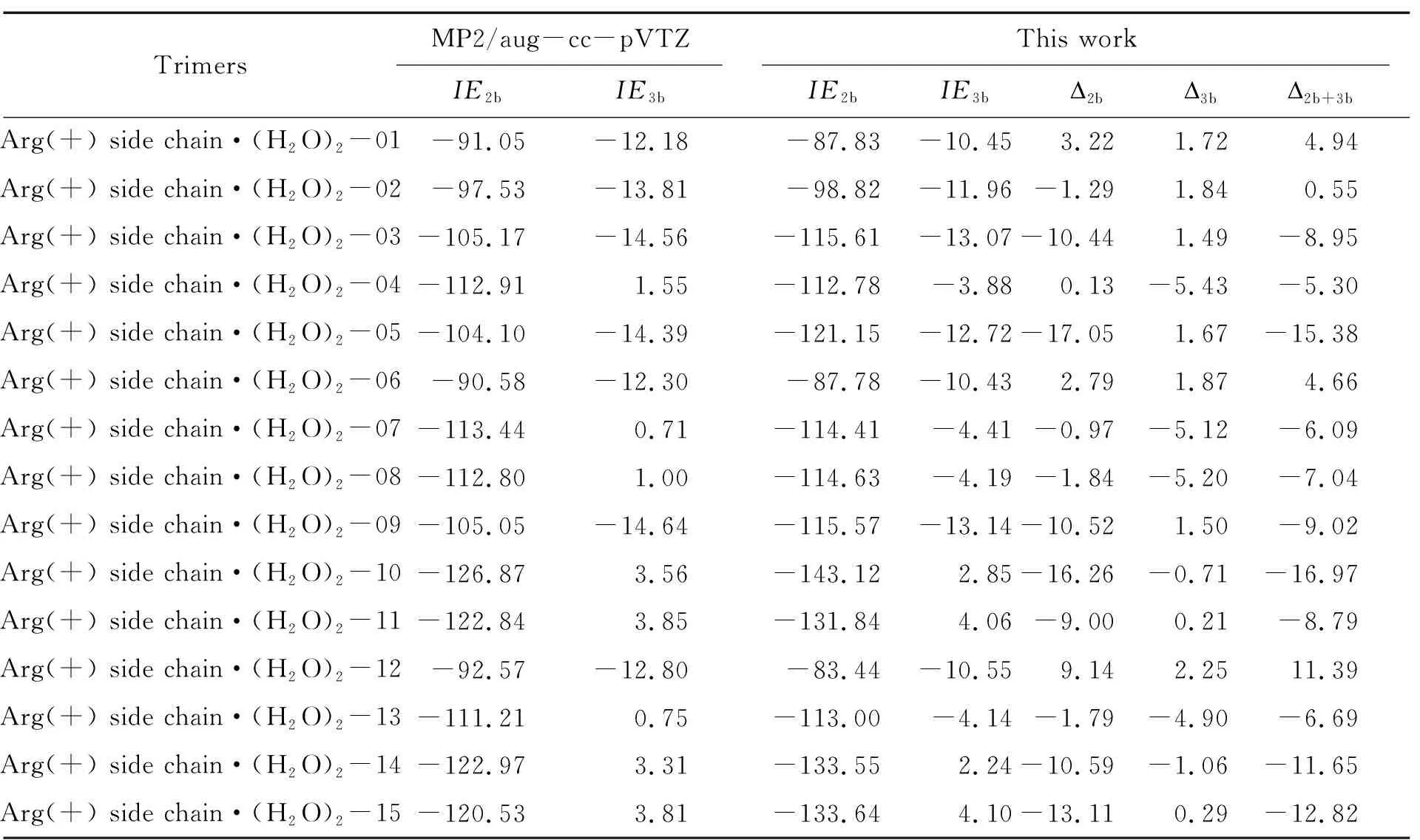
表2 采用不同方法計(jì)算15個(gè)質(zhì)子化的精氨酸側(cè)鏈與水分子復(fù)合物的二體作用能、三體作用能及相應(yīng)絕對(duì)誤差Table 2 Two-body interaction energies,three-body interaction energies,and corresponding absolute errors calculated using different methods for 15 protonated arginine side chain-water complexes kJ·mol-1
2 應(yīng)用
利用前述優(yōu)化后的偶極-偶極作用模型式(5)和式(6)和表1中提供的參數(shù),對(duì)一系列含有質(zhì)子化精氨酸側(cè)鏈的水分子團(tuán)簇[Arg(+) side chain·(H2O)n,(n= 8,10,12,15,18,20)]的二體和三體作用能進(jìn)行了研究,并與高精度的MP2/aug-cc-pVTZ水平結(jié)果進(jìn)行比較. 一系列含有質(zhì)子化精氨酸側(cè)鏈的水分子團(tuán)簇的結(jié)構(gòu)均取自分子動(dòng)力學(xué)模擬. 分別以軌跡中精氨酸側(cè)鏈分子及其周圍的8、10、12、15、18和20個(gè)水分子組成的復(fù)合物為基礎(chǔ),在B3LYP/6-31+G(d,p)水平上進(jìn)行結(jié)構(gòu)優(yōu)化,得到了如圖2所示的6個(gè)質(zhì)子化精氨酸側(cè)鏈與水分子形成的穩(wěn)定團(tuán)簇結(jié)構(gòu).

圖2 質(zhì)子化的精氨酸側(cè)鏈分子分別與8、10、12、15、18和20個(gè)水分子形成的團(tuán)簇Fig.2 Clusters formed by protonated arginine side chain with 8,10,12,15,18,and 20 water molecules
從測(cè)試團(tuán)簇分子結(jié)構(gòu)上講,6種不同尺寸的水分子團(tuán)簇中含有大量的分子間氫鍵作用. 不同于中性團(tuán)簇分子,質(zhì)子化的精氨酸側(cè)鏈分子與水分子間的氫鍵作用更強(qiáng),構(gòu)建的穩(wěn)定團(tuán)簇中,N-H…O型氫鍵的平均鍵長(zhǎng)僅為0.211 nm. 其中,最短氫鍵鍵長(zhǎng)為0.184 nm,最長(zhǎng)氫鍵鍵長(zhǎng)為0.293 nm.
二體和三體相互作用在分子間相互作用研究中扮演著至關(guān)重要的角色,其重要性不言而喻. 事實(shí)上,這兩種相互作用的貢獻(xiàn)在分子之間的總相互作用中可占95%以上. 作為一種分子力場(chǎng)模型,它們能夠以極高的準(zhǔn)確性預(yù)測(cè)分子團(tuán)簇中的二體和三體相互作用,這對(duì)于深入探討大分子系統(tǒng)的性質(zhì)以及理解分子間相互作用的本質(zhì)至關(guān)重要.
表3列出了MP2/aug-cc-pVTZ和本文方法計(jì)算的6個(gè)質(zhì)子化精氨酸側(cè)鏈與水分子形成的團(tuán)簇的分子間二體和三體相互作用能,以及本文方法與MP2/aug-cc-pVTZ的絕對(duì)誤差. 以二體作用能的計(jì)算結(jié)果為例,以MP2/aug-cc-pVTZ方法計(jì)算結(jié)果為基準(zhǔn),本文方法在計(jì)算這6個(gè)團(tuán)簇的二體作用能時(shí),絕對(duì)誤差的平均值為8.52 kJ·mol-1,相對(duì)誤差的平均值為 -1.22%. 這顯示出了本文方法在計(jì)算準(zhǔn)確度方面的卓越表現(xiàn). 具體而言,本文方法計(jì)算Cluster-B [(Arg(+) side chain· (H2O)10)]團(tuán)簇的二體作用能與標(biāo)準(zhǔn)數(shù)據(jù)僅相差0.17 kJ·mol-1,而最大絕對(duì)誤差出現(xiàn)在Cluster-D[(Arg(+) side chain· (H2O)15)]團(tuán)簇,其計(jì)算的二體作用能的絕對(duì)誤差為25.41 kJ·mol-1,相對(duì)誤差為 -3.9%.
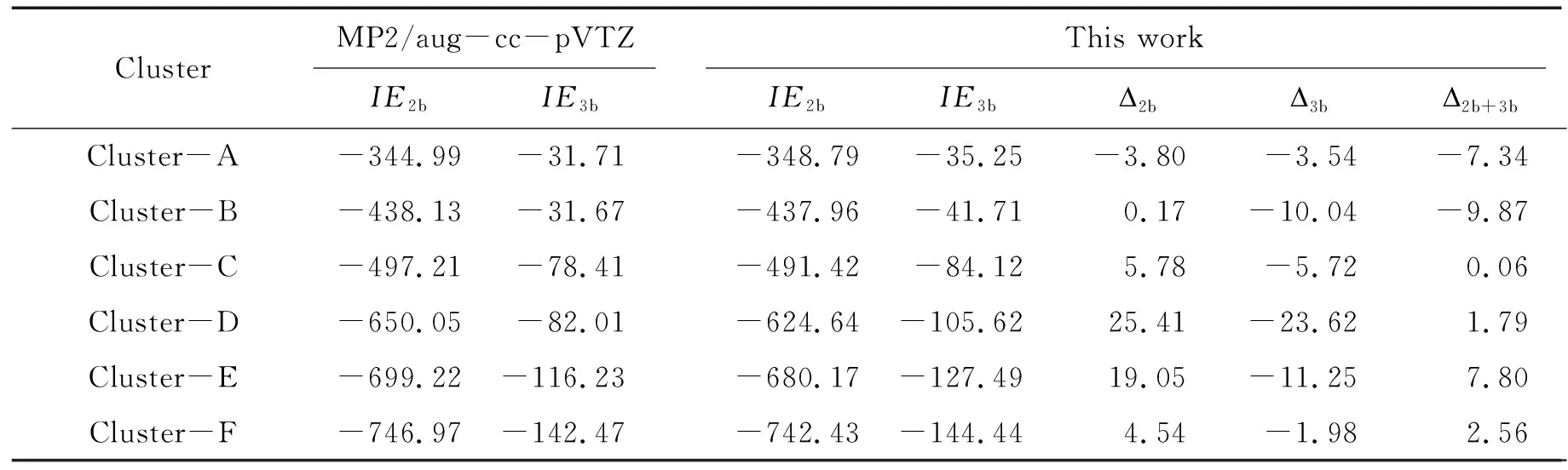
表3 采用不同方法計(jì)算質(zhì)子化精氨酸側(cè)鏈與水分子團(tuán)簇的二體作用能、三體作用能及相應(yīng)絕對(duì)誤差Table 3 Two-body interaction energies,three body interaction energies,and corresponding absolute errors calculated using different methods for protonated arginine side chain and water molecules clusters kJ·mol-1
不同于僅能描述分子間二體相互作用的非極化力場(chǎng)模型,本文方法基于誘導(dǎo)化學(xué)鍵偶極方案將極化作用引入模型. 采用簡(jiǎn)單而有效的誘導(dǎo)偶極與其他偶極或電荷之間的相互作用勢(shì)來(lái)描述體系的三體及以上相互作用能.在三體作用能計(jì)算方面,本文方法也顯示出了較高的計(jì)算準(zhǔn)確度,其計(jì)算結(jié)果的絕對(duì)誤差的平均值為 -9.36 kJ·mol-1. 這不僅顯示出了本方法能夠較好地描述分子間的三體作用,同時(shí)也和二體作用能計(jì)算誤差形成了有益的互補(bǔ),能夠更準(zhǔn)確地描述這類團(tuán)簇分子間的總相互作用.
總的來(lái)說(shuō),本文方法在預(yù)測(cè)本文所研究團(tuán)簇的二體和三體相互作用能方面表現(xiàn)出了高準(zhǔn)確度,絕對(duì)誤差的絕對(duì)值最大為 9.87 kJ·mol-1,絕對(duì)誤差的平均值為 -0.83 kJ·mol-1. 這不僅反映了本文方法在分子間相互作用能計(jì)算方面的卓越表現(xiàn),同時(shí)也表明了本文方法在三體相互作用能與二體相互作用能計(jì)算的誤差之間的互補(bǔ)性,能更準(zhǔn)確地描述了這類團(tuán)簇分子間的相互作用. 另外,值得一提的是,本文方法在不同研究系統(tǒng)中的計(jì)算誤差沒(méi)有明顯地隨體系規(guī)模增大而增加,這顯示出了它在應(yīng)用和推廣方面的出色潛力.
為了更全面地評(píng)估本研究中新的誘導(dǎo)化學(xué)鍵偶極計(jì)算方法的可靠性,以及新的擬合參數(shù)在計(jì)算蛋白質(zhì)分子中質(zhì)子化精氨酸片段與水分子形成的團(tuán)簇中的二體和三體相互作用能上的可靠性,重新構(gòu)建了包含完整質(zhì)子化精氨酸側(cè)鏈的水團(tuán)簇分子結(jié)構(gòu).具體過(guò)程如下:首先,將質(zhì)子化的精氨酸分子(兩端分別用氮甲基和乙酰基封端飽和)置于水盒子中,并使用NPT系綜下的GTH-PBE[9]方法進(jìn)行了10 ps的分子動(dòng)力學(xué)模擬;其次,在平衡后的模擬中,每1 ps保存一個(gè)結(jié)構(gòu),共獲得了5個(gè)質(zhì)子化精氨酸分子與水分子形成的團(tuán)簇. 需要強(qiáng)調(diào)的是,為了保證參考數(shù)據(jù)的計(jì)算準(zhǔn)確度,僅截取距離質(zhì)子化胍基C原子0.45 nm以內(nèi)的水分子與質(zhì)子化精氨酸殘基構(gòu)成團(tuán)簇. 這些團(tuán)簇的結(jié)構(gòu)如圖3所示.
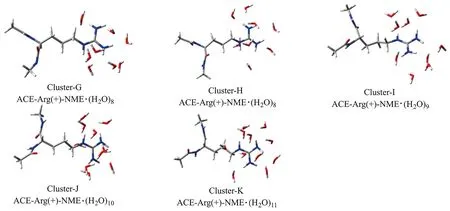
圖3 質(zhì)子化精氨酸二肽分子與水分子形成的團(tuán)簇Fig.3 Clusters formed by protonated arginine dipeptide interacting with water molecules
分別采用RI-MP2/aug-cc-pVTZ、AMOEBAbio18[10-11]和本文方法計(jì)算上述5個(gè)團(tuán)簇的總二體作用能和總?cè)w作用能,計(jì)算結(jié)果列于表4中. 表中展示了作為基準(zhǔn)的RI-MP2/aug-cc-pVTZ方法在計(jì)算這5個(gè)隨機(jī)團(tuán)簇中二體和三體作用能的結(jié)果. 同時(shí),本文方法和常用的AMOEBAbio18可極化力場(chǎng)方法的計(jì)算結(jié)果也列于表中. 此外,還列出了各組數(shù)據(jù)之間的絕對(duì)誤差,以便更清晰地評(píng)估這些計(jì)算方法的性能. 表中的Δ2b+3b為二體作用能和三體作用能絕對(duì)誤差之和.

表4 采用不同方法計(jì)算封端飽和的質(zhì)子化精氨酸與水分子團(tuán)簇的二體作用能、三體作用能及相應(yīng)絕對(duì)誤差Table 4 Two-body interaction energies,three-body interaction energies and corresponding absolute errors calculated using different methods for protonated arginine dipeptide-water clusters kJ·mol-1
首先,對(duì)于Cluster-G和Cluster-H這兩個(gè)擁有相同水分子數(shù)量的團(tuán)簇進(jìn)行討論. 不論是使用AMOEBAbio18方法還是本文提出的方法,都能夠成功預(yù)測(cè)它們的相對(duì)穩(wěn)定性. 不過(guò),值得注意的是,相較于AMOEBAbio18方法,本文方法采用了一種更為高效的非迭代化學(xué)鍵偶極距方案,從而實(shí)現(xiàn)了相當(dāng)高的計(jì)算準(zhǔn)確度. 這也反映了本文方法在計(jì)算效率上的優(yōu)勢(shì). 此外,本文方法在對(duì)其他隨機(jī)團(tuán)簇的二體和三體相互作用能進(jìn)行計(jì)算時(shí),同樣表現(xiàn)出了令人滿意的計(jì)算準(zhǔn)確度,這也部分證實(shí)了該計(jì)算方法和參數(shù)的可靠性.
然而,需要特別注意的是,本文中使用了原有的基于中性氨基酸的主鏈參數(shù)來(lái)完成質(zhì)子化精氨酸主鏈相關(guān)作用的計(jì)算. 這導(dǎo)致了在含有質(zhì)子化精氨酸片段的水團(tuán)簇的多體相互作用能計(jì)算中,相對(duì)于含有質(zhì)子化精氨酸側(cè)鏈的水團(tuán)簇,計(jì)算誤差較大. 為解決這一問(wèn)題,我們計(jì)劃在未來(lái)的研究工作中進(jìn)一步有針對(duì)性的優(yōu)化精氨酸主鏈相關(guān)基團(tuán)的參數(shù),以期獲得更高的計(jì)算準(zhǔn)確度. 這個(gè)優(yōu)化過(guò)程將有助于更準(zhǔn)確地描述蛋白質(zhì)中精氨酸殘基與水分子的相互作用,從而提高模擬結(jié)果的可靠性.
總的來(lái)說(shuō),通過(guò)這些結(jié)果,不僅證實(shí)了本文方法在多體相互作用計(jì)算中的有效性,還展示了其在計(jì)算效率上的優(yōu)勢(shì). 然而,在應(yīng)對(duì)其他氨基酸殘基的挑戰(zhàn)時(shí),還將繼續(xù)努力,以進(jìn)一步完善和改進(jìn)本方法的計(jì)算準(zhǔn)確度,使其更符合實(shí)際情況. 這將為分子模擬和計(jì)算化學(xué)領(lǐng)域提供更為可靠的工具和方法,有望在藥物設(shè)計(jì)和生物化學(xué)研究中產(chǎn)生廣泛的應(yīng)用前景.
3 結(jié) 論
本研究通過(guò)引入一種新的誘導(dǎo)化學(xué)鍵偶極計(jì)算方法,成功應(yīng)用于蛋白質(zhì)分子中質(zhì)子化精氨酸片段與水分子形成的團(tuán)簇的相互作用能計(jì)算.結(jié)果表明,新方法在預(yù)測(cè)本文涉及的尺寸較大的含有質(zhì)子化精氨酸側(cè)鏈、二肽的隨機(jī)水分子團(tuán)簇的二體、三體總作用能的絕對(duì)誤差的平均值為 -8.3 kJ·mol-1,相對(duì)誤差的平均值為3.8%,表現(xiàn)出了良好的計(jì)算準(zhǔn)確度.在計(jì)算量上還明顯小于常用的可極化力場(chǎng)方法.然而,在處理精氨酸主鏈相關(guān)作用時(shí),也面臨一些挑戰(zhàn),需要進(jìn)一步改進(jìn)相關(guān)參數(shù)以提高計(jì)算準(zhǔn)確度. 這一研究為理解分子間相互作用,尤其是帶電荷片段間的相互作用提供了重要的工具和方法,對(duì)于藥物設(shè)計(jì)、生物物理化學(xué)等領(lǐng)域的研究具有積極的影響,為未來(lái)的科學(xué)研究提供有益的參考.
 遼寧師范大學(xué)學(xué)報(bào)(自然科學(xué)版)2023年4期
遼寧師范大學(xué)學(xué)報(bào)(自然科學(xué)版)2023年4期
- 遼寧師范大學(xué)學(xué)報(bào)(自然科學(xué)版)的其它文章
- 大學(xué)生乒乓球選項(xiàng)課運(yùn)動(dòng)技能學(xué)習(xí)評(píng)價(jià)指標(biāo)模型構(gòu)建
- 哈長(zhǎng)城市群局部收縮識(shí)別與城市競(jìng)爭(zhēng)力研究
- 遼寧沿海經(jīng)濟(jì)帶“三生空間”功能耦合協(xié)調(diào)時(shí)空分異及影響因素
- 設(shè)計(jì)思維視域下“現(xiàn)代教育技術(shù)”公共課教學(xué)模式構(gòu)建與應(yīng)用研究
- 遼寧省土地利用碳排放空間關(guān)聯(lián)性及碳平衡分區(qū)
- HQEFT框架內(nèi)半輕衰變的相關(guān)研究
