核桃花粉活力測定方法的選擇及花粉特性的研究
劉誠誠, 彭建勇, 李 恒, 藺雨陽, 宋長勇, 張春花
(1.攀枝花市農林科學研究院, 四川 攀枝花 617061;2.攀枝花市金沙林場同德管護站, 四川 攀枝花 617007)
花粉活力的高低由植物本身的基因型、花粉類型和遺傳特性所決定,其次還受溫度、濕度、光照等環境因子影響[1]。花粉活力的檢測方法主要有離體萌發法、授粉法、染色法等。因離體萌發法操作較復雜,花費時間長,不適宜花粉活力的快速檢測[2];而授粉法受環境因子影響大,近年來研究人員少有采用;染色法因具有快速簡便的優點,被廣泛采用。
在核桃的雜交育種工作中,父本的花粉活力直接影響雜交試驗的成敗。肖真真等[3]和張煥玲等[4]都選用了TTC、I2-KI、MTT染色劑測定核桃花粉活力,認為MTT更適宜快檢;但是在胡青等[5]、趙建建等[6]的核桃花粉活力研究中,TTC染色劑更為有效。因此,不同品種的核桃其花粉活力對染色劑的反應不盡相同,參與雜交育種的品種,需要與之配套的花粉活力快檢方法。本地圓核桃是項目組長期跟蹤觀測的優良品種,具有果面光滑,縫合線不緊密,果仁飽滿,仁色米白,遺傳性狀穩定等優點。是甄選出來供雜交育種的優良親本,潛在育種價值高,掌握其花粉特性,摸索出花粉活力規律迫在眉睫。本試驗通過本地圓核桃花粉活力的測定方法及花粉特性的研究,遴選花粉活力簡便、準確的測定方法,并探尋花粉活力變化規律和儲存方法。
1 材料和方法
1.1 試驗材料及采集方法
試驗材料為攀枝花本地優良核桃,本地稱為圓核桃,樹齡10年,2018年開始結果,現處于盛果期,位于攀枝花市仁和區啊喇鄉起查那村。花粉采集選在無風的早上,采集試驗所需的雄花序,裝入硫酸紙袋中,放入保溫箱中迅速帶回實驗室陰干,待花藥自然開裂散粉后,收集于棕色小藥瓶中待測。
1.2 試驗方法
1.2.1花粉活力測定方法的篩選
取少量收集到的花粉置于烘箱中,100 ℃烘干24 h,至花粉失活作為ck。另取收集到的新鮮花粉,選用醋酸洋紅染色法[7]、氯化三苯基四氮唑(TTC)法[8]、MTT染色法[9]、碘-碘化鉀(I2-KI)[10]染色法分別對花粉進行活力測定后篩選出適宜檢測該花粉活力的方法。
1.2.2不同采集時期花粉活力測定
選擇散粉始期、散粉盛期、散粉末期采集花序,陰干后抖落收集花粉進行活力測定。
1.2.3不同儲存方式花粉活力測定
將采集到的花粉分成兩份,一份置于常溫中存儲,另一份置于冰箱中冷藏,定時對兩份花粉進行活力測定。
1.2.4花粉泡水活力測定
取少量花粉模擬泡水噴施處理,將花粉混入清水中,并加入少量白糖,分別在0 min、5 min、10 min、15 min、20 min測定泡水后的花粉活力。
1.2.5自然散粉活力測定
收集樹下掉落的核桃雄花序,常溫保存,定時對其進行活力測定。
1.3 數據統計
花粉活力測定時,每處理設置3個重復,每個重復在顯微鏡下隨機選取3個視野,每個視野觀察的花粉數不低于50粒。
花粉活力/%=(有活力的花粉數量/總花粉數量)×100%。
1.4 數據處理
采用單因素方差分析(one-way ANOVA)和最小顯著差異法(LSD)進行多重比較。采用SPSS22.0軟件完成數據分析,Excel2019軟件完成制圖。
2 結果與分析
2.1 花粉活力測定染色劑的比較與選擇
如圖1所示,醋酸洋紅對花粉染色后,視野內活力花粉和失活花粉均呈橙紅色,活力花粉染色較深,失活花粉染色較淺,不能很好區分花粉是否具有活力;TTC對花粉染色后,視野內的活力花粉染色情況不理想,大部分活力花粉不能染色,失活花粉都不能染色,且多次試驗結果不穩定,時常出現活力花粉染色失敗,花粉均無法染色的情況;碘-碘化鉀對花粉染色后,視野內的活力花粉和失活花粉均呈紅棕色,不能區分花粉是否具有活力;MTT對花粉進行染色后,活力花粉呈玫紅色,失活花粉呈黃色或淺粉色,能很好區分活力花粉和失活花粉。比較四種染色法對花粉的染色情況MTT法最佳,醋酸洋紅法次之,再次為TTC法,最后為碘-碘化鉀。因此,可采用MTT染色法對該品種花粉進行活力測定。
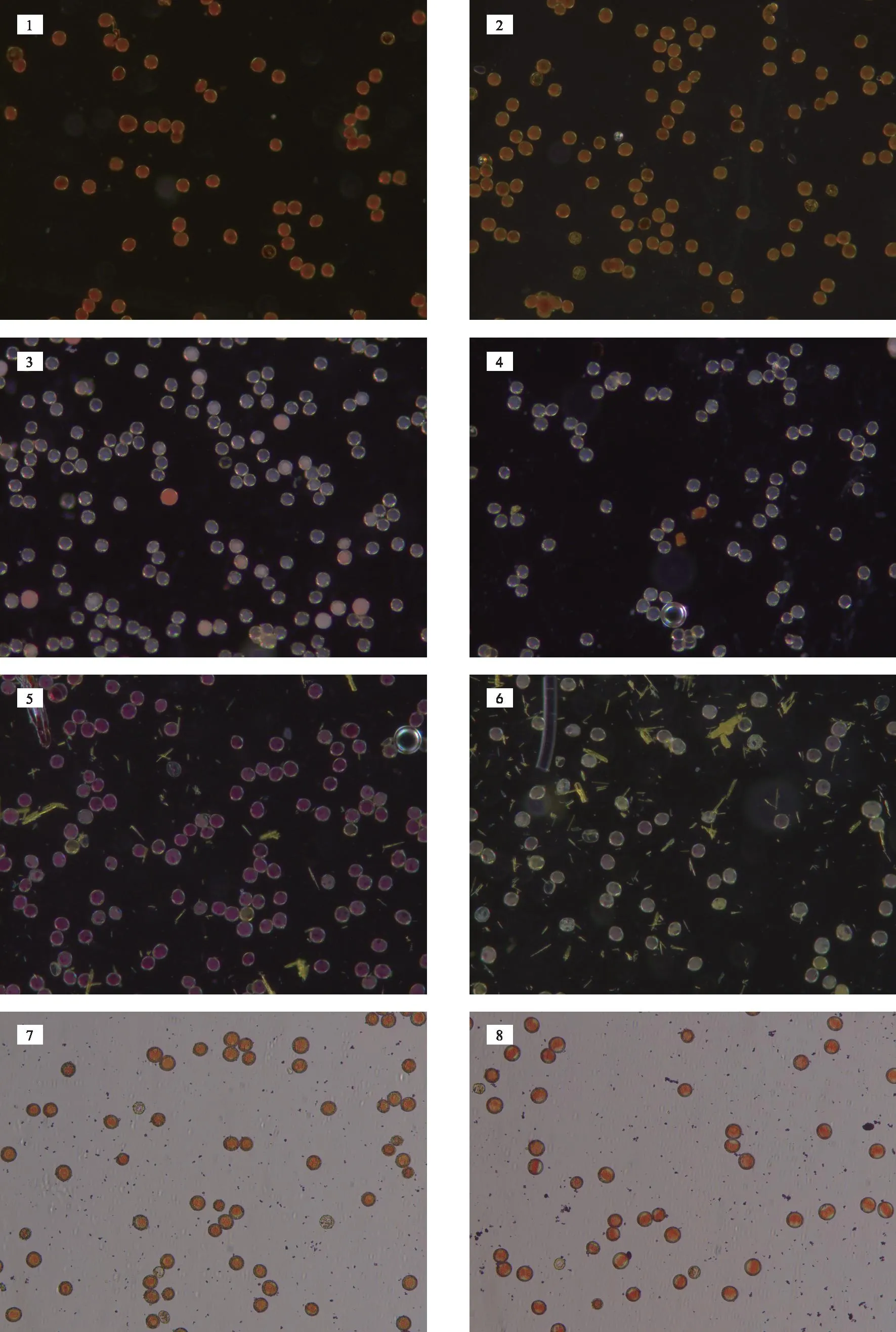
注:1號為活力花粉被I2-KI染色,2號為失活花粉被I2-KI染色,3號為活力花粉被TTC染色,4號為失活花粉被TTC染色,5號為活力花粉被MTT染色,6號為失活花粉被MTT染色,7號為活力花粉被醋酸洋紅染色,8號為失活花粉被醋酸洋紅染色。圖1 4種染色法對花粉的染色情況
2.2 不同采集時期花粉活力
結果如表1所示,花粉活力在散粉始期較低,為48.442%,在散粉盛期和散粉末期較高,分別為96.136%,93.606%。經方差分析顯示,散粉始期花粉活力與散粉盛期、散粉末期在0.05水平上差異顯著。

表1 不同采集時期花粉活力
2.3 不同存儲方式花粉活力
圖2表明,花粉活力隨時間的延長呈下降趨勢,但是冷藏保存的花粉活力下降速度較常溫保存緩慢。花粉在剛采收時,活力為93.849%,在冷藏5 d內,花粉活力為96.285%,差異不顯著,冷藏31 d內,花粉活力在0.05水平上差異顯著,下降趨勢不明顯,冷藏31 d后,花粉活力差異顯著,下降趨勢明顯;常溫儲藏花粉,花粉活力差異顯著,活力下降趨勢明顯,在儲藏10 d后,花粉活力為0。

注:圖中數值為平均值,不同大、小寫字母表示不同處理間差異顯著(p<0.05)。A為不同儲存方式花粉活力變化;B為泡水后花粉活力變化;C為自然散粉花粉活力變化。圖2 不同處理的花粉活力
2.4 花粉泡水活力變化
如圖2所示,花粉初始活力為93.606%,在泡水后花粉活力下降,且在0.05水平上差異顯著。泡水前5 min,花粉活力下降緩慢,下降至89.935%;泡水10 min,花粉活力迅速下降至6.859%;泡水15 min,花粉活力下降至1.854%;泡水20 min,花粉活力下降至0.518%。
2.5 自然散粉的花粉活力變化
如圖2所示,自然散粉的花粉活力為85.862%,自然儲藏后花粉活力下降,且在0.05水平上差異顯著。在自然儲藏13 d后,花粉活力下降至13.32%,16 d后花粉活力為0。
3 結論與討論
3.1 討 論
3.1.1核桃花粉活力測定的選擇
被子植物的有性生殖過程須經活力花粉傳到可授性柱頭完成授精[11],因而了解品種花粉活力對于核桃雜交育種愈發關鍵。本研究選用的4種染色劑檢測花粉活力,并將失活花粉作為對照,能夠直觀區分活力花粉和失活花粉的染色情況,準確篩選出檢測方法。本研究中,MTT染色法能快速有效的檢測本地圓核桃花粉活力,而醋酸洋紅染色法、氯化三苯基四氮唑(TTC)法、碘-碘化鉀(I2-KI)不能穩定準確測定其花粉活力。
在本研究中,核桃活力花粉和失活花粉均可被I2-KI染成紅棕色,活力花粉著色較深,失活花粉則較淺。該方法通過花粉內淀粉染色情況來判斷花粉活力,活的花粉有淀粉積累,被I2-KI染成藍色,而發育不良的花粉不積累淀粉,用I2-KI染色時不顯藍色,另外,其著色程度由花粉壁的薄厚和花粉內支鏈淀粉和直鏈淀粉比例高低決定,且直鏈淀粉顯藍色,支鏈淀粉為紅棕色[12]。本研究中,花粉被I2-KI染色后呈紅棕色,這可能是由于該品種內支鏈淀粉占主導,直鏈淀粉較少,因而I2-KI染色后呈紅棕色,該顏色與溶液自身顏色相似,故染色后的活力花粉與失活花粉無法區分。另外,該花粉被I2-KI染色不明顯,可能是因為該品種花粉壁通過性不好,本研究中TTC法不能對花粉進行染色,也進一步說明這一論證,也有學者提出TTC染色法對花粉要求較高,難以準確測定花粉活力[13]。在前人的研究中,漾濞大炮[5]、綠嶺[6]、川早1號[14]等品種的花粉可以被TTC染色,而新新2號[3]、云新14號[15]、清香[16]等品種花粉只能被MTT染色。
3.1.2花粉的處理、儲藏與花粉活力關系
通過將花粉泡水后檢測其活力,圓核桃花粉經泡水處理后5 min幾乎完全失活,孔令通[17]在對薄殼山核桃的花粉進行研究時,發現泡水噴施花粉液坐果率低,可佐證核桃特定品種的花粉不宜采用泡水噴施的方法授粉。花粉活力在散粉盛期最強,末期稍差,初期最弱(圖2),花粉的自然成熟散粉是品種在漫長進化后的時機選擇,與特定雌蕊的花期進行適配,來保證品種下品系多樣性的最優策略。不適宜的人工方法和時機干預會表現為花粉活力的“固執現象”(以快速失活或累積不夠為主要表現)。這種花粉活力的“固執現象”,是收集花粉進行人工授粉或雜交育種中需要注意或設法利用的參考。劉天鳳等[15]對不同時期的花粉活力進行了研究,其結果與本研究不同,說明不同品種的核桃花粉活力特性不同,在雜交育種以及配置授粉樹等工作中,花粉活力的研究顯得尤為重要。
3.2 結 論
本地圓核桃花粉活力可采用MTT染色法快速、有效檢測其活力,冷藏處理有利于延緩花粉失活,泡水處理可能加速花粉失活,在核桃授粉中應謹慎使用;本研究模擬了自然條件下花粉活力的變化,研究表明,在自然條件下,自然散粉的核桃花粉參考壽命為16 d,可為核桃選擇授粉樹配置提供理論指導。

