靶向膽固醇穩態小分子藥物治療膠質瘤的研究進展
姜偉,王君萍,周鵬,黃玲玲,張梅,陳學冉,2,王宏志,2,方志友,2
作者單位:1中國科學院合肥腫瘤醫院藥學中心,安徽 合肥230031;2中國科學院合肥物質科學研究院健康與醫學技術研究所,安徽 合肥230031
膠質瘤是成人最常見的原發性惡性中樞神經系統腫瘤之一,起源于神經上皮細胞。Ⅳ級膠質瘤也稱為膠質母細胞瘤(GBM),惡性程度最高并且最難治愈,病人總生存期更短,具有極高病死率[1]。GBM 細胞生長十分迅速,且可快速侵襲進入周圍的組織間隙,導致相鄰的正常組織被血管和淋巴管破壞[2]。替莫唑胺(TMZ)是治療GBM最為代表性的口服烷化劑,但GBM 對TMZ 易產生耐藥性,僅能提高病人兩個月的中位生存期。因此探索GBM 發病機制以及研究新的潛在治療策略具有非常重要意義。
1 細胞代謝與腫瘤發生發展
腫瘤細胞的主要特征是會以最大限度地合成膜、核酸和蛋白質的底物進行自我調整,從而提高增殖率。能量代謝重編程被認為是腫瘤的新標志,腫瘤細胞通過調節能量代謝促進其快速增殖。
葡萄糖代謝主要包括細胞質中的糖酵解途徑、磷酸戊糖途徑、絲氨酸合成途徑和線粒體中的三羧酸循環。腫瘤細胞在有氧條件下選擇糖酵解途徑來為大分子合成提供中間底物,合成核苷酸、脂肪酸和氨基酸進而加速細胞分裂。每分子葡萄糖通過糖酵解產生三磷酸腺苷(ATP)的效率較低,但產率比氧化磷酸化要快得多,可以滿足腫瘤細胞快速生長和增殖的需求,是腫瘤細胞的主要能量來源[3]。
脂肪酸和氨基酸,尤其是谷氨酰胺、絲氨酸和甘氨酸的合成分解失調也是支持腫瘤細胞生長的代謝調節劑。谷氨酰胺通過提供其氮和碳參與癌細胞中能量產生、大分子合成和信號傳遞的一系列途徑。增加谷氨酰胺在線粒體依賴性生物能量產生和細胞生物合成中的使用是許多腫瘤細胞的一個關鍵特征[4]。
近年大量研究報道了膽固醇代謝在調節腫瘤生物學過程中的作用,特別是致癌信號通路、鐵死亡和腫瘤微環境[5]。致癌基因的增加和抑癌基因的喪失是癌細胞的重要特征,并重編程膽固醇代謝途徑。越來越多的證據表明,膽固醇及其代謝物是促進腫瘤發展的信號分子[6]。鑒于膽固醇代謝在癌癥中的這些重要功能,針對膽固醇代謝的新關鍵分子和策略的篩選已成為癌癥研究領域的熱點,且近年來取得了重大進展。
2 膽固醇穩態
2.1 膽固醇合成途徑膽固醇是哺乳動物細胞膜的必需脂質成分,是維持機體正常生理功能的必要物質。膽固醇的生物合成在內質網上進行,包括甲羥戊酸(MVA)途徑、角鯊烯生物合成等近30 種酶促反應[7]。前兩個反應是由硫解酶和3-羥基-3-甲基戊二酰輔酶A(HMG-CoA)催化的可逆反應,隨后發生的反應是調節膽固醇合成的關鍵點,由3-羥基-3-甲基戊二酰輔酶A(HMG-CoA)還原酶(HMGCR)催化[8]。固醇調節元件結合蛋白2(SREBP2)和肝臟X受體(LXRs)兩組轉錄因子是參與膽固醇合成基因的關鍵固醇元件調節蛋白,它能夠調節HMGCR、HMG-CoA 合成酶(HMGCA)、甲羥戊酸激酶(MVK)和攝取膽固醇的低密度脂蛋白LDL(LDL)受體(LDLR)等蛋白的表達[9]。
2.2 膽固醇運輸途徑
2.2.1 膽固醇外排 大多數外周細胞和組織缺乏代謝膽固醇的能力,主要依靠外排途徑來維持細胞穩態。有多種機制導致細胞膽固醇流出,其中主動外排途徑主要由ATP 結合盒(ABC)轉運蛋白ABCA1 和ABCG1 介導。ABCA1 對膽固醇和磷脂流出至載脂蛋白和高密度脂蛋白(HDL)生物發生至關重要。ABCG主要促進膽固醇流出至HDL顆粒。膽固醇流出率取決于細胞中的膽固醇負荷、HDL 的組成、大小和濃度以及流出轉運蛋白的表達。
2.2.2 膽固醇內吞 細胞膽固醇來源于內質網(ER)中的從頭合成或來源于細胞外環境的攝取。這種攝取可以通過天然或修飾的LDL 的內吞作用,或從脂蛋白中選擇性攝取游離或酯化膽固醇而發生。LDLR 是SREBP2 的轉錄靶點,是外周細胞獲取膽固醇的主要參與者。LDL與LDLR結合后,通過內吞作用被轉移到細胞內體后再解離出來,并進一步轉移到溶酶體,在溶酶體中膽固醇酯被酸性脂肪酶水解以釋放游離膽固醇。NPC蛋白是游離膽固醇從溶酶體中轉運出來所必需的。在甾醇轉運蛋白的幫助下,膽固醇最終被轉移到細胞膜或內質網(ER)膜上[10]。LXR 激動劑GW3965能夠激動下游的信號通路進一步降低細胞內膽固醇含量殺死GBM 細胞,延長荷瘤小鼠的生存期。而NPC缺失在引起膽固醇積累的同時會導致自噬囊泡向溶酶體的運輸缺陷。
2.3 膽固醇代謝途徑膽固醇的穩態對維持細胞的功能非常重要,膽固醇合成代謝途徑的異常活化是很多腫瘤發生的標志之一,大量的膽固醇能夠提供腫瘤細胞在侵襲和遷移過程中所需要的各種物質[11]。腫瘤細胞表現出代謝異常,以滿足與腫瘤快速生長相關的高能量和生物合成需求。SREBPs 在調節膽固醇穩態中起關鍵作用,在GBM 中,抑制SREBP 的水平可以抑制低氧狀態下腫瘤細胞的脂質合成和細胞增殖。越來越多的研究表明腫瘤細胞需要吸收足夠的膽固醇來維持自身的生長和增殖[12],針對膽固醇穩態的干預在腫瘤治療過程中的作用也被越來越多的研究者認同。我們調研總結了針對不同靶標的膽固醇穩態調控相關小分子藥物及腫瘤治療的臨床應用,如表1所示。
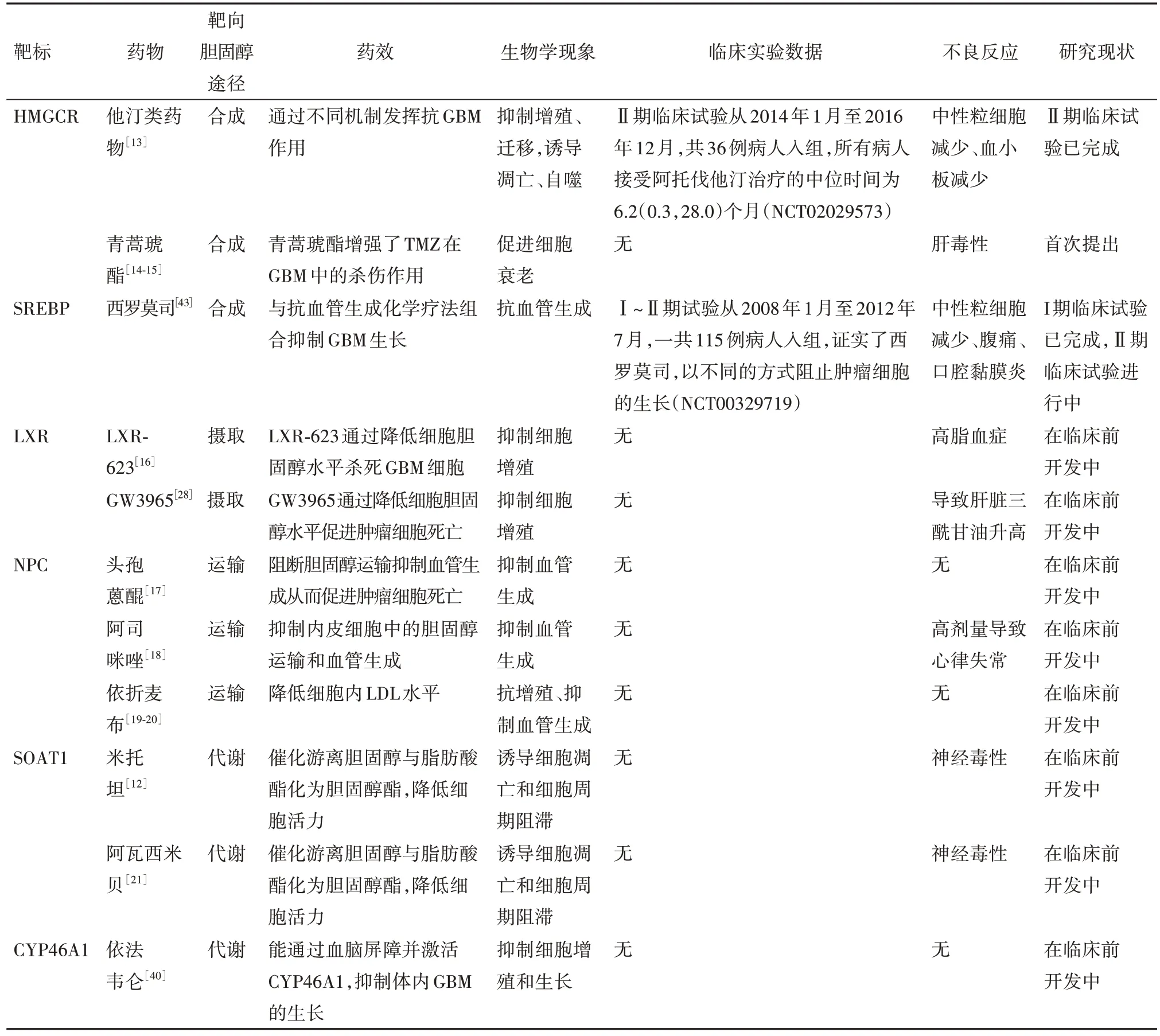
表1 靶向腫瘤細胞中膽固醇代謝的小分子藥物
3 針對GBM中膽固醇代謝新方法
3.1 靶向膽固醇合成HMGCR 在GBM 的發展中起著至關重要的作用,在臨床的GBM 樣本中可以觀察到HMGCR 的上調,甲羥戊酸途徑是合成膽固醇的重要途徑之一,阻斷該途徑會顯著影響細胞活動。臨床前研究表明,HMGCR 抑制劑,通常被稱為“他汀類藥物”,除具有降低膽固醇和改善心血管風險的作用外,還具有良好的抗腫瘤特性[22]。他汀類藥物通過抑制甲羥戊酸途徑發揮抗癌活性,無論是在體內還是體外,他汀類藥物作為單藥治療或聯合治療,對腫瘤都有一定療效[23]。
辛伐他汀可以通過多種人類腫瘤細胞系的內在凋亡途徑誘導細胞死亡,包括星形細胞瘤、神經母細胞瘤和GBM[24]。臨床GBM 治療中連續使用TMZ 會導致耐藥性。最近發現他汀類藥物治療被證明在體外可以改善TMZ的抗GBM作用[25]。例如,阿托伐他汀通過異戊二烯化依賴性方式抑制Ras信號傳導來提高TMZ 在GBM 中的療效[26]。有研究表明,洛伐他汀可能通過絲氨酸-蘇氨酸蛋白激酶(Akt)∕雷帕霉素靶蛋白(mTOR)信號級聯抑制觸發自噬誘導,通過抑制溶酶體相關膜蛋白和動力蛋白,可能影響自噬體-溶酶體融合機制[24]。最新的臨床研究發現,在18 例惡性GBM 病人的Ⅰ~Ⅱ期試驗中,洛伐他汀聯合TMZ治療具有良好的耐受性[27]。
3.2 靶向膽固醇攝取關鍵調控因子與非腫瘤細胞相比,腫瘤細胞表現出重新編程的代謝能力,因此腫瘤代謝關鍵因子成為治療靶標。LXRs屬于核受體超家族,被激活后會導致細胞內膽固醇的降低,膽固醇的這種急性流出通過增加其合成得到補償[28]。通過藥理學驅動LXR途徑來限制細胞內甾醇的可用性會抑制快速分裂細胞類型(如淋巴細胞)的增殖。LXR激動劑,例如LXR623和GW3965,已經進入臨床試驗[29]。在黑色素瘤和膠質母細胞瘤的模型系統中,LXR的激活使幾種臨床前模型系統的病人生存期延長。
LXR 激動劑GW3965 可以調節LXR 的活性,在體外通過ABAC1 的生物學功能從而促進膽固醇的轉運,進而影響膽固醇和磷脂在質膜外的分布,使細胞質膜發生重造。研究表明用GW3965處理膠質瘤細胞后,出現劑量依賴性抑制生長并促進腫瘤細胞的死亡,而添加LDL 后這種死亡得以挽救,表明GW3965 對腫瘤的殺死作用是通過改變細胞膽固醇的水平來驅動。ABAC1 是LXR 的直接轉錄靶標,GW3965 處理后強烈誘導了ABAC1 的表達并且降低了LDLR 的含量,并伴隨著59%的腫瘤生長抑制和GBM 中細胞凋亡的增加。這些數據表明LXR 激動劑通過上調轉運蛋白基因ABAC1 的外排和降解LDLR來降低LDL攝取,擾亂GBM的膽固醇穩態,從而有效抑制GBM細胞增殖與體內腫瘤生長[30]。
3.3 靶向膽固醇運輸蛋白LDL 在內吞作用發生后被細胞吸收并運送到溶酶體,在溶酶體內膽固醇酯被酸性細胞酶裂解以釋放游離膽固醇供細胞使用[5]。NPC1 是分布在溶酶體上,具有13 個跨膜結構域的跨膜轉運蛋白,其介導的囊泡內吞途徑是吸收胞外膽固醇所必需的。NPC2 蛋白是一種小分子量的球狀的抗原呈遞蛋白,位于溶酶體腔內,它與NPC1 結合后將LDL 釋放的膽固醇運輸到受體區室,例如內質網、高爾基體和質膜[31]。
在GBM 中,重新編程膽固醇代謝譜是癌癥的一個新標志[32]。當細胞缺乏NPC1 時,膽固醇大量積聚在溶酶體腔內,導致溶酶體擴大,并表現出形態、運輸和功能缺陷,且伴隨著其他細胞區室的功能障礙,包括自噬體、線粒體和過氧化物酶體。有證據表明,NPC 缺失在引起的膽固醇積累的同時會導致自噬囊泡向溶酶體的運輸缺陷[33]。綜上所述,靶向NPC 調節膽固醇和自噬可能是治療GBM的新方法。
3.4 靶向膽固醇代謝調控因子
3.4.1 靶向SOAT1 SREBP-1調節的脂肪合成升高是GBM 的一個新特征,它是一種在脂質代謝中起核心作用的轉錄因子,SREBP激活受到內質網(ER)中膽固醇的負調控。SOAT1 是SREBP-1 活化的關鍵調控因子之一,可催化游離膽固醇與脂肪酸酯化為膽固醇酯,然后轉移到脂滴(LD)中作為儲存池用于膽固醇和脂肪酸。SOAT1 已被證明與多種腫瘤的預后相關,是潛在治療靶點,抑制SOAT1 可有效地阻斷SREBP-1,從而抑制GBM的生長[34-35]。
正常細胞中膽固醇維持在相對穩定的水平,內質網中膽固醇水平升高時,會觸發負反饋回路抑制其從頭合成。在GBM 細胞中會將多余的膽固醇轉化為膽固醇酯儲存在脂滴中,以防止膽固醇在內質網膜上的積累,避免對SREBP 和腫瘤生長的反饋抑制[36]。通過抑制SOAT1 酶活性使膽固醇在ER 中積累,可抑制SREBP-1 的轉錄活性。SOAT1 抑制劑已經在心血管病人的臨床試驗中進行了測試,因此可以迅速將其應用于癌癥病人的臨床試驗。抑制SOAT1 可能對含有大量脂滴的腫瘤特別有效,例如GBM。通過抑制SOAT1 來阻斷膽固醇酯化是一種通過抑制SREBP-1 靶向GBM 的有前景的治療策略[37]。
3.4.2 靶 向 膽 固 醇24- 羥 化 酶(CYP46A1)CYP46A1 是一種可以將膽固醇轉化為24-羥化膽固醇(24-OHC)進而將其排出中樞神經系統的腦組織特異性酶,對調節膽固醇的代謝非常關鍵。24-OHC不僅能夠促進膽固醇的外排,還能作為激活LXR 的核轉錄因子,從而促進其下游膽固醇基因如ApoE和ABAC1 的表達來進一步增加膽固醇的分泌。大數據的生信分析確定了CYP46A1 是參與GBM 中膽固醇穩態的調節基因,其下調最為明顯[38]。通過藥物激活或者過表達CYP46A1∕24-OHC能夠在體內外抑制GBM 細胞的生長,提示CYP46A1∕24-OHC 是導致膽固醇穩態失調的一個重要因素,靶向CYP46A1∕24-OHC可能是治療GBM治療的新靶點。
CYP46A1 的缺失部分導致膠質母細胞瘤細胞中過多的膽固醇積累,這有助于維持腫瘤細胞的活力和惡性狀態。依法韋侖(EFV)是一種可通過血腦屏障與酶的變構位點結合來激活CYP46A1 的抗HIV 藥物。有研究顯示,EFV 顯著抑制GBM 細胞生長并且誘導腫瘤細胞死亡。在分子水平上,EFV 刺激CYP46A1的活性,導致24-OHC水平升高,進一步減少膽固醇的積累[39]。外源性膽固醇處理或CYP46A1 敲低部分恢復了EFV 誘導的GBM 細胞生長抑制,表明EFV 抗癌作用至少部分是通過調節膽固醇水平介導的[38]。綜上所述,CYP46A1 的缺失會導致GBM 中膽固醇的積累和膽固醇穩態失調,這可能是一個GBM 中可行的治療靶點。CYP46A1 的激活劑通過增加膽固醇代謝物24-OHC 的產生,在體外和體內抑制腫瘤生長,從而擾亂GBM 中的膽固醇穩態。此外,EFV 恢復CYP46A1∕24-OHC 信號軸的活性可能是一種有前途的GBM治療策略。
4 靶向膽固醇穩態治療膠質瘤的研究進展
與未接觸過他汀類藥物的GBM 病人相比,他汀類藥物使用時間或強度的增加與GBM 病人預后之間存在著劑量關系,使用他汀類藥物相關的GBM 風險降低,表明他汀類藥物暴露可能會影響膠質瘤的發展。雖然研究證明了長期使用他汀類藥物對GBM 病人的生存率具有潛在的積極影響,但是為了更好地排除外在其他條件的影響,需要更詳細的臨床和分子數據進行更大規模的研究[40]。西羅莫司是一種有效的免疫抑制藥物,被批準用于預防實體器官同種異體移植排斥。有臨床研究在病人已有的化療方案中加入西羅莫司的Ⅰ期劑量遞增實驗,按照規定的周期進行一些指標的檢測,發現隨著西羅莫司用藥劑量的增加,可能會出現中性粒細胞減少、腹痛、口腔黏膜炎等一些不良反應,但總體來說該方案的耐受性較好。參與評估的15例病人中,有8 例病人評價為SD,但其中1 例GBM 病人由于反復腹痛在沒有得到額外治療后被評價為PD。西羅莫司對免疫途徑的抑制以及潛在的反應生物標志物,將在正在進行的Ⅱ期試驗中進一步評估[41]。
5 總結與展望
膽固醇代謝對腫瘤生物學過程,特別是對致癌信號通路、鐵死亡和腫瘤微環境的新興作用,還需要在各種腫瘤類型中進一步闡明。腫瘤中膽固醇代謝依賴性和選擇性的機制對于靶向代謝治療是必不可少的,它仍然是癌癥研究領域的主要挑戰之一。
膽固醇穩態由復雜的反饋回路調節,單一抑制一種膽固醇代謝途徑可能對腫瘤生長幾乎沒有影響。隨著膽固醇代謝抑制劑的發展,應進一步探索同時阻斷膽固醇合成、攝取、酯化和運輸癌癥的不同抑制劑的組合,并為下一代代謝療法提供理論基礎。

