環狀RNA同源性蛋白激酶3靶向微RNA-338促進膠質瘤細胞侵襲、遷移的實驗研究
劉瑩,連海偉,易偉,張淑娣,朱曉楠
作者單位:武漢大學人民醫院神經外科,湖北 武漢430060
膠質瘤是最常見的顱內原發性腫瘤,具有較高的病死率[1-2]。目前對于膠質瘤的治療方法主要包括手術切除、放療、化療和腫瘤電場治療(TTfields)等綜合治療方案,雖然取得了很大進展,但由于膠質瘤具有很強的轉移能力,病人生存率依然很低[3]。所以探究膠質瘤轉移的分子機制可能為膠質瘤的診斷和治療提供更多的方向。越來越多的研究表明,circRNA 在各種疾病尤其是癌癥的發展中發揮重要作用[4]。CircHIPK3 作為一種circRNA,已有研究報道,CircHIPK3 在神經膠質瘤組織和細胞中高表達,沉默CircHIPK3 抑制了膠質瘤細胞增殖和侵襲能力[5]。表明沉默CircHIPK3 可抑制膠質瘤的進展。但具體機制尚不完全清楚。本研究通過生物信息學分析發現CircHIPK3 與miR-338 存在結合位點。相關研究顯示,上調miR-338 可抑制膠質瘤細胞增殖[6]。但CircHIPK3 能否通過調控miR-338 影響膠質瘤細胞的惡性生物學行為尚不清楚。因此,2021 年2—12 月進行本研究,旨在通過體外研究深入探究CircHIPK3 對膠質瘤細胞U251 細胞遷移、侵襲的影響以及其作用的分子機制。
1 材料與方法
1.1 細胞與試劑膠質瘤細胞(U251)(上海復祥生物 公 司,貨 號CL-0014)。 胎 牛 血 清(貨 號10100147)、DMEM 培養基(貨號31331093)、0.25%胰蛋白酶(貨號12605036)等,購自美國Gibco 公司;兔抗人基質金屬蛋白酶(MMP)-2(貨號ab92536)、MMP-9(貨號ab228402)、GAPDH(貨號ab181602)及山羊抗兔IgG 二抗(貨號ab205718)購自英國Abcam公司。
1.2 方法
1.2.1 生物信息學分析 通過Circular RNA Interactome、RegRNA2.0、CircBank Database 網 站 預 測CircHIPK3(ID:hsa_circ_0000284)的靶向miRNA,然后將3個網站預測得到的靶向miRNA進行交集。
1.2.2 細胞培養 將U251 細胞株置于37 ℃水浴鍋中快速融化,移至EP管中,懸浮接種于培養瓶,培養過程均用含1%雙抗、10%胎牛血清的DMEM 培養液,于37 ℃、5%二氧化碳的條件下培養,每兩天更換一次培養液,傳代培養。
1.2.3 細胞轉染及分組 將對數生長期的U251 細胞分別轉染用羧基熒光素(綠色熒光)標記的sh-control、sh-CircHIPK3,并 命 名 為sh-control 組、sh-CircHIPK3 組,另取正常培養的U251 細胞作為空白(NG)組。轉染48 h后,利用熒光顯微鏡觀察細胞轉染效率。轉染效率=(綠色熒光細胞數∕總細胞數)×100%。
1.2.4 實時定量聚合酶鏈反應(quantitative realtime PCR,qRT-PCR)檢測CircHIPK3、miR-338 表達水平變化 Trizol 試劑提取U251 細胞中總RNA,使用Nanodrop? 2000 分光光度計測量RNA 的濃度和純度。用RNA 逆轉錄試劑盒將RNA 逆轉錄為cDNA后,以cDNA為模板進行qRT-PCR反應。擴增條件如下:95 ℃,10 min;95 ℃,10 s;60 ℃,60 s;40個循環。GAPDH、U6 分別作為CircHIPK3、miR-338的內參,通過2-ΔΔCt法計算CircHIPK3、miR-338 的表達。引物序列見表1。

表1 CircHIPK3、miR-338、GAPDH、U6 qRT-PCR引物序列
1.2.5 Transwell法檢測各組U251細胞侵襲、遷移能力 細胞侵襲的測定,按方法“1.2.2”進行分組,將各組細胞以2×105個∕孔懸浮于預涂有Matrigel 的Transwell 上室中。再將含有10%胎牛血清的500 μL DMEM培養基加入到下室中。孵育48 h后,用棉簽除去上室下表面未侵襲的細胞,將侵襲的細胞用甲醇固定30 min,0.1%結晶紫染色20 min。利用倒置顯微鏡觀察侵襲細胞數。
細胞遷移的測定,按方法“1.2.2”進行分組,將各組細胞以2×105個∕孔懸浮于Transwell上室中。再將含有10%胎牛血清的500 μL DMEM 培養基加入到下室中。孵育48 h 后,用棉簽除去上室下表面未遷移的細胞,將遷移的細胞用甲醇固定30 min,0.1%結晶紫染色20 min。利用倒置顯微鏡觀察遷移細胞數。
1.2.6 劃痕愈合實驗檢測各組U251 細胞遷移能力 將1×106個細胞接種到6孔板中,當其匯合度達到90%時,使用10 μL 無菌移液管尖端刮擦細胞層表面以產生劃痕。孵育24 h 后,利用倒置顯微鏡觀察劃痕寬度。用W0、W24分別表示0 h、24 h的劃痕寬度。劃痕愈合率(%)=(1-W24∕W0)×100%。
1.2.7 流式細胞術檢測細胞周期 收集各組細胞,用PBS 洗滌1 次后用PBS 制成細胞懸液,再加入體積分數為70%的乙醇,在4 ℃下避光過夜孵育。次日,經1 000 r∕min 離心5 min 并收集細胞沉淀,用PBS重懸細胞,再加入PI染液,室溫避光孵育15 min后,利用流式細胞儀檢測細胞周期。
1.2.8 雙螢光素酶報告基因
1.2.8.1 突變型載體的制備 TargetScan 數據庫顯示人CircHIPK3 基因3"UTR 區域含有miR-338 結合位點。對CircHIPK3 3"-UTR 區域進行擴增、酶切連至pGL4 螢光素酶報告載體,構建p-GL4-HIPK3-WT質粒,以此質粒為模板進行定點突變,測序確認突變成功,構建p-GL4-HIPK3-MUT質粒。
1.2.8.2 螢光素酶報告基因實驗 U251 細胞鋪48孔板,24 h 后,將miR-338 NC 和miR-338 mimics 分別與p-GL4-HIPK3-WT 和p-GL4-HIPK3-MUT 共轉染,24 h后,觀察螢光素酶相對活性變化。
1.2.9 蛋白質印跡法檢測 RIPA 裂解液提取各組細胞總蛋白,使用BCA 蛋白測定試劑盒對總蛋白進行定量。10% SDS-PAGE 分離30 μg蛋白質,然后將分離的蛋白質轉移到PVDF 膜上。將膜在室溫下用5%脫脂牛奶封閉1 h,再向膜中加入一抗MMP-2(1∶1 000)、MMP-9(1∶500)、GAPDH(1∶500)在4 ℃中孵育過夜,用TBST 洗滌后添加兔二抗(1∶5 000)常溫下孵育2 h。采用蛋白成像凝膠儀對MMP-2、MMP-9蛋白水平進行半定量分析。實驗重復3次。
1.3 統計學方法采用SPSS 19.0(SPSS Inc.Chicago,IL,USA,2011)進行統計學分析。計量數據用±s的形式表示,多組間比較采用方差分析,組間兩兩比較采SNK-q檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 CircHIPK3 靶向miRNA 的預測通過Circular RNA Interactome、RegRNA2.0、CircBank Database網站預測CircHIPK3(ID:hsa_circ_0000284)的靶向miRNA,然后將3 個網站預測得到的靶向miRNA 進行交集,發現3 個網站同時預測到的miRNA 中有感興趣的miR-338,因此選用miR-338進行后續研究。
2.2 細胞轉染效率的檢測NG 組、sh-control 組、sh-CircHIPK3 組細胞轉染效率分別為0%、(86.52±6.42)%、(89.73±7.21)%,見圖1。

圖1 熒光顯微鏡檢測各組U251細胞轉染效率(電轉染×200) 圖3 Transwell檢測各組U251細胞遷移能力(結晶紫染色×200) 圖4 倒置顯微鏡觀察各組U251細胞侵襲能力(結晶紫染色×200)
2.3 qRT-PCR 檢測CircHIPK3、miR-338 表達水平與NG 組相比,sh-control 組CircHIPK3、miR-338表達水平差異無統計學意義(P>0.05);與NG 組、shcontrol組相比,sh-CircHIPK3組CircHIPK3表達水平顯著下降(P<0.05),miR-338 表達水平顯著升高(P<0.05)。見表2。
表2 qRT-PCR檢測CircHIPK3、miR-338表達水平∕ ± s

表2 qRT-PCR檢測CircHIPK3、miR-338表達水平∕ ± s
注:NG 組為空白組,Sh-control 為轉染對照組,Sh-CircHIPK3 為環狀RNA 同源域相互作用蛋白激酶3 轉染組,CircHIPK3 為環狀RNA同源域相互作用蛋白激酶3,miR-338為微核糖核酸-338。①與NG組比較,P<0.05。②與sh-control組比較,P<0.001。
miR-338 1.00±0.00 1.12±0.19 1.89±0.28①②46.42<0.001組別NG組sh-control組sh-CircHIPK3組F值P值重復次數6 6 6 CircHIPK3 1.00±0.00 1.06±0.26 0.56±0.06①19.47<0.001
2.4 敲減CircHIPK3 對U251 細胞遷移、侵襲能力的影響與NG 組相比,sh-control 組U251 細胞劃痕愈合率、遷移細胞數沒有顯著變化;與NG 組、sh-control 組比較,CircHIPK3 敲減組U251 細胞劃痕愈合率、遷移細胞數顯著降低(P<0.05),見表3;圖2,3。

圖2 劃痕實驗檢測敲減CircHIPK3對U251細胞遷移能力的影響(結晶紫染色×200)
表3 敲減CircHIPK3對U251細胞遷移、侵襲能力的影響∕ ± s

表3 敲減CircHIPK3對U251細胞遷移、侵襲能力的影響∕ ± s
注:NG 組為空白組,Sh-control 為轉染對照組,Sh-CircHIPK3 為環狀RNA同源域相互作用蛋白激酶3轉染組。①與NG組比較,P<0.001。②與sh-conqrol組比較,P<0.001。
重復次數6 6 6劃痕愈合率∕%25.66±2.37 26.38±2.53 10.36±1.53①②組別NG sh-control sh-CircHIPK3遷移細胞數∕個196.72±18.75 194.65±17.86 95.58±8.66①②侵襲細胞數∕個164.89±12.55 165.77±12.16 80.13±11.37①②104.42<0.001 F值P值88.61<0.001 101.74<0.001
與NG 組相比,sh-control 組U251 細胞侵襲細胞數沒有顯著變化;與NG 組、sh-control 組比較,CircHIPK3 敲減組U251 細胞侵襲數明顯減少(P<0.05),見表3,圖4。
2.5 敲減CircHIPK3對U251細胞MMP-2、MMP-9蛋白表達的影響與NG 組、sh-control 組相比,sh-CircHIPK3 組MMP-2、MMP-9 蛋白表達顯著降低(P<0.05),見表4,圖5。
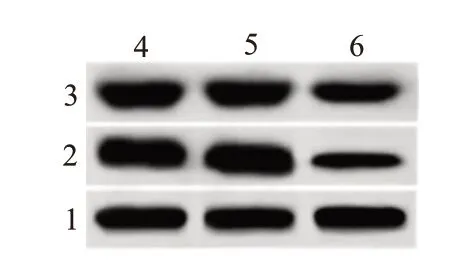
圖5 敲減CircHIPK3對MMP-2、MMP-9蛋白表達的影響
表4 敲減CircHIPK3對MMP-2、MMP-9蛋白表達的影響∕ ± s
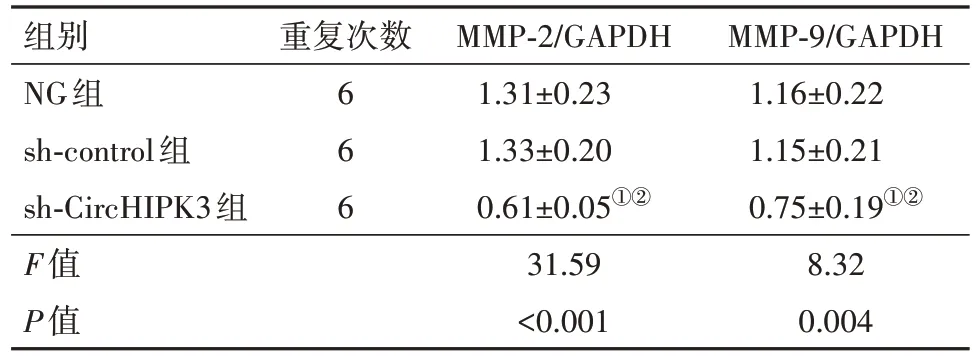
表4 敲減CircHIPK3對MMP-2、MMP-9蛋白表達的影響∕ ± s
注:NG組為空白組,Sh-control為轉染對照組,Sh-CircHIPK3為環狀RNA 同源域相互作用蛋白激酶3轉染組,MMP-9為基質金屬蛋白酶-9 ,MMP-2為基質金屬蛋白酶-2,GAPDH為甘油醛-3-磷酸脫氫酶。①與NG組比較,P<0.05。②與sh-control組比較,P<0.05。
MMP-9∕GAPDH 1.16±0.22 1.15±0.21 0.75±0.19①②8.32 0.004組別NG組sh-control組sh-CircHIPK3組F值P值重復次數6 6 6 MMP-2∕GAPDH 1.31±0.23 1.33±0.20 0.61±0.05①②31.59<0.001
2.6 敲減CircHIPK3對U251細胞周期的影響與NG 組、sh-control 組相比,sh-CircHIPK3 組中G1期細胞比例升高,S 期細胞比例降低(P<0.05),而G2期細胞比例變化差異無統計學意義,見表5。
表5 敲減CircHIPK3對U251細胞周期的影響(n=6)∕(%, ± s)

表5 敲減CircHIPK3對U251細胞周期的影響(n=6)∕(%, ± s)
注:NG 組為空白組,Sh-control 為轉染對照組,Sh-CircHIPK3 為環狀RNA同源域相互作用蛋白激酶3轉染組。①與NG組比較,P<0.001。②與sh-control組比較,P<0.001。
S期細胞比例26.45±0.39 26.57±0.41 20.72±0.18①②567.82<0.001組別NG組sh-control組sh-CircHIPK3組F值P值重復次數6 6 6 G1期細胞比例58.72±0.36 58.45±0.27 64.72±0.47①②588.06<0.001 G2期細胞比例14.83±0.15 14.98±0.14 14.56±0.16 10.26 0.002
2.7 CircHIPK3 靶向調控基因的關系驗證TargetScan數據庫預測結果顯示,mir-338 在CircHIPK3 3"UTR 有相應的結合位點;螢光素酶報告實驗結果顯示,與p-GL4-HIPK3-WT+miR-338 NC 組相比,p-GL4-HIPK3-WT+miR-338 mimics 組U251 膠質瘤細胞熒光素酶活性顯著降低(P<0.05),p-GL4-HIPK3-MUT+miR-338 NC 組與p-GL4-HIPK3-MUT+miR-338 mimics 組相比差異無統計學意義(P>0.05),見表6。
表6 熒光素酶報告實驗檢測mir-338與Circ HIPK3的靶向作用關系∕ ± s

表6 熒光素酶報告實驗檢測mir-338與Circ HIPK3的靶向作用關系∕ ± s
注:①與miR-338 NC+WT組相比,P<0.05。
組別MiR-338 NC+WT組MiR-338 mimics+WT組MiR-338 NC+MUT組MiR-338 mimics +MUT組F值P值相對熒光素酶活性1.00±0.24 0.51±0.11①1.01±0.23 0.97±0.22 32.36<0.001重復次數6 6 6 6
3 討論
膠質瘤是最常見的侵襲性原發性腦腫瘤,由于其很強的侵襲性,導致預后較差[7-8]。CircHIPK3 是一種長度為1 099 bp的環狀RNA,對多種癌癥(包括肺癌,結腸直腸癌和神經膠質瘤)的進展具有顯著的促進作用[9-11]。CircHIPK3 能夠通過結合許多腫瘤的miRNA 來增強細胞生長和轉移[12-13]。例如,在肝癌細胞中CircHIPK3可以吸附miR-124,從而調節miR-124 的靶基因PDK2 促進肝癌細胞的細胞增殖和侵襲[14];在非小細胞肺癌中,CircHIPK3 可以吸附miR-149 促進FOXM1 的表達,從而影響細胞增殖和凋亡[15]。盡管已有研究證明在神經膠質瘤組織中CircHIPK3 表達的增加可以作為預后生物標志物,但是CircHIPK3 在神經膠質瘤中的具體機制尚不完全清楚。本研究發現,與NG 組、sh-control 組相比,CircHIPK3 敲減組膠質瘤U251 細胞劃痕愈合率、遷移、侵襲細胞數明顯減少,G1期細胞比例升高,S 期細胞比例降低。說明沉默CircHIPK3 可能通過抑制膠質瘤U251 細胞侵襲、遷移能力與細胞周期,進而抑制膠質瘤的進展。
大量研究顯示,環狀RNA 可以與miRNA 相互作用來調節下游基因,進而促進許多癌癥的發展。miRNA 是一類小分子單鏈RNA,廣泛存在于真核生物中。已有研究證明,miRNA 可以直接參與腫瘤的發生發展[16]。有研究報道,過表達miR-338-3p 通過下調KIF2A 抑制非小細胞肺癌細胞增殖、侵襲[17-18]。miR-338 通過下調ZEB2 抑制肝癌細胞的侵襲與遷移[19-20]。本研究發現,miR-338 是CircHIPK3 潛在靶基因。當沉默CircHIPK3 時,qPCR 結果顯示CircHIPK3 表達水平顯著下調,而miR-338 表達水平顯著升高。猜測CircHIPK3 可能通過調控miR-338 的表達進而在膠質瘤的發生發展中起到重要的作用。本研究通過雙螢光素酶報告實驗證實了CircHIPK3可靶向調控miR-338基因。此外,CircHIPK3敲減可顯著抑制膠質瘤U251 細胞中MMP-2、MMP-9 蛋白表達,表明在膠質瘤U251 細胞中,CircHIPK3 敲減可顯著促進miR-338 基因表達,并可能通過抑制MMP-2、MMP-9蛋白表達來細胞侵襲、遷移。
綜上所述,CircHIPK3 在膠質瘤U251 細胞中高表達,其可能通過靶向miR-338 表達促進膠質瘤U251細胞的遷移、侵襲,并影響細胞周期,CircHIPK3可能成為治療膠質瘤的潛在靶標。然而,本研究尚存在不足之處,關于膠質瘤中CircHIPK3 靶向miR-338具體調控過程,需深入研究并進行驗證。
(本文圖1,3,4見插圖1-3)

