刺激響應型光聲納米探針的構建及其生物醫(yī)學應用研究
袁 茜,李一榮
(武漢大學 中南醫(yī)院檢驗科,湖北 武漢 430071)
1949 年,萊納斯·鮑林于《科學》雜志上發(fā)表論文《鐮狀細胞性貧血,一種分子疾病》[1],首次從分子水平上解釋了鐮狀細胞性貧血的成因,揭示了疾病的發(fā)生與發(fā)展在分子層面的重要意義,并開啟了分子生物學在生命科學研究中的序幕。隨著研究進程的深入,美國國立衛(wèi)生研究院(NIH)腫瘤研究所卡普和布羅德兩位學者于1994 年在《癌研究》雜志發(fā)表題為《分子醫(yī)學的新方向》的論述[2],正式提出了分子醫(yī)學的概念。過去的七十多年中,分子醫(yī)學對生命醫(yī)學的發(fā)展起到了巨大推動作用。分子醫(yī)學旨在通過從分子層面對重大疾病進行識別、量化以及動態(tài)定位,以了解疾病發(fā)病機制,并制定合理的診斷策略以及干預手段。在惡性疾病的治療中,實現病灶的及時識別與精準評估對于改善患者的發(fā)病率以及死亡率至關重要[3]。因此以解決重大疾病的早期診斷需求為導向,為重要生物分子的傳感及成像提供有效的功能分子探針,是分子醫(yī)學研究領域的關鍵所在。
目前,已經有一系列非侵入型分子傳感及成像技術被應用于重大疾病的早期診斷[4],包括光學成像、磁成像、超聲成像等。在眾多的成像手段中,光學成像技術特異性好、分析靈敏度佳、時空分辨率高,能夠在分子、細胞、組織乃至器官水平,對分子事件進行實時、動態(tài)的可視化成像,在分子醫(yī)學研究領域受到了廣泛的關注[5]。近年來,熒光、表面增強拉曼散射、光聲等光學技術的發(fā)展極大促進了光學成像技術的應用。其中,光聲成像技術是一種新興的非侵入性光學成像技術,具有重要的臨床轉化潛力[6]。光聲成像依賴于光聲效應[7-8],即當脈沖激光照射至生物組織時,光聲探針吸收光能引起組織結構瞬間熱彈性膨脹,從而產生超聲信號。這種信號經高靈敏的超聲探測器接收,并通過算法重構形成光聲圖像(圖1)。因此光聲成像探針兼具光學探針以及聲學探針的優(yōu)勢[9],即高的成像對比度以及深的組織穿透性。通過調控激光波長,光聲成像技術能夠利用多種生色團在體內的映射實現在體的有效監(jiān)測[10]。例如,通過對一系列內源性成分進行監(jiān)測,如血紅蛋白、肌紅蛋白、黑色素等,光聲成像手段能夠有效獲得在體血氧等身體指標信息。然而內源性光聲探針數量有限,極大程度上限制了光聲成像技術的發(fā)展[11]。基于此,具有良好生物相容性以及優(yōu)秀光聲轉化性能的小分子有機染料,如吲哚菁綠(ICG)、亞甲基藍、吡咯硼(BODIPY)系列染料,受到了研究者們廣泛的關注,并在重大疾病的早期診斷中展現出良好的應用潛力[12]。然而,小分子有機染料在活體應用中存在腎臟清除率高、生物利用率低、易光漂白等局限性[13-14],限制了其進一步的應用。
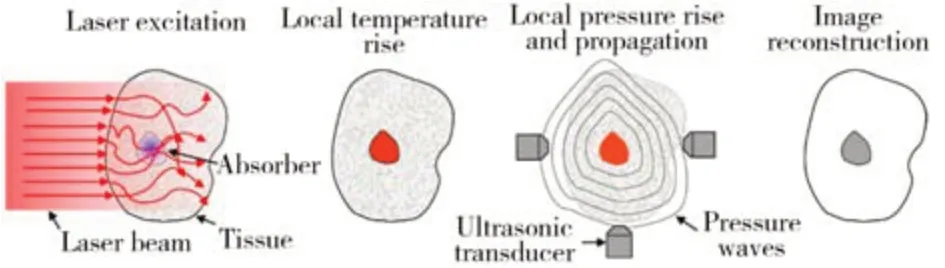
圖1 光聲成像原理圖[7]Fig.1 Schematic of the principle of photoacoustic imaging[7]
得益于納米生物技術的快速發(fā)展,基于納米功能材料所設計的光學納米探針為解決這些問題帶來了契機。與傳統基于染料的光學探針相比,納米探針本身固有的光學性質以及可設計的物化性質為改善光學探針的靈敏度、特異性、靶向性提供了可能。然而傳統納米光聲探針的信號輸出主要為“信號常亮”模式。這種絕對強度依賴型的信號采集方式可能受到非特異性作用影響[15-17],例如病理組織與正常組織的組織滲透性與滯留性的差異;納米探針在活體中潛在的脫靶效應等,從而降低探針的特異性以及信背比。考慮正常組織與病理組織微環(huán)境的差異性,通過合理設計開發(fā)刺激響應型光聲納米探針能夠有效改善探針的特異性,提升探針的信背比,有助于更好地理解及診斷癌癥、神經退行性疾病、心血管疾病、炎性疾病等重要疾病。本文闡述了激活型光聲納米探針在分子診斷中的研究進展,討論了激活型納米光聲探針在生物醫(yī)學領域的挑戰(zhàn)與前景。
1 刺激響應型光聲成像探針設計策略
與傳統“信號常亮”型光聲探針相比,激活型光聲成像探針可通過響應刺激實現光聲信號特異性轉變[15],設計策略包括“單因素激活”與“雙因素激活”兩種構建方式。
1.1 單因素刺激響應型設計策略
在“單因素激活”的探針策略中,通常一種光聲信號代表一類待測事件,相關信號輸出有“打開型”與“關閉型”兩種方式。在“打開型”探針中,探針一般處于猝滅態(tài)或僅具有微弱信號,通過響應刺激從而實現信號“打開”。在“關閉型”探針中,成像模式則相反。相比之下,“打開型”光聲探針能夠有效降低假陽性信號的干擾。Miao 課題組開發(fā)了Caspase-3 活化的組裝型光聲成像探針dCyFF(圖2A)[18],用于監(jiān)測放射療法的療效。dCyFF 探針以半花菁染料為核心,并連接有Caspase-3 可裂解的肽底物以及促進自組裝的肽段。在Caspase-3存在的情況下,該探針發(fā)生水解并實現自組裝成更大的納米顆粒,從而激活光聲信號,實現放療反應的及時評估。然而,這一類“單因素激活,單信號輸出”光聲探針的傳感能力高度依賴于單信號光聲探針的采集性能,探針堆積不均、成像靈敏度低、光漂白等潛在問題均會影響此類光聲探針的成像效果。相比之下,“單因素激活,雙信號輸出”型光聲探針可通過信號內置校準功能,有效改善單信號輸出方式存在的上述問題,進一步提升探針準確度。Song 課題組利用納米金等離子體共振效應,通過精準調控納米金表面聚合物比例,同時引入半導體光聲參比探針SD-825,構建了不對稱構型的有機-無機納米組裝體(圖2B)[19]。隨著環(huán)境pH 值變化,該不對稱組裝探針中金納米模塊的光聲信號發(fā)生相應變化,結合參比探針SD-825 信號,從而實現pH 值激活式精準的比例型光聲定量監(jiān)測,顯著降低了外界因素對成像結果的影響。

圖2 Caspase-3介導dCyFF納米探針激活用于增強型成像[18](A);pH響應型不對稱構型納米組裝體的比率型光聲探針[19](B);pH與還原態(tài)雙刺激響應型診療探針的作用機制[20](C);GSH/H2O2雙響應型BSA-Cy-Mito納米探針用于炎性的光聲成像[21](D)Fig.2 Caspase-3-activatable dCyFF nanoprobe for enhanced imaging[18](A);pH-responsive Janus nanocomposite as ratiometric PA probe[19](B);responsive mechanism of pH/reduction dual stimuli-responsive theranostic probes[20](C);GSH/H2O2-responsive BSA-Cy-Mito nanoprobe for PA inflammation imaging[21](D)
1.2 雙因素刺激響應型設計策略
為進一步改善光聲探針在復雜環(huán)境中的特異性,研究者們開發(fā)了一系列雙因素刺激響應型光聲探針。雙因素刺激響應型探針主要包括“雙因素激活,單信號輸出型”與“雙因素激活,雙信號輸出型”兩種探針類型。由于一種異常病理分子可能同時存在于不同病理事件中,因此開發(fā)“雙因素激活,單信號輸出型”光聲探針可有效提升疾病診斷的特異性。Shi 課題組開發(fā)了能夠同時響應腫瘤微環(huán)境低pH 以及谷胱甘肽的光聲探針Cy-1(圖2C)[20],通過發(fā)生分子間的CBT-Cys 縮合反應實現探針的組裝聚集,從而顯著提升探針光聲成像的性能。此外,具有兩個檢測窗口的“雙因素激活,雙信號輸出型”探針能夠實現多重目標的邏輯化檢測,進一步拓展了光聲成像的通用性。Tang 課題組通過引入牛血清白蛋白用于組裝谷胱甘肽響應型熒光探針Cy3-NO2以及過氧化氫響應的熒光探針Mito-NIRHP,開發(fā)了組裝型探針BSA-Cy-Mito(圖2D)[21],從而實現了谷胱甘肽以及過氧化氫的同時響應與雙光聲信號輸出,為構建多生物標志物檢測光聲探針的設計提供了參考。
2 刺激響應型光聲成像探針應用
近年來,刺激響應型光聲成像探針已被廣泛應用于重要疾病的成像與診療中,主要應用可分為內源性刺激響應成像與外源性刺激響應成像兩種類型。
2.1 內源性刺激響應成像
每種疾病都具有自身獨特的病理特征,例如異常的pH值、自由基含量、酶水平,用以支持疾病的發(fā)生與發(fā)展。基于此,研究者們以這些異常的生理參數作為內源性刺激源,開發(fā)了一系列分子探針以實現激活型光聲成像,為疾病的早期診斷與干預提供更為有效的監(jiān)測手段。
2.1.1 pH 響應型成像pH 值是衡量細胞穩(wěn)態(tài)的重要生理參數。異常的pH 值與癌癥、炎癥性疾病等息息相關[22-24]。例如為了支持腫瘤的快速生長與增殖,與正常細胞相比,腫瘤細胞能量代謝方式發(fā)生改變,導致代謝物(如乳酸等)的胞外積累,胞外間質pH值降低。基于這種獨特的病理環(huán)境,研究者們設計了一系列pH響應型探針用于激活型光聲成像。溶酶體是一種由單層膜包被的,含有多種酸性水解酶的囊狀異質性細胞器。與正常細胞相比,腫瘤細胞的溶酶體具有數量偏多、體積偏大、組織蛋白酶活性偏高等特點。Song 課題組[25-26]基于腫瘤酸性微環(huán)境的特點(pH 值在6.5~6.9 區(qū)間)及腫瘤細胞溶酶體過度發(fā)育的特征(pH 值在4.6 左右),以牛血清白蛋白(BSA)為模板開發(fā)了粒徑在6 nm 左右的Cu2-xSe-BSA 納米探針(圖3)。該探針隨著環(huán)境pH 值降低會逐步發(fā)生聚集。在到達腫瘤區(qū)域后,Cu2-xSe-BSA 納米探針在腫瘤酸性微環(huán)境中會進行自組裝,并進一步地在腫瘤細胞溶酶體中組裝形成超團簇,實現pH值響應的增強型光聲成像及協同治療療效。

圖3 Cu2-xSe-BSA納米探針用于增強型多模態(tài)成像及協同治療[25]Fig.3 Cu2-xSe-BSA nanoprobe for enhanced multimodal imaging guided synergistic therapy[25]
2.1.2 酶響應型成像酶作為維持機體功能的重要組成成分,在多種重要生命活動中發(fā)揮著重要的作用,例如增殖、遷移、分化、血管生成、衰老、凋亡等[11,27-28]。類似于其他重要生物標志物,酶水平的異常表達與眾多疾病的進程息息相關。弗林蛋白酶是一種反式高爾基蛋白轉化酶,在多種惡性腫瘤中均呈上調狀態(tài),是腫瘤診療的重要生物標志物。Wang 課題組[29]基于縮合反應,開發(fā)了弗林蛋白酶介導的聚合響應型金納米顆粒光聲診療探針。當內化入癌細胞后,探針在胞內弗林蛋白酶以及還原型谷胱甘肽的識別及響應作用下,通過剪切掉保護基團并裸露出縮合反應基團,從而誘導金納米顆粒胞內聚集,實現增強型光聲成像以及治療效果。動脈粥樣硬化起病具有隱蔽性與突發(fā)性的特點。患者發(fā)病前沒有明顯癥狀及征兆,往往難以實現及時治療。因此,實現對于動脈粥樣硬化斑塊的早期診斷與及時預防極其重要。一系列研究表明,組織蛋白酶B 參與了血管病變的發(fā)生、進展、破裂的全過程。異常升高的組織蛋白酶B 會擾亂易損斑塊完整性,引發(fā)斑塊破裂,是預測斑塊易損性的潛在性指標物。基于此,Zhang 課題組[30]將親脂烷基鏈和親水組織蛋白酶B 底物偶聯至半花菁支架上,開發(fā)了雙響應型組織蛋白酶B 探針L-CRP 用于監(jiān)測親脂環(huán)境中組織蛋白酶B 的活性。該探針使用脂質與組織蛋白酶B 作為“激活因素”,只有當兩種“激活因素”同時存在時,才能激活光聲信號,從而實現動脈粥樣硬化斑塊組織蛋白酶B 的特異性識別(圖4)。

圖4 雙鎖型L-CRP探針用于監(jiān)測親脂環(huán)境中的組織蛋白酶B[30]Fig.4 Double-locked L-CRP nanoprobe for the imaging of intraplaque CTB levels[30]
2.1.3 自由基響應型成像自由基作為生命體關鍵的信號分子之一,在維持細胞代謝穩(wěn)態(tài)、調控細胞生理功能等方面發(fā)揮了重要作用[31]。正常情況下,生命體的自由基水平受到嚴格調控以滿足機體正常需求。一旦機體內自由基代謝失衡,機體將發(fā)生氧化損傷,進而誘發(fā)一系列級聯病理反應。當前已有大量證據證實癌癥、心血管疾病、神經退行性疾病等重大疾病的發(fā)生發(fā)展與自由基代謝失衡相關[32-34]。然而自由基在體含量低、壽命短,如何開發(fā)光聲成像策略用于監(jiān)測在體自由基水平變化是當前亟待解決的問題。急性肝衰竭起病及進展迅速,實現急性肝衰竭的早期診斷對于患者有效治療極具意義。活性氧作為急性肝衰竭重要的早期病理標志物,其過度積累會觸發(fā)肝細胞損傷乃至壞死,導致氨酸轉氨酶(ALT)釋放至血液中,并刺激肝巨噬細胞產生一系列促炎因子,加重肝損傷進程。為實現急性肝衰竭的早期診斷,Li課題組[35]克服自由基成分壽命短、原位成像困難的問題,開發(fā)了活性氧響應的增強型光聲納米探針(RSPN)用于急性肝衰竭的早期診療。RSPN 探針以活性氧敏感的兩親性二硒化物作為偶聯單元,整合近紅外光聲造影劑酞菁鋅與能夠催化分解活性氧并生成氧氣氣泡的鈰納米催化劑兩大功能單元,形成兩親性功能結構。在血液循環(huán)過程中,被包覆在疏水核中的酞菁鋅與鈰納米催化劑處于“關閉狀態(tài)”。當暴露在富含活性氧的受損肝臟微環(huán)境中時,RSPN 探針中的二硒鍵經活性氧切割,導致探針構型轉變,從而釋放酞菁鋅與鈰納米催化劑。由于分子間的疏水作用與芳香族π-π堆疊作用,釋放的酞菁鋅重新聚集為大顆粒并通過非輻射熱失活途徑生成光聲信號。此外釋放的鈰納米催化劑通過催化自由基生成氧氣氣泡,并利用慣性空化效應進一步放大光聲成像信號,從而實現急性肝衰竭的早期高效診斷。此外,針對自由基代謝失衡的細菌感染性疾病,Song 課題組[36]制備了銀殼包覆鈀尖端金納米探針(Au-Pd@Ag)用于原位監(jiān)測細菌感染誘發(fā)炎癥模型中的標志物H2O2。在炎癥部位,H2O2通過刻蝕銀殼結構釋放Ag+,從而導致納米銀層光聲信號(近紅外一區(qū),700 nm)降低,而裸露出的鈀尖端金納米棒相應的光聲信號(近紅外二區(qū),1 260 nm)增強。通過監(jiān)測比例型光聲信號的變化,該光聲探針能夠更好地反映炎癥過程中H2O2的含量。
2.1.4 miRNAs 響應型成像MicroRNAs(miRNAs)是一類內源性非編碼單鏈短分子RNA(18~22 nt)。在一系列生理過程中,miRNAs均起著至關重要的調節(jié)作用。盡管細胞內miRNAs豐度較低,其異常表達水平仍與眾多疾病緊密相關[37-38],實現胞內miRNAs的動態(tài)成像可為監(jiān)測生命病理行為提供重要參考信息。急性腎損傷是一種腎臟功能迅速衰竭和喪失的疾病,是臨床住院患者常見并發(fā)癥之一,具有高的發(fā)病率與死亡率,已成為全球性重大公共衛(wèi)生問題。對急性腎損傷患者的及時診斷可為病患提供關鍵的治療時間窗口,避免病情發(fā)展至慢性腎病或終末端腎病。然而當前臨床診斷方法主要依賴于血清學生化檢測,這些方法并不能有效地實現急性腎損傷的早期診斷。鑒于此,He 課題組[39]開發(fā)了miR-21 響應的納米天線用于實現急性腎損傷的早期診斷與治療。該納米天線由矩形DNA 納米折紙連接兩個金納米棒(rDONs@AuNR 二聚體)組成,其表面等離子體共振峰位于近紅外窗口內,使得探針能夠實現深層組織的光聲成像(圖5)。在血液循環(huán)過程中,rDONs@AuNR 二聚體光聲信號一直處于“打開狀態(tài)”。基于miR-21在急性腎損傷小鼠腎部高表達的現象,在損傷腎組織中通過miR-21 引發(fā)納米天線粘性末端介導的鏈置換反應,使金納米棒與DNA 納米折紙解離,二聚體結構遭到破壞,進而導致光聲信號下調。研究結果表明,在注射10 min 后,該探針即可實現缺血再灌注誘導急性腎損傷小鼠的及時診療,這種策略的開發(fā)為急性腎損傷的早期診斷提供了新途徑。

圖5 rDONs@AuNR納米天線用于急性腎損傷的早期診斷與治療[39]Fig.5 rDONs@AuNR nanoantenna for early diagnosis and smart treatment of acute kidney injury[39]
2.1.5 其他因子響應型成像內源性氣體是生命機體信號轉導的必要信號分子。其中硫化氫分子作為強還原性氣體分子,在維持生命體氧化還原穩(wěn)態(tài)上發(fā)揮了重要作用。在異常分子事件中動態(tài)監(jiān)測硫化氫分子含量變化有助于更好地理解病理進程,為疾病的及時干預提供重要手段。Ye課題組[40]構建了能夠快速、可逆響應硫化氫以及羥基自由基的比率型光聲探針(1-PAIN)。可逆型1-PAIN 探針在PA690/PA825 處展現較低的比值,在羥基自由基的氧化作用下PA690/PA825 比值強度增加了近5 倍,而在硫化氫的還原作用下PA690/PA825 比值強度降低至較低水平,因此該探針能夠動態(tài)監(jiān)測生理環(huán)境下硫化氫以及羥基自由基的含量變化。在脂多糖誘導的小鼠肝炎模型中,1-PAIN被證明能夠動態(tài)成像炎癥部位的羥基自由基水平。此外在使用N-乙酰半胱氨酸給予小鼠進行抗炎治療過程中,1-PAIN能夠可視化硫化氫分子生成的過程。生物硫醇,例如同型半胱氨酸、谷胱甘肽、半胱氨酸等,在維持生命機體活動中發(fā)揮著重要作用。谷胱甘肽作為細胞內含量眾多的小分子硫醇類抗氧化劑,在腫瘤組織中的含量遠高于正常細胞。基于此,Zhao 課題組[41]開發(fā)了腫瘤微環(huán)境誘導吸收光譜紅移型鐵、銅共摻雜聚苯胺納米探針(Fe-Cu@PANI)。在腫瘤微環(huán)境中,Fe-Cu@PANI二價銅離子與谷胱甘肽發(fā)生氧化還原反應,誘導探針表面刻蝕,隨著谷胱甘肽濃度增高,探針粒徑逐漸減小,并產生質子化聚苯胺,誘導Fe-Cu@PANI 吸收光譜從可見光區(qū)域紅移至近紅外光區(qū)域,從而激活探針光聲成像,實現腫瘤微環(huán)境激活的原位動態(tài)光聲成像。
2.2 外源性刺激響應成像
外源性刺激主要包括光、熱、超聲等刺激形式。以外源能量作為刺激源的成像模式具有刺激源強度與靶點精準可控的優(yōu)勢,因此受到研究者們的廣泛關注。
2.2.1 光響應型成像光學刺激源具有清潔、可控的優(yōu)勢,通過調控照射光的波長、功率以及曝光時間,能夠實現光響應型探針的實時、精準成像[42]。與可見光相比,近紅外光具有更深的組織穿透性,在生物醫(yī)學應用領域具有天然的優(yōu)勢。Zhang課題組[43]構建了負載二酮吡咯聚合物以及吲哚菁綠的上轉換納米顆粒用于實現近紅外光響應生物正交的安全型光聲成像(圖6)。在激發(fā)光源為980 nm 的連續(xù)光激發(fā)下,上轉換顆粒能夠發(fā)射出較強的800 nm 近紅外光以激活吲哚菁綠從而實現有效的光學動力學治療。通過精準調節(jié)激發(fā)光的脈沖寬度,在980 nm的短脈沖激光下,上轉換顆粒在800 nm 處的近紅外發(fā)射光幾乎消失,產生的可見發(fā)射光被二酮吡咯聚合物捕獲,因此上轉換顆粒可在不產生明顯光毒性的情況下展現出強烈的光聲信號,實現在體腫瘤的長期性實時成像。

圖6 紅外光切換型上轉換納米復合物用于光聲成像與正交激活型治療[43]Fig.6 Orthogonal regulation of UCNPs-DI for photoacoustic imaging-guided on-demand treatment[43]
2.2.2 溫度響應型成像溫度響應型納米探針的發(fā)展進一步拓寬了分子影像的應用,然而現有的溫敏型納米探針所需轉變溫度普遍偏高,并且可逆性較低,極大程度限制了溫敏型探針在體實現長期有效的檢測。基于此,Xing 課題組[44]開發(fā)了一種熱響應型聚乙二醇包覆的鎢摻雜二氧化釩納米探針(圖7)。該探針在超過臨界溫度(41.1 ℃)的環(huán)境下發(fā)生絕緣體-金屬相變,導致其近紅外二區(qū)的光學吸收性能急劇增強,探針在1 064 nm 處的光聲信號相應增強。而當溫度回歸正常時,該納米探針迅速轉變?yōu)榈臀招阅艿慕^緣體相。在10 個溫度循環(huán)后,探針仍能保持較強的轉換能力。該探針的構建為開發(fā)高性能溫敏型光聲成像探針提供了新的指導。

圖7 溫度響應型W-VO2@PEG復合物用于動態(tài)增強型光聲成像[44]Fig.7 Temperature-responsive W-VO2@PEG NPs for dynamicenhanced photoacoustic imaging [44]
2.2.3 超聲響應型成像超聲是一種周期性的高頻機械波,其頻率超過人類聽力閾值,具有可操控性、無創(chuàng)性、安全性、高度穿透性等特點,目前已被廣泛應用于臨床診斷中[45]。然而超聲成像分辨率較低,限制了其在臨床診療中進一步的應用。基于此,Liu課題組[46]結合超聲高頻可控性以及光聲近紅外成像的特點,開發(fā)了一種基于金納米顆粒的微泡型超聲響應光聲成像探針(Au@lip MBs),用于實現“零背景”光聲成像(圖8)。在近紅外光激發(fā)下,Au@lip MBs僅表現出較低強度的光聲信號。當探針暴露在超聲脈沖下時,Au@lip MBs會破裂,形成Au@lip納米級的聚集體。由于聚集體表面等離子體共振吸收峰的紅移,探針展現出超聲響應的增強光聲信號。因此通過扣除超聲脈沖前探針展現的信號,即可實現超聲響應的“零背景”高靈敏光聲成像,為復雜環(huán)境中待測物的精準檢測提供了新的思路。

圖8 超聲響應型Au@lip微泡用于無背景光聲成像[46]Fig.8 Ultrasound-responsive Au@lip MBs for background-free photoacoustic imaging[46]
3 結論與展望
分子影像技術已成為解析復雜生物現象及實現精準醫(yī)療的重要工具。在眾多分子影像技術中,光聲成像技術具有良好生物安全性,能夠實現高分辨的實時動態(tài)成像。得益于材料學與生物醫(yī)學交叉學科的發(fā)展,基于納米生物技術的可激活型光聲造影平臺能夠特異性響應刺激,實現復雜病理模型的精準診斷,在多種疾病體系中均展現出良好的應用前景。相比于傳統的“信號常亮”型光聲探針,激活型光聲成像探針能夠通過響應外源性或內源性的刺激,實現光聲信號的特異性變化。本文從刺激響應模式與信號輸出模式的角度出發(fā),介紹了單因素刺激響應型策略以及雙因素刺激響應型策略的設計原理以及具體應用。根據所總結的激活構建策略,本文以內源性及外源性刺激響應方式作為分類,通過綜述當前光聲成像探針在多種重要生物靶點中的檢測方法,詳細討論了內源以及外源激活型光聲成像探針在生物醫(yī)學中的應用,回顧和總結了響應型光聲成像探針設計策略的研究進展。盡管激活型光聲成像技術已取得了一定進展,然而仍面臨一系列挑戰(zhàn):(1)當前響應型光聲成像探針的設計策略仍集中于“單信號輸出”類型,未來亟需開發(fā)新型“雙信號輸出”光聲成像策略,用于精確定量靶標分子。(2)近紅外二區(qū)成像探針具有活體穿透度深,組織自發(fā)熒光低及信噪比高等特點,在光聲成像領域展現了極大的應用前景。然而當前近紅外二區(qū)型光聲成像探針設計較為困難,量子產率較低,設計開發(fā)新型高效的近紅外二區(qū)影像探針對于光聲成像具有重要意義。(3)每種成像技術都具有自身獨特的性質,單一的成像方式無法全面反映生命體的整體特征。通過將光聲成像與其他成像技術融合,設計并構建多模態(tài)成像技術是實現精準成像的有效途徑[47]。隨著分子醫(yī)學的進一步發(fā)展,使用光聲探針用于特異性疾病的成像已不足以滿足研究需求,開發(fā)特定疾病靶點活化型的光聲探針對于相應疾病的診斷與治療具有重要的應用前景。這些激活型光聲成像探針能夠特異性區(qū)分病灶部位以及健康組織,有效地降低外源性探針的系統毒性,并實現疾病的實時監(jiān)測。然而如何優(yōu)化外源性探針的穩(wěn)定性、生物相容性以及生物降解性,并且利用激活型光聲探針進一步引導手術干預,給藥治療,仍是當前臨床轉化中亟需解決的問題。我們相信,隨著研究的進一步深入,激活型光聲成像技術將得到更加全面的探索,并進一步推動光聲成像的臨床應用,助力于精準分子醫(yī)學研究。

