托法替布治療頑固性SAPHO綜合征一例
賽雯雯 王廣進
1山東第一醫科大學附屬皮膚病醫院,山東濟南,250022;2山東省皮膚病性病防治研究所,山東濟南,250022
臨床資料患者,女,36歲。因“胸骨疼痛10年,掌跖部膿皰8年,復發10個月”于2022年4月2日就診于我院,患者10年前胸骨出現疼痛,反復發作,未予處理。8年前雙手、雙足掌跖部出現紅斑、膿皰,伴脫屑,就診于當地醫院,診為“掌跖膿皰病”,給予甲氨蝶呤、阿維A膠囊等藥物治療,癥狀有所好轉,仍反復發作,無法完全控制。患者既往體健,家族中無類似疾病史。
體格檢查:雙側胸鎖關節腫脹(圖1a),壓痛(+),叩痛(+)。皮膚科查體:雙手掌、足趾散發暗紅斑、脫屑,其上可見散在粟粒大小膿皰、小水皰(圖1b、1c),部分手指甲甲板表面粗糙,遠端缺損(圖1d)。
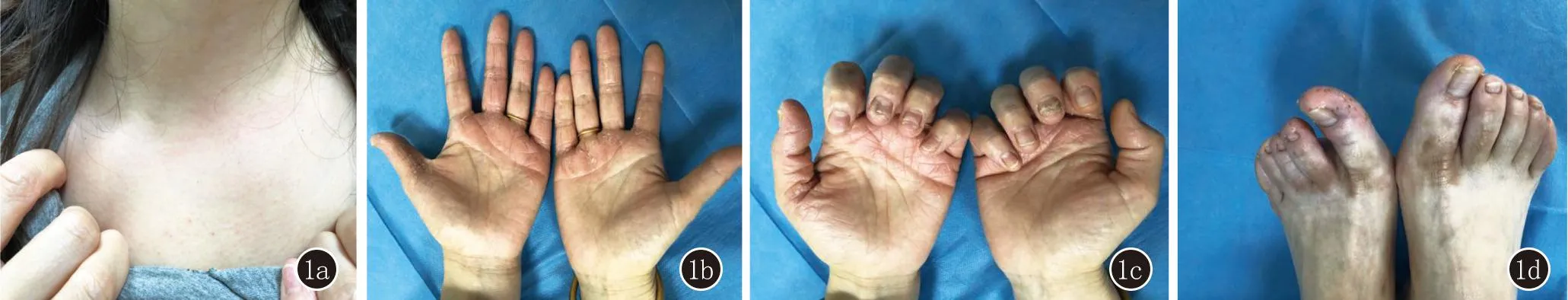
圖1 1a:雙側胸鎖關節腫脹;1b:雙手掌散發暗紅斑、脫屑,其上可見散在粟粒大小膿皰、小水皰;1c:部分手指甲甲板表面粗糙,遠端缺損;1d:雙足趾散發暗紅斑、脫屑,其上可見散在粟粒大小膿皰、小水皰
實驗室檢查:血常規、生化常規無異常,乙肝HBsAb(+)、HBeAb(+)、HBcAb(+),乙肝病毒載量0,丙肝HCV-Ab(-)、梅毒TP-Ab(-)、HIV抗體(-),結核感染T細胞試驗(IGRA)陰性。雙側胸鎖關節超聲:關節囊擴張,可見不均質低回聲區,周圍肌腱增厚,回聲減低,臨近關節骨質表面凹凸不平,呈蟲蝕狀(左側為著)。符合雙側胸鎖關節炎。皮膚組織病理結果:(左手中指)表皮角化過度,棘層增厚,棘層內皰,皰內嗜中性粒細胞移入。真皮淺層血管周圍少許淋巴細胞浸潤(圖2)。
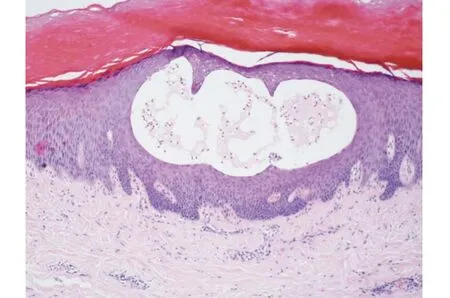
圖2 表皮角化過度,棘層增厚,棘層內皰,皰內嗜中性粒細胞移入。真皮淺層血管周圍少許淋巴細胞浸潤(HE,×100)
診斷:SAPHO綜合征。治療方案:皮下注射阿達木單抗160 mg,1周后80 mg,后每2周1次80 mg。治療第5周(阿達木單抗共注射3次)掌跖膿皰減輕,偶有少量復發,第6周軀干四肢出現粟粒大小膿皰,脫屑,無疼痛,右側胸鎖關節出現腫脹壓痛。將治療方案調整為皮下注射依奇珠單抗160 mg,后每2周皮下注射依奇珠單抗80 mg,患者自訴治療3天后胸鎖關節疼痛消失,掌跖膿皰消退,偶有新發針端大小水皰,共皮下注射依奇珠單抗4次,胸鎖關節無疼痛,但掌跖膿皰仍有反復發作。再次調整治療方案為托法替布5 mg,每日2次,治療45天后膿皰逐漸消退,紅斑減輕,脫屑減少,胸鎖關節無疼痛,指甲近端有新甲生長。治療75天后癥狀完全緩解,胸鎖關節無壓痛、腫脹(圖3a),雙側掌跖無紅斑脫屑,無水皰、膿皰(圖3b、3c),指趾甲近端見光滑新甲(圖3d)。后電話隨訪至今未復發,未發現其他不良反應,包括貧血、白細胞減少、肝功能損害或腎功能損害等。
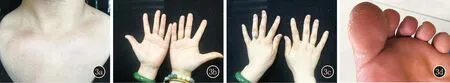
圖3 3a:雙側胸鎖關節無腫脹;3b:患者雙手掌無紅斑脫屑,無水皰、膿皰;3c:患者雙側指甲近端見光滑新甲;3d:雙足趾無紅斑脫屑,無水皰、膿皰
討論SAPHO綜合征是主要累及皮膚、骨和關節的一種慢性疾病。1987年Charmot等[1]提出SAPHO綜合征的命名,并把本綜合征的骨關節病變分為與痤瘡(聚合性痤瘡、暴發性痤瘡以及化膿性汗腺炎),掌跖膿皰病,胸鎖骨肥厚和慢性復發性骨髓炎有聯系的風濕性表現四組。所有病人均累及胸鎖關節,并引起無菌性骨肥厚性骨炎。國外報道 SAPHO 綜合征的患病率為0.04%[2]。本病臨床少見,病因不明,可能與感染、自身免疫及遺傳相關。
SAPHO綜合征的診斷標準在提出來后不斷進行修改,以下為目前最常用的納入及排除標準[3]:入選標準:(1)骨關節表現+聚合性痤瘡和暴發性痤瘡或化膿性汗腺炎;(2)骨關節表現+掌跖膿皰病;(3)骨肥厚(上胸壁、肢端骨、脊柱)伴或不伴皮膚損害;(4)慢性多灶性復發性骨髓炎包含中軸或外周骨,伴或不伴皮膚損害。排除標準:(1)膿毒血癥的骨髓炎(痤瘡丙酸桿菌感染除外);(2)感染性前胸壁關節炎;(3)感染性的掌跖膿皰;(4)掌跖角化病;(5)彌漫性特發性骨肥厚癥;(6)維A酸類藥物治療引起的骨關節損害。滿足以上四個條件之一,并不符合排除標準中的任意一條即可診斷為 SAPHO綜合征。即便明確了診斷標準,但是臨床診斷仍然是非常困難的,只有約 1/4 的患者骨關節病變與皮膚病特征同時出現,而其他病例中兩者發生時間并不平行。實驗室檢查常不具特異性,部分患者可有CRP、ESR 及 HLA-B27 增高,但不能用以診斷SAPHO綜合征。本例患者以胸鎖關節疼痛起病,伴有掌跖膿皰病,符合第二條診斷標準,故可診斷為SAPHO綜合征。
由于其罕見性,國內外尚無針對該疾病的治療指南,臨床工作中主要基于病例報告、病例系列[4]、專家判斷,并從類風濕性關節炎、銀屑病關節炎等相關疾病中學習,以控制疼痛和炎癥過程。因此非甾體類抗炎藥被認為是現今的一線治療用藥,其他治療方法包括秋水仙堿、糖皮質激素、甲氨蝶呤、柳氮磺吡啶等藥物。當上述藥物療效不滿意時,考慮為難治性 SAPHO 綜合征[5]。有研究表明,SAPHO患者外周血IL-1、IL-8、IL-17、IL-18、Th17水平升高[6,7,8]。外周血和骨組織中TNF-α表達增加,外周血中IL-10水平降低,導致自身炎癥[9]。免疫細胞被眾多細胞因子激活,通過不同的途徑產生更多的細胞因子,這可以使炎癥反應放大級聯。針對 TNF-α[10]、抗 IL-1[11]和IL-23或IL-17[12]等生物制劑的靶向治療已被證明對大多數難治性 SAPHO 患者有效[6]。然而,在臨床實踐中經常觀察到這些抑制劑的藥物超敏反應、治療失敗或矛盾效應[13,14],我們的病例也顯示應用TNF-α抑制劑以及 IL-17抑制劑均未達到理想治療效果。常見的生物制劑在細胞外發揮抑制作用,并靶向單一細胞因子,JAK 是重要的細胞內信號轉導介質。不同的細胞因子通過不同的 JAK 組合發出信號;阻斷JAKs可以直接或間接阻斷多種細胞因子的作用。JAK 抑制劑可以通過抑制細胞因子作用來治療多種炎癥性疾病[15,16]。
本例患者在外院應用多種傳統治療藥物未得到明顯緩解,后給予多種生物制劑治療后癥狀有所緩解,仍反復發作,最終給予托法替布治療,后病情得到快速控制,胸鎖關節疼痛緩解,皮疹完全消退,療效確切,因此,JAK 抑制劑托法替布可以作為SAPHO綜合征一種新的治療手段,但其長期療效及安全性仍需進一步觀察。

