不同時機微創顱內血腫穿刺引流術治療高血壓腦出血的可行性及對神經功能的改善作用
劉中濤
(菏澤市中醫醫院神經外科,山東 菏澤,274000)
高血壓腦出血是高血壓嚴重并發癥之一,由于長期血壓控制不佳,引起顱內小動脈破裂出血。高血壓腦出血發生后,腦室內、顱內釋放多種補體復合物、凝血酶等炎性因子,損傷腦組織,出現頭痛、嘔吐、肢體麻木、失語、昏迷等臨床表現,其致死率居于腦血管疾病的首位,嚴重危害患者的生命安全[1-2]。及時清除腦內血腫,解除或減輕血腫對周圍腦組織的壓迫、降低顱內壓是改善患者預后的關鍵[3-4]。微創顱內血腫穿刺引流術是當前治療高血壓腦出血的常用手段,具有創傷小、操作簡便的優勢,臨床上普遍認為出血后超過24 h手術預后效果不如在24 h內手術,但關于出血后6 h內、出血后6~12 h手術的臨床療效及預后臨床尚存在一些爭議。基于此,本研究旨在分析不同時機微創顱內血腫穿刺引流術治療高血壓腦出血的可行性及對神經功能的改善作用,現將本研究結果闡述如下。
1 資料與方法
1.1 一般資料
選擇2017年10月—2023年2月菏澤市中醫醫院收治的80例高血壓腦出血患者作為研究對象,以手術時機不同將其分成三組,出血后6 h內進行手術的27例為超早期組,出血后6~12 h進行手術的27例為早期組,出血后超過24 h進行手術的26例為晚期組。三組一般資料比較,差異無統計學意義(P>0.05),有可比性,見表1。所有患者和家屬對本研究知情同意,已簽署知情同意書,菏澤市中醫醫院醫學倫理委員會對本研究進行詳細審核是否符合規范要求,已批準進行。
表1 三組一般資料比較[( )/n(%)]
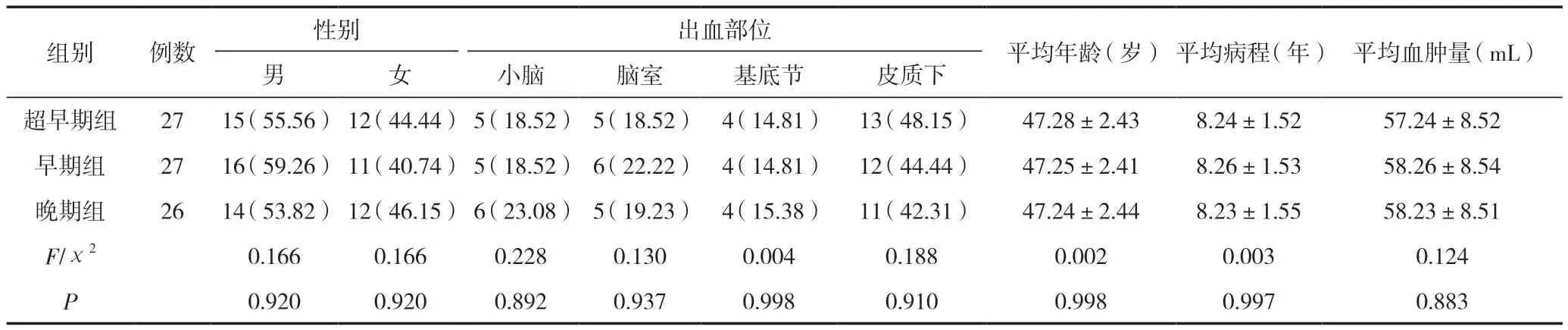
表1 三組一般資料比較[( )/n(%)]
出血部位平均年齡(歲)平均病程(年)平均血腫量(mL)男女小腦腦室基底節皮質下超早期組2715(55.56)12(44.44)5(18.52)5(18.52)4(14.81)13(48.15)47.28±2.438.24±1.5257.24±8.52早期組2716(59.26)11(40.74)5(18.52)6(22.22)4(14.81)12(44.44)47.25±2.418.26±1.5358.26±8.54晚期組2614(53.82)12(46.15)6(23.08)5(19.23)4(15.38)11(42.31)47.24±2.448.23±1.5558.23±8.51 F/χ20.1660.1660.2280.1300.0040.1880.0020.0030.124 P 0.9200.9200.8920.9370.9980.9100.9980.9970.883組別例數性別
1.2 納入與排除標準
納入標準:①符合《中國腦出血診治指南(2014)》[5]中高血壓腦出血診斷標準,經顱腦CT確診者;②無手術禁忌證,首次發病者;③出血時間<72 h者。
排除標準:①合并顱內感染、全身性感染疾病、血液系統疾病、惡性腫瘤者;②顱內血管畸形、外傷等其他原因導致的腦出血者;③心臟、肝臟、腎臟等臟器功能不全者等。
1.3 方法
三組患者手術前均接受控制血壓、糾正水電解質平衡、穩定顱內壓等常規治療。通過頭顱CT掃描確定出血位置,避開動脈血管、重要功能區等危險結構,在血腫最大層面選取穿刺點,確定穿刺路徑、計算穿刺引流管長度。依據血腫和穿刺點距離選擇粗細合適的軟通道,一般12或14號引流管,在穿刺點處2%利多卡因局部浸潤麻醉,麻醉成功后尖刀破皮,手搖鉆鉆透顱骨,顱錐鉆透硬腦膜,帶針軟通道沿術前預定穿刺方向及計算深度穿刺置入血腫中心,導芯拔出,使用0.9氯化鈉溶液緩慢置換出30%~40%的血腫,接顱腦外引流裝置。術后復查顱腦CT證實引流管的位置、殘留血腫及排除有無穿刺道出血,自三通處血腫腔注入用尿激酶2~4萬單位(操作前簽署特殊治療告知書),夾閉引流管2 h,之后開放引流管引流,q12 h,尿激酶注入。CT復查殘余血腫量<10 mL、無顱內壓增強情況出現后進行拔管,一般置管時間是3~5 d。手術完成后予以營養神經、抗感染、控制血液等常規措施,監測生命體征。術后隨訪1個月。
1.4 觀察指標
①格拉斯哥預后評分(GOS)[6]優良率。術后2周,使用GOS評估三組患者恢復情況,5分為優:正常生活,不存在精神障礙或存在輕度精神障礙;4分為良:可以生活自理,但存在中度病殘;3分為中:意識清醒,但生活無法自理;1~2分為差:存在嚴重意識障礙,處于植物生存狀態或死亡。優良率=(優+良)例數/總例數×100%。②不同時間美國國立衛生研究院卒中量表(NIHSS)[7]評分。術前、術后2周、術后1個月,使用NIHSS評估三組神經功能缺損情況,分值0~42分,分值越高意味著神經功能受損越嚴重。③血清白細胞介素-6(IL-6)、白細胞介素-2(IL-2)、超敏C反應蛋白(hs-CRP)、腫瘤壞死因子-α(TNF-α)水平。術前、術后2周,患者空腹狀態下采集靜脈血5 mL,放入離心設備,3 100 r/min離心10 min取上清,使用酶聯免疫吸附法測定血清IL-6、IL-2、hs-CRP、TNF-α水平。④術后并發癥發生情況及再出血率。術后1個月內,統計三組肺部感染、消化道出血、顱內感染發生情況及再出血情況。并發癥發生率=(肺部感染+消化道出血+顱內感染+再出血)例數/總例數×100%。
1.5 統計學分析
本研究采用SPSS 20.0軟件分析數據,計數資料以[n(%)]表示,組間比較經χ2檢驗,多組比較通過χ2趨勢檢驗進行分析;計量資料經K-S法檢驗,符合正態分布,以()表示,組內比較使用獨立、配對樣本t檢驗,多組多時間點比較采用重復方差分析。以P<0.05為差異有統計學意義。
2 結果
2.1 三組GOS優良率比較
術后2周,相比晚期組,早期組、超早期組GOS優良率更高,差異有統計學意義(P<0.05);早期組和超早期組比較,差異無統計學意義(P>0.05),見表2。
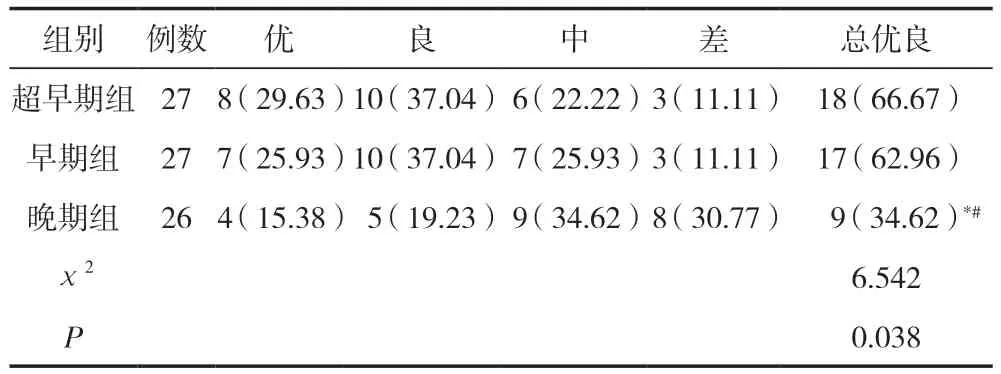
表2 三組GOS優良率比較 [n(%)]
2.2 三組不同時間NIHSS評分比較
與術前比較,術后2周、術后1個月三組NIHSS評分呈依次降低趨勢,相比晚期組,早期組、超早期組NIHSS評分更低,差異有統計學意義(P<0.05);早期組和超早期組比較,差異無統計學意義(P>0.05),見表3。
表3 三組不同時間NIHSS評分比較 ( ,分)
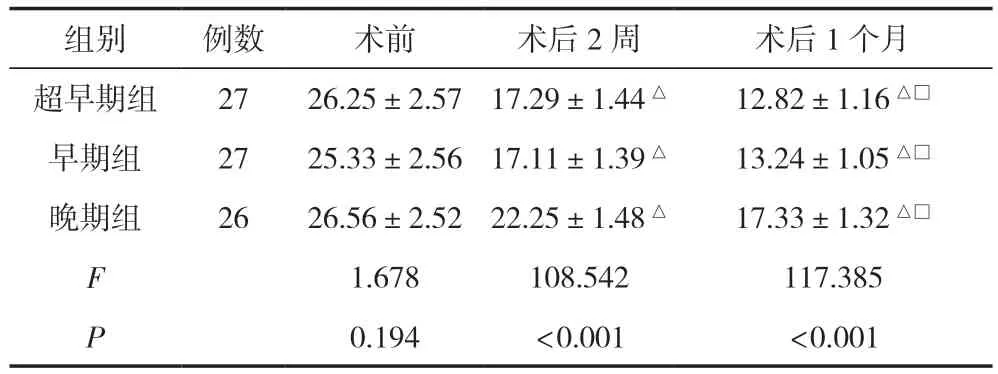
表3 三組不同時間NIHSS評分比較 ( ,分)
注:與同組術前比較,△P<0.05;與同組術后2周比較,□P<0.05。
組別例數術前術后2周術后1個月超早期組2726.25±2.5717.29±1.44△12.82±1.16△□早期組2725.33±2.5617.11±1.39△13.24±1.05△□晚期組2626.56±2.5222.25±1.48△17.33±1.32△□F 1.678108.542117.385 P 0.194<0.001<0.001
2.3 三組血清IL-6、IL-2、hs-CRP、TNF-α水平比較
與術前比較,術后2周三組血清IL-6、hs-CRP、TNF-α水平均降低,相比晚期組、早期組,超早期組更低,且早期組低于晚期組,差異有統計學意義(P<0.05);術后2周三組血清IL-2水平均升高,相比晚期組、早期組,超早期組更高,且早期組高于晚期組,差異有統計學意義(P<0.05),見表4。
表4 三組血清IL-6、IL-2、hs-CRP、TNF-α水平比較 ()
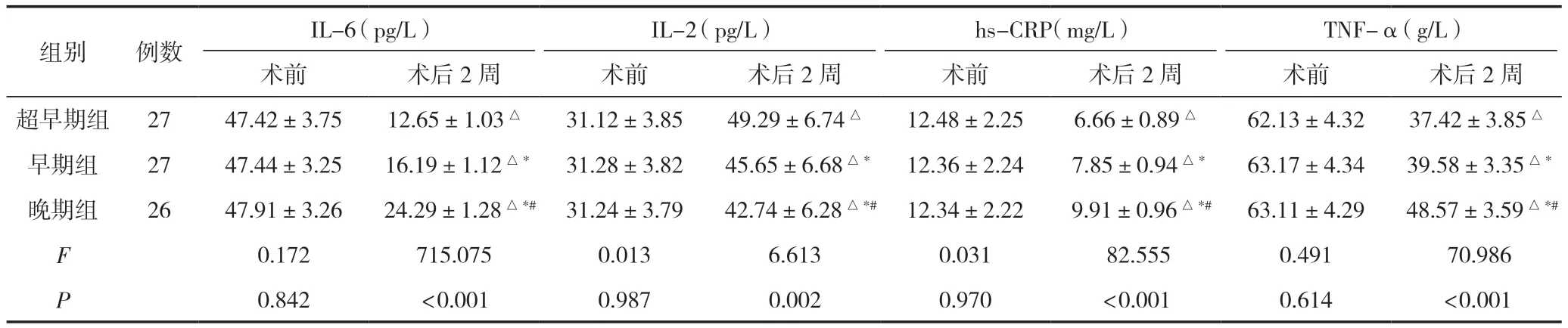
表4 三組血清IL-6、IL-2、hs-CRP、TNF-α水平比較 ()
注:與同組術前比較,△P<0.05;與超早期組比較,*P<0.05;與早期組比較,#P<0.05。
TNF-α(g/L)術前術后2周術前術后2周術前術后2周術前術后2周超早期組2747.42±3.7512.65±1.03△31.12±3.8549.29±6.74△12.48±2.256.66±0.89△62.13±4.3237.42±3.85△早期組2747.44±3.25 16.19±1.12△*31.28±3.82 45.65±6.68△*12.36±2.24 7.85±0.94△*63.17±4.34 39.58±3.35△*晚期組2647.91±3.26 24.29±1.28△*#31.24±3.79 42.74±6.28△*#12.34±2.22 9.91±0.96△*#63.11±4.29 48.57±3.59△*#F 0.172715.0750.0136.6130.031 82.5550.491 70.986 P 0.842<0.0010.9870.0020.970<0.0010.614<0.001組別例數IL-6(pg/L)IL-2(pg/L)hs-CRP(mg/L)
2.4 三組術后并發癥發生情況及再出血率比較
術后1個月內,相比早期組、晚期組,超早期組并發癥總發生率更低,且早期組低于晚期組,差異有統計學意義(P<0.05);相比晚期組、超早期組,早期組再出血率更低,差異有統計學意義(P<0.05);晚期組、超早期組再出血率比較,差異無統計學意義(P>0.05),見表5。
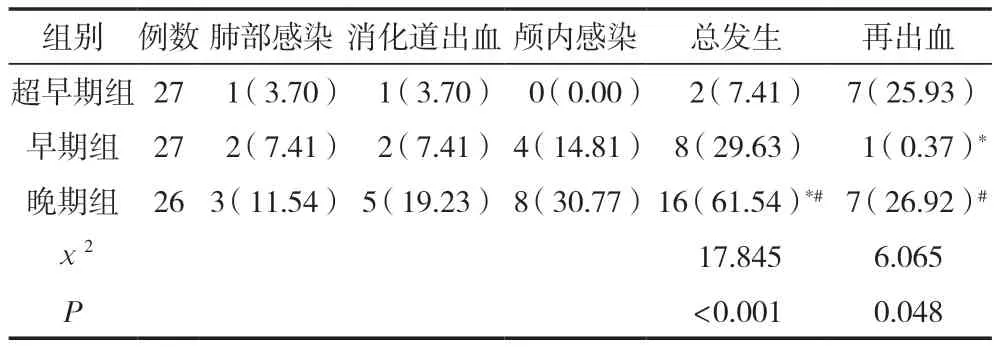
表5 三組術后并發癥發生情況及再出血率比較 [n(%)]
3 討論
高血壓腦出血在中老年人群中發病率較高,病情進展速度快,對于血腫量較大的患者,保守治療效果不理想,外科手術通過解除血腫壓迫,減少繼發性腦損害的發生,是高血壓腦出血主要治療方法[8-10]。微創顱內血腫穿刺引流術在臨床上被廣泛應用,但不同手術時機的選擇對手術效果和術后恢復有非常重要的影響。
高血壓腦出血一般在出血30 min時血腫開始形成,6~7 h血腫壓迫占位效應會造成腦組織水腫、壞死,并且隨著時間的延長其嚴重程度不斷增加。超早期微創顱內血腫穿刺引流術可以盡早清除血腫,解除血腫對腦組織的壓迫,阻斷或減輕半暗帶區神經細胞產生的一系列繼發不良病理生理改變,為神經功能的改善提供有利條件[11-12]。本研究結果顯示,術后2周、術后1個月三組NIHSS評分呈依次降低趨勢,相比晚期組,早期組、超早期組NIHSS評分更低,表明超早期微創顱內血腫穿刺引流術可有效改善高血壓腦出血患者神經功能,促進病情恢復。
高血壓腦出血不僅破壞出血部位腦組織,血腫分解產生物的毒性也會導致血腫周圍腦組織發生水腫、變性及炎癥反應,釋放IL-6、hs-CRP、TNF-α等炎癥因子,造成血腦屏障、腦微血管通透性改變,加快血腫周圍組織損傷病理進程,加重病情。超早期微創顱內血腫穿刺引流術能夠盡早阻斷炎癥反應、腦水腫、神經損傷的惡性循環,調節血清IL-6、hs-CRP、TNF-α、IL-2水平,減輕炎癥反應,減少并發癥的發生,促進患者康復[13-15]。本研究結果顯示,術后2周,相比晚期組、早期組血清IL-6、hs-CRP、TNF-α水平,超早期組更低,且早期組低于晚期組;相比晚期組、早期組血清IL-2水平,超早期組更高,且早期組高于晚期組;術后1個月內,相比早期組、晚期組,超早期組并發癥總發生率更低,且早期組低于晚期組,表明超早期微創顱內血腫穿刺引流術可調節高血壓腦出血患者炎癥因子水平,降低術后并發癥發生率。術后2周,相比晚期組,早期組、超早期組GOS優良率更高;術后1個月內,相比晚期組、超早期組,早期組再出血率更低,表明超早期微創顱內血腫穿刺引流術與早期微創顱內血腫穿刺引流術治療效果相當,但超早期微創顱內血腫穿刺引流術存在再出血率較高的不足。分析原因可能是:高血壓腦出血患者在超早期血腫形成不完全,穩定性差,若在此時間進行手術,止血難度大,出血血管容易再出出血,增加再出血風險。
綜上所述,超早期微創顱內血腫穿刺引流術可有效改善高血壓腦出血患者神經功能,調節炎癥因子水平,降低術后并發癥發生率,但存在再出血率較高的不足,與早期微創顱內血腫穿刺引流術治療效果相當。本研究存在樣本量較少的不足,后續仍需多渠道、多中心擴大樣本量進一步探究不同時機微創顱內血腫穿刺引流術治療高血壓腦出血的可行性及對神經功能的改善作用。

