阿帕替尼聯合白蛋白紫杉醇化療二線治療晚期胃癌的療效及不良反應分析
張曉潔
(赤峰市醫院腫瘤內科,內蒙古 赤峰,024000)
胃癌是一種嚴重的疾病,危及患者的生命和健康,尤其是晚期胃癌,給患者的治療帶來了巨大的挑戰。當前,手術切除、化療、放療等治療方法仍然是治療晚期胃癌的主要手段,然而,治療的效果仍然不理想,生存率令人擔憂[1]。阿帕替尼是一種口服酪氨酸激酶抑制劑,已被廣泛用于多種腫瘤的治療中。近年來,阿帕替尼聯合化療治療晚期胃癌的應用也引起了研究人員的關注。然而,對于阿帕替尼聯合化療治療晚期胃癌的臨床療效及不良反應方面的研究仍然不足[2]。因此,本研究選取2021年3月—2022年5月赤峰市醫院收治的120例晚期胃癌患者作為研究對象,旨在評估阿帕替尼聯合化療治療晚期胃癌的臨床療效及不良反應,以期提供更有效、安全和個體化的治療策略,以改善患者的生存質量和延長生存期。
1 資料與方法
1.1 一般資料
選取2021年3月—2022年5月赤峰市醫院收治的120例晚期胃癌患者作為研究對象,應用隨機數表法分為對照組和觀察組,每組60例。觀察組中,男性32例,女性28例;年齡38~69歲,平均年齡(56.92±4.20)歲;病灶大小:>5 cm 25例,≤5 cm 35例;發病部位:胃底29例,胃體21例,胃竇10例;病理類型:管狀腺癌35例,印戒細胞癌25例。對照組中,男性31例,女性29例;年齡37~69歲,平均年齡(56.99±4.34)歲;病灶大小:>5 cm 19例,≤5 cm 41例;發病部位:胃底27例,胃體21例,胃竇12例;病理類型:管狀腺癌36例,印戒細胞癌24例。兩組患者一般資料比較,差異無統計學意義(P>0.05),具有可比性。本研究所有患者及其家屬均簽署了知情同意書。本研究通過赤峰市醫院醫學倫理委員會審批。
1.2 納入與排除標準
納入標準:① 符合《中華醫學會胃癌臨床診療指南(2021版)》[3]中的相關診斷標準;②入院后,所有患者均經常規檢查并結合臨床表現確診;③年齡≥18歲,伴有癌細胞腫瘤四期遠隔臟器轉移者;④無溝通障礙和意識障礙。
排除標準:① 嚴重精神障礙者;②患有其他惡性腫瘤疾病者;③病歷數據缺失或未主動提供自己的臨床數據;④研究依從性低;⑤對本研究中使用的治療藥物表現出嚴重不耐受的患者。
1.3 方法
對照組接受注射用紫杉醇(白蛋白結合型)(生產企業:石藥集團歐意藥業有限公司,國藥準字H20183044,規格:100 mg)治療,用量130~150 mg/m2。
觀察組在對照組治療方案上聯合甲磺酸阿帕替尼片(生產企業:江蘇恒瑞醫藥股份有限公司,國藥準字H20140105,規格:0.425 g)治療,250 mg/d。兩組患者均接受為期6個周期的治療,在治療過程中根據患者化療反應對用藥劑量進行實時調整。
1.4 觀察指標
均于治療6周后對以下指標進行觀察比較評價。①治療近期療效:參考RECIST1.1標準對近期治療展開判定,完全緩解(CR,所有病灶消失,沒有新的病灶出現)、部分緩解(PR,目標病灶的總和直徑減小了至少30%,并沒有新的病灶出現)、疾病穩定(SD,病灶的總和直徑沒有明顯變化,沒有新的病灶出現)及疾病進展(PD,病灶的總和直徑增加了至少20%,或者有新的病灶出現)。記錄評價組間客觀緩解率(Objective Response Rate,ORR):指患者在干預后出現完全緩解(CR)或部分緩解(PR)的比例。疾病控制率(Disease Control Rate,DCR):指患者在干預后出現完全緩解(CR)、部分緩解(PR)或疾病穩定(SD)的比例。它是評估治療是否能夠控制腫瘤進展的指標。計算公式:DCR =(CR+PR +SD)例數/總例數×100%。ORR=(CR+PR)例數/總例數×100%。②血清腫瘤標志物:評價兩組患者接受干預后腫瘤標志物水平的變化情況:應用酶聯免疫吸附法(ELISA 試劑盒,生產企業:武漢賽培生物,規格:96T/48T)對鱗狀細胞癌相關抗原(Squamous Cell Carcinoma Antigen,SCC-Ag)水平進行檢測;應用化學發光法( REK-20N型化學發光定氮儀)對癌胚抗原(Carcino-Embryonic Antigen,CEA)水平進行檢測;應用雙抗體夾心ELISA檢測法(癌胚抗原測定試劑盒,生產企業:上海科華生物工程股份有限公司)對人糖類抗原125(CA125)水平進行檢驗。③判定患者的免疫功能: 應用酶聯免疫吸附法(血管內皮生長因子測定試劑盒,生產企業:北京鍵平九星生物醫藥科技有限公司)和放射免疫測定法(放射免疫試劑盒,生產企業:上海恒遠生物科技有限公司)檢測免疫球蛋白M(Immunoglobulin M,IgM)和免疫球蛋白G(Immunoglobulin G,IgG)、免疫球蛋白A(Immunoglobulin A,IgA),流式細胞術檢查患者自然殺傷細胞(Natural Killer Cell,NK)。④記錄評價組間用藥不良反應: 血小板降低、嘔吐、中性粒細胞降低。不良反應發生率=(血小板降低+嘔吐+中性粒細胞降低)例數/總例數×100%。
1.5 統計學分析
采用SPSS 24.0統計學軟件分析數據,計數資料采用[n(%)]表示,結果行χ2檢驗;計量資料采用()表示,結果行t檢驗。以P<0.05為差異有統計學意義。
2 結果
2.1 兩組近期療效比較
經為期6個周期化療干預后,觀察組患者客觀緩解率、疾病控制率均明顯高于對照組,差異有統計學意義(P<0.05),見表1。
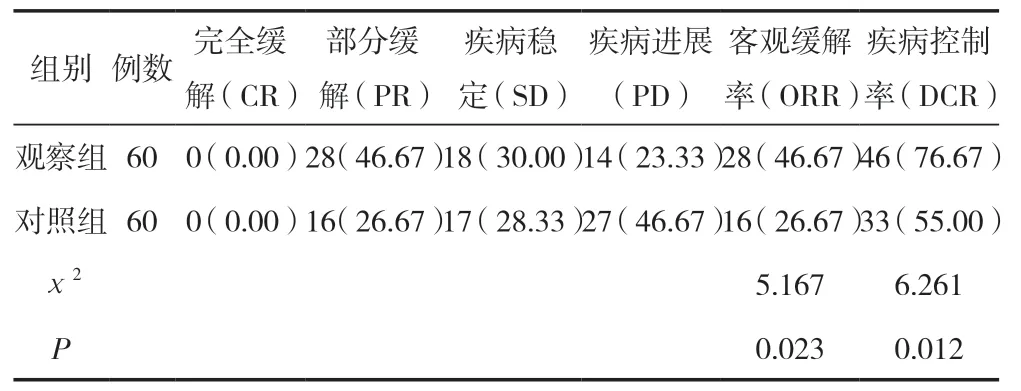
表1 兩組近期療效比較 [n(%)]
2.2 兩組患者干預前后腫瘤標志物水平的變化情況比較
干預前,兩組患者的血清SCC-Ag、CEA及CA125水平比較,差異無統計學意義(P>0.05);干預后,觀察組血清SCC-Ag、CEA、CA125水平低于對照組,差異有統計學意義(P<0.05),見表2。
表2 兩組患者干預前后腫瘤標志物水平的變化情況比較 ()

表2 兩組患者干預前后腫瘤標志物水平的變化情況比較 ()
組別例數SCC-Ag(μg/L)tPCEA(μg/L)tPCA125(ku/L)tP干預前干預后干預前干預后干預前干預后觀察組604.88±0.522.49±0.213.002<0.00128.21±3.1014.98±2.878.992<0.00138.29±1.2924.72±4.565.023<0.001對照組604.67±0.563.35±0.563.022<0.00128.27±3.4520.61±2.728.152<0.00138.71±1.2131.51±4.835.203<0.001 t 2.128 11.1380.100 11.0291.839 7.918 P 0.035<0.0010.920<0.0010.068<0.001
2.3 干預后2周兩組患者的免疫功能各評價維度比較
干預后2周,觀察組患者的IgM、IgG、IgA、NK細胞活性等指標均明顯高于對照組,差異有統計學意義(P<0.05),見表3。
表3 干預后2周兩組患者的免疫功能各評價維度比較 ()
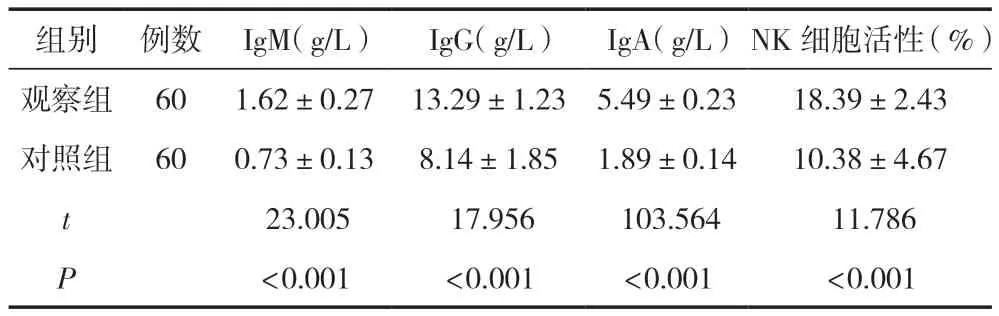
表3 干預后2周兩組患者的免疫功能各評價維度比較 ()
組別例數IgM(g/L)IgG(g/L)IgA(g/L)NK細胞活性(%)觀察組601.62±0.2713.29±1.235.49±0.2318.39±2.43對照組600.73±0.138.14±1.851.89±0.1410.38±4.67 t 23.005 17.956 103.564 11.786 P<0.001<0.001<0.001<0.001
2.4 兩組用藥不良反應發生率比較
兩組用藥不良反應發生率比較,差異無統計學意義(P>0.05),見表4。
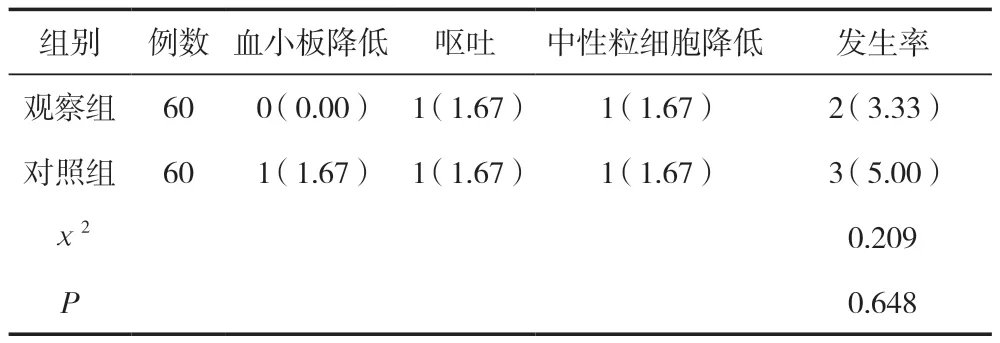
表4 兩組用藥不良反應發生率比較 [n(%)]
3 討論
晚期胃癌是一種嚴重的疾病,其治療方法包括化療、手術和放療等,其中化療是最為常用的治療方式之一,白蛋白紫杉醇和阿帕替尼是常用的化療藥物,它們可以通過不同的機制抑制腫瘤生長和擴散。最近的研究表明,白蛋白紫杉醇聯合阿帕替尼治療晚期胃癌可以顯著提高患者的生存率并緩解癥狀,而且藥物不良反應發生率與單獨使用白蛋白紫杉醇治療相比并沒有顯著差異[4]。首先,白蛋白紫杉醇和阿帕替尼的藥理作用機制不同,白蛋白紫杉醇通過靶向微管蛋白,干擾腫瘤細胞有絲分裂和增殖,從而達到抑制腫瘤生長和擴散的效果,阿帕替尼則是一種多靶點酪氨酸激酶抑制劑,可以抑制腫瘤細胞的增殖和侵襲,并誘導腫瘤細胞凋亡,兩種藥物的作用機制不同,可以相互補充,從而提高治療效果[3]。其次,白蛋白紫杉醇可以通過白蛋白作為載體,提高其在體內的穩定性和溶解度,降低其不良反應,而且,白蛋白作為一種生物大分子,可以在體內降解為氨基酸,不會對機體產生明顯的不良反應,阿帕替尼的不良反應比較輕,主要表現為惡心、嘔吐、腹瀉等,而且可以通過調整劑量和給藥時間來減輕不良反應[4-5]。最后,白蛋白紫杉醇聯合阿帕替尼治療晚期胃癌需要在醫生的指導下進行,嚴格控制用藥劑量和用藥時間,以避免不良反應的發生,同時,患者也需要積極配合治療,按時接受化療并遵循醫囑,以提高治療效果和減少不良反應的發生[6-7]。因此,白蛋白紫杉醇聯合阿帕替尼治療晚期胃癌與單獨使用白蛋白紫杉醇治療相比,藥物不良反應發生率差異性不大的原因主要是兩種藥物的作用機制不同,可以相互補充,而且白蛋白作為載體可以提高藥物的穩定性和溶解度,降低不良反應,在治療過程中,醫生和患者都需要積極配合,以提高治療效果和減少不良反應的發生[8]。
對患者近期療效展開統計分析可見,經為期6個周期化療干預后,觀察組患者ORR、DCR均明顯高于對照組,差異有統計學意義(P<0.05)。丁根樹[9]在其研究中為晚期胃癌患者實施阿帕替尼聯合化療治療,近期療效得到改善,結論與本研究高度一致。近年來,針對晚期胃癌的治療出現了許多新的方案,阿帕替尼聯合化療方案是其中之一。阿帕替尼作為一種靶向治療藥物,可以抑制腫瘤細胞的生長和擴散,同時可以減輕化療的不良反應。阿帕替尼聯合化療治療晚期胃癌的療效得到改善的原因,可能與其對腫瘤細胞的作用有關,具體包括抑制血管生成、減少腫瘤細胞增殖、增強化療敏感性等多種機制[10]。
對腫瘤標志物水平進行檢驗比較可見,接受干預前,兩組患者的血清SCC-Ag、CEA及CA125水平比較,差異無統計學意義(P>0.05);干預后,觀察組血清SCC-Ag、CEA、CA125水平低于對照組,差異有統計學意義(P<0.05)。與韓俊偉等[11]研究結果高度一致。阿帕替尼是一種針對血管內皮生長因子受體(VEGFR)的酪氨酸激酶抑制劑,可通過阻斷血管生成和誘導腫瘤細胞凋亡等機制發揮抗腫瘤作用,在阿帕替尼聯合化療方案下,阿帕替尼可與化療藥物相互作用,通過抑制腫瘤細胞增殖和誘導腫瘤細胞凋亡等多種途徑發揮抗腫瘤作用。具體來說,阿帕替尼通過靶向VEGFR的作用,能夠抑制腫瘤新生血管的形成,減少腫瘤的血液供應,從而降低腫瘤的代謝活性和生長速率。此外,阿帕替尼還可調節免疫系統的功能,增強機體對腫瘤的免疫反應,該藥物可抑制腫瘤細胞釋放的免疫抑制因子,激活免疫細胞,促進T細胞的增殖和活化,從而促進機體免疫殺傷腫瘤細胞[12-13]。
統計分析患者免疫功能變化情況可見,干預后2周,觀察組患者的IgM、IgG、IgA、NK細胞活性等指標均明顯高于對照組,差異有統計學意義(P<0.05)。與馬馨等[14]研究結果(研究組IgM 、IgG 、IgA 、NK細胞活性顯著高于對照組)結論一致。阿帕替尼能夠抑制一些免疫細胞,如NK和T細胞,從而抑制腫瘤生長和擴散,同時,阿帕替尼也可以促進其他類型的免疫細胞的活化和功能,如B細胞和巨噬細胞,這些免疫細胞的活化和功能可以促進免疫系統的應答,從而提高患者的免疫功能。其次,阿帕替尼可以影響腫瘤細胞的免疫逃逸機制,腫瘤細胞通過減少表達抗原、增加免疫抑制分子的表達等方式來逃避免疫系統的攻擊[15]。而阿帕替尼可以逆轉這種免疫逃逸機制,增加腫瘤細胞表達抗原,并減少免疫抑制分子的表達,這些作用可以增強免疫系統對腫瘤的攻擊,從而提高患者的免疫功能。最后,阿帕替尼可以影響腫瘤微環境,腫瘤微環境是指腫瘤周圍的細胞和分子環境,包括腫瘤細胞、免疫細胞、血管和基質等,腫瘤微環境對腫瘤的生長和轉移有重要影響,而阿帕替尼可以抑制腫瘤微環境的形成,減少免疫細胞的浸潤,從而增強患者的免疫功能。
對用藥不良反應進行統計比較可見,兩組患者不良反應發生率比較,差異無統計學意義(P>0.05)。阿帕替尼聯合化療與白蛋白紫杉醇治療在藥理學方面存在顯著差異,阿帕替尼是一種酪氨酸激酶抑制劑,可以靶向性地抑制腫瘤細胞生長和擴散,具有較好的抗腫瘤效果。相比之下,白蛋白紫杉醇是一種紫杉醇類抗腫瘤藥物,具有廣泛的抗腫瘤作用,但也有一定的不良反應,但與聯合使用患者用藥不良反應比較雖有一定的差異,但差異性不大,表明了聯合方案的安全性[16]。
綜上所述,為晚期胃癌患者實施阿帕替尼聯合化療治療,可改善患者近期療效,提升患者免疫功能,用藥不良反應可控,值得作為晚期胃癌治療方案展開應用。

