富血小板血漿聯合玻璃酸鈉對骨質疏松性骨折大鼠的影響
馬超 潘浩 崔潤之 劉振 崔路寬
河北省滄州中西醫結合醫院,河北 滄州 060000
骨質疏松癥是骨科常見的全身代謝性骨骼疾病,研究表明,骨質疏松患者平時受到輕微的創傷就可能發生骨折,故骨質疏松性骨折(osteoporosis fracture,OPF)是其最嚴重的并發癥之一[1-2]。眾所周知,骨折的愈合是一個復雜且相對漫長的生物學過程,OPF患者相比于正常骨折患者,更易出現骨折延遲愈合、甚至不愈合的情況,這對患者及其家屬、甚至是社會都造成了一定負擔,因此,如何促進骨折愈合一直是臨床亟需解決的問題[3-5]。
近年來研究發現,松質骨中血流下降與骨折發生率升高有關,且骨折后極易伴隨血管及神經損傷,而這也是影響骨折愈合的關鍵因素,因此無論是對骨質疏松患者還是對OPF患者,促進血管生成都尤為重要,其可提供更好的血供,從而改善骨組織代謝,促進新骨形成[6]。活化T細胞核轉錄因子c1(nuclear factorof activated T-cells cytoplasmic 1,NFATcl)是一種重要的轉錄因子,研究發現,其所在信號通路可參與破骨細胞形成及分化的調控,而OPF的發生與破骨細胞的過度激活密切相關,由此可見NFATcl信號通路可能在OPF發生、發展中發揮至關重要的作用[7]。
富血小板血漿是一種血小板濃縮制劑,所含血小板濃度是全血的4~6倍,此外還含有大量的生長因子及高濃度活性纖維蛋白,具有顯著的組織修復能力,且大量研究證實其在促進骨折愈合方面具有顯著作用[8]。玻璃酸鈉作為關節液、關節軟骨主要成分,在維持關節生物力學、保護軟骨功能等方面具有重要作用,已被廣泛應用骨關節炎等骨科疾病的治療,且近年來對于骨折愈合也已取得了喜人的效果[9]。但富血小板血漿及玻璃酸鈉對OPF方面的研究相對較少,因此本研究以富血小板血漿聯合玻璃酸鈉對骨質疏松性骨折大鼠骨愈合、血管生成及NFATc1信號通路的影響進行探討,以期為臨床治療提供新的治療靶點。
1 材料與方法
1.1 材料
1.1.1動物材料:60只SPF級SD雌性大鼠選自廣州弗爾博生物科技有限公司[合格證書:SCXK(粵)2021-0012],平均體重210~270 g,單籠喂養,環境溫度為(21±4)℃,濕度為46%~62%,模仿12 h晝夜交替,無菌自由進食、飲水2周,按照《實驗動物管理條例》規定進行實驗。本實驗經過河北省滄州中西醫結合醫院倫理委員會批準(批準文號:2022-0309)。
1.1.2實驗材料:富血小板血漿(貨號:PR0229,北京普非有限公司);玻璃酸鈉(貨號:AVT00001,上海艾偉拓有限公司);小動物骨密度儀(型號:RZ,上海然哲有限公司);生物力學試驗機(型號:HY-0350,上海衡翼有限公司);蘇木素染液(貨號:ZY1850,上海澤葉有限公司);伊紅染液(貨號:BL703B,杭州銘特有限公司);光學顯微鏡(型號:E100,上海普赫有限公司);酶聯免疫吸附(ELISA)試劑盒(貨號:JEH-01,上海中喬新舟有限公司);RIPA裂解液(貨號:E-BC-R327,武漢伊萊瑞特有限公司);SDS-PAGE凝膠電泳試劑盒(貨號:BM0687,上海圻明有限公司);BCA蛋白濃度測定試劑盒(貨號:PR1711,北京普非有限公司);NFATc1抗體(貨號:XGK0377,上海西格有限公司);OSCAR抗體(貨號:GOY-01K1393,上海谷研有限公司司);GAPDH抗體(貨號:WB2197,上海威奧有限公司);ECL檢測試劑盒(貨號:KL-D3095,上海康朗有限公司)。
1.2 方法
1.2.1建模:隨機選取50只大鼠,通過腹腔注射3%戊巴比妥納麻醉大鼠,行雙側卵巢切除術,術畢逐層縫合傷口,并肌肉注射5萬U青霉素鈉以預防感染。將大鼠放回籠內,常規飼養12周,用小動物骨密度儀檢測大鼠骨密度,若骨密度顯著低于造模前則視為骨質疏松模型構建成功。然后經腹腔注射3%戊巴比妥納麻醉大鼠,暴露左側股骨,將股骨中段橫行鋸斷,用克氏針固定后,生理鹽水沖洗,術畢逐層縫合傷口,造模過程中死亡3只,其余均建模成功。
1.2.2分組及給藥:隨機選取成功建模大鼠40只,并隨機分為模型(MO)組,富血小板血漿(PP)組,玻璃酸鈉(SH)組,富血小板血漿聯合玻璃酸鈉(PS)組,每組10只,取剩余10只健康大鼠作為正常(NO)組,對PP組骨折斷端注射0.2 mL/只富血小板血漿,對SH組骨折斷端注射10 mg/kg玻璃酸鈉,對PS組骨折斷端注射0.2 mL/只富血小板血漿及10 mg/kg玻璃酸鈉,兩組均每天給藥1次,治療2個月,NO組、MO組同期對骨折斷端注射同體積生理鹽水。
1.2.3標本采集:實驗完成后,經腹腔注射3%戊巴比妥納麻醉處死大鼠,取靜脈血,離心取上清液于無菌離心管中,在冰箱中密封保存。然后取1 cm骨折端骨痂組織用小動物骨密度儀檢測骨密度,檢測完成后,取左側股骨,用生物力學試驗機檢測骨生物力學。檢測完成后,在含4%多聚甲醛溶液中固定48 h,10%乙二胺四乙酸脫鈣14 d,進行常規石蠟包埋、切片后,放入冰箱中密封保存。
1.2.4HE染色:取各組股骨組織,脫蠟、復水后,流水沖洗1 min,蘇木素染色30 s,流水沖洗5 min,分色、返藍處理后,流水沖洗5 min,伊紅染色3 min,PBS洗滌3次,脫水、透明、中性樹膠封片后,在光學顯微鏡下觀察,選8個視野觀察新生血管情況,收集血管面積及新生血管數。
1.2.5ELISA檢測:取各組大鼠血清,檢測血管內皮生長因子(vascular endothelial growth factor,VEGF)、堿性成纖維細胞生長因子(basic fibroblast growth factor,bFGF)、血管生成素-1(angiopoietin-1,ANG-1)等血管形成相關因子,實驗步驟嚴格按試劑盒說明書進行操作,實驗完成后,通過標準曲線,計算VEGF、bFGF、ANG-1的含量。
1.2.6免疫印跡檢測:取各組股骨組織,加入少許液氮研磨成勻漿后,加入RIPA裂解液,4 ℃搖床過夜裂解,離心取上清液,用BCA法提取細胞核蛋白,變性后進行電泳、轉膜處理,洗滌液洗滌后封閉2 h,加入稀釋的NFATc1、破骨細胞關聯受體(osteoclast associated receptor,OSCAR)一抗(1∶1 000),4 ℃孵育過夜,洗膜,加入稀釋的二抗(1∶5 000),37 ℃孵育2 h,洗膜,ECL試劑盒測定結果后,計算與GAPDH比值求得NFATc1、OSCAR蛋白表達。
1.3 統計學
采用GraphPad Prism8.0對各組大鼠骨愈合、血管生成、NFATc1信號通路相關指標進行統計分析,組間進行t檢驗、多組間比較采用單因素方差分析,描述采用均數±標準差,P<0.05表示差異有統計學意義。
2 結果
2.1 各組大鼠骨密度及骨生物力學結果
與NO組相比,MO組骨密度、剛度、最大載荷、最大壓強、彈性模量顯著降低(P<0.05),與MO組相比,PP、SH、PS組骨密度、剛度、最大載荷、最大壓強、彈性模量明顯升高(P<0.05),且SH、PP組比較無明顯差異(P>0.05),PS組比SH組升高明顯(P<0.05),這說明富血小板血漿聯合玻璃酸鈉可顯著改善骨質疏松性骨折大鼠骨密度及骨生物力學,見表1。
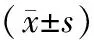
表1 各組大鼠骨密度及骨生物力學比較
2.2 各組HE染色結果
NO組股骨組織結構正常,骨小梁生長旺盛,可見大量成熟骨組織,MO組股骨組織遭到破壞,骨小梁明顯減少,骨密質明顯變薄,與MO組比較,PP、SH、PS組病理結構明顯改善,骨小梁變粗變密,空骨陷窩明顯減少,這說明富血小板血漿聯合玻璃酸鈉可顯著改善骨質疏松性骨折大鼠骨組織病理形態,見圖1。

圖1 各組大鼠骨組織HE染色(×200倍)
2.3 各組大鼠股骨組織血管生成結果
與NO組相比,MO組血管數量及血管面積明顯降低(P<0.05),與MO組相比,PP、SH、PS組血管數量及血管面積明顯升高(P<0.05),且SH、PP組比較無明顯差異(P>0.05),PS組比SH組升高明顯(P<0.05),這說明富血小板血漿聯合玻璃酸鈉可顯著促進骨質疏松性骨折大鼠血管生成,見表2。
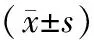
表2 各組大鼠股骨組織血管數量及血管面積比較
2.4 各組大鼠血清血管形成相關因子水平結果
與NO組比較,MO組血清VEGF、bFGF、ANG-1水平明顯降低(P<0.05),與MO組相比,PP、SH、PS組血清VEGF、bFGF、ANG-1水平明顯升高(P<0.05),且SH、PP組比較無明顯差異(P>0.05),PS組比SH組升高明顯(P<0.05),這說明富血小板血漿聯合玻璃酸鈉可顯著促進骨質疏松性骨折大鼠血管生成,見表3。

表3 各組大鼠血清中血管形成因子水平比較
2.5 各組大鼠骨組織NFATc1信號通路蛋白表達結果
與NO組比較,MO組骨組織NFATc1、OSCAR蛋白表達明顯升高(P<0.05),與MO組比較,PP、SH、PS組股骨組織NFATc1、OSCAR蛋白表達明顯降低(P<0.05),且SH、PP組比較無明顯差異(P>0.05),PS組比SH組降低明顯(P<0.05),這說明富血小板血漿聯合玻璃酸鈉可顯著抑制骨質疏松性骨折大鼠NFATc1信號通路,見表4、圖2。

圖2 各組大鼠骨組織NFATc1、OSCAR蛋白表達電泳圖
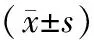
表4 各組大鼠股骨組織NFATc1、OSCAR蛋白表達比較
3 討論
眾所周知,骨質疏松患者骨強度較低,發生骨折后多為粉碎性,這使得OPF患者不僅骨愈合能力差,也極易發生內固定松動及再骨折情況,故OPF也是患者致殘、致死的主要原因。因此,如何促進骨折愈合、防止再骨折情況的發生是目前醫學領域亟待解決的問題[10]。近年來,富血小板血漿因其制備簡單、價格低廉、安全性高的優點被廣泛應用于臨床,在骨折治療方面也取得了令人滿意的效果。研究發現,其可提供一種富含生長因子的微環境,從而更有利于促進成骨、破骨細胞的增殖及遷移,進而加快骨折的修復與重建,促進骨愈合[11]。玻璃酸鈉是一種高分子多糖體生物材料,具有抗感染、潤滑關節、防止軟骨基質破壞、維持骨生物力學及鎮痛等多種生理功能,由此可見其在治療OPF方面應該具有一定前景[12]。通過將富血小板血漿與玻璃酸鈉聯合使用,可以起到互補作用,從而更利于達到促進骨折愈合和骨重建的目的。因此,本研究選擇富血小板血漿與玻璃酸鈉聯用進行實驗,以期為臨床提供更多治療方案。本研究發現,富血小板血漿聯合玻璃酸鈉對OPF大鼠具有顯著療效,可顯著促進骨折愈合。對于OPF大鼠,富血小板血漿聯合玻璃酸鈉可能是通過多途徑、多功能,來促進成骨細胞增殖,抑制破骨細胞功能,從而刺激細胞有絲分裂,促進骨基質細胞分化,誘導軟骨基質合成,進而促進骨形成,抑制骨吸收,達到促進骨痂生成的目的,最終有效促進骨折愈合。黃星等[13]研究表明,對于OPF大鼠,富血小板血漿具有顯著效果,可顯著促進骨折愈合,這與本研究結果類似。
骨折的修復和再生是一個復雜的生物學過程,而大量研究已經證實,骨愈合需要血管生成過程,故促進血管生成是促使骨折愈合的首要條件,其不僅可以參與膜內成骨和膜外化骨,還可以保證良好的血供,為骨折愈合提供有利條件,因此如何促進血管生成已經成為近年來骨科領域關注的焦點之一[14]。VEGF、bFGF、ANG-1是促進新生血管生成的重要因子,在血管生成中扮演著重要角色,其可調控多種信號通路,從而加速血管內皮等細胞增殖,促進新生血管生成,因此檢測其水平的變化可有效反映血管生成情況[15]。本研究結果表明,富血小板血漿聯合玻璃酸鈉可顯著提高骨組織血管數量及血管面積,并升高血清VEGF、bFGF、ANG-1含量,這說明其可顯著促進OPF大鼠血管生成。對于OPF大鼠,富血小板血漿聯合玻璃酸鈉可能是通過提供骨折愈合所需要的生長因子及營養,從而為組織修復提供了一個載體及框架,進而加快VEGF、bFGF、ANG-1等促血管生成因子的分泌,加快骨質礦化,加快細胞外基質及纖維合成等,最終達到促進血管生成,加快骨折愈合的目的。袁園等[16]研究發現,富血小板血漿可促進缺血下肢血管生成,從而促進其血流恢復,與本研究結果相似。
近年來研究發現,破骨細胞過度激活是骨質疏松患者易發生骨折的根本原因,其可造成骨吸收和重建的不平衡,從而導致骨微結構遭到破壞,進而導致骨量減少,骨強度下降,最終導致骨折,因此如何抑制破骨細胞過度激活是目前臨床研究的關鍵所在[17-18]。NFATc1信號通路作為調控破骨細胞功能的網絡中心,其在破骨細胞形成及分化過程中發揮著極為重要的作用,因此臨床對其越來越關注及重視[19]。本研究結果發現,富血小板血漿聯合玻璃酸鈉可顯著抑制股骨組織NFATc1、OSCAR蛋白表達,這說明其可顯著抑制OPF大鼠NFATc1信號通路。而對于OPF大鼠,富血小板血漿聯合玻璃酸鈉可能是通過調節相關基因表達,來介導細胞信號轉換,從而抑制NFATc1信號通路的激活,抑制破骨細胞活性及骨基質降解,進而抑制骨吸收,促進骨形成,最終有效促進骨愈合。王琮仁等[20]研究發現,對于OPF大鼠,阿托伐他汀可顯著促進骨愈合,其作用機制可能與抑制NFATc1信號通路有關,這與本研究結果相似。
綜上所述,富血小板血漿聯合玻璃酸鈉對骨質疏松性骨折大鼠具有顯著療效,可有效促進骨愈合及血管生成,并抑制NFATc1信號通路。但本研究仍存在一定的問題,由于時間原因,未深入到細胞層面,也未進行更多信號通路及指標的研究。后續會逐步展開進一步的深入研究,以期為臨床提供更多、更有利的診療依據。

