經(jīng)皮穴位電刺激對去勢后大鼠血清骨代謝平衡的影響
鄭小花 徐穎 林超琴 胡德婷 鄭啟斌
1.福建省婦幼保健院 福建醫(yī)科大學婦兒臨床醫(yī)學院,福建 福州 350001
2.中國人民解放軍聯(lián)勤保障部隊第九○○醫(yī)院倉山院區(qū)婦產(chǎn)科,福建 福州 350025
3.福建醫(yī)科大學附屬第一醫(yī)院神經(jīng)外科,福建 福州 350001
4.福建醫(yī)科大學附屬第一醫(yī)院濱海院區(qū)國家區(qū)域醫(yī)療中心神經(jīng)外科,福建 福州 350212
絕經(jīng)后骨質(zhì)疏松癥(postmenopausal osteoporosis,PMOP)是原發(fā)性骨質(zhì)疏松癥(osteoporosis,OP)中最常見的一種類型,常發(fā)生于女性絕經(jīng)后 5~10 年內(nèi)[1]。目前我國OP患病人數(shù)約為9 000萬,女性約7 000萬[2]。2023年國家統(tǒng)計局發(fā)布2022年末我國60歲及以上人口占19.8%,65歲及以上占14.9%[3]。人口的老齡化使PMOP在女性中的患病率快速攀升。PMOP最嚴重的后果是骨質(zhì)疏松性骨折,更年期的女性發(fā)生較嚴重的骨折后的剩余壽命較發(fā)生乳腺癌后的剩余壽命要短[4]。高發(fā)病率及其并發(fā)癥的高致殘率、高致死率等問題使PMOP成為我國醫(yī)療衛(wèi)生面臨的重大挑戰(zhàn),亟需有效的PMOP防治措施[5]。電刺激作為一種傳統(tǒng)安全且經(jīng)濟有效的康復治療手段在OP的應用較多,經(jīng)皮穴位電刺激(transcutaneous electrical acupoint stimulation,TEAS)治療可緩解疼痛、增強肌力、促進神經(jīng)修復,改善肢體功能[6]。TEAS 是以經(jīng)絡穴位理論為指導,并結(jié)合經(jīng)皮神經(jīng)電刺激的一種物理療法[7],其將電極片貼在目標穴位對應的皮膚,設定所需要的頻率、脈寬等參數(shù)電流輸入人體,刺激人體的穴位和周圍神經(jīng)或經(jīng)絡以達到治療OP等疾病的目的,較傳統(tǒng)針灸更無創(chuàng)及可控性。本實驗通過觀察TEAS對去卵巢骨質(zhì)疏松模型大鼠血清骨代謝指標及骨密度的影響,探討不同頻率TEAS在調(diào)節(jié)骨平衡方面的療效,為其防治PMOP的機理提供實驗依據(jù)。
1 材料與方法
1.1 實驗材料
1.1.1實驗動物:32只清潔級Sprague-Dawley(SD)雌性健康大鼠,5月齡,體重為320~388 g,購于中國斯貝福(北京)生物技術有限公司[許可證號:SCXK(京)2019-0010],動物飼養(yǎng)于聯(lián)勤保障部隊第九○○醫(yī)院基礎醫(yī)學實驗室實驗動物中心,并由實驗動物中心提供專用飼料飼養(yǎng),通風良好的潔凈層流環(huán)境(SPF級環(huán)境),室溫18 ℃~25 ℃,模擬晝夜各12 h的光照,相對濕度(50±5)%,每周更換2次墊。自由攝食和飲潔凈水,所有進入實驗室的物品均嚴格高溫消毒或紫外線消毒處理。本實驗依照實驗動物管理委員會指導方案進行實驗及管理,已得到福建省婦幼保健院動物實驗倫理委員會的批準(倫理號:2021KLD667)。
1.1.2主要儀器與試劑:LGT-231手持神經(jīng)肌肉電刺激儀(廣州龍之杰科技有限公司),雙能X線骨密度儀(美國HOLOGIC DISCOVERY W型);上海西唐生物科技有限公司ELISA檢測試劑盒:骨特異性堿性磷酸酶(BALP)、Ⅰ型原膠原C端前肽(PICP)、Ⅰ型原膠原N端前肽(PINP)、Ⅰ型膠原羧基端肽(ICTP)、吡啶啉(Pyr)、脫氧吡啶啉(D-Pyr)。
1.2 實驗方法
1.2.1分組與造模:SD大鼠適應性生長1周后采取隨機編號,分為假手術組(Sham組)、OVX 組(模型對照組)、2 Hz組(0VX+TEAS 2 Hz組)、50 Hz組(0VX+TEAS 50 Hz組)。后3組均進行卵巢去勢骨質(zhì)疏松模型的建立:采用國內(nèi)外公認的雌性大鼠PMOP模型[8]。術前注射10%水合氯醛溶液麻醉(0.2 mL/100 g體質(zhì)量),無菌操作下摘除大鼠雙側(cè)卵巢,Sham組則只切除卵巢附近等體積的脂肪,術后縫皮封口,每日觀察大鼠皮膚傷口情況,碘伏消毒傷口,根據(jù)傷口情況腹腔注射青霉素G 5萬~10萬單位,1 次/d,連續(xù) 3 d,防止術后感染。
1.2.2干預方法:造模后1個月2 Hz 組、50 Hz 組大鼠背部進行消毒,剃毛、脫毛,暴露出需要貼電極片的皮膚,根據(jù)大鼠穴位圖譜,在大鼠背部“命門穴”(雙側(cè))、“環(huán)跳穴”(雙側(cè))相應的部位粘上電極片(電極片定期更換),LGT-231手持神經(jīng)肌肉電刺激儀,調(diào)整相應頻率,電流強度設置為大鼠局部肌肉輕度收縮為度,4~10 mA,治療時間為 30 min,每日1次,每周治療 5 d休息2 d,連同休息日,共12周。Sham組、OVX組不予TEAS治療及其他干預,同實驗組一同飼養(yǎng)、管理。
1.2.3指標檢測:3個月后左心室采血并處死各組大鼠,全血室溫放置30 min后離心10 min,取上層血清于無菌凍存管中,行ELISA測定,按照各定量測定試劑盒操作規(guī)程進行,所有樣品同批次測定,以避免批間誤差。分離出腰椎和右側(cè)股骨,剝除附著的軟組織,用經(jīng)生理鹽水浸透的醫(yī)用紗布包裹右側(cè)股骨和椎骨,放置于-80 ℃冰箱中保存待用。檢測時將解凍后的骨樣本整齊地擺放在檢測床上開始檢測,用雙能X線骨密度儀對大鼠第4~6腰椎及右股骨頸Ward’s三角區(qū)BMD進行測量。選擇大鼠骨密度高分辨模式,行間距0.070 0 cm,點分辨率0.062 2 cm,6.10×0.10 Coll,140/100kVp。結(jié)果用g/cm2表示。
1.3 統(tǒng)計學方法
采用 SPSS 20.0 軟件進行統(tǒng)計分析,組間比較采用單因素方差分析進行方差齊性檢驗,正態(tài)分布且方差齊者采用LSD檢驗,方差不齊者采用Games-Howell檢驗,非正態(tài)分布數(shù)據(jù)采用非參數(shù)檢驗(秩和檢驗),結(jié)果均以均值±標準差表示,檢驗水準 ɑ=0.05,P<0.05為差異有統(tǒng)計學意義。
2 結(jié)果
2.1 各組大鼠骨形成標志物
OVX組較Sham組血清BALP、PICP、PINP均顯著增高(P<0.05),TEAS 2 Hz組較OVX組血清BALP、PICP、PINP均顯著降低(P<0.05),且與Sham組無差別;50 Hz組較OVX組相比無顯著變化,與Sham組相比血清BALP、PINP升高,PICP與Sham組無差別(P=0.336)。2 Hz組較50 Hz組相比差異均無統(tǒng)計學意義,見表1。
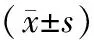
表1 各組大鼠血清骨形成標志物比較
2.2 各組大鼠骨吸收標志物
OVX組較Sham組血清ICTP、Pyr、D-Pyr均顯著增高(P<0.05),TEAS 2 Hz組、50 Hz組較OVX組血清ICTP、Pyr、D-Pyr均顯著降低(P<0.05),TEAS 50 Hz組較Sham組血清ICTP、Pyr、D-Pyr無明顯區(qū)別(P>0.05),2 Hz較50 Hz組差異無統(tǒng)計學意義(P均>0.05),見表2。
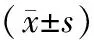
表2 各組大鼠血清骨吸收標志物比較
2.3 腰椎及右股骨骨密度的影響
OVX組較Sham組腰椎及右股骨骨密度均顯著降低(P<0.05 ),TEAS 2 Hz組較OVX組腰椎及股骨骨密度均顯著增高(P<0.05),且腰椎骨密度較Sham組無差異;TEAS 50 Hz組較Sham組顯著降低(P<0.05 ),較OVX組骨密度無區(qū)別,2 Hz腰椎骨密度較50 Hz組高(P=0.048),但股骨骨密度均無區(qū)別,見表3。
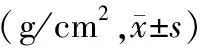
表3 各組大鼠腰椎及右股骨骨密度比較
3 討論
PMOP是由于女性絕經(jīng)后雌激素缺乏,進而引起骨代謝紊亂,導致骨量丟失、BMD下降及骨微結(jié)構(gòu)破壞、骨折風險增加的全身代謝性骨病。骨組織通過骨重塑的過程不斷發(fā)生變化[9]。PMOP是一種高轉(zhuǎn)換代謝型骨病,骨吸收率大于骨形成率,從而導致骨丟失。細胞因子、骨吸收標志物、骨形成標志物、基因、受體等決定骨代謝的內(nèi)環(huán)境和代謝調(diào)節(jié)過程,而且也是決定骨質(zhì)量、骨強度的重要因素[10]。骨形成標志物反映成骨細胞活性及骨吸收水平,骨吸收標志物反映破骨細胞活性及骨形成狀態(tài)。推薦敏感性較高的骨形成標志物包括BALP、PICP、PINP等,以及骨吸收標志物主要包括ICTP、Pyr、D-Pyr等[11]。既往臨床及實驗研究證實TEAS在OP中治療有效,本實驗通過骨形成及骨吸收標志物探討TEAS在骨轉(zhuǎn)換生化標志物中的作用,以期探討其抗OP機制。
BALP是成骨細胞的一種細胞外酶,其主要作用是在成骨過程中水解磷酸酶,為羥基磷灰石的沉積提供磷酸,同時水解焦磷酸鹽,有利于成骨[11]。高轉(zhuǎn)換型骨質(zhì)疏松、骨折患者中,血清BALP明顯升高。本實驗中,與Sham組相比,OVX組術后3個月BALP顯著升高,體現(xiàn)了OVX造模術后呈高轉(zhuǎn)換代謝型OP模型。TEAS 2 Hz干預后較OVX組相比降低,50 Hz無明顯變化,說明2 Hz TEAS可能參與BALP的調(diào)節(jié)促進骨形成。血清Ⅰ型前膠原水解,去除其羧基及氨基端的附加肽段,生成原膠原,前膠原去除下來的羧基端附加肽段稱PICP,氨基端附加肽段稱PINP。PICP、PINP由成骨細胞合成,其在血清中的含量反映成骨細胞合成骨膠原的能力,即Ⅰ型膠原的合成速率,是新骨形成的特異性的敏感指標[12]。TEAS 2 Hz組PINP、PICP較OVX組降低,體現(xiàn)了TEAS可能通過促進PICP、PINP從而促進Ⅰ型膠原的合成,干預OP的過程。
本研究結(jié)果顯示,OVX大鼠 ALP、PINP、PICP等較Sham組升高,提示模型組大鼠骨代謝處于高轉(zhuǎn)換狀態(tài),成骨細胞代謝活躍所致。經(jīng)電刺激干預后,TEAS 2 Hz組較OVX組血清BALP、PICP、PINP均顯著降低(P<0.05),且與Sham組無差別,提示其參與骨形成過程,且促進新骨的形成療效顯著,可能通過骨形成途徑。結(jié)論與其他學者一致,如王巧靈[13]予補腎壯骨湯聯(lián)合針灸對骨質(zhì)疏松患者進行治療,ALP、PINP均低于對照組。Wiesmann等[14]研究顯示,電刺激能明顯調(diào)節(jié)成骨細胞的增殖及分化,進而影響骨代謝和重建,達到抑制骨吸收,促進骨形成和逆轉(zhuǎn)骨質(zhì)疏松的作用。50 Hz組血清骨形成標志物與OVX組相比無顯著變化,但血清BALP、PINP與Sham組相比,差異有統(tǒng)計學意義,且50 Hz TEAS干預后與OVX組相比腰椎、股骨骨密度均未增加,提示其可能未參與骨形成過程。
ICTP是Ⅰ型膠原在骨吸收過程中的降解產(chǎn)物之一,是骨吸收的特異及敏感的生化指標,同時不受飲食和腎濾過率的影響,是反映破骨細胞膠原降解的重要指標[15]。Pyr和D-Pyr是骨Ⅰ型膠原的特異組分,在骨膠原合成膠原纖維時,骨溶解時在羥賴氨酰氧化酶的作用下,由骨膠原分子蛋白水解釋放出來,進入血循環(huán),排入尿中[16]。Pyr和D-Pyr幾乎僅存在于骨骼和牙組織中,在血液和尿中以游離和肽結(jié)合形態(tài)存在。以上3種骨吸收標志物能夠及時直觀地反映骨溶解程度和敏感反應骨丟失范圍。本實驗中OVX組術后ICTP、Pyr、D-Pyr均高于Sham組,說明OVX術后破骨細胞的骨吸收活性增強,骨丟失增加,但經(jīng)TEAS治療后兩組骨吸收指標均較OVX組降低,且與Sham組無區(qū)別,TEAS可能通過調(diào)節(jié)骨吸收標志物干預骨代謝平衡,增加腰椎、股骨骨密度以達到抗PMOP的作用。
2020年發(fā)布的《中醫(yī)藥防治原發(fā)性骨質(zhì)疏松癥專家共識》中明確指出針刺、穴位貼敷法可有效緩解骨質(zhì)疏松性疼痛[17]。電針是應用中醫(yī)理論,用針刺入腧穴得氣后,在針上連接人體生物電的微量電流波以加強持續(xù)刺激穴位,從而達到治療疾病的一種療法。TEAS 兼具針刺及低頻電刺激的療效,通過刺激肌纖維的收縮帶動骨骼肌的運動,提高肌肉的質(zhì)量,維持對骨的應力刺激,促進骨重建[18]。TEAS能避免患者對傳統(tǒng)針刺疼痛的顧慮,依從性好。時克昌等[19]的臨床研究證實,TEAS可改善骨質(zhì)疏松癥狀,但其未闡述相關作用機制。本實驗TEAS組ALP、PINP、PICP等較OVX組低,同時ICTP、Pyr、D-Pyr降低,提示可能通過骨代謝平衡參與其調(diào)節(jié)OP。
低頻電的參數(shù)包括頻率、周期、波寬、通斷比、波形等,臨床儀器中很多參數(shù)相對固定,對生物效應影響較大的是頻率及強度[20],陳善堂等[21]指出固定頻率(15 Hz)脈沖電磁場在1.10~4.10 mT的強度下對小鼠MC3T3-E1細胞的增殖能力無明顯影響,因此對頻率的可調(diào)節(jié)性及爭議也較大。低頻電流式指頻率1 000 Hz以下的脈沖電流,每次通電能使運動神經(jīng)發(fā)生興奮,超過1 000 Hz則不能引起興奮。臨床常用的低頻電是在100 Hz以下。有學者將電極連接到100 MHz任意波形發(fā)生器以各種頻率(1、2.5、5、10、15、20、30、40、50、60和100 Hz)行電刺激,探討動態(tài)骨骼肌電刺激在刺激肌肉收縮、誘導骨骼髓內(nèi)壓變化的最佳頻率。發(fā)現(xiàn)在20、50 Hz肌肉電刺激時股骨骨小梁質(zhì)量改善更明顯[22]。但Swift等[23]對脊髓損傷患者股四頭肌、腘繩肌和臀肌進行連續(xù)性刺激電刺激(50 Hz),結(jié)果發(fā)現(xiàn)腰椎和股骨頸區(qū)域的BMD均無變化。本實驗中選擇TEAS頻率為2 Hz及50 Hz,是文獻報道比較常見的兩種頻率,以此作為低頻率及中高頻的代表,結(jié)果證實這兩種頻率均有參與血清骨代謝的調(diào)節(jié),2 Hz的TEAS均可降低骨形成標志物BALP、PINP、PICP及骨吸收標志物ICTP、Pyr、D-Pyr,50 Hz僅降低骨吸收標志物,表明2 Hz TEAS參與骨吸收及骨形成過程,且干預后腰椎及股骨BMD均升高,50 Hz TEAS只參與骨吸收過程,且50 Hz干預的大鼠的骨密度并未升高,考慮2 Hz頻率的TEAS可能更有利于臨床抗OP的治療。
在電針治療中,多數(shù)文獻報道的頻率低于10 Hz,結(jié)論均提示抗OP效果顯著。如柏中喜等[24]以電脈沖頻率2 Hz(120 r/min),強度為1 mA行經(jīng)皮穴位電刺激,發(fā)現(xiàn)增加絕經(jīng)后骨質(zhì)疏松癥大鼠模型的骨密度及生物力學。經(jīng)皮電刺激的治療模式中針灸樣刺激頻率是1~4 Hz,脈沖寬度是0.2~0.3 ms,出現(xiàn)脈沖式肌肉抽搐,適用于急慢性疼痛、長期止痛及周圍循環(huán)障礙。絕經(jīng)后肌肉骨關節(jié)癥狀常見肩、頸腰背部肌肉和肌腱疼痛,肩、膝、腰骶關節(jié)和手指關節(jié)等部位的疼痛,常伴有骨關節(jié)炎[25]。因此2 Hz頻率的TEAS可能較50 Hz頻率更適合緩解PMOP引起的急慢性骨關節(jié)肌肉疼痛癥狀。
綜上所述,本研究采用TEAS干預PMOP大鼠模型,結(jié)果提示2 Hz TEAS參與骨吸收及骨形成過程,且干預后腰椎及股骨BMD均升高,50 Hz TEAS只參與骨吸收過程,且50 Hz干預的大鼠的BMD并未升高,考慮TEAS改善 PMOP 可能與其參與血清骨轉(zhuǎn)化標志物調(diào)節(jié)骨平衡代謝有關,且2 Hz頻率的TEAS可能更有利于臨床抗OP的治療。本實驗初步探討了TEAS改善PMOP及方案,為TEAS防治PMOP的臨床應用提供了理論依據(jù)。

