上皮性卵巢癌患者腫瘤細(xì)胞減滅術(shù)術(shù)后復(fù)發(fā)的影響因素
沈冰燕,沈 謙,徐玲玲
(江蘇省啟東市婦幼保健院 婦產(chǎn)科,江蘇 啟東,226299)
卵巢癌為婦科常見的惡性腫瘤,其為婦科惡性腫瘤患者死亡的主要原因[1]。卵巢癌臨床癥狀特異性較差,因此在早期難以被發(fā)現(xiàn)和診斷,而晚期卵巢癌因?yàn)閺?fù)發(fā)率較高[2-3],導(dǎo)致預(yù)后較差,因此尋找有效治療方法降低卵巢癌復(fù)發(fā)概率及改善卵巢癌預(yù)后、延長(zhǎng)患者生存期限為婦科腫瘤學(xué)者們關(guān)注的重點(diǎn)問題。腫瘤細(xì)胞減滅術(shù)(CRS)指比較大的腫瘤或是腫瘤產(chǎn)生一些顯著的壓迫癥狀,且無(wú)法完全切除腫瘤、通過切除部分腫瘤減輕癥狀,減輕腫瘤負(fù)荷的手術(shù)[4]。利用細(xì)胞減滅術(shù)治療卵巢癌,可以使體內(nèi)殘留癌細(xì)胞得到殺滅或是抑制,可延長(zhǎng)患者生存期。但是也有研究[5-6]發(fā)現(xiàn),該種模式治療下的卵巢癌患者1年內(nèi)復(fù)發(fā)率較高,爭(zhēng)議較多。1年內(nèi)復(fù)發(fā)的原因主要與術(shù)前患者分期、手術(shù)結(jié)局、術(shù)后化療等危險(xiǎn)因素有關(guān)。基于此,本研究探討術(shù)前新輔助化療聯(lián)合CRS治療卵巢癌患者術(shù)后1年復(fù)發(fā)的獨(dú)立危險(xiǎn)因素。
1 資料與方法
1.1 一般資料
選取 2018年 6 月—2021年6月行CRS治療的卵巢癌患者90例為研究對(duì)象。所有患者均在化療結(jié)束后隨訪1年,以是否復(fù)發(fā)將90例卵巢癌患者分為復(fù)發(fā)組(54例)和無(wú)復(fù)發(fā)組(36例)。
1.2 方法
所有患者均采用CRS治療,手術(shù)包含闌尾與轉(zhuǎn)移灶、大網(wǎng)膜、全子宮雙附件等,并聯(lián)合采用TC方案進(jìn)行術(shù)前新輔助化療,術(shù)后1個(gè)月采用紫杉醇+卡鉑(TC方案) 化療:第1天采用紫杉醇(北京協(xié)和藥廠,LLC,批準(zhǔn)文號(hào)H10980068) 135~175 mg/m2,卡鉑(昆明貴研藥業(yè)有限公司生產(chǎn),國(guó)藥準(zhǔn)字H20053908 ); 第2天采用靜脈滴注生理鹽水,1個(gè)療程為3周,共治療3個(gè)療程。化療結(jié)束后隨訪1年。
1.3 觀察指標(biāo)
比較2組的一般資料(年齡、分期等,其中分期按照國(guó)際婦產(chǎn)科聯(lián)合會(huì)FIGO進(jìn)行)、術(shù)式(開腹、腹腔鏡等)等情況,然后利用多元回歸分析來對(duì)上皮性卵巢癌患者CRS化療結(jié)束后隨訪1年復(fù)發(fā)的獨(dú)立危險(xiǎn)因素進(jìn)行分析,并以相關(guān)危險(xiǎn)因素建立卵巢癌CRS治療預(yù)后的預(yù)測(cè)模型。
本研究采用FIGO分期,按照腫瘤在盆腹腔的侵犯程度以及是否遠(yuǎn)處轉(zhuǎn)移,分為Ⅰ~Ⅳ期。卵巢癌腫瘤局限在卵巢為Ⅰ期,當(dāng)擴(kuò)散到盆腔臟器時(shí)為Ⅱ期,侵犯腹腔內(nèi)臟器時(shí)則為Ⅲ期,如出現(xiàn)遠(yuǎn)處轉(zhuǎn)移,比如肺、胸腔、肝、骨轉(zhuǎn)移時(shí)為Ⅳ期。
1.4 統(tǒng)計(jì)學(xué)分析

2 結(jié) 果
2.1 2組一般資料比較
90例上皮性卵巢癌患者均采用術(shù)前新輔助化療,術(shù)后紫杉醇加卡鉑化療,從化療結(jié)束后開始隨訪,隨訪1年,復(fù)發(fā)54例,復(fù)發(fā)率為60.00%。2組一般資料比較,差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05)。見表1。

表1 2組患者的一般資料比較[n(%)]
2.2 2組術(shù)前分期比較
術(shù)前,復(fù)發(fā)組高分期患者占比高于未復(fù)發(fā)組,差異有統(tǒng)計(jì)學(xué)意義(P<0.05)。見表2。

表2 2組患者的術(shù)前分期比較[n(%)]
2.3 術(shù)式和術(shù)中淋巴結(jié)的清掃
采用開腹或是腹腔鏡CRS治療,復(fù)發(fā)組和無(wú)復(fù)發(fā)組比較,差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05)。無(wú)復(fù)發(fā)組患者清掃淋巴結(jié)比例高于復(fù)發(fā)組,差異有統(tǒng)計(jì)學(xué)意義(P<0.05)。見表3。

表3 2組患者的術(shù)式比較[n(%)]
2.4 2組的術(shù)前部分血清指標(biāo)比較
復(fù)發(fā)組的血清CA125、HE4、CEA及AMH水平均高于無(wú)復(fù)發(fā)組,差異有統(tǒng)計(jì)學(xué)意義(P<0.05)。見表4。
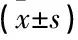
表4 2組的術(shù)前部分指標(biāo)的比較

表5 上皮性卵巢癌患者CRS術(shù)后1年復(fù)發(fā)的多因素非條件Logistic回歸分析
2.5 2組術(shù)前新輔助化療次數(shù)
復(fù)發(fā)組的術(shù)前新輔助化療次數(shù)為(3.23±1.21)次,無(wú)復(fù)發(fā)組為(3.14±1.03)次。2組術(shù)前新輔助化療次數(shù)比較,差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05)。
2.6 上皮性卵巢癌患者CRS術(shù)后1年復(fù)發(fā)的影響因素分析
回歸設(shè)計(jì):為了對(duì)各個(gè)變量的綜合效應(yīng)加以正確估計(jì),混雜因素干擾結(jié)果的情況得到有效控制,文章采用似然比檢驗(yàn)分析前述單因素中P<0.05的變量,采用多因素非條件Logistic回歸分析,用逐步后退方法,以P<0.05為保留條件擬合回歸方程。此外,考慮到本研究樣本量較小,故對(duì)納入的自變量采取降維處理,即原為連續(xù)型數(shù)值變量的術(shù)前血清CA125、術(shù)前血清HE4、術(shù)前血清CEA、AMH等,均參考2組總均值或中位數(shù)轉(zhuǎn)化為二分類變量,多分類變量也適當(dāng)合并成二分類,以提高回歸的穩(wěn)健性。
分析結(jié)果,最終被納入回歸模型的因素有:術(shù)前分期、清掃淋巴結(jié)及術(shù)前血清CA125、術(shù)前血清HE4、術(shù)前血清CEA、AMH等指標(biāo)。年齡、術(shù)前分期、清掃淋巴結(jié)及術(shù)前血清CA125、HE4、CEA、AMH均為上皮性卵巢癌患者CRS術(shù)后1年復(fù)發(fā)的影響因素(因果關(guān)系)或關(guān)聯(lián)影響因素(果因關(guān)系)(P<0.05)。見表5。
2.7 評(píng)估上皮性卵巢癌患者CRS術(shù)后1年內(nèi)復(fù)發(fā)的預(yù)測(cè)價(jià)值
進(jìn)一步探討上述4個(gè)指標(biāo)(術(shù)前血清CA125、HE4、CEA、AMH等)預(yù)測(cè)上皮性卵巢癌患者CRS術(shù)后1年復(fù)發(fā)中的應(yīng)用價(jià)值:以復(fù)發(fā)組54例為陽(yáng)性樣本,以未復(fù)發(fā)組36例為陰性樣本,建立ROC預(yù)測(cè)分析模型。① 單獨(dú)應(yīng)用:上述4個(gè)指標(biāo)均為臨床和既往文獻(xiàn)中所見,劃分成若干個(gè)組段,然后用軟件來擬合,得到ROC曲線后對(duì)約登指數(shù)最大值點(diǎn)加以讀取,對(duì)各項(xiàng)參數(shù)和理論閾值(適當(dāng)取整)進(jìn)行測(cè)算,并根據(jù)實(shí)測(cè)樣本對(duì)敏感度、準(zhǔn)確度和特異度加以計(jì)算。② 聯(lián)合應(yīng)用(LogP模式):以前述Logistic回歸結(jié)果,建立回歸風(fēng)險(xiǎn)評(píng)估/預(yù)測(cè)模型,以其Log[P/(1-P)]=術(shù)前血清CA125+1.276×術(shù)前血清HE4+0.979×術(shù)前血清CEA+0.840×AMH為聯(lián)合應(yīng)用的虛擬概率量指標(biāo),再行ROC分析。聯(lián)合應(yīng)用虛擬指標(biāo)的閾值系依據(jù)該Log[P/(1-P)]模型(無(wú)常數(shù)項(xiàng))計(jì)算所得,其中各指標(biāo)陽(yáng)性閾值按二分類化后的變量形式讀取,即均為1。③ 分析結(jié)果顯示:術(shù)前血清CA125、術(shù)前血清HE4、術(shù)前血清CEA、AMH等指標(biāo)單獨(dú)及聯(lián)合預(yù)測(cè)的曲線下面積(AUC,95%CI)分別為0.740(0.516~0.937)、0.730(0.467~0.990)、0.731(0.477~0.977)、0.743(0.515~0.967)和0.884(0.829~0.924)。見表6、圖1。

圖1 上皮性卵巢癌患者CRS術(shù)后1年復(fù)發(fā)的預(yù)測(cè)因素/指標(biāo)的預(yù)測(cè)評(píng)估價(jià)值

表6 上皮性卵巢癌患者CRS術(shù)后1年復(fù)發(fā)的預(yù)測(cè)因素/指標(biāo)的預(yù)測(cè)評(píng)估價(jià)值分析
3 討 論
上皮卵巢癌在女性生殖系統(tǒng)惡性腫瘤中病死率居于首位,且可能會(huì)出現(xiàn)輸卵管、大網(wǎng)膜、子宮等盆腹腔臟器的轉(zhuǎn)移[7-8]。既往研究對(duì)卵巢癌的診斷價(jià)值成果比較集中,對(duì)其CRS術(shù)后1年內(nèi)復(fù)發(fā)的危險(xiǎn)因素的研究和預(yù)測(cè)模型研究較少。本研究探討術(shù)前新輔助化療聯(lián)合CRS治療卵巢癌術(shù)后1年復(fù)發(fā)的獨(dú)立危險(xiǎn)因素及部分血液檢測(cè)指標(biāo)對(duì)化療結(jié)束后隨訪1年復(fù)發(fā)的預(yù)測(cè)評(píng)估價(jià)值。
卵巢癌屬于高齡段多發(fā)者,即隨著年齡的增高,卵巢癌的發(fā)病率和復(fù)發(fā)率均隨之升高[9-11]。因此本研究將年齡作為配比因素,以控制年齡對(duì)術(shù)后復(fù)發(fā)的混雜作用[12-13]。社會(huì)經(jīng)濟(jì)地位(SES)作為一個(gè)綜合指標(biāo),其數(shù)值的高低與多數(shù)腫瘤的發(fā)生密切相關(guān)。研究[14-16]發(fā)現(xiàn),SES往往與其他一些因素相關(guān),如地區(qū)分布、生活方式、發(fā)育情況、職業(yè)分布、營(yíng)養(yǎng)狀況、醫(yī)療保障水平、飲食習(xí)慣等,而這些因素均可能與卵巢癌的發(fā)生有關(guān)。因此,本研究將地區(qū)、職業(yè)與文化程度作為因素進(jìn)行相關(guān)性分析,結(jié)果發(fā)現(xiàn),這些因素與術(shù)后1年內(nèi)復(fù)發(fā)情況無(wú)顯著相關(guān)性。既往研究[17-19]認(rèn)為,分期、術(shù)中未清掃淋巴結(jié)等均是術(shù)后1年內(nèi)復(fù)發(fā)的主要原因。故本研究納入了術(shù)前分期和清掃淋巴結(jié)等情況作為觀察術(shù)后1年內(nèi)復(fù)發(fā)因素的指標(biāo),結(jié)果發(fā)現(xiàn),術(shù)前分期和清掃淋巴結(jié)均與上皮性卵巢癌患者CRS術(shù)后1年內(nèi)復(fù)發(fā)有相關(guān)性。本研究發(fā)現(xiàn),2組間在開腹或是腹腔鏡CRS治療方面比較無(wú)顯著差異(P>0.05),說明上皮性卵巢癌患者CRS術(shù)后1年內(nèi)復(fù)發(fā)與術(shù)式無(wú)關(guān),分析原因可能與樣本量和近年腹腔鏡手術(shù)開展較多有關(guān)。本研究發(fā)現(xiàn)年齡、術(shù)前分期、清掃淋巴結(jié)及術(shù)前血清CA125、HE4、CEA、AMH均為上皮性卵巢癌患者CRS術(shù)后1年內(nèi)復(fù)發(fā)的影響因素或關(guān)聯(lián)影響因素(P<0.05),提示應(yīng)在術(shù)前新輔助化時(shí)對(duì)術(shù)前血清CA125、HE4、CEA、AMH等指標(biāo)進(jìn)行監(jiān)測(cè)。
研究認(rèn)為AMH是CRS術(shù)后復(fù)發(fā)的獨(dú)立危險(xiǎn)因素,提示其與患者1年內(nèi)后復(fù)發(fā)密切相關(guān)。AMH是直接表征卵巢功能之一的指標(biāo),故本研究將其納入預(yù)測(cè)指標(biāo)模型。AMH是由卵巢中小卵泡的顆粒細(xì)胞分泌的一種激素,其代表卵巢的儲(chǔ)備功能,即檢查AMH可了解卵巢的儲(chǔ)備功能。當(dāng)卵巢當(dāng)中小卵泡比較多時(shí),日后可以排卵的卵泡就會(huì)越多。AMH越高,提示儲(chǔ)備功能越好; 反之,則卵巢的儲(chǔ)備功能較差。通常大于35歲的女性卵巢功能開始逐漸衰退,儲(chǔ)備功能下降。如果AMH特別低,容易發(fā)生卵巢早衰,懷孕的概率隨之較小,需及時(shí)改善卵巢功能。
綜上所述,血清CA125、HE4、CEA、AMH聯(lián)合預(yù)測(cè)上皮性卵巢癌患者CRS術(shù)后1年內(nèi)復(fù)發(fā)的AUC為0.884(0.95CI:0.829~0.924)。血清CA125、HE4、CEA、AMH聯(lián)合預(yù)測(cè)的診斷效能高,其AUC及靈敏度、特異度、準(zhǔn)確度均高于上述指標(biāo)單獨(dú)預(yù)測(cè)。

