環狀RNA調控卵巢癌及其化療耐藥的研究進展*
陳小英,柯瑤,劉夏,蘇宇婷,王聰,尹富強
(廣西醫科大學 1.基礎醫學院,2.長壽與老年相關疾病教育部重點實驗室,3.生命科學研究院與區域性高發腫瘤早期防治研究教育部重點實驗室,廣西 南寧 530021)
卵巢癌是女性生殖系統第3大惡性腫瘤,據統計,2022年我國預計有57 090例卵巢癌新發病例和39 306例卵巢癌死亡病例,病死率在女性腫瘤中穩居第5位[1]。以鉑類和紫杉烷類為主的化療是卵巢癌術后治療的主要手段,但多數晚期患者會不同程度地對化療藥物產生耐藥,導致復發和死亡[2]。卵巢癌化療耐藥的機制十分復雜,至少包括編碼基因和非編碼RNA調控及腫瘤微環境變化,涉及多藥耐藥、上皮間充質轉化(epithelial-mesenchymal transition,EMT)、細胞周期、凋亡、自噬和異常信號通路等[3-4]。因此,調控卵巢癌發生、發展的機制研究一直是基礎和臨床研究中的重點問題,并在卵巢癌治療及耐藥方面取得了一定進展,但至今仍未找到非常有效的途徑以提高卵巢癌患者的生存率。
環狀RNA(circular RNA,circRNA)是由信使RNA前體通過可變剪接形成的一類不具有5′-末端帽子和3′-末端poly(A)尾巴的單鏈共價閉合非編碼RNA,不易被核糖核酸酶降解,在多種腫瘤中顯著差異表達,可作為競爭性內源RNA(competing endogenous RNA,ceRNA)、與功能蛋白互作、翻譯成多肽和蛋白質等方式影響卵巢癌及其他腫瘤的發生、發展,正迅速成為癌癥的潛在早期分子診斷標志物和耐藥治療靶點[5]。因此,本文對已報道與卵巢癌及其耐藥調控相關的62個circRNAs進行了系統綜述,其中45個為腫瘤驅動因子,17個為腫瘤抑制因子,主要在細胞質中發揮癌基因作用;15個與順鉑和紫杉烷類化療耐藥顯著相關,9個存在于體液中具有高效診斷價值,24個與預后相關,主要影響卵巢癌細胞的凋亡、EMT、細胞周期和自噬等過程;梳理并探討了circRNA調控卵巢癌及其耐藥的分子機制,以期為后續circRNA與卵巢癌及其耐藥治療的相關研究提供新思路。
1 circRNA的形成和功能機制
本文首先系統地對circRNA的形成和功能機制進行了梳理(見圖1)。circRNA根據序列來源分為外顯子circRNA(exonic circRNA,ecircRNA)、內含子circRNA(circular intronic RNA,ciRNA)及外顯子-內含子circRNA(exon-intron circRNA,EIciRNA),其中ecircRNA包括單外顯子circRNA和多外顯子circRNA。與線性RNA相比,circRNA以外顯子來源為主,通常定位于細胞質中,而內含子和外顯子-內含子來源的circRNA通常定位于細胞核,且可定位于外泌體中,種類多,表達豐富,序列高度保守[5]。
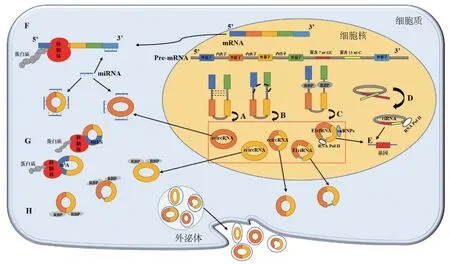
圖1 circRNA的形成機制和功能機制
1.1 circRNA形成機制
①內含子配對驅動環化:外顯子兩側的內含子反向互補配對后可變剪接形成ecircRNA或EIciRNA(見圖1A);②套索驅動環化:外顯子跳躍使被跨越的區域形成環形RNA中間體,再通過套索剪接形成ecircRNA或EIciRNA(見圖1B);③RNA結合蛋白(RNA binding proteins,RBPs)驅動環化:RNA結合蛋白的外顯子側翼與內含子緊密結合,可變剪接形成ecircRNA或EIciRNA(見圖1C);④依賴剪接體兩側保守序列的內含子套索環化:保守序列由接近5′剪接位點富含7 nt-GU的元件和接近3′分支位點富含11 nt-C的元件構成,該位點通過脫支酶避免內含子套索物降解,形成ciRNA(見圖1D)[6]。上述4種形成機制來源的circRNA中,內含子配對和套索驅動環化形成的circRNA是當前的研究熱點。
1.2 circRNA功能機制
①充當ceRNA,具有微小RNA(microRNA,miRNA)反應元件(miRNA response elements,MREs)(見圖1F);②與功能蛋白質相互作用,形成RNA蛋白質復合物(見圖1H);③調控基因轉錄,ciRNA/ecircRNA結合RNA聚合酶Ⅱ(RNA Pol Ⅱ)/U1小核核糖核蛋白(U1 small nuclear ribonucleoproteins,U1 snRNP)(見圖1E);④翻譯成多肽和蛋白質,翻譯機制可歸類為內部核糖體進入位點(internal ribosome entry site,IRES)依賴性或非依賴性,N6-甲基腺苷(N6-methyladenosine,m6A)可充當IRES(見圖1G)[5,7]。上述4大功能機制中,circRNA充當ceRNA是當前研究最多且最易在腫瘤發生、發展中發揮調控作用的功能機制。
2 circRNA 調控卵巢癌的發生、發展
基于對以往62個與卵巢癌調控相關的circRNAs系統分析,發現大多數circRNA在細胞質中發揮癌基因作用,主要通過調控細胞凋亡、EMT、細胞周期和自噬等方式影響卵巢癌增殖、遷移、侵襲和耐藥等惡性生物學行為,最終導致不良預后,且少數存在于外泌體、血清和血漿中的circRNA具有高效的卵巢癌早期診斷價值。
在本文綜述的62個circRNAs中[8-37,39-46](見圖2),circ_0078607[8]、circ_0015326[9]和circ-PGAM1[10]等29個circRNAs通過調控細胞凋亡發揮其生物學功能,circ_0000554[11]、circ-LNPEP[12]和circ-FGFR3[13]等15個circRNAs則通過調控EMT影響細胞增殖、遷移和侵襲,circ-CELSR1[14]和circ-ATL2[15]等6個circRNAs可調控細胞周期,僅有circ-MUC16[16]和circ-RAB11FIP1[17]與卵巢癌自噬調控相關,且circ-HIPK2[18]、circ-NRIP1[19]和circ_0006404[20]等15個circRNAs與卵巢癌順鉑和紫杉烷類化療耐藥相關;此外,存在于外泌體中的circ-WHSC1[21]和circ-PUM1[22]等5個circRNAs和血清中的circ-ITGB6[23]和circ-MUC16[16]等3個circRNAs以及血漿中的circ-N4BP2L2[24]經受試者工作特征曲線分析發現,其均具有高度的診斷敏感性和特異性;24個circRNAs可作為卵巢癌預后的生物標志物,其中circularRNAS-7[25]和circ-UBAP2[26]等20個circRNAs與總體生存期(overall survival,OS)顯著相關,circ-PVT1[27]和circ-SETDB1[28]等5個circRNAs與無進展生存期(progression-free survival,PFS)顯著相關,circ-FBXO7[29]和circ-PTK2[30]等5個circRNAs與無復發生存期(relapse-free survival,RFS)顯著相關,circ-Foxp1[31]與OS、RFS 和無病生存期(disease-free survival,DFS)顯著相關。
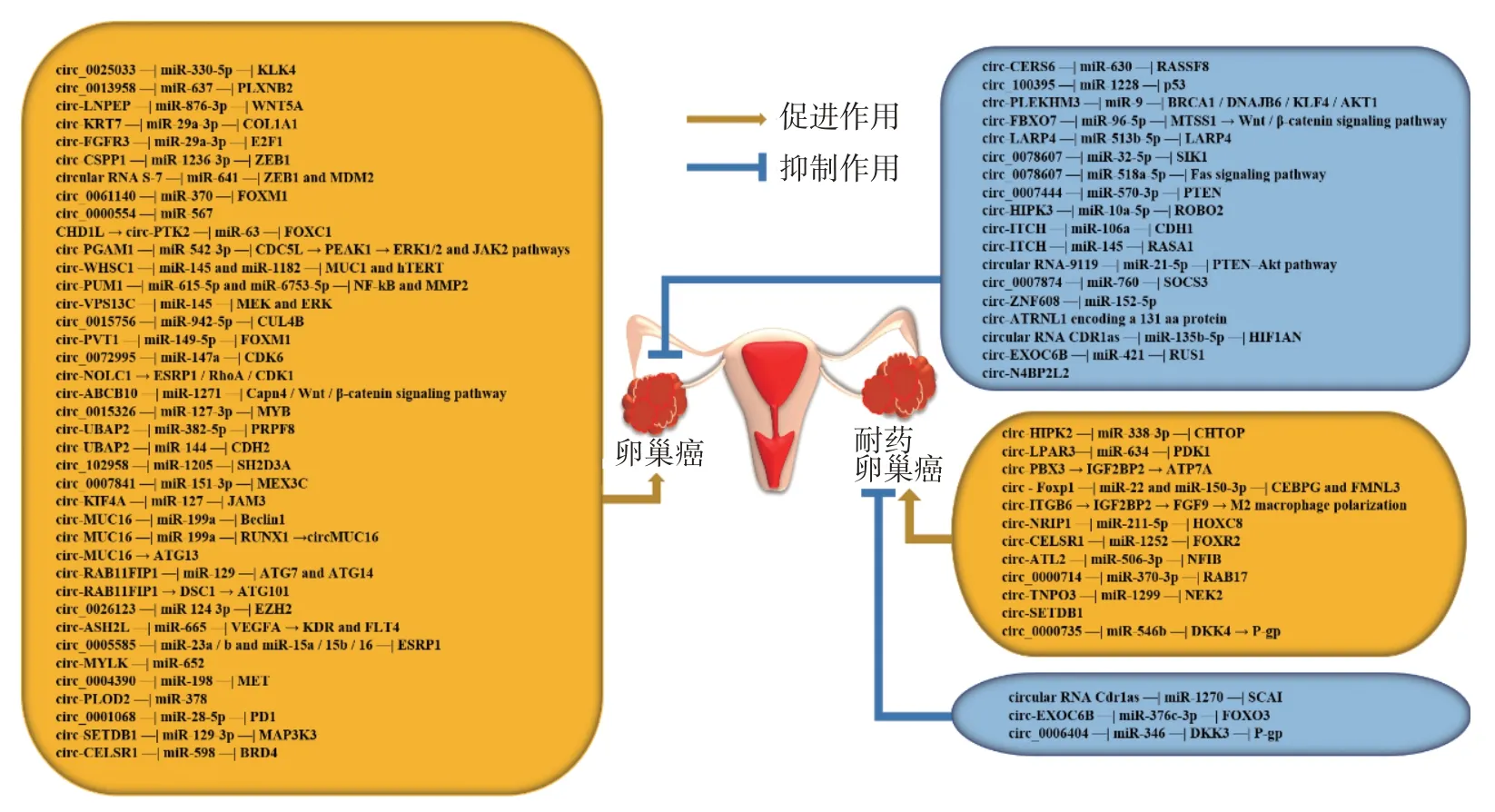
圖2 62個circRNAs在卵巢癌和耐藥卵巢癌中的作用機制
3 circRNA調控卵巢癌化療耐藥
3.1 circRNA調控卵巢癌順鉑耐藥
順鉑是卵巢癌最有效的化療藥物之一,但耐藥性很常見。本文中有6個circRNAs作為癌基因或抑癌基因參與調控卵巢癌順鉑耐藥,且有望成為卵巢癌順鉑耐藥的早期診斷和預后標志物(見圖2)。circ-HIPK2[18]、circ-LPAR3[32]、circ-PBX3[33]、circ-Foxp1[31]和circ-ITGB6[23]均在卵巢癌順鉑耐藥組織和/或細胞中高表達。敲低circ-HIPK2、circ-LPAR3可干擾相應的ceRNA調控軸,進而抑制卵巢癌順鉑耐藥細胞的增殖、遷移、侵襲能力及細胞周期和糖酵解進程,并促進細胞凋亡;而circ-PBX3和circ-ITGB6可直接通過與功能蛋白結合促進卵巢癌細胞順鉑耐藥,其中circ-ITGB6在順鉑耐藥的卵巢癌患者血清中顯著上調表達并與OS和RFS呈負相關;另外circ-Foxp1可通過作為活性蛋白和RNA載體的外泌體分泌到腫瘤微環境中促進卵巢癌順鉑耐藥,且與卵巢癌患者的OS、RFS和DFS不良預后相關。與上述不同的是,circRNA Cdr1as是卵巢癌順鉑耐藥的抑制因子,在順鉑耐藥患者的血清外泌體、組織和細胞中低表達,體外過表達Cdr1as能顯著抑制卵巢癌耐藥細胞增殖和侵襲,促進細胞凋亡,且通過調控miR-1270/SCAI分子信號軸提高卵巢癌耐藥細胞對順鉑的敏感性[34]。
3.2 circRNA調控卵巢癌紫杉醇耐藥
紫杉醇是一種長期應用于卵巢癌臨床治療的一線化療藥物,患者對其產生耐藥性仍是卵巢癌治療失敗的主要原因之一。本文中有7個circRNAs有望成為克服卵巢癌紫杉醇耐藥性的潛在靶標(見圖2)。circ-NRIP1[19]、circ-CELSR1[14]、circ-ATL2[15]、circ_0000714[35]和circ-TNPO3[36]在卵巢癌紫杉醇耐藥組織和細胞中高表達,其中circ-TNPO3預警OS不良預后,干擾circRNAs表達可抑制細胞活力、克隆形成、遷移和侵襲能力,阻滯細胞周期G0/G1期,促進細胞凋亡,進而增強卵巢癌耐藥細胞對紫杉醇的敏感性;而血清中的circ-SETDB1[28]在鉑-紫杉烷聯合化療耐藥和復發的高級別漿液性卵巢癌中顯著上調表達,且其可有效診斷高級別漿液性卵巢癌和正常卵巢[受試者工作特征曲線下面積為(0.803±0.040)]、原發性化療耐藥和原發性化療敏感的高級別漿液性卵巢癌[受試者工作特征曲線下面積為(0.811±0.064)],并與PFS呈負相關,是一種新型的生物標志物。此外,circ-EXOC6B可作為腫瘤抑制因子,介導miR-376c-3p/FOXO3軸提高體內外卵巢癌細胞對紫杉醇的敏感性,且其高表達與OS良性預后相關[37]。
3.3 circRNA調控卵巢癌多西紫杉醇耐藥
多西紫杉醇是卵巢癌治療的紫杉烷類化療藥物之一,其耐藥機制與ABC超家族多藥外排轉運蛋白表達(如P-glycoprotein,P-gp/ABCB1)和抑制細胞凋亡等相關[38]。研究報道,circ_0000735[20]和circ_0006404[20]均通過調控P-gp表達影響卵巢癌對多西紫杉醇的敏感性,其中circ_0000735在卵巢癌多西紫杉醇耐藥細胞系中上調表達,降低其表達水平可促進miR-546b和DKK4表達、抑制P-gp表達,導致細胞凋亡率升高和增殖能力下降;而circ_0006404則在耐藥細胞系中低表達,干擾其表達可進一步促進其介導miR-346/DKK3/P-gp軸參與卵巢癌多西紫杉醇耐藥(見圖2)。
4 circRNA調控卵巢癌及其化療耐藥的分子機制
4.1 circRNA調控卵巢癌及其化療耐藥的主要分子機制
ceRNA包括長鏈非編碼RNA、circRNA、偽基因和mRNA等,通過與miRNA競爭結合靶基因mRNA上的MREs發揮“miRNA海綿”作用,影響腫瘤的發生、發展[5]。本文綜述的62個circRNAs中,除circ-NOLC1[39]、circ-ATRNL1[40]、circ-N4BP2L2[24]、circ-PBX3[33]和circ-ITGB6[23]外,其余circRNAs均通過ceRNA機制調控卵巢癌及其化療耐藥進展。
circ-UBAP2[26,41]、circ-KRT7[42]和circ-FGFR3[13]等作為ceRNA調控EMT、細胞周期和凋亡等,加劇卵巢癌細胞的惡性發展,其中circ-UBAP2充當miR-382-5p或miR-144的ceRNA,上調PRPF8或CDH2的表達,其高表達與卵巢癌患者TMN分期和5年生存率呈負相關,而circ-KRT7和circ-FGFR3是miR-29a-3p的海綿分子,且circ-FGFR3高表達與卵巢癌患者的低生存率和高復發率顯著相關。此外,與卵巢癌化療耐藥相關的15個circRNAs中大部分依賴于ceRNA機制響應卵巢癌耐藥,如circ_0000735[20]和circ_0006404[20]均通過ceRNA機制調控P-gp蛋白表達影響卵巢癌多西紫杉醇耐藥。
4.2 circRNA與功能蛋白互作調控卵巢癌及其化療耐藥
circRNA除了充當miRNA海綿分子外,還可與功能蛋白質結合發揮其“支架”作用。本文綜述的62個circRNAs中,有5個circRNAs與功能蛋白互作參與調控卵巢癌及其化療耐藥的進程(見圖2)。在上皮性卵巢癌細胞質中高表達的circ-MUC16[16]和circ-RAB11FIP1[17]分別與自噬相關蛋白ATG13和DSC1蛋白直接結合,增加卵巢癌細胞中的自噬通量,進而加劇癌細胞增殖和侵襲;另外有研究報道,circ-NOLC1[39]可能通過結合ESRP1調節CDK1和RhoA表達,加劇上皮性卵巢癌細胞的惡性進展。而在順鉑耐藥的卵巢癌細胞中,circ-PBX3[33]和circ-ITGB6[23]分別通過與RNA結合蛋白IGF2BP2相互作用,提高ATP7A mRNA和FGF9 mRNA的穩定性,誘導腫瘤相關巨噬細胞向M2表型極化,增強卵巢癌細胞的順鉑耐藥性。
4.3 circRNA翻譯成多肽和蛋白質調控卵巢癌
目前研究發現,具有開放閱讀框(open reading frame,ORF)的circRNA可以翻譯成致癌或抑制腫瘤活性的功能多肽和蛋白質影響腫瘤的發生、發展[5]。在該文綜述的62個circRNAs中(見圖2),僅有1篇文獻報道circRNA的翻譯功能與卵巢癌調控相關。circ-ATRNL1[40]主要定位于卵巢癌細胞質中,過表達circ-ATRNL1可抑制卵巢癌細胞增殖和侵襲能力,同時進一步通過生物信息學分析和實驗驗證發現,circ-ATRNL1包含1個編碼131aa蛋白的IRES與1個ORF重疊啟動翻譯,提示circ-ATRNL1可能通過編碼131aa蛋白發揮抑癌作用;不足的是,該研究尚未進一步通過實驗驗證和卵巢癌臨床大樣本評估131aa蛋白的抑癌作用。
5 circRNA調控卵巢癌進展的通路分析
為進一步從整體上了解circRNA調控卵巢癌進展的分子機制,該文對62個circRNAs中的54個靶基因(40個靶基因由作為腫瘤驅動因子circRNA所調控,而另外14個靶基因由作為腫瘤抑制因子circRNA所調控)進行了通路分析,共富集到106條通路(Q<0.05),聚類為5大類功能(即C1~C5)(見圖3),其中C1和C3都是實體瘤相關的信號通路,包括膀胱癌、胰腺癌、子宮內膜癌和腎細胞癌等;C2包括有絲分裂原活化蛋白激酶等癌基因通路,C4為細胞自噬通路,C5包括癌癥中程序性細胞死亡配體-1的表達及程序性細胞死亡受體-1檢查點等免疫調控相關信號通路;此外,其他信號通路中還包含鐵死亡等信號通路。上述結果提示circRNA可能主要通過調控上述信號通路特別是細胞自噬通路調控卵巢癌進展。
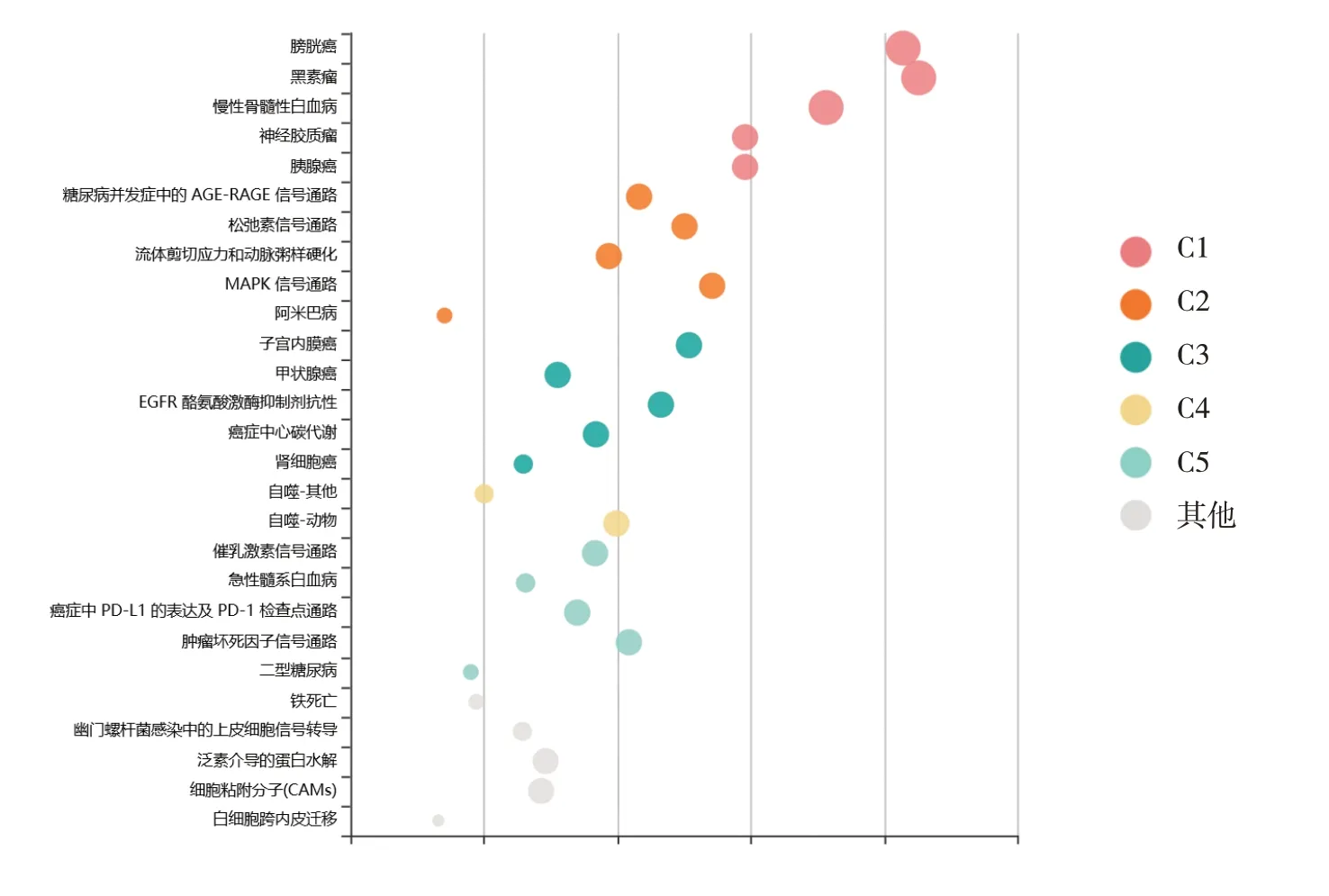
圖3 通過KOBAS數據庫對54個circRNAs靶基因進行通路富集和功能聚類分析
細胞自噬是指細胞內受損的蛋白質或細胞器被具有雙層膜結構的自噬體包裹后進入溶酶體降解循環的過程,這種保守的細胞自我消化機制,對于機體發育和緩解多種環境壓力至關重要。研究表明,自噬是一把雙刃劍,抑制或促進自噬均可影響腫瘤細胞增殖、遷移、侵襲和耐藥[47]。和上述通路富集結果相一致的是,在所綜述的62個circRNAs中,circ-MUC16[16]和circ-RAB11FIP1[17]均通過與自噬相關蛋白結合或充當miRNA分子海綿促進自噬,進而加劇卵巢癌細胞遷移和侵襲等惡性行為。值得關注的是,經檢索發現,circRNA通過介導自噬調控腫瘤的相關研究有限,其中調控卵巢癌的研究極少(3篇左右)。本文綜述的5個circRNAs(circ-VPS13C[43]、circ-MUC16[16]、circ-RAB11FIP1[17]、circ_0007444[44]和circ-9119[45])的靶基因(ERK、Beclin-1、ATG7、ATG14、PTEN)又主要富集在自噬通路上。因此,自噬很可能成為circRNA調控卵巢癌及其他腫瘤進展的重要信號通路,值得進一步關注和深入研究。
6 總結與展望
本文系統綜述了62個circRNAs在卵巢癌及其化療耐藥中的研究進展,發現circRNA主要基于ceRNA網絡和與功能蛋白互作參與卵巢癌及其耐藥調控,并主要與細胞增殖、遷移、侵襲、凋亡和周期相關,且通路富集結果表明可能和細胞自噬及鐵死亡通路相關,但是否通過調控細胞自噬等信號通路影響卵巢癌耐藥知之甚少,提示基于這些通路的circRNA研究有待深入探索。此外,circRNA調控卵巢癌順鉑和紫杉烷類化療耐藥的研究仍處于初級階段,大部分研究僅限于細胞耐藥功能研究,未針對化療藥物特有的耐藥機制(如DNA損傷修復、微管-蛋白質相互作用、ABC超家族多藥外排轉運蛋白和自噬等)深入研究;同時尚未有研究報道circRNA參與調控卵巢癌卡鉑耐藥,因此,circRNA在卵巢癌耐藥調控中的作用仍需進一步研究,且其是否參與卵巢癌卡鉑耐藥是卵巢癌化療耐藥調控值得揭示的科學問題。在診斷和預后標志物方面,部分circRNA與卵巢癌患者預后顯著相關,且有限的研究表明體液中的circRNA具有更高效的診斷敏感性和特異性,提示體液circRNA在標志物和臨床應用方面更具研究價值。
綜上所述,circRNA在卵巢癌及其耐藥調控方面取得了較大的進展,在卵巢癌診斷、治療和預后方面均顯示出越來越多的非凡潛力,值得進行全面而深入的探討,以進一步提高婦女健康水平,服務醫療衛生事業發展。

