食欲素受體拮抗劑類抗失眠藥物的研究進展
于景嫻,池里群
北京市海淀區婦幼保健院藥劑科,北京 100080
失眠是最常見的睡眠問題之一,長期失眠會嚴重影響個人的工作和生活。《中國失眠癥診斷和治療指南》(2017 年版)[1]中指出,失眠癥是以頻繁而持續的入睡困難和(或)睡眠維持困難并導致睡眠感不滿意為特征的睡眠障礙。根據病程對其進行分類:病程<3 個月為短期失眠,病程≥3個月為慢性失眠。失眠具有入睡困難、睡眠維持困難或早醒的特征,并對日間功能和整體健康產生顯著負面影響。日間功能障礙主要表現為疲勞、情緒低落或激惹、軀體不適、認知障礙等問題。此外,慢性失眠還可能導致工作效率下降、社交孤立[2],并增加精神障礙和心血管疾病等其他疾病的發生風險。研究表明[3-4],通過充分、適當地治療失眠可改善心理健康和心血管疾病的結局。
目前,臨床常用的改善失眠癥狀的藥物主要為鎮靜催眠藥,可分為兩類:一類是苯二氮 類藥物(benzodiazepine drugs, BZDs),如地西泮、勞拉西泮、艾司唑侖、阿普唑侖等;另一類是非苯二氮 類藥物(nonbenzodiazepine drugs, non-BZDs),如唑吡坦、扎來普隆、佐匹克隆、右佐匹克隆等。BZDs存在生理依賴性問題,長期使用后停用會引發戒斷癥狀,在我國被歸為二類精神藥品管理。此外,長期服用BZDs 還可能導致身體對藥物產生耐受性或出現日間困倦、頭昏、肌張力減低、跌倒、認知功能減退等不良反應。而non-BZDs 具有與BZDs 類似的催眠療效,一般不產生日間困倦,且產生藥物依賴的風險較傳統BZDs 低。但需要注意,non-BZDs 有可能會在突然停藥后發生一過性的失眠反彈。實際應用過程中患者往往難以忍受這些不良反應[5-6]。治療失眠的理想藥物是在短期和長期使用中均安全有效的藥物,既能改善定量指標(如總睡眠時間、入睡后清醒時間和入睡潛伏期),又能提高睡眠質量、日間功能表現以及整體健康水平的藥物[7]。隨著人們對生活質量要求的不斷提高,開發一種新型改善睡眠和治療失眠的藥物具有重要意義。
食欲素(orexin)是一種在下丘腦外側區域合成和分泌的促進覺醒的神經肽。食欲素受體(orexin receptor)與食欲素結合,可以發揮調節睡眠-覺醒狀態的作用。如果夜間食欲素分泌過多,會導致覺醒系統過于強大,不能順利切換成睡眠系統,就會出現失眠。如果能夠抑制夜間食欲素的活性或阻斷食欲素與食欲素受體的結合,就會抑制食欲素的促清醒作用,減少覺醒信號、增加睡意、恢復正常睡眠節奏。食欲素受體拮抗劑在治療失眠癥方面表現出巨大潛力,已成為近期研究的熱點之一。
1 食欲素及其受體的發展
1998 年,有2 個獨立的研究小組對大鼠下丘腦進行了信使核糖核酸(messenger RNA,mRNA)和蛋白質的研究并有重要發現[8-9],即在大鼠下丘腦中發現了2 種未知的神經肽,分別被稱為食欲素A 和B 或下丘腦泌素(hypocretin)1和2[8-9]。2012 年,國際基礎和臨床藥理學聯合會(International Union of Basic and Clinical Pharmacology)建議使用“食欲素”一詞來描述這些多肽及其受體,并同時保留“下丘腦泌素”(縮寫為HCRT)一詞來描述其各自的基因和mRNA。HCRT基因可編碼一種前體肽,分解成食欲素A和食欲素B 2 種活性肽,并可廣泛投射到大腦各個區域,進而調節喚醒、清醒和食欲[10]。食欲素多肽是G 蛋白偶聯的食欲素1 型受體(orexin-1 receptor , OX1R)和食欲素2 型受體(OX2R)的配體。食欲素A 以相似效力激活OX1R 和OX2R,而食欲素B 則優先激活OX2R[11]。
2 食欲素受體拮抗劑的發展
食欲素受體拮抗劑根據其結合親和力可分為選擇性OX1R 拮抗劑(selective orexin-1 receptor antagonists,SORA1s)、 選擇性OX2R 拮抗劑(selective orexin-2 receptor antagonists,SORA2s)和雙重食欲素受體拮抗劑(dual orexin receptor antagonists, DORAs)。OX2R 在睡眠調控中起關鍵作用,并可與OX1R 協同調節快速眼動(apid eye movement,REM)睡眠[12]。近20年來,國內外醫藥公司針對食欲素受體研發了幾十個化合物,然而對于SORA1s 而言,并沒有明顯改善失眠的效果[13]。雖然部分SORA2s 在動物實驗中顯示出強大的催眠作用,但仍需要進一步進行臨床研究[14]。由于DORAs 具有良好的抗失眠效果和安全性,在過去10 年里已成為新型抗失眠藥物研發的主要方向。本文主要介紹DORAs 中的3 個明星藥物,分別為suvorexant、lemborexant 和daridorexant,其已先后在美國上市,但目前在我國均尚未上市。
2.1 Suvorexant
Suvorexant 于2014 年在美國獲批用于治療由于入睡困難和(或)睡眠維持困難而導致的失眠,是首個獲批的DORAs[15]。2016 年的一項研究顯示[16],suvorexant 能夠延長所有睡眠階段的時長,特別是對REM 睡眠的改善效果較好。其可以使REM 睡眠在整個睡眠周期中所占比例提高達3.9%,且不改變總體睡眠結構,對于睡眠期間功率譜曲線的影響幾乎可以忽略不計。2017 年發表的一篇系統綜述發現[17],原發性失眠患者應用suvorexant后,在1 個月和3 個月內主觀入睡時間和主觀睡眠質量方面均有良好改善。2019 年的一項針對非老年(18~64 歲)和老年(≥65 歲)失眠患者為期3 個月的suvorexant 試驗結果顯示[18],根據年齡調整(非老年/老年患者)的給藥劑量分別為40/30mg和20/15mg,且其在失眠嚴重指數方面改善睡眠程度均優于安慰劑組。
Suvorexant 最常見的不良反應是嗜睡、疲勞。有研究顯示,服用suvorexant 20mg 劑量時,嗜睡發生率為5.1%,頭痛發生率為6.7%,其他常見的不良反應包括上呼吸道感染、頭暈、異常夢境和咳嗽等(>3%)。值得注意的是,嗜睡的發生與所服用的劑量呈正相關,劑量越高則發生率越高[18-19]。Suvorexant 主要通過細胞色素P450 3A(CYP3A)代謝,因此其藥動學可能受到CYP3A 調節劑的影響,在使用CYP3A 激活劑或抑制劑時需謹慎[20]。另一項研究顯示[21],suvorexant 在男性和女性中均表現出良好的耐受性和有效性,且對于絕經期患者可能將是一種較優的治療選擇。
Suvorexant 在老年人中顯示出良好的臨床療效,并且可能對阿爾茨海默病伴失眠者有積極作用,同時具備良好的耐受性和輕微不良反應(以嗜睡最為常見)[22]。而一項對于年輕健康志愿者進行的研究表明[23],患者在服用suvorexant 20mg 或40mg 后的第二天早上駕車時,沒有嗜睡的不良反應殘留影響,但某些個體確會有影響。在2 型糖尿病患者中,suvorexant 能夠改善睡眠質量和與肥胖相關的參數,包括血糖控制。這與對糖尿病模型小鼠進行臨床前實驗中所得到的數據非常吻合[24]。在接受治療的高血壓和失眠患者中,服用suvorexant 20mg 對白天、夜間或早晨血壓都沒有整體影響[25]。
相關研究發現[26],suvorexant 可能成為一種改善睡眠障礙、幫助戒斷阿片類藥物以及減少丁丙諾啡渴望方面的新的治療方法。但是需要注意藥物濫用等問題,包括非法使用或過量使用處方藥。一項對健康者娛樂性多藥使用進行的研究中發現了suvorexant 有被濫用的潛在風險,但相關研究認為suvorexant 的濫用傾向與唑吡坦相似甚至可能更低[26]。
2.2 Lemborexant
Lemborexant 屬于DORAs,分別于2019 年12 月在美國和2020 年1 月在日本獲得批準,用于治療以入睡或保持睡眠困難為主要特征的成人失眠患者。與suvorexant 相比,lemborexant 對食欲素受體的抑制作用更強,且在OX1/2R 上表現出可逆的競爭性拮抗作用。其對于OX2R 的抑制作用明顯優于OX1R,并具有較高的選擇性,因此能夠提供更強的抗失眠效果。同時,其與食欲素受體結合和解離速度快,相關研究顯示與[27-28],安慰劑相比,lemborexant 并未影響次日日間功能,且可有效減少次日殘留等不良反應。Lemborexant 的推薦劑量為5mg,受個體臨床反應及耐藥性等影響,其最大劑量可增至10mg,建議在睡前立即服用,并確保至少在計劃蘇醒時間前7h 服用,可有效減少入睡后覺醒[29]。2021 年的一項薈萃分析[30]比較了不同類別的失眠藥(包括lemborexant、suvorexant、唑吡坦、佐匹克隆、右佐匹克隆、曲唑酮、氟硝西泮、艾司唑侖、三唑侖、溴替唑侖、替馬西泮和雷美替安)在睡眠質量、入睡時間以及總睡眠時間方面的指標,結果顯示lemborexant 可能是最佳的治療方案。
與苯二氮 類相比,lemborexant 能顯著減少相關頭暈和姿勢不穩的風險,且沒有明顯的藥物相互作用;而對于老年人來說,lemborexant 可能比苯二氮 類藥物更安全[30]。需要注意的是,對于那些可能對lemborexant 敏感的患者來說,在考慮到第二天早上駕車時可能出現的認知損傷風險,可能需要減少劑量[31]。Moline 等[28]通過對9 項臨床試驗數據進行分析,評估了lemborexant 在次日的殘留效應,包括清晨的身體穩定性、認知能力、駕駛功能影響、主觀困倦和嗜睡情況。結果顯示,與安慰劑組相比,lemborexant 并沒有明顯影響次日白天的功能表現,并且經過長達6 個月的治療后,使用lemborexant 的患者在第二天早上更加警覺;服用lemborexant 5mg 的患者嗜睡發生率為8.6%,稍高于suvorexant。一項針對日本人群的回顧性研究表明[32],在持續用藥6 個月后停藥時,因為嗜睡、疲勞和噩夢等原因引起的不適癥狀可以自行緩解,這可能與該藥半衰期較長有關。
2.3 Daridorexant
Daridorexant 作為一種新型高效的DORAs,于2022 年1 月在美國批準上市,其劑量包括25mg和50mg。與安慰劑相比,daridorexant 25mg 和50mg 劑量在1 個月和3 個月時可以改善成人患者(包括老年人)的夜間睡眠和日間狀態,能夠幫助患者達到與生理睡眠周期相似的睡眠效果,可增加總體睡眠時長,提升睡眠質量,并具有良好的安全性[33-34]。Daridorexant 的體內藥動學曲線更優越,其半衰期為5.9~8.8h,更符合人體自然睡眠周期,既能保持夜間睡眠質量,同時又對次日日間功能影響較小;生物利用度高,能夠迅速吸收和代謝[35]。Kunz 等[36]進行了為期52 周的研究,設置了安慰劑作為對照組,觀察了daridorexant 的治療安全性、夜間有效性以及對日間功能的影響。研究結果顯示,在失眠患者中,服用daridorexant 10mg、25mg和50mg 劑量組均表現出良好的長期安全性和耐受性,沒有出現身體依賴、耐受或失眠反彈。有效性分析顯示,相較于安慰劑組,daridorexant 50mg劑量組患者臨床效果最好,并有助于改善患者的總睡眠時間和日間功能,且該研究結束時未發現相關益處逐漸消退的跡象。
Daridorexant 最常見的不良反應包括頭痛和嗜睡,發生率均<3%;頭暈和疲勞的發生率均<2%。與安慰劑組相比,服用daridorexant 的患者未表現出日間過度嗜睡[33]。在52 周停止研究治療后[36],各治療組的苯二氮 類藥物戒斷癥狀問卷(benzodiazepine withdrawal symptom questionnaire,BWSQ)評分相似且均較低,且daridorexant 組和安慰劑組間無統計學差異。在試驗結束時,沒有患者達到BWSQ 評分>20 分;未觀察到劑量依賴性;沒有證據表明其有任何與停藥相關的癥狀或者反跳性失眠,提示濫用可能性低[36-37]。
2.4 3 種DORAs 類藥物對比
本文主要介紹的3 個DORAs 明星藥物均經CYP3A4 代謝,主要通過糞便和尿液排泄,藥動學的主要區別在于半衰期不同。3 種DORAs 藥品相關情況比較見表1[38]。
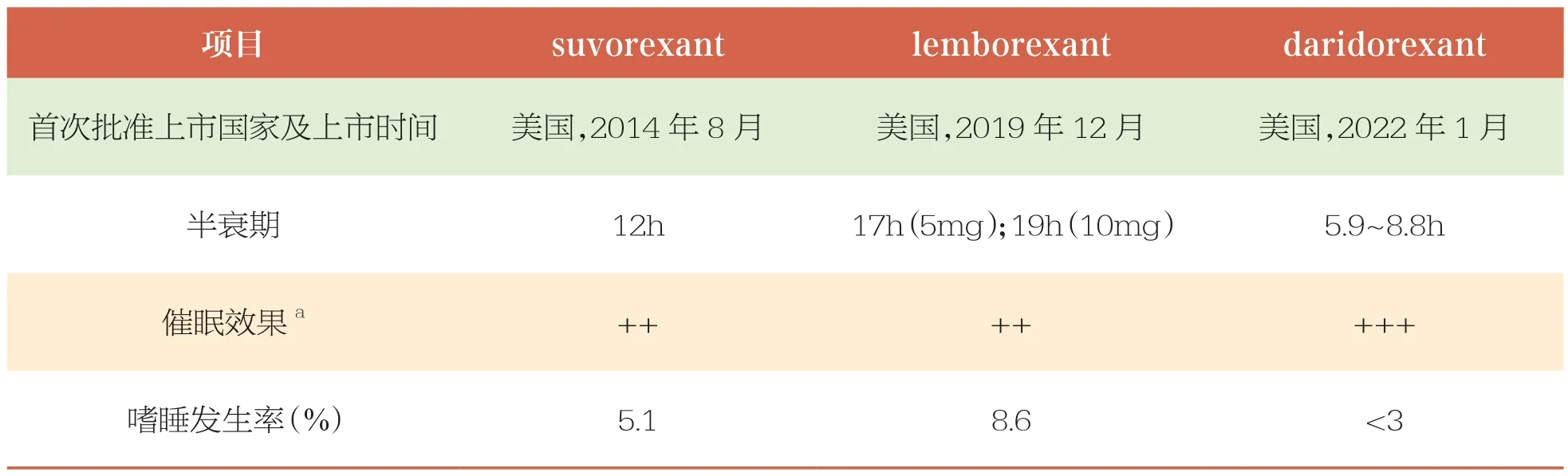
表1 3 種DORAs 藥品相關情況比較
3 小結
綜上所述,食欲素受體拮抗劑是一種具有很大潛力的治療失眠的方法,有著廣闊的應用前景,為解決睡眠障礙、焦慮癥和藥物成癮治療提供了突破口。作為新一代抗失眠藥物,食欲素受體拮抗劑通過獨特的機制減弱覺醒信號,從而抑制清醒狀態而非誘導鎮靜,在一定程度上解決了傳統鎮靜催眠藥物存在的一些缺點。另外,此類藥對次日日間功能影響較小、成癮性較低,尤其最新上市的daridorexant 能夠幫助患者達到與生理睡眠周期相似的睡眠效果,提高睡眠質量。但需要注意的是,目前對于特殊人群,如兒童、妊娠期和哺乳期婦女等,使用該類藥物的數據幾乎為零,且其應用于失眠患者的長期安全性和有效性仍需開展更多臨床前和臨床研究。
suvorexant

