華蟾素通過抑制谷胱甘肽合成酶表達誘導肝癌細胞發生鐵死亡的作用機制研究
兀琦,楊靜依,陳啟梅,王安美,孫藝軒,張加余,楊愛琳
(濱州醫學院藥學院,山東 煙臺 264003)
癌癥是導致人類死亡的主要原因之一,據2020年GLOBOCAN項目研究表明肝癌的死亡率位居世界第三,占癌癥總死亡率的8.3%[1]。肝細胞癌(hepatocellular carcinoma,HCC)是原發性肝癌最常見的一種類型。早期發現可通過手術切除、射頻消融術、肝移植等方法治療,然而大多數肝癌患者確診時已為中晚期[2]。截至目前,化療依舊是晚期肝癌治療的主要方法,但在臨床治療中,化療往往會引起一系列不良反應,例如肝功能異常、高血壓、腹瀉等。因此迫切需要開發新的有效、低毒性抗肝癌藥物。
中醫藥有著悠久的歷史,近年來在抗腫瘤領域引起廣泛關注。中醫藥能夠增強化療療效,提高生存期。華蟾素是從蟾蜍科動物中華大蟾蜍或黑眶蟾蜍(BufoBufogargarizansCantor)蟾蜍干皮中提取所得,其主要活性成分為蟾蜍二烯內酯、生物堿和肽類[3]。華蟾素膠囊、華蟾素注射液等廣泛應用于臨床肝癌的治療[4-5]。臨床研究表明,華蟾素聯合化療藥物能夠顯著提高晚期癌癥患者藥物療效和生活質量[6]。另外,有研究表明華蟾素能夠通過抑制細胞增殖、誘導細胞凋亡、抑制上皮間充質轉化和抑制腫瘤血管生成等多方面機制發揮抗腫瘤功效[7]。
鐵死亡是由于失去對膜脂質過氧化的控制而導致的細胞死亡的形式,其發生過程中伴隨鐵依賴性脂質累積、谷胱甘肽過氧化物酶4(GPX4)功能異常、活性氧(ROS)升高和還原型谷胱甘肽(GSH)含量下降[8-9]。GSH是人體內重要的抗氧化劑,能夠清除活性氧。此外,有研究表明GSH合成障礙導致脂質活性氧累積,導致鐵死亡發生[10]。GSS催化λ-谷氨酰半胱氨酸與甘氨酸反應生成還原性GSH,不受GSH反饋抑制的調節[11]。另有資料顯示,在肝癌細胞中,核糖核苷酸還原酶M2肽(RRM2)依賴于GSS刺激GSH合成,從而抑制鐵死亡[12],且有研究表明通過藥物誘導鐵死亡為目前腫瘤治療的新策略及研究熱點[13]。關于華蟾素能否誘導肝癌細胞發生鐵死亡及作用機制目前鮮有報道,本研究從鐵死亡角度探討華蟾素抑制肝癌細胞生長的機制。
1 材料與方法
1.1 試驗藥物華蟾素膠囊(批號:OD04)來自于陜西東泰制藥有限公司。
1.2 細胞系人肝癌HepG2細胞(American Type Culture Collection)。
1.3 試劑DMEM基礎培養基、胎牛血清(FBS)、青霉素-鏈霉素混合液和0.25%的胰蛋白酶(美國康寧公司);CCK-8細胞活性檢測試劑、還原型谷胱甘肽(批號:BN27005,北京百瑞極生物科技有限公司);鐵螯合劑(DFO,批號:D9533,Sigma公司);MDA檢測試劑盒、GSH和氧化型谷胱甘肽(GSSG)檢測試劑盒、ROS檢測試劑盒(上海碧云天生物技術有限公司);BCA蛋白濃度測定試劑盒(北京索萊寶科技有限公司);GSS(批號:sc-166882)和β-actin(批號:sc-47778)(美國Santa Cruz公司);HRP標記的羊抗鼠二抗(美國Cell Signaling Technology公司)。
1.4 儀器SpectraMAX M2型多功能酶標儀(美國Molecular Devices公司);LightCycler 96型實時熒光定量PCR(德國羅氏公司);DYY-6D電泳儀電源(北京六一生物科技有限公司);C600多功能熒光化學發光成像儀(Azure Biosystems公司);TUS-200P震蕩型恒溫金屬浴(上海恒科有限公司)。
1.5 方法
1.5.1 細胞培養與細胞活性檢測將細胞培養在含89% DMEM基礎培養基、10% FBS和1%的青霉素-鏈霉素的完全培養基中,放入含5% CO2的37 ℃恒溫培養箱中進行培養。通過細胞活性檢測實驗研究華蟾素對人肝癌HepG2細胞增殖的影響。首先,將HepG2細胞(3.5 × 103個/孔)鋪于96孔板中,24 h后,吸出上清,將細胞與華蟾素藥液0、2、4、6、8 μg·mL-1單獨或者分別與DFO 50 μmol·L-1、GSH 5 mmol·L-1聯合處理48 h。之后,吸出上清,每孔加入100 μL 10% CCK-8工作液,將培養板放入培養箱敷育1 h后用酶標儀在450 nm波長下進行檢測。
1.5.2 細胞MDA含量檢測將肝癌細胞鋪于6孔板中,待細胞密度達到90%時進行藥物干預,設置華蟾素濃度為0、8 μg·mL-1,培養24 h。細胞樣品處理方法:用胰蛋白酶消化后,加入1 mL DMEM完全培養液吹打收集細胞,1 000×g 離心5 min。移除上清,將細胞用1 mL PBS清洗,再次離心5 min,移除上清,加入70 μL PBS。細胞樣品采用反復凍融的方法進行裂解細胞,將其放入-80 ℃冷凍,10 min后取出冷凍的細胞放置于37 ℃金屬浴融化5 min。反復凍融4次后,收集上清。之后根據MDA檢測試劑盒說明書對細胞樣品進行檢測。MDA含量通過樣品的蛋白濃度歸一化,蛋白濃度由BCA蛋白測定試劑盒測定。
1.5.3 細胞內GSH含量檢測將肝癌細胞鋪于6孔板中,待細胞密度達到90%時進行藥物干預,設置華蟾素濃度為0、8 μg·mL-1,培養24 h。之后根據試劑盒說明書對細胞樣品進行處理檢測。GSH含量通過細胞數量進行歸一化。
1.5.4 細胞內ROS水平測定將肝癌細胞鋪于6孔板中,待細胞密度達到90%時進行藥物干預,設置華蟾素濃度為0、8 μg·mL-1,培養24 h。之后收集細胞,懸浮于稀釋好的DCFH-DA(1∶1 000)中。放置于37 ℃培養箱中避光敷育20 min,并每間隔5 min顛倒混勻一下,使探針與細胞充分接觸。敷育結束后,用無血清DMEM基礎培養基洗滌細胞3次,以充分去除未進入細胞內的探針。最后將細胞懸浮于200 μL PBS中,在30 min內進行流式細胞儀上機檢測。采用FlowJo軟件分析熒光強度。
1.5.5 實時熒光定量PCR (QRT-PCR)將肝癌細胞鋪于6 cm皿中,待密度達到85%時進行藥物干預,設置華蟾素藥物濃度為0、8 μg·mL-1,培養24 h。使用E.Z.N.A.?Total RNA Kit I (OMEGA) 根據試劑盒說明書進行總RNA抽提。使用NanoDrop 2000分光光度計測定RNA濃度。使用Takara PrimeScript RT Reagent Kit進行cDNA逆轉錄。以下引物用于QRT-PCR:
Human actin(Forward):5′-GGGACCTGACTGACTACCTC-3′
Human actin (Reverse):5′-TCATACTCCTGCTTGCTGAT-3′
Human GSS (Forward):5′-GTACTCACTGGATGTGGGTGAAGA-3′
Human GSS (Reverse):5′-CGGCTCGATCTTGTCCATCAG-3′
1.5.6 Western blotting肝癌細胞用不同濃度的華蟾素藥液(0、2、4、8 μg·mL-1)處理24 h。細胞用預冷的PBS洗滌兩次,加入細胞裂解液,充分裂解后收集細胞裂解物。在SDS-PAGE凝膠上分離細胞裂解物,之后轉移到PVDF膜上。膜在4 ℃下用含5%脫脂牛奶的TBST緩沖液封閉過夜。第2天,將膜與特異性一抗(1∶1 000)在4 ℃下孵育過夜,將膜用TBST緩沖液洗滌40 min,然后與HRP偶聯的二抗(1∶2 000)在4 ℃下孵育過夜。最后,用TBST緩沖液洗滌40 min后,使用ECL超敏發光液檢進行蛋白檢測,并通過凝膠圖像系統(Azure Biosystems C600,美國)顯示條帶。
1.5.7 siRNA轉染將肝癌細胞鋪于6孔板中,待細胞密度達到50%進行轉染。將Lipofectamine 2000 5 μL與opti-MEM培養液250 μL混合在一起,用槍輕輕吹勻。將siRNA 10 μL加到opti-MEM培養液250 μL中,與加有Lipofectamine 2000的opti-MEM培養液混合在一起,室溫靜置20 min。之后將6孔板中的培養基棄掉,加入opti-MEM培養液1 500 μL,將含有Lipofectamine 2000的siRNA溶液500 μL,補齊至每孔2 mL體系,放入細胞培養箱中6 h后將上清替換為DMEM完全培養基。siRNA序列如下:
siNC(negative control,NC):5′-UUCUCCGA-ACGUGUCACGUTT-3′;
siGSS:5′-AGGAAATTGCTGTGGTTTA-3′。
1.6 統計學方法所有數據統計及分析作圖采用GraphPad Prism 8。數據比較采用t檢驗。P<0.05表明組間差異具有統計學意義。
2 結果
2.1 華蟾素誘導肝癌細胞發生鐵死亡前期通過研究發現華蟾素能夠明顯抑制肝癌細胞的生長[3]。為了研究華蟾素抑制肝癌細胞生長的形式,采用細胞鐵螯合劑DFO干預不同濃度華蟾素處理的細胞。結果顯示,DFO能夠部分逆轉華蟾素對人肝癌HepG2細胞的增殖抑制能力,HepG2細胞用不同濃度華蟾素藥液(0、2、4、6、8 μg·mL-1)或與DFO(50 μmol·L-1)聯合處理48 h,采用CCK-8檢測細胞活力,結果見圖1。由此可見,華蟾素能夠通過誘導人肝癌HepG2細胞發生鐵死亡的形式抑制增殖。
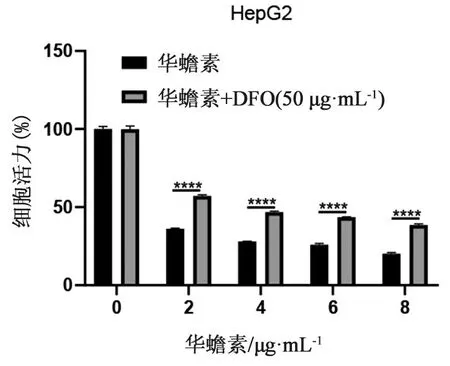
圖1 華蟾素對肝癌細胞鐵死亡的影響
2.2 華蟾素能夠增強肝癌細胞ROS和脂質過氧化水平鐵死亡的直接表現是誘導細胞內ROS累積和脂質過氧化誘導的細胞損傷[14]。因此,首先通過流式細胞術檢測人肝癌HepG2細胞經過華蟾素處理后的ROS水平。用濃度為0、8 μg·mL-1的華蟾素藥液處理HepG2細胞48 h后,用DCFH-DA染色并通過流式細胞儀分析結果顯示,HepG2細胞經華蟾素處理后熒光強度增強,說明華蟾素能夠誘導HepG2細胞產生ROS(見圖2A)。為了進一步研究華蟾素是否通過鐵死亡介導的脂質過氧化誘導細胞發生損傷,通過檢測細胞內MDA水平發現,用華蟾素藥液(0、8 μg·mL-1)處理HepG2細胞24 h,檢測MDA水平與對照組相比,HepG2細胞內MDA水平顯著升高(見圖2B),暗示細胞脂質過氧化程度和細胞損傷的加重。
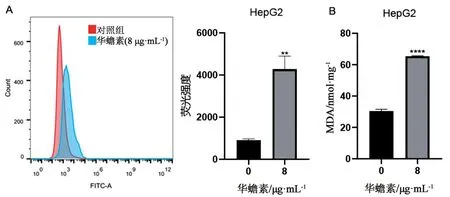
圖2 華蟾素對肝癌細胞活性氧(ROS)和丙二醛(MDA)的影響
2.3 華蟾素通過降低肝癌細胞GSH水平抑制細胞增殖前期文獻報道,GSH能夠避免細胞發生氧化性損傷,更重要的是鐵死亡途中伴隨著GSH的損失,除了MDA檢測,鐵死亡的脂質過氧化的指標還有GSH合成的變化[10,15]。細胞中存在多個對抗鐵死亡的防御途徑,其中最主要的一個是由GPX4所介導的,通過GSH特異性催化過氧化脂質來抑制鐵死亡的發生[16]。用華蟾素藥液(0、8 μg·mL-1)處理HepG2細胞24 h,檢測GSH水平,相比空白對照組,華蟾素干預組GSH水平顯著降低(見圖3A)。為了進一步探究華蟾素是否通過下調GSH水平抑制腫瘤細胞生長, HepG2細胞用不同濃度華蟾素藥液(0、2、4、6、8 μg·mL-1)或與GSH(5 mmol·L-1)聯合處理48 h,采用CCK-8檢測細胞活力。結果顯示,GSH能夠部分逆轉華蟾素對肝癌細胞的增殖抑制作用(見圖3B)。綜上,華蟾素可能通過降低肝癌細胞內的GSH水平誘導鐵死亡從而表現出抑制肝癌生長的作用。
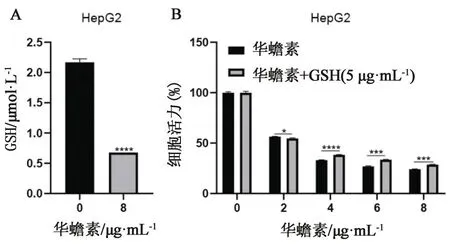
圖3 華蟾素對肝癌細胞谷胱甘肽(GSH)含量的影響
2.4 華蟾素能夠抑制肝癌細胞GSS水平GSS能夠催化λ-谷氨酰半胱氨酸與甘氨酸反應形成GSH[11]。我們首先檢測華蟾素對人肝癌HepG2細胞中的GSS水平的影響。用華蟾素藥液(0、8 μg·mL-1)處理HepG2細胞24 h,采用QRT-PCR檢測GSS的mRNA水平。如圖4A所示,與對照組相比,華蟾素干預后肝癌細胞GSS的mRNA水平降低,表明華蟾素干預導致GSS的轉錄抑制。此外, HepG2細胞采用0、2、4、8 μg·mL-1的華蟾素藥液處理24 h,通過Western blotting檢測GSS蛋白水平。華蟾素給藥干預后肝癌細胞中GSS蛋白表達減弱(見圖4B)。
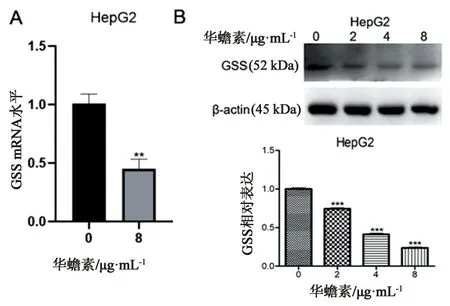
圖4 華蟾素對肝癌細胞中谷胱甘肽合成酶(GSS)水平的影響
2.5 抑制肝癌細胞GSS水平能夠降低GSH產生接下來,我們研究在肝癌細胞中GSS是否影響GSH產生。用靶向GSS(siGSS)或陰性對照(siNC)的siRNA轉染肝癌HepG2細胞。通過Western blotting檢測敲低GSS后HepG2細胞GSS蛋白水平的變化。如圖5A所示,敲低GSS能夠顯著抑制HepG2細胞GSS的蛋白表達。同時我們對HepG2細胞敲低GSS后其GSH含量進行檢測,結果表明敲低GSS組與siNC組相比,細胞內GSH含量降低(見圖5B)。以上結果表明華蟾素可能通過抑制肝癌細胞GSS水平進而抑制GSH的產生。
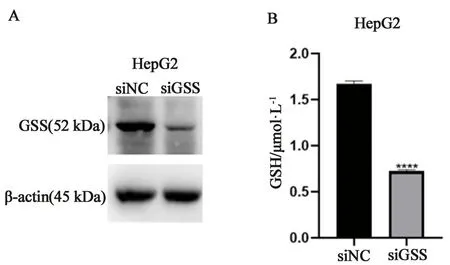
圖5 敲低GSS對肝癌細胞GSH含量的影響
2.6 華蟾素誘導肝癌細胞鐵死亡部分通過干預GSS實現我們進一步研究華蟾素是否部分通過抑制GSS誘導肝癌細胞鐵死亡,HepG2細胞(轉染siNC或siGSS)用不同濃度華蟾素藥液(0、0.5、1、2 μg·mL-1)或與DFO(50 μmol·L-1)聯合處理48 h,采用CCK-8檢測細胞活力。如圖6A所示,敲低GSS會削弱DFO對華蟾素增殖抑制的逆轉作用。HepG2細胞(轉染siNC或siGSS)用不同濃度華蟾素藥液(0、0.5、1、2 μg·mL-1)處理48 h,采用CCK-8檢測細胞活力。如圖6B所示,敲低GSS在一定程度上能夠抑制肝癌細胞的生長,并能夠增強華蟾素對腫瘤細胞的增殖抑制作用。上述結果表明華蟾素誘導肝癌細胞鐵死亡可能通過干預GSS水平來實現。
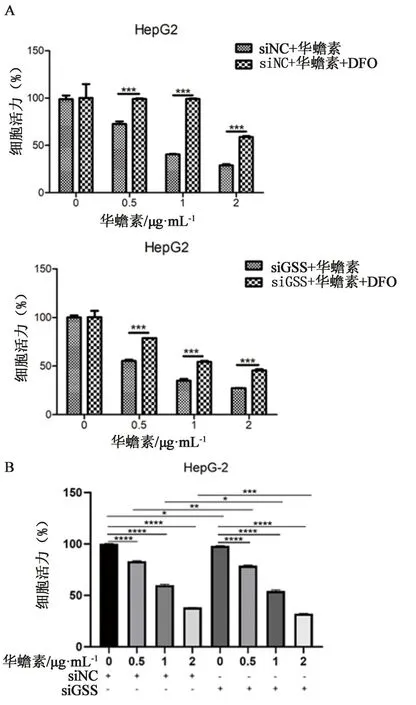
圖6 華蟾素部分通過抑制GSS誘導肝癌細胞鐵死亡
3 討論
目前,大多數肝癌患者確診時已為晚期,只有15%患者能夠手術治療。索拉非尼是FDA批準唯一用于肝癌晚期治療的藥物[17],然而其具有較強的毒副作用,因此迫切需要開發新的抗肝癌藥物。在臨床中,中藥應用于癌癥治療歷史悠久[18]。華蟾素作為中成藥已廣泛應用于臨床治療肝癌、胃癌和胰腺癌等[19-20]。
鐵死亡是一種獨特的細胞死亡方式。研究表明通過藥物誘導鐵死亡能夠抑制腫瘤發生發展[21],其發生的主要機制為多不飽和脂肪酸途徑誘導脂質過氧化導致ROS累積最終造成細胞損傷[22]。MDA是脂質過氧化的副產物[23],是鐵死亡的標志物。通過研究發現鐵螯合劑DFO能夠部分逆轉華蟾素對肝癌細胞的增殖抑制作用,我們又進一步檢測了鐵死亡標志物ROS與MDA,結果顯示華蟾素能夠誘導肝癌細胞內ROS和MDA的累積,可見華蟾素能夠誘導肝癌細胞發生鐵死亡。GSH缺失可誘導腫瘤細胞鐵死亡[24]。研究表明抑制GSH能夠增加脂質ROS含量,增強HCC對鐵死亡的敏感性,GSH合成的變化能夠反映鐵死亡的脂質過氧化程度[25]。細胞中存在多個對抗鐵死亡的防御途徑,其中最主要的一個是由GPX4所介導的,通過GSH特異性催化過氧化脂質來抑制鐵死亡的發生[9]。此外,研究證實Erastin能夠通過直接降低GSH水平,誘導缺乏GPX4的敏感細胞發生鐵死亡[26]。因此,抑制GSH合成是誘導鐵死亡的主要方法。我們檢測華蟾素干預后肝癌細胞內GSH含量,結果發現華蟾素干預后GSH水平降低,且GSH能夠減弱華蟾素對肝癌細胞的增殖抑制作用。因此,華蟾素可能通過抑制GSH誘導人肝癌HepG2細胞發生鐵死亡進而表現出抑制肝癌細胞生長的作用。GSS是GSH生物合成的關鍵酶,研究表明GSS在腫瘤組織中呈現升高趨勢[13]。此外,有研究證實抑制GSS能夠降低肝癌細胞活性,且GSH能夠減弱由GSS抑制所誘導的細胞增殖抑制作用[27]。通過研究發現華蟾素能夠抑制GSS水平,且敲低GSS能夠抑制GSH水平。進一步研究結果顯示敲低GSS能夠削弱DFO對華蟾素增殖抑制的逆轉作用,且敲低GSS能夠在一定程度上抑制肝癌細胞生長,并增強華蟾素對腫瘤細胞的增殖抑制作用。綜上,我們認為華蟾素誘導人肝癌細胞鐵死亡可能是通過干預GSS來實現的。本研究有助于闡明華蟾素復雜的抗肝癌作用,為華蟾素應用于肝癌臨床治療提供新的理論支持。

