紅花-牛膝治療口腔黏膜下纖維化作用機制的網絡藥理學分析
唐智群,鮑喆煊,聶敏
(1.廣州醫科大學附屬口腔醫院口腔黏膜病科,廣東省口腔組織修復與重建工程技術研究中心,廣州市口腔再生醫學基礎與應用研究重點實驗室,廣東 廣州510182;2.廣州醫科大學附屬口腔醫院牙周病科,廣東省口腔組織修復與重建工程技術研究中心,廣州市口腔再生醫學基礎與應用研究重點實驗室,廣東 廣州510182)
口腔黏膜下纖維化(OSF)又稱口腔黏膜下纖維性變,是一種常見的慢性進行性口腔黏膜疾病,臨床上常表現為進食刺激性食物疼痛、進行性張口受限、吞咽困難[1],典型的病理變化為黏膜固有層及黏膜下層膠原纖維堆積、變性,因其具有癌變傾向,在1987年被世界衛生組織列為癌前狀態[2]。OSF病因復雜,發病機制尚不明確,目前認為,咀嚼檳榔是OSF的高危因素。在我國湖南、海南、臺灣等有咀嚼檳榔習慣的地區,OSF的發病率可達0.9%~17.6%[3-4],癌變率可達1.2%~4.32%[3,5]。隨著檳榔產業的擴大及咀嚼檳榔習慣的流行,OSF及癌變的患者數量在逐年增加且有全國蔓延的趨勢,已逐漸成為嚴重危害公共健康的社會問題。目前OSF的治療主要使用糖皮質激素類藥物,但是長期使用此類藥物會出現全身不良反應。中醫學歷史悠久,且中醫藥具有患者依從性好、副作用少、作用靶點多的特點,近年來各種具有活血化瘀功效的中藥已逐漸被應用于OSF的臨床治療中[6]。
紅花-牛膝有活血散瘀、通經止痛的功效,藥理研究發現兩者具有調節免疫系統、抗炎、抗氧化、擴張血管改善微循環障礙等作用。含有紅花-牛膝的活血化瘀方劑已被廣泛應用于OSF的臨床治療中,但由于其成分靶點眾多,很難確定其具體機制,因此對紅花-牛膝的潛在作用機制進行研究,有助于更好地處理紅花-牛膝臨床常用劑量、配伍及量效之間的關系。本文采用網絡藥理學的方法對紅花-牛膝的有效成分及紅花-牛膝與OSF的靶點進行預測與分析,以期為臨床上應用紅花-牛膝治療OSF提供理論基礎。
1 資料與方法
1.1 收集紅花-牛膝活性成分及其靶點以類藥性(DL)>0.18、口服生物利用度(OB>30%)為篩選條件[7],在TCMSP平臺(https://tcmspw.com/tcmsp.php)檢索“紅花”“牛膝”的活性成分。通過數據庫SwissTargetPrediction (http://www.swisstargetprediction.ch)[8]獲得這些活性成分的潛在作用靶點。合并相關數據庫去重后,得到紅花-牛膝的活性成分的相關靶基因。
1.2 收集OSF疾病相關靶點以“oral submucous fibrosis”為檢索詞在GeneCards數據庫(https://www.genecards.org)和DisGeNET數據庫(https://www.disgenet.org)[9]中得到OSF的靶點并去重。
1.3 繪制“活性成分-靶點”網絡取紅花-牛膝活性成分的靶點和OSF靶點的交集,利用Cytoscape 3.9.1繪制“活性成分-靶點”網絡圖,主要活性成分通過度值(degree)篩選[9]。
1.4 蛋白質相互作用(PPI)網絡的構建紅花-牛膝的活性成分和OSF的交集靶點在STRING平臺(https://string-db.org)繪制PPI網絡構建圖,核心蛋白通過度值進行篩選。
1.5 分子對接將“1.3”項下得到的度值排名前5的活性成分與“1.4”項下得到的PPI網絡中度值前6的核心蛋白進行分子對接分析。活性分子的結構從PubChem(https://pubchem.ncbi.nlm.nih.gov)獲取[10],而核心蛋白的結構從Protein Data Bank(PDB)數據庫中獲取,利用AutoDock Vina進行分子對接分析。結合能<-5.0 kcal·mol-1表示結合力良好[11]。對接結果應用PyMOL繪制結合模式圖進行展示。
1.6 GO和KEGG富集分析在DAVID數據庫(https://david.ncifcrf.gov)[12]中對交集靶點進行GO和KEGG通路富集分析[9],用R語言繪圖。在Cytoscape中進行“藥物-活性成分-關鍵靶點-疾病-信號通路”圖的繪制[9]。
2 結果
2.1 紅花-牛膝靶點收集到紅花的活性成分16個、牛膝的活性成分15個,其中有6個為共有活性成分(見表1)。25個活性成分共2 745個相關基因,去重后最終共收集到靶點基因631個。

表1 紅花-牛膝主要活性成分信息
2.2 OSF靶點整合GeneCards數據庫得到669個OSF靶點基因,DisGeNET數據庫106個,去重后為703個OSF靶點基因。疾病與活性成分交集靶點為77個。
2.3 “中藥活性成分-靶點”網絡對“2.2”項下得到的77個靶點進行“活性成分-靶點”網絡圖的繪制(見圖1)。其中度值前15的活性成分見表2。其中木犀草素(luteolin)、γ-谷甾醇(poriferast-5-en-3beta-ol)、黃芩苷(baicalin)、黃連素(berberine)、黃連堿(coptisine)等活性成分度值較大。
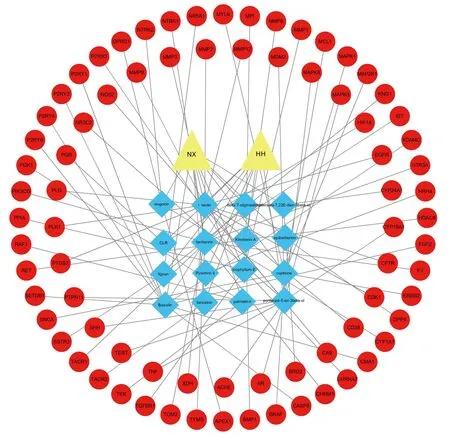
▲牛膝為NX、紅花為HH;■為靶點基因;○內為活性成分
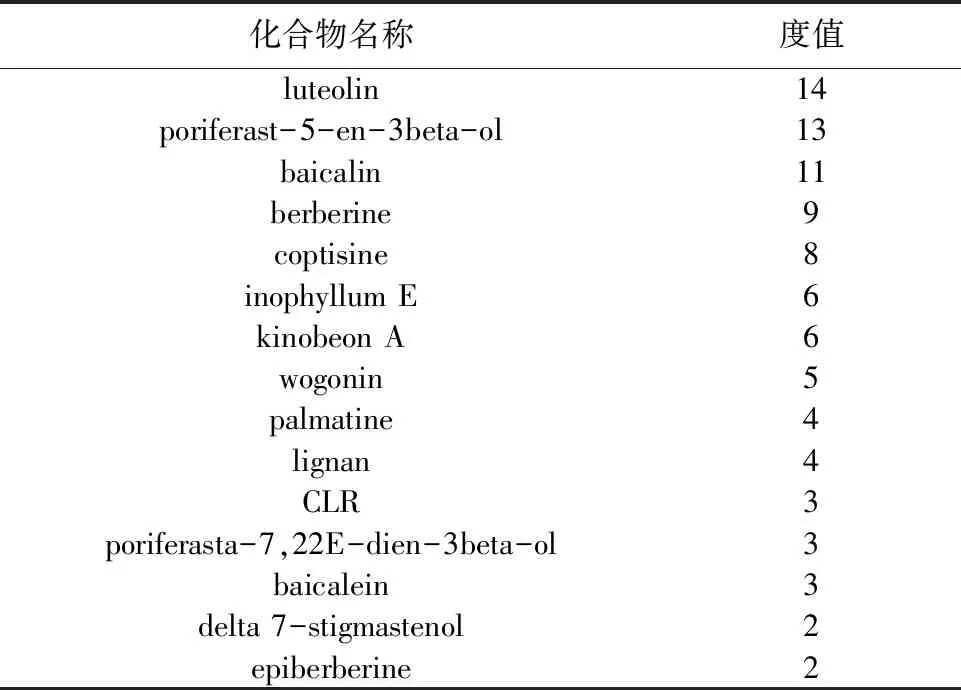
表2 “活性成分-靶點”中度值前 15 的活性成分
2.4 PPI 網絡分析將“2.2”項下得到的77個交集靶點繪制PPI網絡圖(見圖2),得到77個節點,446條邊,平均度值11.6,其中為腫瘤壞死因子(TNF)、表皮生長因子受體(EGFR)、基質金屬蛋白酶9(MMP9)、絲裂原活化蛋白激酶3(MAPK3)、酪氨酸激酶受體2(ERBB2)、低氧誘導因子1α(HIF-1α)度值較大(見表3),說明與其他蛋白互作力強。
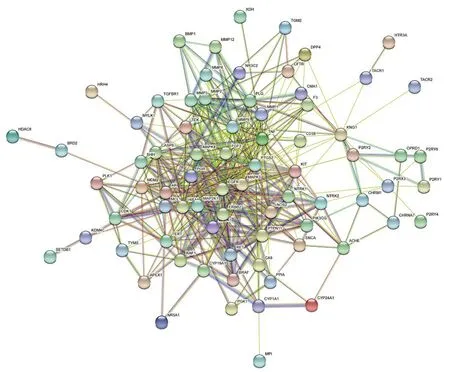
圖2 藥物與疾病蛋白-蛋白互作圖
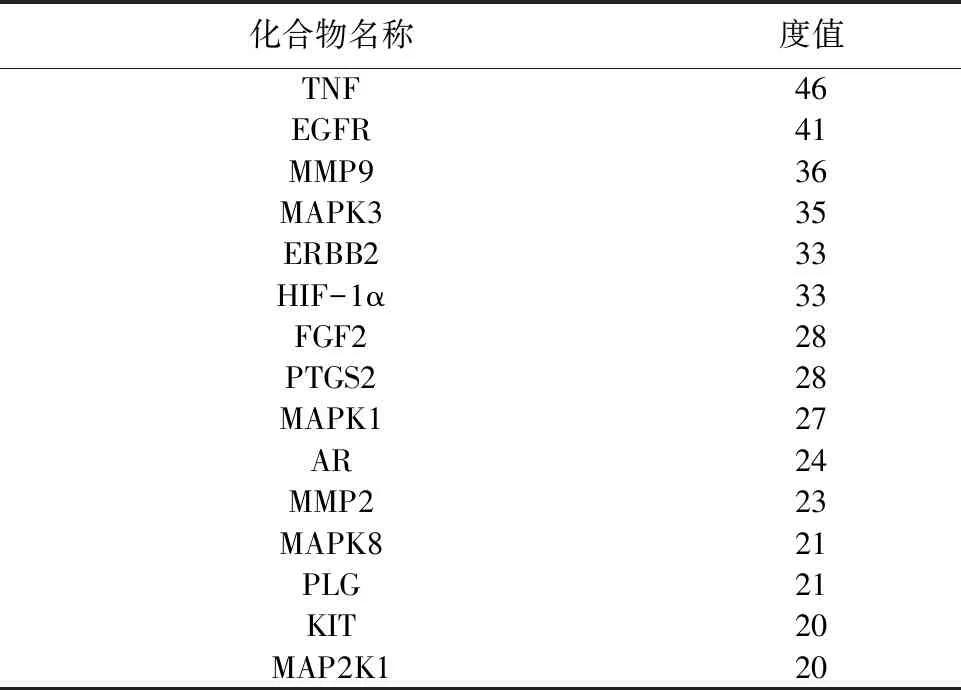
表3 度值前 15 的蛋白
2.5 分子對接分析將“2.3”項下度值最高的5個活性成分與“2.4”項下得到的度值最高的6個核心蛋白進行分子對接,結合能均≤-5 kcal·mol-1(見表4)。輸出三維分子對接圖(見圖3)。
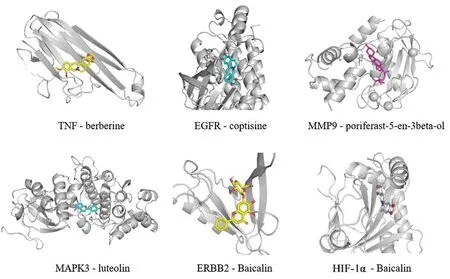
圖3 成分-靶點對接相互作用模式圖
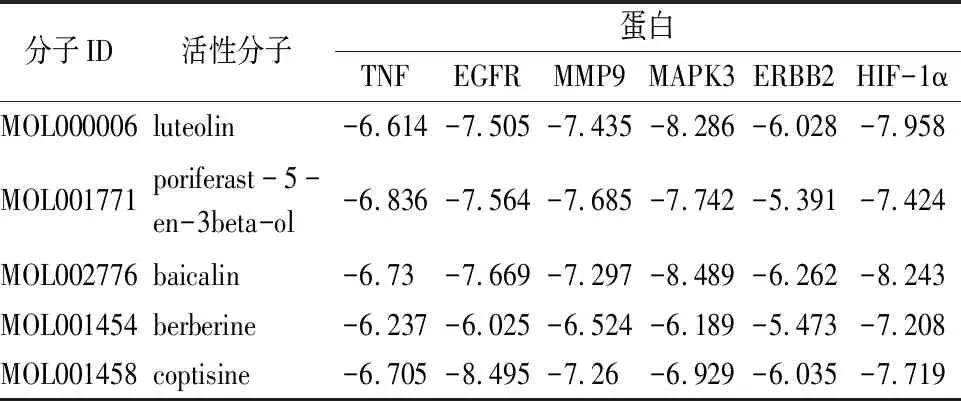
表4 主要活性分子與核心蛋白分子對接結合能(kcal·mol-1)
2.6 GO和KEGG富集分析77個靶基因進行GO富集分析后得到299個生物過程(BP)條目,包括negative regulation of apoptotic process、positive regulation of gene expression、protein phosphorylation、positive regulation of MAPK cascade、response to hypoxia、extracellular matrix disassembly等過程;49條細胞成分(CC)條目,包括plasma membrane、integral component of plasma membrane、extracellular space、mitochondrion等成分;66條分子功能(MF)條目,包括ATP binding、identical protein binding、zinc ion binding、protein kinase activity和enzyme binding等功能。對排名前10的3種聚類分析條目進行繪圖(見圖4)。
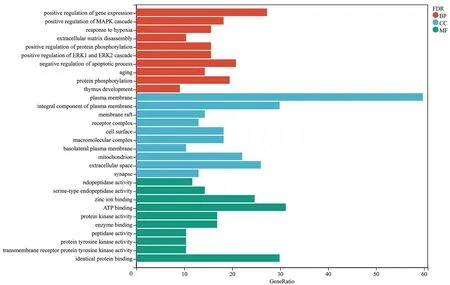
圖4 交集靶點GO富集分析
使用DAVID對77個交集靶點進行KEGG富集分析,得到117條相關通路(見圖5)。以P<0.05篩選出110條信號通路,排除與OSF無明顯相關性的通路后,P值最小的前11條通路主要為:癌癥信號通路(pathways in cancer、proteoglycans in cancer、central carbon metabolism in cancer)、鈣離子信號通路(calcium)、松弛素信號通路(relaxin)、炎癥信號通路(IL-17、C-type lectin receptor、MAPK)、缺氧誘導因子1信號通路(HIF-1)、細胞凋亡信號通路(PI3K-Akt、FoxO)等(見表5)。

圖5 交集靶點KEGG富集分析
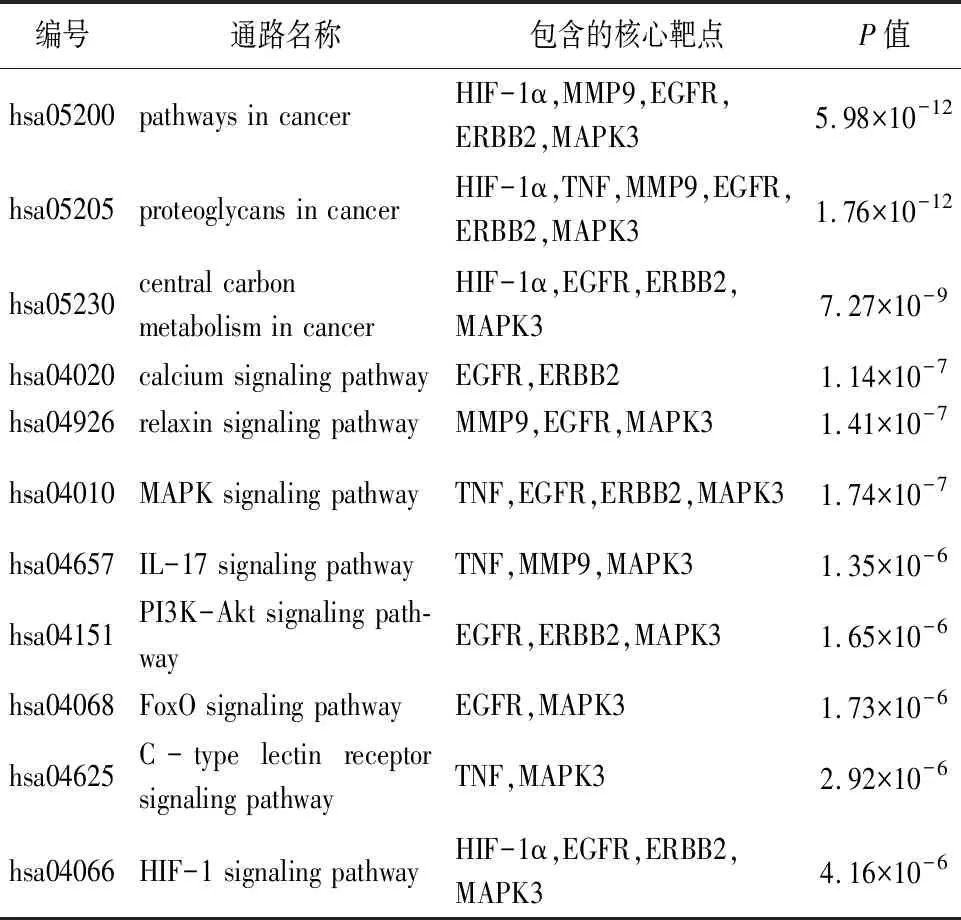
表5 關鍵信號通路與核心靶點
3 討論
中醫學認為口腔黏膜局部的毒邪郁積、氣機不暢、血運受阻、氣血失和導致了OSF的發生,治療以理氣活血、化瘀軟堅為主要原則,使用具有活血化瘀作用的中藥可通過促進病變部位血管生成及增加血液流量來治療OSF[13]。紅花具有活血散瘀、通經止痛的功效[14],牛膝具有逐瘀通經、補肝腎、強筋骨、利尿通淋、引血下行的功效[15],兩者是各類活血方劑中的重要組成部分,活血化瘀解毒湯、自擬解纖飲就包含了紅花,而清代王清任的血府逐瘀湯里更是包含了紅花、牛膝等多種活血化瘀的中藥[13,16]。
本研究中,我們發現紅花-牛膝與 OSF 交集靶基因77個,紅花-牛膝共有16種有效成分協同作用于OSF的疾病靶點,主要為木犀草素、黃芩苷、黃連素和黃連堿,有效成分作用于OSF的核心靶點為TNF、EGFR、MMP9、MAPK3、ERBB2、HIF-1α,且主要活性成分與核心蛋白具有良好的結合能力。現代藥理學認為木犀草素、黃芩苷均屬于黃酮類化合物,而黃連素、黃連堿都屬于異喹啉類生物堿,四者都具有調節酶活性、抗血小板聚集、參與細胞凋亡和干細胞信號轉導等藥理活性,能發揮抗炎、抗氧化、抗腫瘤、改善微循環等多種作用[17-19]。這些結果說明紅花-牛膝可能通過其抗炎、抗氧化、抗腫瘤以及改善微循環障礙等作用來治療OSF。
進一步通過GO和KEGG富集分析,紅花-牛膝治療 OSF以細胞凋亡負調控、缺氧反應及MAPK級聯反應正調控生物過程為主,主要通過癌癥、鈣離子、炎癥及細胞凋亡相關信號通路起作用。其中與癌癥和炎癥相關的信號通路條數最多,富集的核心蛋白基因最多,提示在紅花-牛膝的抗炎和抗腫瘤作用在治療OSF中具有重要意義。
C-type lectin receptor信號通路、IL-17信號通路以及MAPK信號通路中的JNK 和 p38-MAPK路徑是3條經典的炎癥信號通路,在多種炎癥反應及自身免疫性疾病的病理過程中都起著關鍵作用,且三者存在著相互調控的關系。C-type lectin receptor的活化可促進IL-17的表達[20],而IL-17家族可通過其相應受體發出信號,激活下游的 MAPK信號通路,誘導抗菌肽、細胞因子和趨化因子的表達,激活體內的炎癥級聯反應[21]。OSF的病理過程與炎癥反應密切相關,研究認為檳榔堿等刺激因素可通過引發口腔組織表達TNF-α等促炎因子,抑制MMP的表達并促進金屬蛋白酶組織抑制劑(TIMP)的表達,打破細胞外基質蛋白生成與降解的平衡,進而導致膠原纖維異常沉積[22]。此外,細胞炎癥反應還可刺激細胞持續表達轉化生長因子β(TGF-β)和β成纖維細胞生長因子(β-FGF),促進成纖維細胞向肌成纖維細胞轉化,導致膠原纖維的生成增加[2]。Kundu等[23]學者對OSF患者的口腔黏膜軟組織進行了測序分析,他們發現與健康對照組相比,OSF患者中MAPK和IL-17 信號通路都出現異常活化。而木犀草素、黃芩苷、黃連素和黃連堿均具有顯著的抗炎作用。木犀草素可以通過抑制人視網膜色素上皮細胞中的NF-κB和MAPK信號通路,降低IL-1β、IL-6、TNF-α、可溶性細胞間黏附分子-1和單核細胞趨化蛋白-1等炎癥介質的表達[24];還能通過降低人乳腺上皮細胞中的IL-1β、IL-6、TNF-α、MMP-2和MMP-9的表達,上調TIMP-1和TIMP-2的水平來抵抗金黃色葡萄球菌引發的炎癥反應[25]。黃芩苷能通過抑制JAK2-STAT3信號通路,調節Th17/Treg細胞的平衡,降低TNF-α、IL-6、IL-17和IL-1β的表達,減輕關節腔中的炎癥反應[26]。黃連素能通過顯抑制大鼠體內JNK1的磷酸化,降低 TNF-α和IL-6的表達[27],還能通過降低TNF-α、TGF-β1的表達和增加MMP-2的水平來促進膠原蛋白的降解,從而減輕肝臟的纖維化[28]。黃連堿也能通過抑制MAPK信號通路降低動脈粥樣硬化小鼠血清中IL-6、 IL-1β、 TNF-α水平,并下調血管內皮細胞中血管細胞黏附分子-1、IL-6和 IL-1β的表達[29]。結合本研究結果,我們推測紅花-牛膝可能通過調控C-type lectin receptor、IL-17以及MAPK信號通路發揮著OSF治療過程中的抗炎作用。
Pathways in cancer、proteoglycans in cancer和central carbon metabolism in cancer是3條調控腫瘤微環境的信號通路,參與了腫瘤的生長和遷移。OSF是一種具有癌變傾向的疾病,檳榔堿等刺激因素誘導的持續性炎癥、膠原沉積、生長因子和細胞因子分泌可能導致OSF向惡性腫瘤轉化。已有研究顯示在晚期OSF和口腔鱗狀細胞癌中存在著共同的生物標記物,如TGF-β1、 HIF-1α、MMP、TIMP和血清免疫球蛋白G等[30-32]。木犀草素可以通過調控AKT/mTOR 信號通路下調MMP9的表達,從而抑制乳腺癌細胞增殖和轉移[33]。黃芩苷能通過抑制HIF-1α和芳香烴受體的表達減弱TGF-β1誘發的人肺動脈平滑肌細胞的異常增殖[34]。黃連素能通過下調EGFR 和 ERBB2的表達抑制卵巢癌細胞的遷移和侵襲[35]。而黃連堿能通過調節JNK信號通路介導人類肝癌細胞的凋亡[36]。木犀草素、黃芩苷、黃連素和黃連堿的抗腫瘤作用可能在紅花-牛膝治療OSF的過程中具有重要作用。
綜上所述,紅花-牛膝可能以木犀草素、黃芩苷、黃連素和黃連堿等主要活性成分,通過C-type lectin receptor、IL-17、MAPK和癌癥相關等信號通路作用于TNF、EGFR、MMP9、MAPK3、ERBB2、HIF-1α等靶點來治療OSF。本研究應用網絡藥理學研究方法分析了紅花-牛膝治療OSF的潛在作用機制,為進一步探究紅花-牛膝治療OSF提供理論線索與依據。但本研究尚未對預測的關鍵靶點以及通路進行驗證,未來將通過體內、外實驗進一步驗證分析,以期能夠促進藥物的研發以及改良。

