紅細胞-納米載體遞藥系統研究進展
蘇艷慧,張文麗,沈雁,鄭春麗
(中國藥科大學藥劑系,江蘇 南京 210009)
近年來,通過包封或吸附將藥物整合于納米合成材料中的納米診療載體具有提高藥物體內穩定性、延長藥物作用時間、降低藥物給藥劑量、降低毒副反應、靶向遞送藥物等作用[1-3]。目前為止,已經有多種納米載體,如脂質體[4]、聚合物納米粒[5]、聚合物膠束[6]、脂質納米粒[7]等被研究用于負載藥物從而實現不同疾病的治療與診斷。但是,當其通過靜脈注射進入體內后,會迅速被體內網狀內皮系統(reticuloendothelial system,RES)識別、捕獲和吞噬,從而導致其在肝、脾等組織中的蓄積,并最終從血液中被清除,極大地降低了藥物在靶組織的藥量,從而影響了藥物的治療效果[8]。目前已經研究出多種方法降低RES對納米載體的清除作用,最常見的策略是采用親水性聚合物高分子材料聚乙二醇(Polyethylene glycol,PEG)表面修飾以延長納米載體在體內的循環時間,解決納米載體在體內的生物相容性問題[9]。然而,長期反復注射PEG修飾納米載體會在體內產生特異性抗體從而激活人體補體系統,反而增強了肝臟庫普弗細胞對納米載體的吞噬作用,最終會加速納米載體在機體的清除[10]。這種缺陷極大地限制了合成納米載體在臨床上的應用,因此,探索一種低免疫原性的新型藥物遞送系統具有重要的研究價值。
研究表明,紅細胞膜表面分布的一種跨膜蛋白CD47可與單核-巨噬細胞表面信號調節蛋白-α(signal regulatory protein-alpha,SIRP-α)受體結合產生抑制信號,從而使其避免被RES吞噬清除[11]。因此將紅細胞與納米載體相結合能夠降低納米載體的血漿蛋白結合率、降低RES的清除作用從而延長其在體內的循環時間。且與合成納米載體相比,紅細胞具有易獲得性、生物相容性好、循環周期長、體積與比表面積大與生物消除機制安全等優點[12-14]。將紅細胞與納米載體相結合構建紅細胞-納米載體遞藥系統不僅能夠延長納米載體的體內循環時間,還可提高納米載體的靶向性,提高藥物的生物利用度,因此具有良好的應用前景。根據紅細胞與納米載體的構建方式不同,可以分為以下3種方式:紅細胞包埋納米載體、紅細胞表面結合納米載體與紅細胞膜包被納米載體。本文主要就這3種構建方式介紹紅細胞-納米載體遞藥系統的最新研究進展。
1 紅細胞包埋納米載體遞藥系統
紅細胞包埋納米載體遞藥系統是指將納米載體封裝入紅細胞內,使納米載體與體循環血液環境基本隔絕,因此能夠保護納米載體不被RES清除從而延長納米載體的循環時間[15]。將納米載體包埋入紅細胞內必須要穿過細胞膜。因此,在不破壞細胞膜的情況下,將其裝載到紅細胞中,是制備的關鍵環節,主要通過低滲預膨脹的方法實現[16]。低滲預膨脹法是將紅細胞置于相對低滲的溶液環境中,使紅細胞發生膨脹打開紅細胞膜的緊密連接,在紅細胞膜表面出現20~50 nm的瞬時孔洞,此時向溶液環境中加入納米載體,納米載體通過孔洞進入紅細胞后再將溶液環境恢復為等滲狀態,紅細胞即恢復到正常狀態,細胞膜表面的孔洞關閉,納米載體被截留封裝進紅細胞內。這種方法通常將粒徑較小的納米載體如磁性無機納米粒封裝入紅細胞,用于藥物遞送與體內成像等。繆婉琳[17]采用低滲透預膨脹方法,將磁性納米粒Fe3O4@DMSA與化療藥物鹽酸阿霉素封裝入紅細胞中,構建一種磁響應性紅細胞遞藥系統。將其回輸到小鼠體內后,通過外磁場的作用可將回輸的紅細胞載藥體系聚集到腫瘤部位。與游離阿霉素相比,紅細胞遞藥系統在抑制腫瘤生長、降低藥物劑量與藥物副作用等方面具有顯著優勢。Antonelli等[18-19]將經美國FDA批準上市的血管造影劑磁性納米粒Ferucarbotran包埋在紅細胞內,小鼠藥代動力學與核磁共振成像實驗結果顯示,紅細胞包埋Ferucarbotran的新型示蹤劑能夠顯著延長其在血液中的循環時間并增強了在器官和腦血管的顯像能力。Hamidi等[20]將負載抗癲癇藥物丙戊酸鈉的殼聚糖納米凝膠包埋入紅細胞內構建紅細胞納米載體遞藥遞藥系統,實驗結果顯示該遞藥遞藥系統能夠延緩藥物釋放,從而達到延長藥物作用時間的目的(見圖1)。然而,通過低滲預膨脹的方法只能用于包封粒徑較小的納米載體,對于粒徑較大的納米載體并不適用。除此之外,通過電穿孔法、化學包埋法等其他包埋方法會對紅細胞造成更大的損傷,降低紅細胞的生物相容性。

圖1 紅細胞包埋納米載體遞藥系統示意圖[21]
2 紅細胞表面結合納米載體遞藥系統
早期對紅細胞的研究多集中在將納米載體包埋入紅細胞內部,忽略了對紅細胞膜的利用。紅細胞表面積高達160 μm2,為納米載體的表面結合提供了充足的空間,而且將納米載體結合在紅細胞膜表面不需要在紅細胞膜表面打孔,一定程度上降低了對紅細胞結構和功能的損傷。紅細胞表面結合納米載體的方式分為特異性結合與非特異性吸附兩種方式。
2.1 紅細胞與納米載體的特異性結合紅細胞表面含有各種豐富的多糖、氨基酸殘基與抗原,使其能夠與納米載體通過化學共價鍵結合或配體-受體特異性結合。
2.1.1 化學共價鍵介導的特異性結合紅細胞膜表面含有大量硫醇基團,可將其生物素功能化,從而與親和素修飾的納米載體偶聯,與紅細胞之間形成一種穩定的特異性結合作用。Wang等[22]制備了一種表面涂覆光敏劑二氫卟吩e6(chlorin e6,Ce6)與PEG的氧化鐵磁性納米粒,并進一步通過生物素-親和素偶聯作用將其結合到載有化療藥物的紅細胞表面構建了載藥紅細胞-磁性納米粒-Ce6磁響應藥物遞送系統(RBC-IONP-Ce6-PEG)(見圖2)。體內成像結果表明,RBC-IONP-Ce6-PEG可顯著延長納米載體在體內的循環時間,當在腫瘤部位外加磁場,可實現納米載體在腫瘤部位的靶向富集。體內藥效結果進一步顯示,載有化療藥物的紅細胞與磁靶向的聯合治療能夠以較低藥物劑量達到抗腫瘤效果,且具有顯著的協同效果。
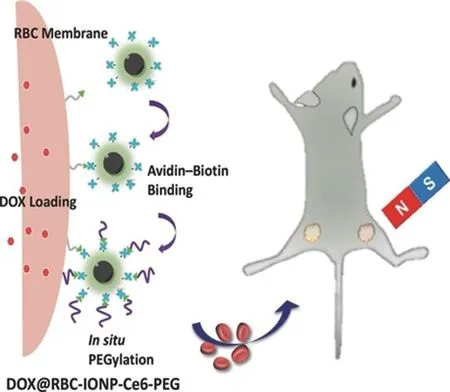
圖2 化學共價鍵介導的紅細胞與納米載體特異性結合示意圖
2.1.2 配體-受體介導的特異性結合紅細胞與納米載體特異性結合的另一種方式是配體-受體介導的特異性結合。近年來,通過噬菌體展示技術篩選了大型隨機肽庫,已發現多種與紅細胞表面受體特異性結合的肽段配體,有助于納米載體與紅細胞的配體-受體偶聯結合[23]。經與紅細胞表面蛋白特異性結合的親和配體(抗體、多肽片段等)修飾的納米載體具有較高的紅細胞表面結合率[24]。血型糖蛋白A(glycophorin A,GPA)是紅細胞膜表面的一種具有受體功能的唾液酸糖蛋白,具有很高的親和力與特異性,可用作配體結合的靶位點[25]。Sahoo等[26]研究發現,在載牛血清白蛋白的納米粒表面修飾了對GPA具有高親和性的12位氨基酸多(ERY1),可使納米粒通過配體-受體特異性結合作用黏附在紅細胞表面,延長載藥納米粒在體內的循環時間(見圖3)。
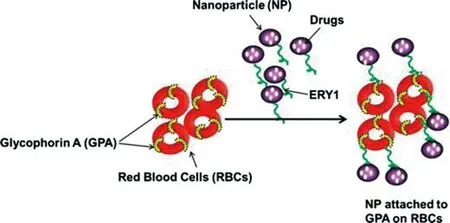
圖3 配體-受體介導的紅細胞與納米載體特異性結合示意圖
配體-受體介導的紅細胞與納米載體的特異性結合方式相對于共價連接的方式對紅細胞的損傷較小。但也有缺點,比如納米載體吸附過多會影響紅細胞表面跨膜蛋白,導致其易被單核-巨噬細胞吞噬,紅細胞的體內循環壽命降低。此外,由于體內多種細胞的表面有相同或相似受體,使納米載體可能與體內其他非特異性細胞結合,影響藥物的體內遞送。
2.2 紅細胞與納米載體的非特異性吸附相比與紅細胞與納米載體特異性結合,紅細胞與納米載體結合的最簡單的方法是將納米載體非特異性物理吸附到紅細胞表面,這種非特異性吸附又稱“紅細胞搭便車”技術(red blood cell-hitchhiking,RH)[27]。紅細胞的質膜表面存在能與疏水納米載體結合的相對疏水的結構域,這些疏水相互作用能使帶正電荷和負電荷的疏水納米粒均能與紅細胞表面結合。紅細胞膜中含有的羧酸、唾液酸和磷酸等帶有負電性的基團使其表面帶有負電荷,有利于帶正電荷納米載體的吸附[28]。Zelepukin等[29]考察了表面帶有不同電荷的粒徑不同的磁性納米粒的紅細胞吸附效率與小鼠體內循環時間,結果顯示帶正電荷的疏水性磁性納米粒紅細胞表面吸附效率較高且能在血液循環中保留較長時間。納米載體可通過范德華力、靜電吸附力、疏水相互作用、氫鍵等驅動力吸附在紅細胞表面,這種非特異性吸附作用是可逆的,能夠改變納米載體的體內行為。
2.2.1 延長體內循環時間正常紅細胞的在體內的壽命約為120 d,其體內循環時間遠高于納米載體,而將納米載體以非特異性吸附的方式附著在紅細胞表面,可以避免RES的巨噬細胞吞噬和清除作用,從而延長納米載體在體內的循環時間。有研究表明,游離納米載體在大鼠血液循環中的保留了5 min,而RH的納米載體在血液環境中保留了10 h[30]。Wang等[31]將負載維生素K1的陽離子殼聚糖納米粒與紅細胞共同孵育,制備了紅細胞表面吸附殼聚糖納米粒,并對其進行藥動學分析,結果顯示與納米粒和游離藥物相比,負載維生素K1殼聚糖納米粒的紅細胞遞藥系統具有較好的緩釋作用,并可實現體內長循環效果。
2.2.2 改變納米載體生物分布除了降低RES的清除作用、延長納米載體的循環時間外,RH還改變了納米載體在生物體內的分布情況,表現為RH能夠增加納米顆粒的肺部蓄積,同時降低肝臟和脾臟的攝取和清除作用。
Anselmo等[30]將羧化聚苯乙烯納米粒吸附到紅細胞表面,然后通過靜脈注射入小鼠體內,結果顯示與游離納米粒相比,紅細胞表面吸附納米粒在肺部蓄積高達7倍。Zhao等[32]采用“紅細胞搭便車”技術,將載有阿霉素的PLGA納米粒遞送至肺部以治療肺轉移黑色素瘤。與游離納米粒相比,RH納米顆粒的肺組織藥物蓄積達到的15倍以上,從而提高肺部治療藥物劑量,顯著抑制肺轉移瘤進展,改善肺癌的預后。RH可以與傳統的抗體靶向相結合,通過協同作用提高藥物在肺部的蓄積。Anselmo等[33]結合“紅細胞搭便車”技術,納米粒棒狀結構和抗體靶向相結合構建ICAM-Rod-Hitchhike遞送藥物并探究其對于肺部炎癥模型的協同作用。由于在肺部炎癥模型肺組織內皮細胞高表達ICAM,利用ICAM單克隆抗體對納米粒進行表面修飾。將ICAM單克隆抗體表面修飾,棒狀結構與“紅細胞搭便車”技術的納米粒單獨及聯合應用進行對比,考察納米粒的炎癥肺部的蓄積作用(見圖4)。結果顯示,這3個方面的聯合應用可以有效降低納米粒在肝、脾中的濃度,同時顯著增加了納米粒在肺部的有效蓄積。Brenner等[34]研究發現RH除了將納米載體靶向遞送至肺組織外,還可通過改變RH注射部位將納米載體選擇性優先遞送至注射部位下游的器官,當將RH注射入頸內動脈、腎動脈或頸總動脈時、RH表面搭載的納米載體分別靶向遞送至腦、腎或面部,為利用RH將表面搭載納米載體進行不同器官的靶向遞送提供了新的可能,并將其擴展于其他臨床應用。
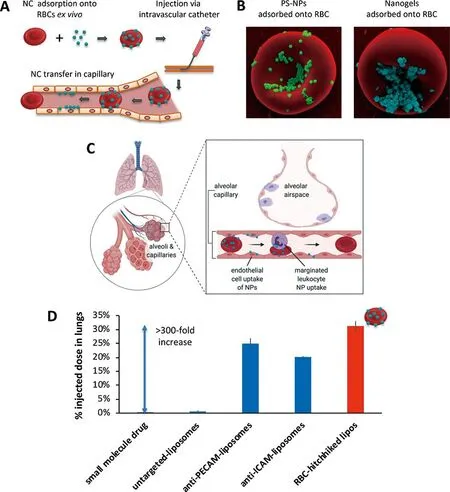
圖4 “紅細胞搭便車”的作用示意圖
RH這種改變納米載體生物分布的機制是由于體內RH流經下游器官致密毛細血管網絡時,由于毛細血管直徑遠小于紅細胞直徑,因此紅細胞表面吸附納米粒在流經狹窄毛細血管高剪切應力環境時納米粒從紅細胞表面可逆脫落并轉移至下游器官中。搭載在紅細胞表面的納米載體的大小和形狀可能會影響它們在體內的藥代動力學和生物分布,研究發現粒徑較大的帶正電荷疏水性納米載體在紅細胞表面吸附效率較高且能在體內循環時間較長,且與球形納米粒相比,桿狀顆粒在肝臟和脾臟中的分布較少,在肺部的分布較多。此外,通過增加非特異性吸附在紅細胞上納米載體的數量使載體紅細胞質膜更堅硬和誘導瞬時膜損傷,這兩種效應會導致產生肺部剪切誘導的納米載體分離的抵抗力,使脾臟中納米載體與免疫細胞之間的相互作用增加,最終導致納米載遞送到脾臟而不是肺部[35]。
3 紅細胞膜包被納米載體
紅細胞膜包被納米載體是將納米粒內核和紅細胞膜結合,能夠提高納米載體穩定性、延長納米載體在血液中循環時間以及實現藥物緩控釋放,是一種已進入臨床研究的極具發展前景的新型藥物載體(總結如表1所示)。紅細胞膜包被納米載體的制備通常包括兩個部分:紅細胞衍生囊泡的提取與囊泡-納米載體融合。紅細胞衍生囊泡一般通過低滲透析擠壓法獲得,首先將紅細胞置于低滲環境下使紅細胞膜孔打開釋出內容物,得到的紅細胞膜經納米膜擠壓得到紅細胞衍生囊泡,然后通過機械擠出將納米載體與囊泡進行融合。自2011年,Hu等[36]首次設計了紅細胞膜包被PLGA納米粒用于開發長循環納米遞藥系統。與傳統的PEG修飾PLGA納米粒15.8 h的半衰期相比,紅細胞膜包被納米粒的半衰期長達39.6 h。然而,紅細胞膜包被納米載體缺乏主動靶向能力限制了其在臨床的應用,基于此,人們提出了將靶向配體與紅細胞膜相結合的脂質插入策略。Su等[37]設計了嵌入腫瘤穿透肽iRGD的紅細胞膜包被負載紫杉醇的雜化聚合物納米粒核心的遞藥系統(RNPs),RNPs與游離納米粒相比血液循環半衰期延長了5.8倍。此外,由于RNPs提高了腫瘤穿透能力,可顯著抑制90%以上的腫瘤生長,并抑制95%的肺轉移。然而,負載在紅細胞膜包被的納米載體中的藥物釋放過程通常是不受控的、基于自由擴散的機制釋放[38]。因此,將藥物可控釋放與長循環相結合是精準給藥的關鍵因素。針對這一問題,提出了刺激響應性紅細胞膜包被納米載體,以實現精準的藥物遞送與釋放[39-40]。Pei等[41]制備了由活性氧響應性的紫杉醇二聚體前藥(PTX2-TK)與光敏劑(5,10,15,20-四苯基氯,TPC)組成的聚合物納米粒,并通過進一步紅細胞膜包被獲得紅細胞膜包被納米顆粒。該納米顆粒在638 nm激光照射下,TPC可以產生ROS,并觸發PTX2-TK裂解,破壞了紅細胞膜,促進PTX在腫瘤組織內的快速釋放。體內實驗結果證實,紅細胞膜表面涂層可延長納米顆粒在血液環境中的循環時間,改善腫瘤藥物蓄積。紅細胞膜包被納米載體已被廣泛研究用于多種應用,包括藥物遞送、成像、光療、納米疫苗和納米解毒劑等,并在癌癥、細菌感染、心血管疾病、自身免疫性疾病等方面均具有極大的應用潛力。
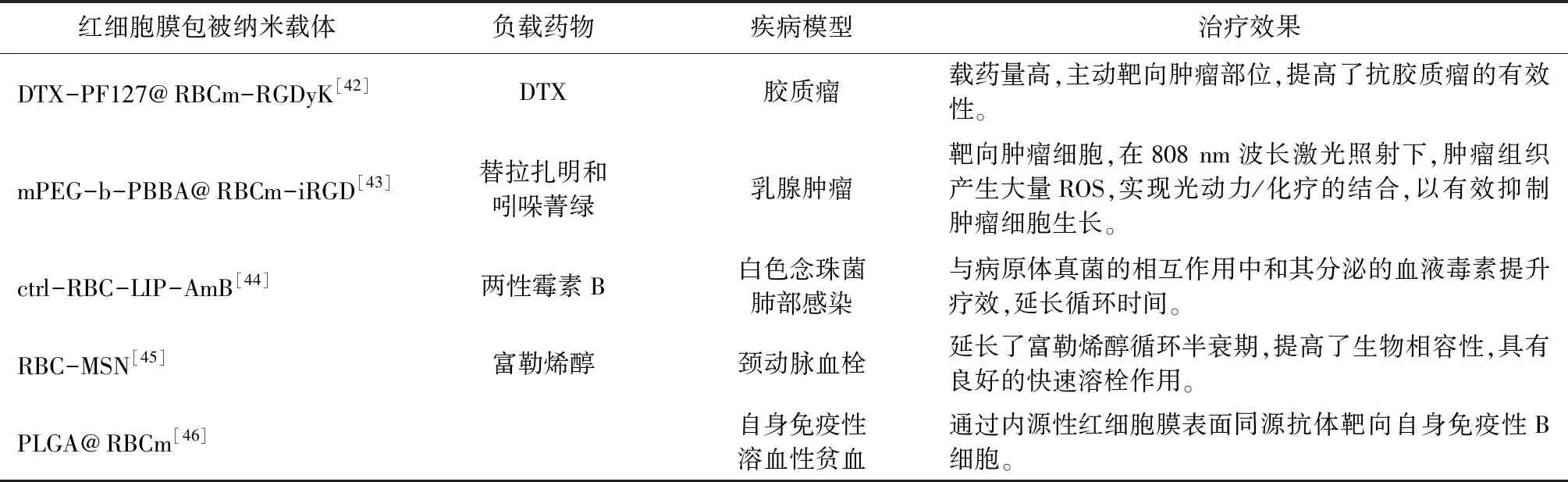
表1 紅細胞膜包被納米載體臨床應用研究
4 結語
紅細胞作為新型藥物遞送載體具有生物相容性好、免疫原性低、循環時間長等特性,在藥物遞送方面有著較為廣闊的發展前景。將紅細胞與納米載體相結合可以克服納米載體在體內被RES系統迅速清除的局限性,在延長藥物在體內的循環時間、提高藥物穩定性與靶向性等方面與其他傳統藥物載體相比具有明顯優勢。但也存在若干不足,如紅細胞包埋納米載體僅用于包載粒徑較小的磁性納米粒或其他無機納米載體,且需要穿透紅細胞膜,容易導致細胞破裂,對紅細胞的損傷較大。將納米載體通過共價或配體-受體介導結合到紅細胞表面相對于包埋對紅細胞的損傷較小,而直接與紅細胞結合的方法仍可能導致紅細胞膜受損,從而使遞藥系統在體內快速清除。納米載體在紅細胞上的非特異性物理吸附被是對紅細胞生物活性影響最小的表面結合方法,并且在納米載體從紅細胞表面解吸后對紅細胞結構的影響也很小,是一種極具有應用前景的新型靶向藥物遞送系統。紅細胞膜包被納米載體能夠實現藥物的靶向遞送與刺激響應性釋放,然而在紅細胞膜提取或與納米顆粒融合過程中可能發生膜錨定片段的構象變化,導致其免疫原性增強激活體內免疫應答。紅細胞-納米載體遞藥系統仍處于初步研究階段,仍存在一些問題有待深入研究:①紅細胞來源于生物體,在提取、載藥和儲存過程中如何控制污染,減少對紅細胞的損傷仍是亟待解決的問題;②目前研究仍局限于小動物水平,還有待于大動物的實驗對其體內性能進行驗證;③在人體臨床應用時,需系統分析紅細胞表型,選擇與機體匹配的紅細胞進行制備。隨著對紅細胞-納米載體遞藥系統研究的不斷深入,這種新型遞藥系統的臨床應用前景會更加廣闊。

