金蕎麥膠囊中間體制備工藝的優選及質量控制
李春霞 童曉東 陳銀銀

【摘?要】?目的:優選金蕎麥膠囊中間體的制備工藝以及質量控制。方法:以表兒茶素為實驗指標,通過正交實驗,圍繞提取時間、回流時間、回流次數考察選取最佳工藝。結果:當溶劑為藥材的6倍量,乙醇濃度為50%,回流為1 h為最佳制備工藝。結論:所建立的方法操作容易,結果準確可靠重現,可顯著提高表兒茶素的提取,可用于金蕎麥膠囊中間體的制備。
【關鍵詞】?金蕎麥;表兒茶素;提取工藝;正交試驗;高效液相
【中圖分類號】R284.1???【文獻標志碼】 A????【文章編號】1007-8517(2024)03-0025-05
DOI:10.3969/j.issn.1007-8517.2024.03.zgmzmjyyzz202403006
Optimization and Quality Control of the Preparation Technology of Gold Buckwheat Capsule
LI Chunxia1?TONG Xiaodong2*?CHEN Yinyin3
1.Nantong RichHospital(FourthClinicalMedical Collegeof Yangzhou University),Nantong 226010,China;
2.Nantong Hospital of Traditional Chinese Medicine(Nantong Hospital to Nanjing University of Chinese Medicine),
Nantong 226001,China;
3.Nanjing University of Chinese Medicine HanLin College, Taizhou 225300,China
Abstract:Objective The preparation technology and quality control of gold buckwheat capsule intermediate were optimized.Methods Taking epicatechin as the experimental index, through orthogonal experiment, the optimal process was selected around extraction time, reflux time and reflux times.Result The solvent was 6 times the amount of medicinal materials, the concentration of ethanol was 50%, and the best preparation process was reflux for 1 hour.Results The method is easy to operate, and the results are accurate and reproducible, The extraction of epicatechin can be significantly improved,and suitable forpreparation technology of Gold buckwheat capsule.
Keywords:Fagopyrum Dibotrys ; (-)-epicatechin; Extracting Technology; Orthogonal Test; HPLC
金蕎麥是蓼科Polygonaceae植物金蕎麥 Fagopyrum dibotrys(D.Don) Hara 的干燥根莖,味道略微辛辣、苦澀、清涼刺激,歸肺經,具有清肺排痰、清熱解毒、祛風化濕、排膿消腫的功效[1]。金蕎麥中含有各種成分,如表兒茶素、蘆丁、槲皮素等有效活性成分,且這些成分具有顯著的抑制癌癥、遏制腫瘤細胞的侵襲和轉移,以及消除炎癥,抗菌等重要作用[2-3],市面上許多抵抗癌癥藥物和預防癌癥的藥物都是與金蕎麥有關[4-5]。
金蕎麥煎劑原本為南通地區民間藥物,后南通市中醫院的程云龍老專家在其基礎上研究制成金蕎麥藥物制劑,其具有清熱解毒、排膿祛瘀、祛痰止咳平喘的作用。臨床常用于治療急慢性氣管炎、急性肺膿瘍、支氣管哮喘等疾病[6],但是具有不宜攜帶性,用量大等缺點,而膠囊卻為更適用得多,便于大規模生產。現有金蕎麥制劑直接以水煎提,工藝及質量不穩定,效率低,為有效控制金蕎麥膠囊的質量,對蕎麥膠囊中間體的制備工藝進行了優化,直接乙醇提取,不僅有效成分的提取率提高,而且節省工作時間,提高了工作效率,能夠更準確、更全面、更有效地控制其質量,方法實用可靠,保證臨床質量要求。
1?儀器與材料
1.1?主要儀器?MS105DU型十萬分之一電子天平(Mettler Toledo貿易有限公司);UltiMate3000高效液相色譜儀(Thermo Fisher Scientific有限公司);HH.S11-4型數顯恒溫水浴鍋(上海博迅醫療生物儀器股份有限公司);OSJ-UP-30超純水機(濟南歐萊博科學儀器有限公司);YM-080T型超聲波清洗機(深圳市方奧微電子有限公司); RE-3000D旋轉蒸發器(上海亞榮);TD4型離心機(湖南凱達科學儀器); C18分析色譜柱(Waters有限公司)。
1.2?藥物和試劑?(-)表兒茶素對照品(批號878-200102):中國藥品生物制品檢定所;金蕎麥中藥飲片(批號20190607、20190924):南通三越中藥飲片有限公司,(批號20191029):江蘇建生源中藥材有限公司;乙腈(分析純):國藥集團化學試劑有限公司;乙腈(色譜純)、甲醇(色譜純):德國默克公司;甲酸、磷酸、甲醇、乙酸乙酯、乙醇(分析純):南京化學試劑股份有限公司;硅膠板(批號20180308):青島海洋化工廠分廠。
2?方法與結果
2.1?藥材的選取?為了控制膠囊中間體的質量,首先從藥材的源頭來選取了三批不同批次的金蕎麥飲片,通過回流提取,以金蕎麥中表兒茶素的含量作為指標來選取最佳的藥材飲片。
2.2?藥材薄層鑒別及含量測定
2.2.1?藥材鑒別中對照品溶液的制備?稱取表兒茶素標準品5 mg放置于5 mL容量瓶中,向其中加入甲醇適量定容至刻度線處,配置制成每1 mL含有1 mg的溶液。
2.2.2?藥材鑒別中供試品溶液的制備?稱取三種不同批次的金蕎麥飲片各2.5 g,放置于圓底燒瓶中,再各自向其中加入20 mL甲醇,靜置1 h,加熱回流1 h,冷確至室溫,過濾,在60 ℃下將濾液濃縮至5 mL,作為供試品溶液備用[7]。
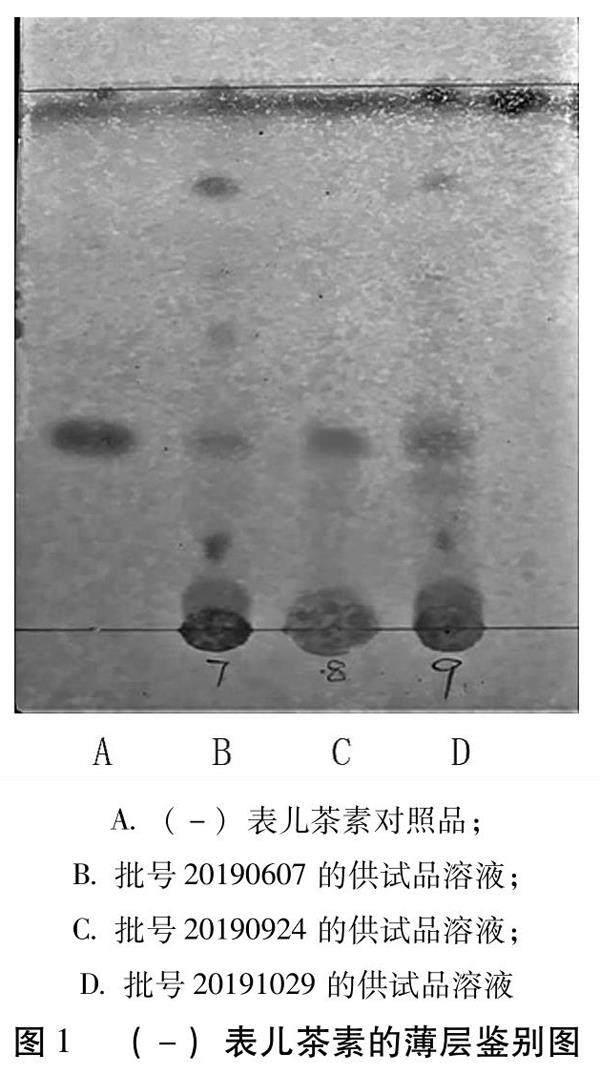
2.2.3?(-)表兒茶素的鑒別?按照薄層色譜法(通則0502)試驗,用毛細管吸取供試品溶液和對照品溶液各5 μL,分別點于同一硅膠薄層板上,以甲苯-乙酸乙酯-甲醇-甲酸作為展開劑比例分別是1∶2∶0.2∶0.1,展開,取出薄層硅膠板,晾干,用25%磷鉬酸乙醇溶液噴薄層板,用吹風機加熱至斑點顯色清晰,供試品在與對照品色譜相應的位置上,顯相同顏色的斑點[7]。因只有單味藥材,所以不做陰性對照。色譜圖如圖1所示。
2.2.4?藥材含量測定對照品溶液的制備?精密稱定表兒茶素標準品0.0041 g放置10 mL容量瓶中,加乙腈-水混合溶液兩者比例為10∶90,定容至容量瓶刻度線。
2.2.5?藥材含量測定供試品溶液的制備?將三種不同批次的金蕎麥飲片(批號20190607、批號20190924、批號20191029)打成粗粉,每批次取2.0 g,精密稱定,放入圓底燒瓶中,向其中加入50 mL稀乙醇,乙醇濃度為50%,用封口膜密封,然后精密稱定,首先放置1 h,再通過水浴鍋加熱回流1 h,然后放冷至室溫,再稱定其重量,用稀乙醇補足失去的重量,充分搖勻,再過濾,精密量取續濾液25 mL,在60 ℃下加熱濃縮至近干,殘渣加比例為10∶90乙腈-水混合溶液分次洗滌,溶解液轉移至10 mL量瓶中,再加乙腈-水混合溶液至刻度,振蕩搖勻,用離心機離心5 min,轉速為每分鐘3000轉,上清液精密量取5 mL,加于聚酰胺柱(濕法裝柱,30~60目,柱長為15 cm,內徑為1.0 cm)上,先用50 mL水洗脫,再用100 mL乙醇洗脫,收集乙醇洗脫液, 低溫濃縮至近干,殘渣用乙腈-水(10∶90)混合溶液溶解,轉移至10 mL量瓶中,加乙腈-水混合溶液稀釋至刻度,搖勻,即得[7]。
2.2.6?測定法?分別精密吸取對照品溶液與供試品溶液各10 μL,注入高效液相色譜儀,記錄峰面積,通過標準曲線法算出相應含量即得,批號20190607、批號20190924、批號20191029的金蕎麥飲片三者含量分別是670.19 μg/g、354.68 μg/g、512.28 μg/g,因此選取批號20190607的金蕎麥飲片進行實驗。
2.3?蕎麥膠囊中間體含量測定
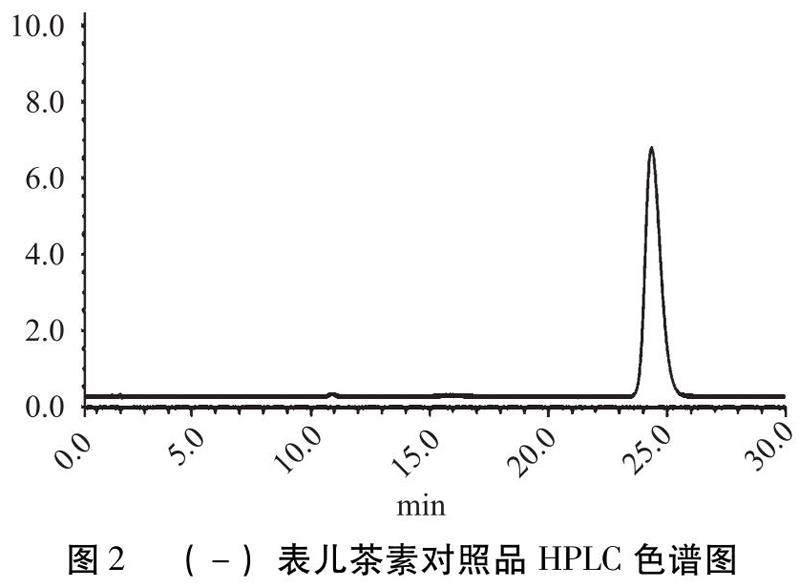
2.3.1?色譜條件與系統適用性條件?XBridgeC18(4.6 mm×150 mm,5 μm);以乙腈-0.004%磷酸溶液(7∶93)為流動相;流速:1.0 mL/min;進樣量為10 μL。檢測波長為280 nm;柱溫30 ℃。色譜分離如圖2、圖3所示。
2.3.2?供試品溶液的制備?取金蕎麥浸膏0.2 g,加入10 mL比例為10∶90乙腈-水混合溶液,超聲直至溶解,量瓶中定容至10 mL,振蕩搖勻,再用離心機(3000 r/min)離心5 min,上清液精密量取5 mL,加于聚酰胺柱(濕法裝柱,30~60目,柱長為15 cm,內徑為1.0 cm)上,先用50 mL水洗脫,再用100 mL乙醇洗脫,收集乙醇洗脫液,低溫濃縮至近干,殘渣用乙腈-水(10∶90)混合溶液溶解,轉移至5 mL量瓶中,加乙腈-水混合溶液稀釋至刻度,搖勻,即得[7]。
2.3.3?方法學考察
2.3.3.1?線性關系考察?精密稱取表兒茶素對照若干,加乙腈-水混合溶液(兩者比例為10∶90)稀釋分別配成82 μg/mL、65.6 μg/mL、49.2 μg/mL、32.8 μg/mL、16.4 μg/mL的溶液,用使用0.45 μm微孔濾膜濾,分別進樣,每個進樣3針,每針進樣10 μL,觀察峰面積。以峰面積平均值對表兒茶素的濃度進行線性回歸,得到回歸方程為Y=0.0911X-1.1961,r=0.9992。表明表兒茶素在16.41~82 μg/mL內線性關系良好。
2.3.3.2?精密度試驗?精密吸取標準溶液10 μL,連續進樣5次,測定峰面積。測得的RSD為0.94%,表明儀器精密性良好。
2.3.3.3?穩定性試驗?取供試品溶液,分別在放置0 h、2 h、4 h、6 h、8 h后進行測定,測得的RSD為0.61%。表明樣品在8 h內穩定。
2.3.3.4?回收率試驗?采用加樣回收法,精密稱取一份金蕎麥浸膏0.2 g,依法按照“2.3.1供試品溶液的制備”制成供試品溶液,并在其中加入定量的表兒茶素標準品,連續進樣5針,每針注入10 μL于高效液相色譜儀中,測量結果見表1,平均回收率為98.28%,RSD為1.56%。
2.4?制備工藝的優選
2.4.1?提取工藝的選擇?溶劑量、回流時間、溶劑濃度是提取過程參考因素中是非常重要的,為了達到最佳的全面實驗等效的結果以最少的次數,采用了三因素三水平正交試驗。見表2。
2.4.2?正交試驗?設計優選制備工藝按照 L9(34) 正交表安排試驗,取9份粉碎成粗粉每份20 g的金蕎麥藥材,按正交表分別加入對應的乙醇,置于圓底燒瓶中進行回流提取,濾過,合并濾液,60℃濃縮成膏,干燥,即得樣品,以表兒茶素的含量為指標篩選制備工藝。結果見表3正交試驗設計及結果。
表兒茶素的含量=(測得表兒茶素的濃度×稀釋體積×干膏)/(金蕎麥的質量×干膏量)
2.4.3?實驗結果的統計學分析?從表4可以分析出在三個因素中,回流時間的顯著水平幾乎無影響,不做考慮,溶劑濃度和溶劑量都具有顯著差異,再結合實際生產選取回流時間為一h,通過圖4的效應曲線圖可知最佳溶劑濃度為50%、最佳溶劑量為6倍量的乙醇。所以乙醇濃度為50%,溶劑量為6倍量,回流1 h為最佳制備工藝。
2.4.4?驗證性試驗?根據正交試驗結果,確定最佳的制備方法,取每份20 g金蕎麥粗粉3份,加入6倍量50%的乙醇,回流兩次,每次1 h,在60 ℃下濃縮至干膏。每份取0.2 g,用比例10∶90乙腈-水混合溶液溶解,按照2.3.2的方法制成供試品溶液,在測量其含量,測得表兒茶素的含量分別是190.1775 μg/g、195.0128 μg/g、193.2148 μg/g,計算RSD結果為1.27%,結果表明此最佳工藝穩定可行、可重復性好。
2.5?金蕎麥膠囊中間體的質量控制?中藥制劑較化學藥來說更加復雜,因為其成分更多,更雜,而且中藥制劑在制備過程和它的貯藏過程中都會產生一些變化,因此它的質量控制比化學藥要復雜得多,而且不同批次的藥材也會影響制成中藥藥物制劑質量的穩定性,因此中藥制劑的質量控制是一項不可缺少的工作。對此我們可以從藥材的質量控制、制法規范、衛生學3個方面來控制。
2.5.1?藥材的質量控制的選擇?中藥制劑質量以藥物的來源、藥物的規格以及藥材的品種為基本[8],在藥物生產過程中占有巨大的影響,因此在制備中藥制劑時必須以藥材的來源、品種與規格作為選用的標準。而且但凡是藥品標準收載的中藥制劑,都應按照藥品的標準規定的方法制備。
2.5.2?制法規范的選擇?中藥制劑制作方式與中藥制劑的質量緊密相連,所以根據不同的需求選用不同的劑型,如臨床的需要,藥材的性質,藥材的不同成分,待選定相應的劑型后,然后再研究藥物制劑的生產過程,選擇最佳的生產工藝,從而保證中藥制劑的質量。因此但凡是在藥品標準中收錄的中藥制劑,在生產制備過程中均應按照藥品標準規定的標準進行生產。
2.5.3?衛生學標準的選擇?為了保證臨床用藥的安全、有效,國家有關部門頒布了藥品衛生標準,對中藥制劑中的致病菌、活螨、細菌、真菌等做了規定。包括熱原檢查、細菌內毒素檢查、無菌檢查、微生物限度檢查[9]。
2.5.4?鑒別與檢查?目前最主要的鑒別方法是薄層色譜法,用來檢查藥材的正確性以及藥物制劑中的主要有效成分。藥物制劑主要的檢查是藥典中制劑通則所規定的項目,如相對密度、干燥失重、崩解時限、重金屬等。
2.5.5?金蕎麥膠囊中間體(-)表兒茶素的鑒別?取金蕎麥膠囊中間體0.10 g,加入10 mL甲醇進行超聲溶解,然后進行過濾,60 ℃下進行濃縮,依2.1.3(-)表兒茶素的鑒別法鑒別,具體操作如下:照薄層色譜法(通則0502)試驗,用毛細管吸取供試品溶液和標準品溶液各5 μL,分別點于同一硅膠薄層板上,用甲苯-乙酸乙酯-甲醇-甲酸作為展開劑,展開,展開劑的比例分別是1∶2∶0.2∶0.1,待展開劑展開至前沿線,取出,晾干,用25%磷鉬酸乙醇溶液噴薄層板,用吹風機加熱至斑點顯色清晰[7]。供試品與對照色譜在相同的位置上,顯相同顏色的斑點因只有單味藥材,所以不做陰性對照。
2.5.6?金蕎麥膠囊中間體(-)表兒茶素的含量測定?按2.3蕎麥膠囊中間體含量測定方法取金蕎麥膠囊中間體配置供試品溶液,精密吸取標準品溶液與供試品溶液各10 μL,注入高效液相色譜儀,記錄兩者峰面積,通過標準曲線法算出相應含量即得。
3?討論
3.1?指標成分的選擇?臨床研究表明,金蕎麥中的表兒茶素的多羥基結構的分子結構特性導致其藥理活性較多,具有抗氧化、降血脂、降血糖、抑制胰島素、防止心血管疾病,此外還具有抗炎、抑菌、提高免疫力等生理活性[10],能夠針對金蕎麥藥物的主治病癥起到主要的治療作用,因此最終選用表兒茶素作為檢測對象。
3.2?流動相比例的選擇?在藥典基礎上對乙腈-水的比例進行改變,分別為8∶92、7∶93、5∶95,結果表明在兩者比例為7∶93和5∶95時分離都比較好,但5∶95時出峰時間遠遠大于7∶93時,考慮到操作的便捷性以及實驗材料的損耗,選擇流動相的比例為7∶93。
3.3?濃縮溫度的選擇?兒茶素類物質,在高溫(100 ℃) 條件下兒茶素主要發生脫沒食子酸和異構化反應[11],在堿性、過高溫度等環境條件下也容易發生改變[12],溫度設在60 ℃,此時通過薄層鑒別能夠很好地觀察到表兒茶素。
該實驗以表兒茶素的含量為指標篩選制備工藝,對于蕎麥膠囊中間體的提取具有方便操作,結果準確可靠重現,可顯著提高表兒茶素的提取率,質量可控。可用于金蕎麥膠囊中間體的制備。以表兒茶素和藥材為對照品對金蕎麥進行薄層鑒別可保證原料藥的質量。
參考文獻
[1]肖培根.新編中藥志第一卷[M].北京:化學工業出版社,2002:607-610.
[2] 艾群,王斌,王國清. 金蕎麥制劑的抑菌研究[J].黑龍江醫學, 2002, 26(9):666.
[3] CHEN P K. 金蕎麥體外抑制腫瘤細胞生長的研究[J].中西醫結合學報, 2003,1(2):128-131.
[4] 張雯潔,李興從,劉玉青,等. 威麥寧的酚性成分[J].南植物研究,1994, 16(4):354-356.
[5] 何顯忠.金蕎麥的藥理作用和臨床應用[J].珍國醫國藥, 2001, 12(4):316-317.
[6] 唐宇,賈洪鋒,孫俊秀,等.金蕎麥果實中有效成分的分析[J].中國野生植物資源,2013,32(1):52-55.
[7] 國家藥典委員會.中國藥典(一部)[S].北京:中國醫藥科技出版社,2010.
[8] 方亮.藥劑學[M].8版.北京:人民衛生出版社,2016:387-388.
[9] 劉敏,劉志春.藥品生產企業微生物實驗室設計[J].醫藥工程設,2008(1):18-21.
[10]童觀珍,付曉萍,楊艷,等.表兒茶素的分布及藥理活性研究進展[J].云南農業大學學報(自然科學),2018,33(2):343-349.
[11] LI Z, XIAO T, GAO L P, et al.Effect of temperature on the color of green tea infusion[J]. Journal of Anhui Agricultural University, 2010,37(3) :465-470.
[12] LI N, TAYLOR L S,FERRUZZI M G, et al. Kinetic study of catechin stability: effects of pH, concentration, and temperature [J].Journal of Agricultural & Food ,2012, 60(51):12531-12539.
(收稿日期:2023-05-06?編輯:劉?斌)
作者簡介:李春霞(1981—),女,漢族,本科,主管中藥師,研究方向為中藥學及中藥制劑。E-mail: ntlicx@163.com

