基于壓力-應變曲線評估心力衰竭病人整體無效做功對心臟再同步化治療應答的預測價值
黃志勇 吳杰瑩 劉譽紅 羅偉權 劉娟娟
摘要 目的:采用壓力-應變曲線(PSL)測定心臟整體無效做功(GWW),評估射血分數減低心力衰竭(HFrEF)病人術前GWW對心臟再同步化治療(CRT)應答的預測價值,及其與長期不良預后的關系。方法:選取2018年1月—2019年1月在中山市中醫院接受CRT治療的50例HFrEF病人為研究對象,于術前及術后9個月測量常規超聲心動圖參數,并采用基于二維斑點追蹤應變成像的壓力-應變曲線(PSL)測定包括GWW在內的心肌做功參數,應用受試者工作特征(ROC)曲線分析術前GWW對CRT應答的預測價值,應用Cox回歸分析模型分析術前GWW與CRT應答及不良事件的關系。CRT應答為從基線檢查到術后9個月隨訪期間左心室舒張末期容積(LVEDV)縮小≥15%,有CRT應答病人列為有效組,其余為無效組。研究的終點為CRT應答或隨訪期間的全因死亡。結果:與術前相比,有效組術后的LVEDV、左心室舒張末期內徑(LVEDD)和左心室收縮末期容積(LVESV)較術前均減小,左室射血分數(LVEF)較術前增大;有效組術后的GWW下降,整體有效做功(GCW)、整體做功指數(GWI)、整體做功效率(GWE)均增高,差異有統計學意義(P<0.05)。術前無效組的GWW與GCW均低于有效組(P<0.05)。ROC曲線分析顯示,相較于其他心肌做功參數,術前GWW預測CRT應答的ROC曲線下面積(AUC)最大,其AUC為0.78[95%CI(0.69,0.88), P<0.01],當GWW為175 mmHg%時預測CRT應答的特異度為85.7%,敏感度為67.8%。Cox回歸分析模型顯示,對HFrEF病人接受CRT的已知預后因素進行校正后,GWW<175 mmHg%與全因死亡的相對風險增加相關[校正HR=2.04,95%CI(1.10,3.84),P=0.024];將GWW添加到包含已知CRT預后因子的基線模型中,該模型呈正相關(改善χ2=4.85,P=0.028);GWW相較于其他心肌做功參數,與CRT應答和預后的相關性最佳。結論:HFrEF病人術前低GWW(<175 mmHg%)與CRT候選者無應答以及全因死亡風險相對增加有關,術前GWW是改善CRT選擇的一個預示參數。
關鍵詞 射血分數減的低心力衰竭;超聲心動描記術;二維斑點追蹤應變成像;心肌應變;心肌做功;心臟再同步化治療
doi:10.12102/j.issn.1672-1349.2024.03.019
基金項目 中山市社會公益科技研究項目(No.2022B1091)
作者單位 中山市中醫院(廣東中山 528400),E-mail:407371975@qq.com
引用信息 黃志勇,吳杰瑩,劉譽紅,等.基于壓力-應變曲線評估心力衰竭病人整體無效做功對心臟再同步化治療應答的預測價值[J].中西醫結合心腦血管病雜志,2024,22(3):502-508.
心臟再同步化治療(CRT)是治療射血分數減低、QRS持續性時間延長心力衰竭病人的有效方法[1]。風險分層仍然是心力衰竭病人治療的關鍵,30%的病人在CRT后不能改善,甚至可能惡化[2]。因此,識別CRT不良預后的預測因素至關重要。近期研究表明,超聲心動圖有助于識別CRT后出現左室逆重構和預后改善的射血分數減低的心力衰竭(HFrEF)病人[3]。在左束支傳導阻滯病人中,收縮早期右室和室間隔首先被激動,產生室間隔的特異性運動即室間隔抖動(septal flash,SF)使未激活的左室側壁先向右拉伸[4-5],由于左室電活動傳導延遲,左室側壁收縮延遲,在收縮晚期出現收縮后收縮,使室間隔再向左拉伸,同時伴隨左室心尖的特征性順時針運動,產生心尖擺動征(apical rocking,Ap Rock)[6]。SF和Ap Rock的識別與左室逆重構和CRT預后存在相關性[7],但其存在局限性,因為識別這些特征高度依賴超聲醫師的經驗,此外,這些指標只考慮到左室激活延遲,并未結合殘余心肌收縮力的影響,這是CRT改善左室功能的先決條件。同時結合了二維斑點追蹤應變成像及非侵入性左心室實時壓力的壓力-應變曲線(PSL)能夠定量評價心肌做功,組內及組間的重復性好,目前已在臨床中應用[8-11]。盡管既往研究已聚焦于心肌做功參數與CRT應答之間的關系[12-14],但缺少關于評價殘余心肌收縮力的心臟整體無效做功(GWW)與臨床預后的相關性研究,且結果存在分歧[13,15]。因此,本研究采用PSL測定心GWW,評估HFrEF病人術前GWW對CRT應答的預測價值,以及與長期不良預后的關系。
1 資料與方法
1.1 一般資料
本研究來源于一項前瞻性隊列研究,選擇2018年1月—2019年1月
在中山市中醫院接受CRT治療并成功植入起搏器的50例HFrEF病人為受試者。將術后9個月隨訪期間左心室舒張末期容積(LVEDV)縮小≥15%的病人列為CRT治療有效組,其余為無效組。
受試者納入標準:符合紐約心臟病協會(NYHA)心功能分級Ⅲ級或Ⅳ級的HFrEF病人;QRS持續時間延長,完全性左束支傳導阻滯(LBBB)病人≥120 ms,或非LBBB病人≥150 ms;左心室舒張末期內徑(LVEDD)>55 mm,左室射血分數(LVEF)≤35%。
排除標準:近期(<3個月)發生急性冠狀動脈綜合征或冠狀動脈血運重建;原發性二尖瓣或主動脈瓣病變(中度及以上);先天性心臟病;因鎖骨下動脈、腋動脈、肱動脈狹窄性病變而影響測量肱動脈血壓;因圖像質量差或心內膜顯示不清而不能進行斑點追蹤應變分析。
1.2 臨床資料收集
包括病人性別、年齡、冠心病史、心房顫動史、NYHA分級、QRS持續時間、LBBB、SF和/或Ap Rock、血漿N-末端腦鈉肽前體(NT-proBNP)水平等。
1.3 CRT設備植入
由電生理學醫師植入,目標位置是冠狀竇靜脈的基外側、前外側或后外側,用于定位LV導線。室間隔間時間設置為0,設定短感知房室間期(80~100 ms)和起搏房室間期(130 ms)以促進雙心室起搏,出院前應注意在心電圖和連續檢測中確認是否存在真性融合波、假性融合波。
1.4 超聲心動圖檢查
1.4.1 儀器與軟件
使用GE Vivid E9超聲診斷儀采集圖像,配備M5S-D超聲探頭(1.7~3.4 MHz)及上臂袖帶同步血壓計,設置成像幀頻50~80(65±10)幀/s。使用EchoPAC對圖像進行應變分析。
1.4.2 圖像采集與記錄實時血壓
病人取左側臥位,在胸骨旁長軸切面測量LVEDD、左心室收縮末期內徑(LVESD)及左房內徑(LAD);在心尖四腔心切面及二腔心切面采用雙平面Simpson法測量LVEDV、左心室收縮末期容積(LVESV)及LVEF。同步連接心電圖,囑病人平靜呼吸,連續采集至少5個心動周期的左心室心尖三腔、四腔、兩腔切面二維動態圖像。于心尖五腔心切面采集主動脈瓣頻譜多普勒血流頻譜。收集起搏器植入術前1 d、出院前和出院9個月隨訪時的圖像。同步連接上臂袖帶血壓計,記錄實時肱動脈血壓數值。左心室機電不同步通過胸骨旁短軸或長軸切面的SF或心尖四腔心切面的Ap Rock來確定。
1.4.3 圖像分析與參數獲取
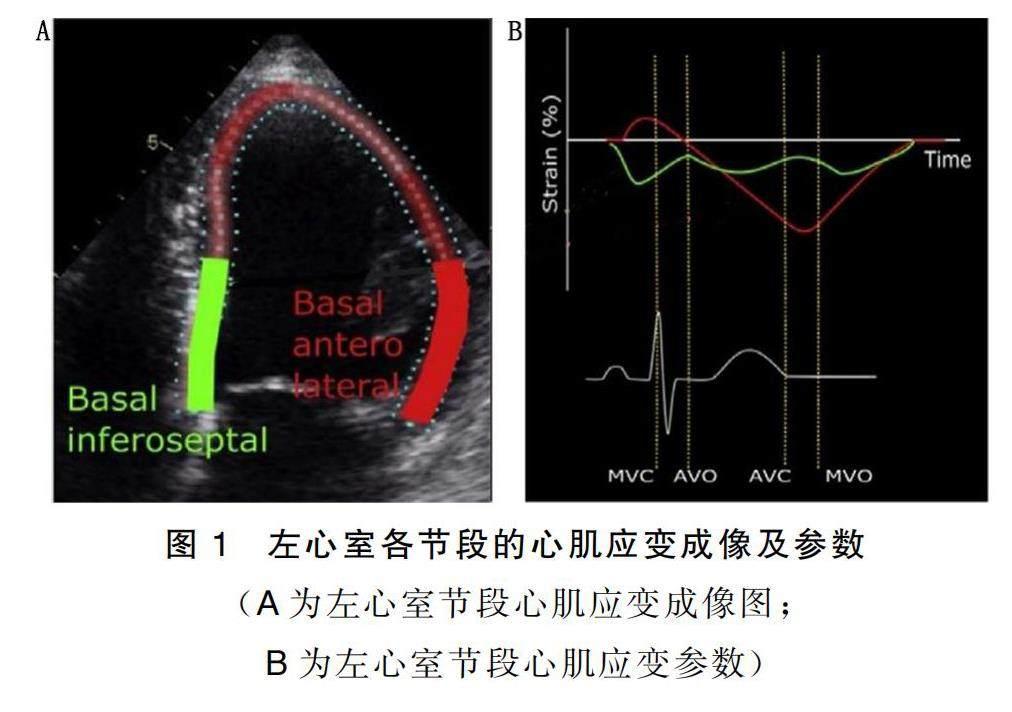
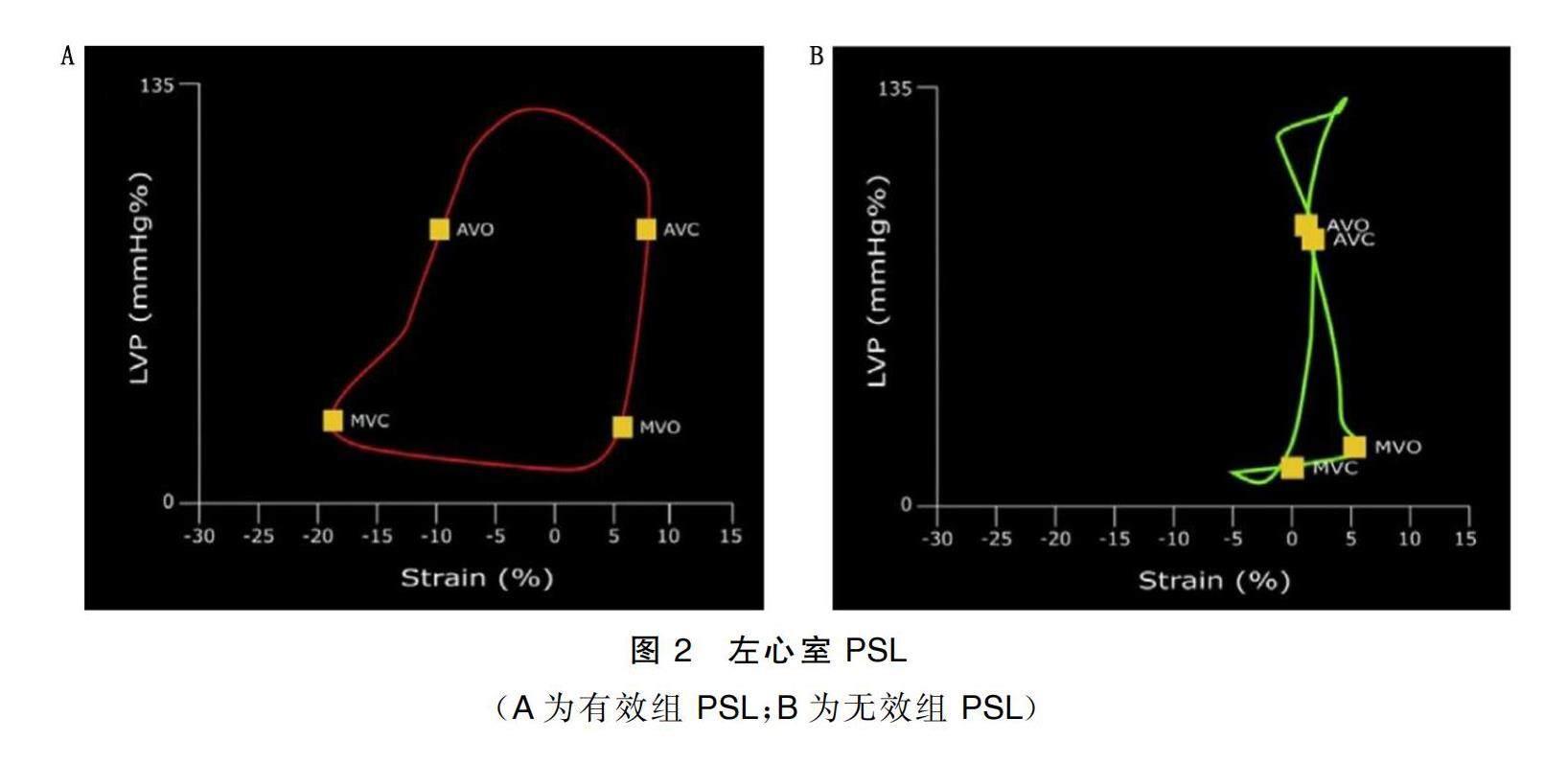
將DICOM格式的原始圖像導入Echo PAC工作站進行脫機分析。首先通過主動脈瓣多普勒頻譜,確定主動脈瓣啟閉時間,標記Event timing,然后進入AFI模式,依次選取左心室心尖三腔、四腔、兩腔心切面的二維動態圖像,于收縮末期自動追蹤左室心內膜邊界生成感興趣區(ROI),并手動調整ROI,以確保最佳的追蹤效果。圖像分析完成后,系統自動生成左心室整體及17個節段的心肌應變參數(見圖1);點擊Myocardiac Work輸入采集圖像時的實時肱動脈血壓數值,可獲得
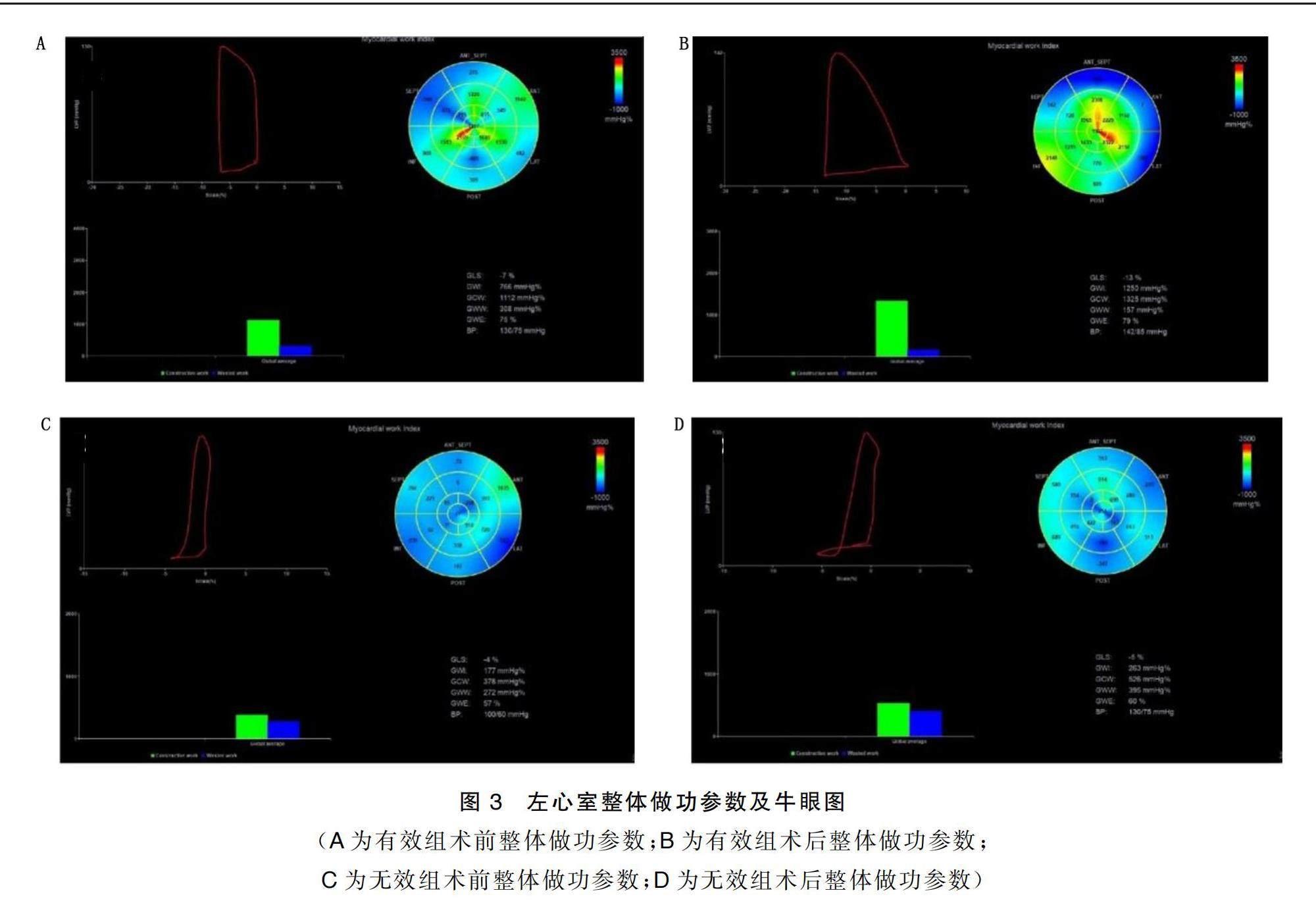
PSL(見圖2);點擊Advanced即可獲得左心室整體縱向應變(GLS)、整體做功指數(GWI)、整體有效做功(GCW)、整體無效做功(GWW)、整體做功效率(GWE)及GWI的牛眼圖(見圖3)。
1.5 結局指標
CRT應答定義為從基線檢查到9個月隨訪期間LVEDV相對減少≥15%。在隨訪期間,通過訪談和/或電話聯系醫生、病人和親屬記錄終點事件,主要研究終點為全因死亡率,如果死亡與心力衰竭、心肌梗死、心律失常或猝死相關,則考慮是心源性死亡。
1.6 統計學處理
應用SPSS 25.0統計軟件分析數據。符合正態分布的定量資料以均數±標準差(x-±s)表示,組間比較采用獨立樣本t檢驗;不符合正態分布的定量資料以中位數(四分位數)[M(P25,P75)]表示,組間比較采用Kruskal-Wallis秩和檢驗。定性資料以例數、百分比(%)表示,組間比較采用χ2檢驗或Fisher精確概率法。應用受試者工作特征(ROC)曲線獲得GWW預測CRT應答的曲線下面積(AUC)、最佳截點值以及靈敏度和特異度。使用多因素Logistic回歸分析低GWW是否為CRT術后不良事件的獨立危險因素。使用Cox比例風險回歸模型分析CRT術后不良事件的危險因素,并確定風險比(HR)。建立Kaplan-Meier生存曲線,用Log-rank檢驗比較組間差異。以P<0.05為差異有統計學意義。
2 結 果
2.1 兩組臨床資料比較
將CRT術后9個月較術前LVEDV相對減少≥15%定義為CRT應答。研究人群為50例接受CRT治療的HFrEF病人,年齡(71±10)歲,其中36例病人治療有效。術前有效組(36例)與無效組(14例)病人的年齡、性別、糖尿病、冠心病、心房顫動史、NYHA Ⅲ級或Ⅳ級、超聲特異性征象(SF或Ap Rock)等比較差異無統計學意義(P>0.05),有效組的QRS寬度及QRS寬度>150 ms所占比例均大于無效組,有效組LBBB所占比例大于無效組,有效組血腦鈉肽水平低于無效組,差異均有統計學意義(P<0.001)。詳見表1。
2.2 超聲心動圖常規參數比較
術前有效組的LVEDD、LVEDV、LVESV低于無效組(P<0.05),LVEF高于無效組(P<0.05),有效組與無效組的LAD差異無統計學意義(P>0.05)。與術前相比,有效組術后的LVEDD、LVEDV和LVESV較術前均減小(P<0.05),LVEF較術前增大(P<0.05),有效組與無效組的LAD較術前無明顯減小(P>0.05)。詳見表2。
2.3 左心室心肌做功參數及GLS比較
術前無效組的GWW與GCW均低于有效組(P<0.05),其余參數比較差異均無統計學意義。與術前相比,有效組術后的GWW下降,GCW、GWI、GWE均增高,差異有統計學意義(P<0.05);無效組各參數比較差異均無統計學意義(P>0.05)。詳見表3。
2.4 左心室心肌做功參數對CRT應答的預測因素
總結ROC曲線分析結果,GWW和GCW為具有高AUC的CRT應答預測因素(GWW為0.78,GCW為0.72),其中GWW的AUC最大,以175 mmHg%為截斷值區分CRT有無應答的特異度為85.7%,敏感度為67.8%。詳見表4。
2.5 GWW與CRT預后的關系
在3年的隨訪期間,有15例病人死亡(30%)。在左心室心肌做功參數中,GWW相較于其他心肌做功參數,與CRT應答和預后的相關性最佳。GWW<175 mmHg%的3年生存率為62%[95%CI(50%,75%)],GWW≥175 mmHg%的3年生存率為83%[95%CI(77%,89%),P=0.002]。對HFrEF病人接受CRT的已知預后因素進行校正后,與GWW≥175 mmHg%相比,GWW<175 mmHg%與全因死亡的相對風險增加相關[校正HR=2.04,95%CI(1.10,3.84),P=0.024];將GWW添加到包含已知CRT預后因子的基線模型中,該模型呈正相關(改善χ2=4.85,P=0.028)。詳見表5、表6及圖4。
3 討 論
對HFrEF病人進行風險分層以改善死亡風險十分重要。一項CARE-HF隨機對照試驗顯示,CRT使QRS時限延長的HFrEF病人顯著獲益,在平均29個月的隨訪期間,全因死亡率降低36%,因心力衰竭惡化的非計劃住院治療減少了50%以上[16]。不協調的室壁運動再同步化可以使左室逆重構,但約30%的心力衰竭病人可能對CRT無應答,因此,尋找新的簡單指標以幫助完善CRT適應證是一個重要的研究領域[17-18]。
Russell等[19]研究顯示,無創評估心肌做功,定量評估各節段PSL面積可以無創獲得心肌做功參數,PSL與使用有創導管測量的做功相關性良好。研究表明,在等候CRT的病人中,PSL無創評估左室功能與PET評估的殘余心肌代謝活性相關[19-20]。應用斑點追蹤超聲心動圖進行全自動評價心肌做功簡便易行,且觀察者內與觀察者間重復性好[8,19]。各節段心肌的無效做功對應節段運動過程中在反方向運動所做功。GWW為左心室各節段無效做功的平均值。Russell等[20]提出,與沒有LBBB的心肌病病人和健康人對照組相比,患LBBB的心肌病病人的GWW增加。GWW能夠全面定量評估心肌浪費的能量。在LBBB和/或激活延遲的病人中,浪費的能量是變化的,正如本研究中GWW的分布一樣。事實上,多個復雜的因素影響病人的GWW。首先,左室的幾何形狀和擴張顯著影響心肌做功[21]。根據定義,功是力與長度的乘積,面積對應于壓力-容積環,縱向縮短很大程度反映左室容積的變化,左室心肌做功可以近似用壓力和應變曲線參數計算。心肌做功高度依賴于左室壁應力,左室壁應力隨著左室擴張而增加,但PSL沒有考慮到這個問題。在兩個不同大小的左心室中,擴張者收縮期室壁應力高于未擴張者,可能導致左室心肌做功的低估。左室節段曲率半徑和室壁厚度的評估先前應用于無創推導室壁應力,以克服這一局限性,但在日常臨床工作中開展較為煩瑣[22]。采用肱動脈收縮壓只是估測左室收縮壓,沒有考慮左室舒張壓和反射波增加的壓力,盡管如此,驗證性研究已經證明通過超聲心動圖無創評價心肌做功的準確性[23]。心肌缺血時出現的收縮不同步和收縮后收縮,都可能導致射血效率降低和無效做功增加[24]。雖然Chan等[25]發現非缺血性心肌病病人的GWW值高于缺血性心肌病病人,但研究中并未發現GWW<175 mmHg%與臨床結局之間存在顯著的相互作用。Aalen等[17]發現心臟磁共振評價的心肌做功和室間隔活力均可預測CRT應答,并具有增量預測價值。
本研究常規超聲心動圖顯示,與術前相比,有效組術后的LVEDD、LVEDV和LVESV較術前均減小,LVEF較術前增大,表明術后左心室收縮功能明顯改善;有效組術后的GWW下降,GCW 、GWI、GWE均增高,這說明有效組術后心肌做功效率、做功能力顯著提升,且心肌做功相關參數可以有效地評估CRT病人術后心臟收縮功能。這可能與CRT病人術前不同節段心肌收縮達峰時間的不同有關。正常人不同節段心肌的電機械活動的起始時間雖然不同,但其收縮達峰時間相同,收縮期左心室各節段心肌同步收縮,將血液泵入主動脈。而心力衰竭病人,尤其左束支傳導阻滯的病人,其左心室后側壁的電機械活動呈病理性滯后,使該節段心肌收縮達峰時間顯著延遲,CRT術后使后側壁的心肌電機械活動提前,使各節段心肌收縮達峰同步,增加心肌運動的協調性,減少無效功。
本研究發現,術前低水平GWW(<175 mmHg%)與死亡風險相對增加相關,而GWW<175 mmHg%與大概率CRT無反應相關。因為GWW低不僅反映了機電不同步對左室壁拉伸的影響,還考慮到左室幾何形態和擴張情況。Lim等[26]先前報道過,應變延遲指數作為一種心肌無效做功的參數,與CRT是否應答相關。Galli等[12]在一項包括97例病人的研究中發現,GWW與CRT應答相關,但其預測價值低于GCW。隨訪中觀察到GCW與心源性死亡的發生之間獨立相關,但GWW與心源性死亡之間相關性不明顯[13]。Van Der等[15]的一項研究包括153例接受CRT病人隨訪中發現,整體無效做功比值與死亡率呈獨立相關。本研究中,術前GWW、CRT應答和死亡率之間呈強相關。雖然SF和/或心尖搖擺特征與CRT應答相關,但如既往研究所述,其鑒別診斷價值低于GWW。隨訪中,SF和/或心尖搖擺特征與CRT應答和死亡率都沒有顯著相關性。這可能是由于SF和/或心尖搖擺特征識別是定性評價,在臨床應用中可重復性或許存在一定問題[7]。本研究心肌做功參數中,GWW與CRT應答和死亡率之間的關系最強,與Galli等[12-14]的研究結果不一致,這可能與樣本量、事件發生率和研究終點(全因死亡率與心源性死亡)存在差異有關。雖然間隔運動和做功在CRT應答的病理機制中非常重要,但觀察到GWW和間隔無效做功對CRT是否應答具有相似的鑒別診斷價值。因此,傾向選擇將GWW應用于臨床工作中,因為這個參數目前能夠從軟件中半自動獲得,CRT對臨床結局的影響至少部分取決于術前無效做功,有效的再同步化治療能夠降低GWW。
PSL評價術前GWW重復性好,較低的GWW與HFrEF病人的長期不良預后和CRT應答率低相關。GWW<175 mmHg%為HFrEF病人提供增量預測價值。但在缺乏隨機對照研究的情況下,即使大多數術前GWW<175 mmHg%的病人似乎沒有從CRT中獲益,這些病人也不應被排除在CRT之外,臨床診療仍應依據當前指南。因此,本研究結果表明,術前GWW較低的病人應在CRT術后仔細監測,以確保在其臨床狀況惡化前及時接受更高級別治療(如心臟移植、左心室或雙心室輔助裝置等)。
參考文獻:
[1] PONIKOWSKI P,VOORS A A,ANKER S D,et al.2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure:the Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology(ESC)Developed with the special contribution of the Heart Failure Association(HFA)of the ESC[J].European Heart Journal,2016,37(27):2129-2200.
[2] HOLZMEISTER J,LECLERCQ C.Implantable cardioverter defibrillators and cardiac resynchronisation therapy[J].Lancet,2011,378:722-730.
[3] MARECHAUX S,MENET A,GUYOMAR Y,et al.Role of echocardiography before cardiac resynchronization therapy:new advances and current developments[J].Echocardiography,2016,33:1745-52.
[4] PARSAI C,BIJNENS B,SUTHERLAND G R,et al.Toward understanding response to cardiac resynchronization therapy:left ventricular dyssynchrony is only one of multiple mechanisms[J].European Heart Journal,2009,30(8):940-949.
[5] BRUNET-BERNARD A,MARECHAUX S,FAUCHIER L,et al.Combined score using clinical,electrocardiographic,and echocardiographic parameters to predict left ventricular remodeling in patients having had cardiac resynchronization therapy six months earlier[J].Am J Cardiol,2014,113:2045-2051.
[6] GHANI A,DELNOY P P H M,OTTERVANGER J P,et al.Association of apical rocking with long-term major adverse cardiac events in patients undergoing cardiac resynchronization therapy[J].European Heart Journal-Cardiovascular Imaging,2016,17(2):146-153.
[7] STANKOVIC I,PRINZ C,CIARKA A,et al.Relationship of visually assessed apical rocking and septal flash to response and long-term survival following cardiac resynchronization therapy(PREDICT-CRT)[J].European Heart Journal-Cardiovascular Imaging,2016,17(3):262-269.
[8] VECERA J,PENICKA M,ERIKSEN M,et al.Wasted septal work in left ventricular dyssynchrony:a novel principle to predict response to cardiac resynchronization therapy[J].European Heart Journal - Cardiovascular Imaging,2016,17(6):624-632.
[9] EL MAHDIUI M,VAN DER BIJL P,ABOU R,et al.Global left ventricular myocardial work efficiency in healthy individuals and patients with cardiovascular disease[J].J Am Soc Echocardiogr,2019,32:1120-1127.
[10] MEIMOUN P,ABDANI S,STRACCHI V,et al.Usefulness of noninvasive myocardial work to predict left ventricular recovery and acute complications after acute anterior myocardial infarction treated by percutaneous coronary intervention[J].J Am Soc Echocardiogr,2020,33:1180-1190.
[11] HIEMSTRA Y L,VAN DER BIJL P,EL MAHDIUI M,et al.Myocardial work in nonobstructive hypertrophic cardiomyopathy:implications for outcome[J].J Am Soc Echocardiogr,2020,33:1201-1208.
[12] GALLI E,LECLERCQ C,HUBERT A,et al.Role of myocardial constructive work in the identification of responders to CRT[J].European Heart Journal-Cardiovascular Imaging,2018,19(9):1010-1018.
[13] GALLI E,HUBERT A,LE ROLLE V,et al.Myocardial constructive work and cardiac mortality in resynchronization therapy candidates[J].Am Heart J,2019,212:53-63.
[14] GALLI E,LECLERCQ C,FOURNET M,et al.Value of myocardial work estimation in the prediction of response to cardiac resynchronization therapy[J].J Am Soc Echocardiogr,2018,31:220-230.
[15] VAN DER BIJL P,VO N M,KOSTYUKEVICH M V,et al.Prognostic implications of global,left ventricular myocardial work efficiency before cardiac resynchronization therapy[J].European Heart Journal-Cardiovascular Imaging,2019,20(12):1388-1394.
[16] CLELAND J G F,DAUBERT J C,ERDMANN E,et al.The effect of cardiac resynchronization on morbidity and mortality in heart failure[J].The New England Journal of Medicine,2005,352(15):1539-1549.
[17] AALEN J M,DONAL E,LARSEN C K,et al.Imaging predictors of response to cardiac resynchronization therapy:left ventricular work asymmetry by echocardiography and septal viability by cardiac magnetic resonance[J].European Heart Journal,2020,41(39):3813-3823.
[18] AALEN J M,REMME E W,LARSEN C K,et al.Mechanism of abnormal septal motion in left bundle branch block:role of left ventricular wall interactions and myocardial scar[J].JACC Cardiovascular Imaging,2019,12(12):2402-2413.
[19] RUSSELL K,ERIKSEN M,AABERGE L,et al.A novel clinical method for quantification of regional left ventricular pressure-strain loop area:a non-invasive index of myocardial work[J].European Heart Journal,2012,33(6):724-733.
[20] RUSSELL K,SMISETH O A,GJESDAL O,et al.Mechanism of prolonged electromechanical delay in late activated myocardium during left bundle branch block[J].Am J Physiol Heart Circ Physiol,2011,301:H2334-2343.
[21] BOE E,SKULSTAD H,SMISETH O A.Myocardial work by echocardiography:a novel method ready for clinical testing[J].European Heart Journal-Cardiovascular Imaging,2019,20(1):18-20.
[22] CVIJIC M,DUCHENNE J,?NL? S,et al.Timing of myocardial shortening determines left ventricular regional myocardial work and regional remodelling in hearts with conduction delays[J].European Heart Journal-Cardiovascular Imaging,2018,19(8):941-949.
[23] HUBERT A,LE ROLLE V,LECLERCQ C,et al.Estimation of myocardial work from pressure-strain loops analysis:an experimental evaluation[J].European Heart Journal-Cardiovascular Imaging,2018,19(12):1372-1379.
[24] SABATINO J,DE ROSA S,LEO I,et al.Non-invasive myocardial work is reduced during transient acute coronary occlusion[J].PLoS One,2020,15:e0244397.
[25] CHAN J,EDWARDS N F A,KHANDHERIA B K,et al.A new approach to assess myocardial work by non-invasive left ventricular pressure-strain relations in hypertension and dilated cardiomyopathy[J].European Heart Journal-Cardiovascular Imaging,2019,20(1):31-39.
[26] LIM P,BUAKHAMSRI A,POPOVIC Z B,et al.Longitudinal strain delay index by speckle tracking imaging:a new marker of response to cardiac resynchronization therapy[J].Circulation,2008,118:1130-1137.
(收稿日期:2022-11-25)
(本文編輯 王雅潔)

