心率變異性與失眠及其非藥物治療關系研究進展☆
林文婷 趙光利 胡代杰 朱天民 余思奕
全球約1/3 成年人受失眠影響,失眠不僅導致日間疲乏、情緒障礙,還可能引起自主神經系統(autonomic nerves system,ANS)紊亂,表現為體溫升高、皮膚電活動增強和心率變異性(heart rate variability,HRV)降低[1-2]。現有研究已證實,HRV 降低是失眠患者的常見特征[3],反映ANS 功能失衡,并且自主神經癥狀改善對失眠癥的治療有一定幫助[4]。然而,關于失眠與HRV 之間的潛在關系,以及如何通過非藥物治療手段調節HRV 以改善失眠癥狀,目前的理解仍然有限。本綜述旨在系統回顧當前關于失眠與HRV 之間關系的文獻,特別關注非藥物治療方法對HRV 的潛在調節作用,探討HRV 在失眠診斷、治療和預后評估中作為生物標志物的可行性。
1 HRV的概述
HRV 即逐搏心跳周期之間差異的變化情況,是評估ANS 動力學的客觀標志物,能夠在生理和病理條件下提供交感神經和副交感神經調節的信息[5]。HRV 由ANS 與心臟、大腦相互作用共同產生,其發生機制復雜,目前仍未完全明了。大量研究表明,失眠患者的ANS 常常處于不平衡狀態,使得HRV 成為了探索失眠病因及病理機制的重要生物標志物[6]。
HRV 的測量可通過動態心電圖或睡眠多導圖實現。HRV的記錄方式可以分為靜態(時間為數分鐘)和動態記錄(時間可長達24 h),其分析方法則可分為線性分析和非線性分析兩類[7]。線性分析法進一步細分為時域分析、頻域分析和時頻分析。如表1所示,常用的時域指標有全部正常竇性心律R-R 間期的標準差(standard deviation of normal R-R intervals,SDNN)、相鄰R-R 間期差值的均方根(root mean square of successive R-R interval differences,RMSSD)以及相鄰R-R 間期之差>50 ms 的心搏次數占總心搏次數百分比(proportion of NN50 divided by the total number of NN intervals,pNN50)。時域指標計算簡單,意義直觀,但其靈敏度和特異度低,不能進一步區分交感、副交感神經的張力及其均衡性的變化。常用的頻域指標包括總功率(total power,TP)、極低頻功率(very low-frequency,VLF)、高頻功率(high frequency,HF)、低頻功率(low frequency,LF)以及低頻功率與高頻功率的比值(low frequency/high frequency,LF/HF)。頻域指標能明確反映ANS 的興奮性活動,但缺乏時間和頻率的定位功能。時頻分析則能打破前兩者單一應用的局限,但分析方法較為復雜。非線性分析方法能反映心率的瞬時變化,并描述心動周期變化的復雜性,從而提高HRV的準確性,但其生理意義尚未明確,且在實際應用中存在困難,尚未得到普遍使用。

Tab.1 Physiological significance of common HRV indicators表1 常見HRV指標的生理意義
2 失眠與HRV
睡眠過程主要由快速眼動睡眠(rapid eye movement sleep,REM)和非快速眼動睡眠(non-rapid eye movement sleep,NREM)兩個階段組成。在REM 階段,自主神經表現出不穩定性,而在NREM 階段相對穩定,這是ANS恢復和代謝活動增強的時期[8]。副交感神經成分隨著睡眠深入而增加,而交感神經成分則與覺醒相關。一方面,研究發現失眠患者的大腦皮質活動、ANS 調節、代謝率和激素分泌等方面都出現了與生理喚醒相關的變化[9-10]。另一方面,HRV 副交感神經參數與睡眠質量及睡眠階段之間存在明顯的線性相關[11-12]。例如,副交感神經指標(RMSSD、pNN50、HF)與睡眠質量存在正相關[13]。研究表明,在入睡前階段,較高的HF 和LF/HF 與較短的睡眠潛伏期、較少的覺醒事件以及睡眠效率的增加有關[14]。這些研究提示,失眠患者的ANS 處于失衡狀態。見圖1A。
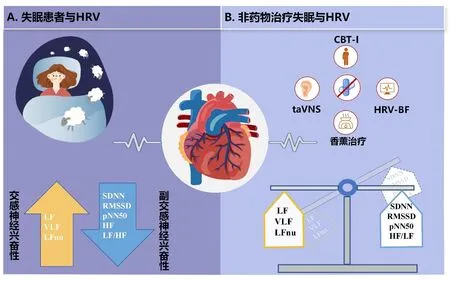
Fig.1 Schematic diagram of the hypothetical mechanism of HRV in insomnia and its non pharmacological therapy for insomnia treatment圖1 HRV 在失眠及其非藥物療法治療失眠中的機制假設示意圖失眠患者交感神經興奮性增加,副交感神經興奮性降低,通過非藥物療法可以平衡交感和副交感神經的興奮性。注:CBT-I,認知行為療法治療失眠;HRV-BF,心率變異性生物反饋;ta VNS,經皮耳穴迷走神經刺激;LF,低頻功率;VLF,極低頻功率;LFnu,低頻的歸一化值;SDNN,正常R-R 間期的標準差;RMSSD,相鄰R-R 間期差值的均方根;pNN50,相鄰R-R 間期之差>50 ms 的心搏次數占總心搏次數的百分比;HF,高頻功率;LF/HF,低頻功率與高頻功率比值。
2.1 失眠患者相較于健康對照的 HRV 變化 BONNET 等[15]采用頻域分析比較12 例失眠患者和相匹配的正常睡眠者,發現失眠患者在所有睡眠階段的LF 增加,而HF 顯著降低。類似地,SPIEGELHALDER 等[16]比較58 例失眠患者與46 名健康對照者,失眠患者的心率、時域指標(SDNN、RMSSD 以及pNN50)和頻域指標中HF 均降低。這些結果提示失眠患者的交感神經興奮性增強,副交感神經興奮性降低。DE ZAMBOTTI 等[17]研究報道,失眠患者的LH/HF 降低,高頻的歸一化值(HF normalized units,HFnu)增加,且整夜持續存在交感神經過度激活狀態。COSGRAVE 等[18]的研究發現,夜間覺醒次數多或覺醒指數高的失眠患者SDNN明顯降低,提示自主神經活性降低。JARRIN 等[19]的研究表明,相較于正常睡眠持續時間(≥6 h)的對照組,客觀睡眠時間短的失眠患者HF降低,LF/HF和心率升高。
如表2 所示,失眠患者的HRV 表現為時域指標(如SDNN、RMSSD 和pNN50)和頻域指標(如HF)呈下降趨勢,且與睡眠質量較差呈正相關。這表明失眠患者的ANS平衡被破壞,副交感神經調節作用減弱,自主神經活性下降,進而影響睡眠質量及其調節機制。該病理過程在未來的研究和臨床工作中值得進一步關注和探索。
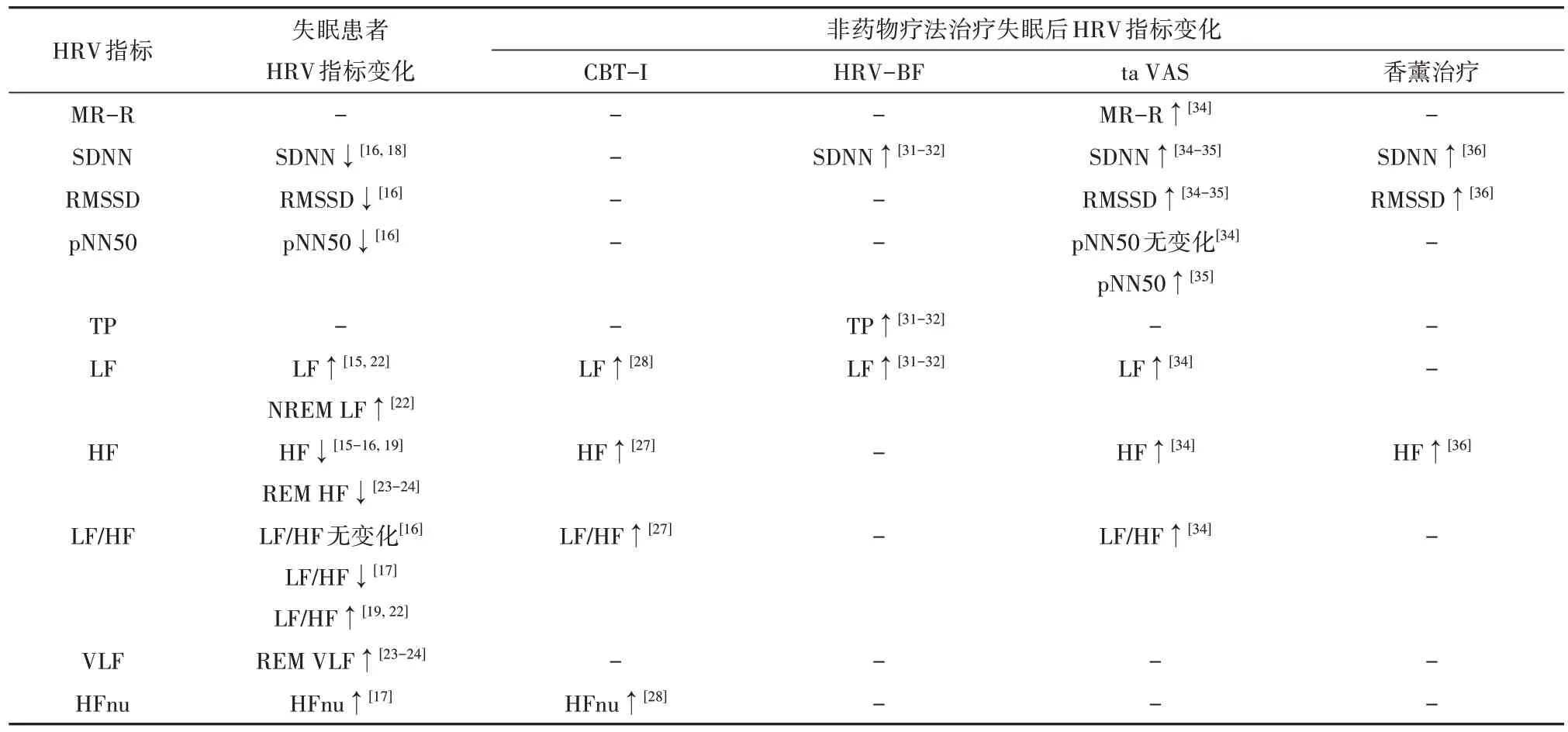
Tab.2 Relationship between HRV and insomnia and non pharmacological treatment表2 HRV與失眠及非藥物治療關系
2.2 失眠患者在不同睡眠階段的HRV 變化 目前,許多研究已經開始探索失眠患者在睡眠不同階段的HRV 變化。研究表明,正常REM 期間,交感神經活動增強,副交感神經活動減弱,而在NREM 期間觀察到相反的趨勢[20-21]。FARINA 等[22]研究指出,失眠患者(85例)相較于健康對照者(55 名),在睡前清醒階段和NREM 第2 階段(N2)表現出心率、LF 和LF/HF 增加,提示交感神經興奮性增加。MIKOTEIT 等[23-24]的兩項研究指出,失眠患者在REM 期間HRV由HF向VLF偏移[23],并且在第1個REM 睡眠階段和相鄰的NREM 階段,其HRV 均顯著降低[24]。JARRIN 等[19]的研究強調在N2 階段觀察到總睡眠時間與HF 降低和LF/HF 升高有關,在REM 階段失眠嚴重程度量表改善與HF 的增加相關。總的來說,失眠患者在NREM 及REM 期間HRV 水平降低,表示ANS的平衡性受到破壞,交感和副交感神經調節失衡。
以上結果表明,失眠患者在REM 階段交感神經通常表現出異常亢奮,這可能導致入睡困難,而在NREM 期間副交感神經興奮性較低(例如,HF 降低,LF/HF 增加),這與較差的睡眠質量有關。更重要的是,這些異常的HRV 變化不僅有潛力作為失眠的早期診斷指標,還有望為失眠的治療和預后提供評估價值。
3 失眠的非藥物治療與HRV
常見的失眠非藥物療法包括認知行為治療和物理治療等,這些非藥物治療方法可能通過調節HRV 來改善失眠癥狀,從而提高睡眠質量。
3.1 認知行為療法與HRV 改變 目前,認知行為療法治療失眠(cognitive behavioral therapy for insomnia,CBT-I)被廣泛認為是失眠的首選治療策略[25]。CBT-I包括睡眠衛生、刺激控制、睡眠限制、認知療法和放松訓練等[26]。JARRIN等[27]對65 例失眠患者進行6 周的CBT-I 后發現,總睡眠時間增加與LF/HF 升高之間存在關聯趨勢,并且在REM 期間失眠嚴重程度指數降低和HF 增加也呈現出關聯趨勢。一項針對57 例急性失眠患者的隨機對照研究證實,一次性CBT-I可有效緩解失眠癥狀,在HRV 方面表現為LF 降低,HF 及HFnu 增高[28]。上述研究提示,CBT-I 可以通過抑制交感神經過度活躍和提高副交感神經活性來調節HRV,進而恢復自主神經功能的平衡。
3.2 物理療法與HRV 改變 生物反饋是一種簡單、便捷的物理治療手段,已成為失眠的重要治療方法。其中,心率變異性生物反饋(heart rate variability biofeedback,HRV-BF)是以HRV 為訓練指標,借助生物反饋設備幫助改善交感和副交感系統反射的調節功能,增強兩個系統之間的平衡調節,該方法在改善失眠方面取得了一定療效[29-30]。LIN 等[31]研究發現,失眠患者進行6 周的HRV-BF 訓練后,總睡眠時間增加、睡眠質量提高,并伴有HRV 指數(SDNN、LF 和TP)的升高。SDNN 和TP 升高的機制涉及壓力感受器或壓力反射敏感性的穩態改善、自主神經調節以及副交感神經傳出的刺激。同樣的,HERHAUS 等[32]的研究指出,HRV-BF 訓練后患者睡眠質量改善與SDNN、TP 和LF 的增加有關。總的來說,HRV-BF 作為一種非藥物、非侵入性的干預手段,可以顯著提高HRV,調節交感與副交感神經平衡,從而提高ANS的穩定性。
近年來,經皮耳穴迷走神經刺激(transcutaneous auricular vagus nerve stimulation,ta VNS)已成為一種治療失眠的新型方法[33]。趙亞楠等[34]對21 例失眠患者進行ta VNS 治療,結果顯示治療后患者LF、HF、LF/HF、SDNN、RMSSD指標均有所增加。提示ta VNS可能通過調節自主神經功能起效,使ANS 偏向以副交感神經為主,從而間接減輕失眠癥狀。WU 等[35]的研究報道在持續ta VNS 狀態下,HRV 與ta VNS療效相關,ANS 對刺激更敏感的患者,其ta VNS 效果更佳,并且對比安慰劑組,治療組的HF 和pNN50 明顯增加,以及RMSSD 指標呈增長趨勢。綜上,通過調節HRV 的時域指標(SDNN、RMSSD)和頻域指標(LF、HF、LF/HF),ta VNS 可以有效調節失眠患者的自主神經功能。
除此之外,研究發現失眠患者經香薰治療后平均心率顯著降低,光譜功率分析顯示其SDNN、RMSDD 和HF 顯著增加[36],這提示香薰治療可以調節失眠患者的ANS 活動。HRV指標改善反映了香薰治療與副交感神經系統的相互作用,有助于調節焦慮并改善自我報告的睡眠質量。
非藥物治療失眠的機制可能涉及增強副交感神經活動以平衡ANS功能(圖1B)。綜上,CBT-I、HRV-BF訓練、ta VNS等多種非藥物治療方法可以通過調節心臟ANS 的活動,提高SDNN、LF 和HF 等HRV 指標,HRV 指標升高反映了ANS的平衡和穩定,從而可促進失眠患者睡眠質量的改善。
4 總結與展望
HRV 能作為與失眠密切相關的生物標志物,在失眠的診斷和治療中頗具潛力。縱覽現有研究,失眠患者HRV 的異常模式主要表現為副交感神經興奮性降低和交感神經興奮性增加,而非藥物治療可能通過調節HRV 進而恢復ANS的動態平衡(圖1)。然而,需要指出的是,HRV 受到多種因素的影響,例如研究對象的異質性、生理信號的捕獲質量及數據處理方法等,這些因素均可能影響HRV 與失眠及其治療之間的關系。
未來的研究應優先關注提升HRV 指標的可靠性和特異性,探索HRV 與其他生物標志物結合的可能性,以促進HRV 在臨床篩查和診斷中的應用。其次,有必要提高HRV監測失眠的準確性,可以從時域、頻域,特別是非線性分析中開發新的分析技術來實現。此外,研究顯示HRV 的改變是失眠和其他精神疾病的共通之處,表明ANS 失調可能影響了睡眠與情緒或焦慮相關疾病之間的雙向關系[37]。未來的研究有必要進行縱向設計和因果分析,以進一步闡明睡眠紊亂、HRV失調與情緒障礙之間的關系。最后,增加非藥物治療對失眠影響的前瞻性研究,有可能為HRV 作為預測治療效應的生物標志物提供證據。

