MMP14調控骨骼肌衛星細胞分化的分子機制研究
劉 媛,李溪月,張維婭
(河北農業大學 河北省山區農業技術創新中心,保定 071000)
骨骼肌是人體運動和代謝的重要器官,在維持身體的運動平衡、葡萄糖代謝[1]和能量代謝[2]等方面起著非常重要的作用。骨骼肌由肌纖維組成,肌纖維是一類含有可收縮功能肌原纖維的圓柱形多核細胞[3]。骨骼肌的生成主要包括胚胎期肌纖維數目的增加和出生后肌纖維的成熟發育。脊椎動物骨骼肌的發育主要起源于胚胎時期的軸旁中胚層,此后軸旁經過增生和肥大分裂形成體節,體節經過進一步發育形成腹側生骨節和背側生皮肌節,生皮肌節發育成肌節,肌節最終形成全身骨骼肌[4]。衛星細胞在骨骼肌形成過程中作為前體的一個子集,也起源于中胚層祖細胞[5]。
骨骼肌衛星細胞是骨骼肌中的成體干細胞。Mauro[6]在1961年首次從青蛙骨骼肌纖維中分離出一類緊密粘附于肌纖維基膜的單核細胞,命名為衛星細胞。衛星細胞定位于骨骼肌微環境中,是骨骼肌中具有增殖分化潛能的肌源性干細胞。衛星細胞的功能受PAX7、MYOD以及MYF5等轉錄因子調控,在肌纖維的生長發育以及損傷修復過程中發揮重要作用[7]。通常情況下,衛星細胞在體內穩態中以靜息狀態存在于肌纖維基膜(基底膜)和肌細胞膜之間[8]。骨骼肌發育或受到損傷時,衛星細胞會被激活并進入細胞周期,激活后的衛星細胞具有增殖、遷移、以及分化融合成肌管的能力,對維持機體穩態有重要作用[9-10]。肌纖維受損時,衛星細胞中肌源性因子MYOD表達上調,細胞開始大量增殖并遷移到受損傷部位,隨后肌源性轉錄因子MYOG和MRFs以及下游的效應因子表達,最終分化融合成新的肌纖維,重塑受損的肌纖維[11-13]。Lyu等[14]研究發現,牛衛星細胞可能由轉錄狀態、增殖速率和肌源性潛能不同的亞群組成。Cai等[15]的研究揭示了骨骼肌發育的不同階段之間不同亞群細胞的比例差異顯著,且特定的轉錄因子會在肌發生過程中調節細胞命運的轉變。
基質金屬蛋白酶(matrix metalloproteinase, MMPs)是鋅依賴性內肽酶,在細胞多種生理功能中發揮作用。MMP14(也稱MT1-MMP)是MMPs家族的重要成員,是一種膜型基質金屬蛋白酶,定位于細胞膜上[16]。Knapinska和Fields[17]通過MMP14在蛋白質圖譜中的亞細胞定位揭示了這種蛋白酶主要定位于胞質溶膠和細胞骨架的中間絲。MMP14作為跨膜蛋白連接細胞外基質和細胞內組分,對衛星細胞的分化過程有重要影響。有研究表明,MMP14可以降解細胞外基質的所有成分,包括纖維膠原、纖維粘連蛋白、層粘連蛋白以及纖維蛋白等,是參與細胞外基質重塑的重要蛋白[18]。MMP14在骨骼肌損傷修復中發揮作用。Ohtake等[19]的結果證明了MMP14可維持肌纖維功能完整性,在成肌分化過程中,通過表觀遺傳影響肌源性調控因子的表達從而調節肌源性分化,抑制MMP14會導致肌源性障礙,表現為肌纖維融合受損以及肌管形成減少。Hotaryk等[20]證明,MMP14是 MMPs家族中唯一在富含膠原蛋白的環境中促進細胞遷移的蛋白酶。Ito等[21]發現,用誘導MMP14過表達和激活的因子刀豆球蛋白A對成肌細胞進行預處理有利于改善成肌細胞的遷移。因此,MMP14在調節骨骼肌衛星細胞的遷移、分化和再生以及維持肌纖維功能完整性中具有重要作用。
雖然前人研究發現MMP14在衛星細胞分化和骨骼肌發育方面發揮重要作用,但研究多聚焦于MMP14介導ECM重塑調控肌纖維發育方面[22]。目前,MMP14直接調控衛星細胞肌源性分化的分子機制尚不明確。本課題組在前期研究中分析不同年齡骨骼肌衛星細胞的分化能力及分子機制,結果發現MMP14的表達水平在骨骼肌發育的不同階段差異顯著,且作為關鍵節點參與調控細胞分化相關的效應因子,表明MMP14可能參與調控衛星細胞肌源性分化。MMP14作為金屬基質蛋白酶可以水解多種基質和非基質蛋白,因此本研究通過蛋白組測序分析衛星細胞中MMP14調控的關鍵蛋白,解析MMP14調控衛星細胞分化的分子機制。
1 材料與方法
1.1 試驗動物
試驗選用4周齡C57/BL6雌性小鼠,小鼠全部購買于斯貝福(北京)生物技術有限公司。所有動物實驗均在生物實驗室進行,并經河北農業大學實驗動物倫理委員會批準。
1.2 試驗材料
膠原酶(Sigma,C1639)、胰酶(Gibco)、磷酸鹽緩沖液(Gibco),RPMI 1640培養基(Gibco,21870076)、胎牛血清(Gibco,10082-147)、馬血清(Gibco,16050122)、雞胚胎提取物(GEMINI,100-163)、Lipofectamine 2000(Invitrogen,11668019)、DMEM/HIGH GLUCOSE(Hyclone,SH30 022.01B)、TransZol(Invitrogen,411503)、反轉錄試劑盒(Takara,RR064A),SYBR qPCR Mix(TOYOBO,246000),哺乳動物蛋白提取試劑(Pierce,CT301337100)。
1.3 儀器設備
低速臺式離心機(TD5B,BIORIDGE)、Axio Observer倒置顯微鏡系統(蔡司)、細胞培養箱(MCO-18AC)、紫外凝膠成像系統(EBOX CX5,Vilber lourmat)、熒光定量PCR儀(ABI QuantStudio 6)Tanon 5200多成像系統(Tanon)、雙板垂直電泳儀(北京六一生物技術有限公司,DYCZ-24DH)等。
1.4 試驗方法
1.4.1 衛星細胞的分離和培養 每次細胞分離需要10只4周齡的野生型雌性C57/BL6小鼠。衛星細胞分離步驟參考本課題組之前研究中所描述的方法。具體方法如下:取小鼠后肢骨骼肌樣本,用膠原酶(2 mg·mL-1)在37 ℃下消化肌肉組織60 min;然后,將消化后的懸液通過100目網過濾,將過篩后的液體離心,利用PBS懸浮沉淀,隨后用200目和400目篩過濾;過篩后離心,用RPMI 1640培養基洗滌沉淀,離心后用生長培養基懸浮(含有15%胎牛血清、雞胚胎提取物、0.25 μg·100 mL-1堿性成纖維細胞生長因子和RPMI 1640培養基),轉移至普通賴氨酸包被的培養皿中,置于37 ℃的細胞培養箱培養;2.5 h后轉移到經基質膠包被的培養皿。分化培養基由DMEM高糖培養基和3%(v/v)馬血清配制而成。
1.4.2 細胞轉染 細胞匯合至約60%時使用轉染試劑Lipofectamine 2000進行siRNA的轉染,轉染步驟按說明書操作。siRNA和陰性對照由銳博生物技術有限公司(中國,廣州)提供。
1.4.3 免疫熒光試驗 在衛星細胞中分別轉染si-MMP14和si-NC,隨后誘導細胞分化48 h進行免疫熒光試驗。試驗步驟如下:用磷酸鹽緩沖鹽水(PBS)洗滌細胞2次,然后用4%多聚甲醛固定15 min;隨后用PBS洗滌細胞2次,用0.25% Triton X-100室溫下孵育10 min;加封閉液(3%牛血清白蛋白、0.3% TritonX-100、10%胎牛血清)室溫孵育2 h;一抗孵育4 ℃過夜(抗體信息見表1);PBS洗滌細胞3次,然后進行二抗孵育,室溫2 h;PBS洗滌細胞3次,然后用4′,6-Diamidino-2-Phenylindole(DAPI)進行細胞核染色;最后使用Axio Observer倒置顯微鏡系統獲取圖像。
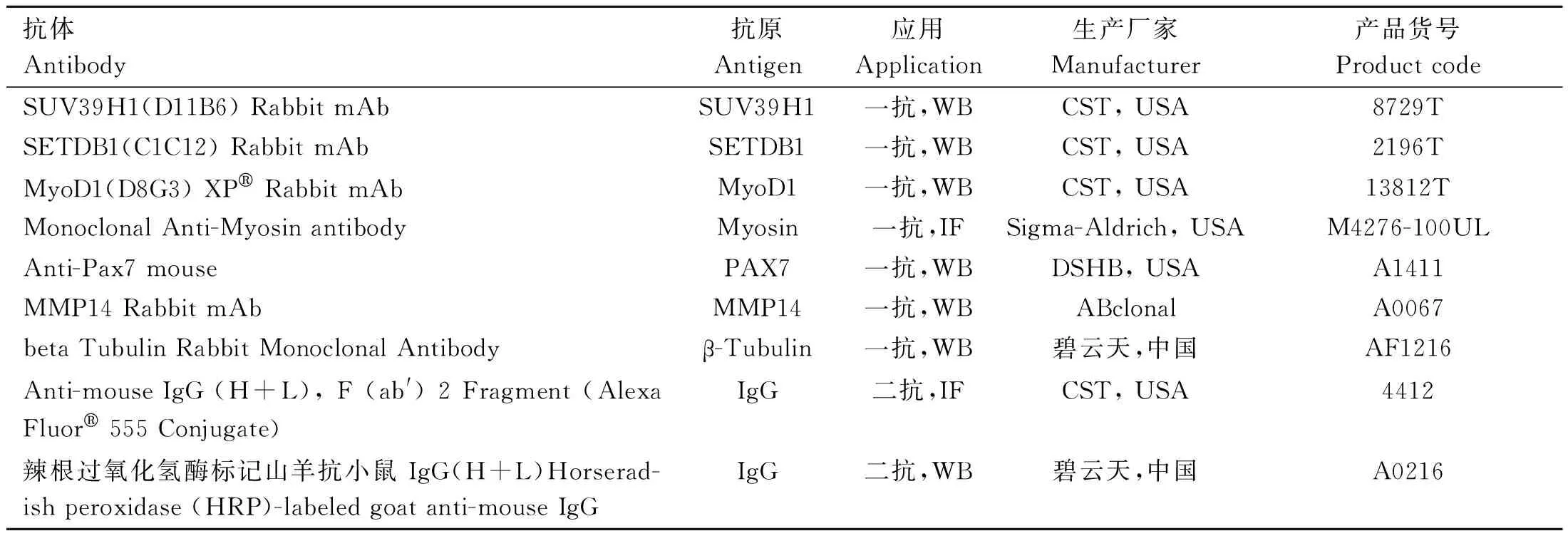
表1 免疫熒光和蛋白質免疫印跡所用抗體Table 1 Antibodies used for immunofluorescence and Western blot
1.4.4 蛋白質免疫印跡(Western blot, WB)檢測 使用哺乳動物蛋白提取試劑獲得約106個細胞的蛋白裂解液。采用雙板垂直電泳儀分離蛋白質并將蛋白質轉移到硝酸纖維膜上。分別用一抗(抗體信息見表1)和辣根過氧化物酶(HRP)標記的二抗孵育,進行免疫印跡。使用Tanon 5200多成像系統檢測ECL化學發光HRP底物(WBKLS0500)產生的信號。
1.4.5 熒光定量PCR(qRT-PCR)檢測 利用Trizol法從約105個細胞中提取總RNA。使用Prime ScriptTM RT試劑盒進行反轉錄,啟動cDNA合成。采用THUNDERBIRD SYBR qPCR Mix進行qRT-PCR,結果采用ABI QuantStudio 6實時熒光定量PCR系統進行監測,引物信息見表2。每個處理組包含3個生物重復,每個生物學重復包含3個樣本,以β-Tubulin為內參。所有結果均用“平均值±s.e.m.”表示,采用不配對的t-檢驗來確定差異統計學意義,P<0.05或P<0.01表示差異顯著。

表2 qRT-PCR引物信息Table 2 Table of qRT-PCR primers information
1.4.6 DIA定量蛋白質組學測序及分析(DIA-seq) DIA-seq由基迪奧生物技術有限公司(中國,廣州)完成,每個處理組包含3個生物學重復。首先,用裂解緩沖液(含1% SDS、8 mol·L-1尿素和1 mg·mL-1蛋白酶抑制劑)提取蛋白,然后進行蛋白質量檢測和酶解。隨后進行質譜預處理,根據試驗需求選擇合適的除鹽柱進行除鹽,取適量樣品,選用皮爾斯定量比色肽測定試劑盒(PierceTMQuantitative Colorimetric Peptide Assay, Thermofisher, 23275)進行肽段定量,計算肽段總量并抽干。建立譜圖數據庫,將肽混合物重新溶解在緩沖液A中(20 mmol·L-1甲酸銨,用氫氧化銨調pH至10.0),然后使用Ultimate 3000系統進行高PH反相分離。將除鹽凍干后的肽段重溶于Solvent A(0.1% 甲酸水溶液)后經由配備在線納噴離子源的 LCMS/MS分析。整套系統為串聯 EASY-nLC 1200 系統的 Orbitrap Fusion Lumos 質譜儀,在數據依賴采集模式下運行,在MS和MS/MS采集間自動切換。質譜參數設置為:MS:掃描范圍 (m/z):350~1 500,分辨率:120 000;AGC target:4×105,最大注入時間:50 ms;動態排除時間:30 s;HCD-MS/MS:分辨率:15 000;AGC target:5×104,最大注入時間:35 ms;碰撞能量:32。原始數據通過Spectronaut X (Biognosys AG)合并分析搜庫,采用軟件默認的參數建庫。數據庫使用 Uniprot或提供的數據庫,設置 Trypsin酶解。搜庫參數固定修飾:Carbamidomethyl (C),可變修飾:methionine氧化。母離子和肽段水平的假陽性率(FDR)都設置為1%。采用 Spectronaut 對DIA數據進行蛋白組學的鑒定、定量及差異蛋白分析、富集分析等。蛋白質定性標準:Precursor Threshold 1% FDR,Protein Threshold 1% FDR。Decoy數據庫采用mutated策略生成,Spectronaut進行自動校正,所有符合篩選條件的MS1都用來計算表達量。篩選 FDR小于1%的前3個MS1肽段的峰面積平均值進行蛋白質定量。蛋白互作分析采用STRING數據庫和Cytoscape作圖軟件,GSEA分析采用Broad Institute研究所開發的GSEA分析軟件和MSigDB基因集數據庫。
2 結 果
2.1 MMP14調控衛星細胞成肌分化
為了研究MMP14在衛星細胞分化過程中的作用機制,采集了4周齡小鼠的后腿骨骼肌進行衛星細胞的分離和培養,并應用qRT-PCR和Western blo試驗檢測MMP14基因在衛星細胞(GM)和分化期(DM,誘導24 h)的表達水平。試驗結果表明,MMP14基因的mRNA和蛋白水平均在衛星細胞分化期下調(圖1A&1B)。進一步應用RNAi技術抑制MMP14蛋白表達(圖1C),并通過qRT-PCR和免疫熒光試驗檢測MMP14對衛星細胞分化能力的影響。結果表明,試驗組(si-MMP14)與對照組(si-NC)相比,分化標志基因MYOG、MYHC和MCK的表達量顯著下調,肌管數量和融合指數下降(圖1D&1E),表明抑制MMP14可以有效抑制衛星細胞肌源性分化。
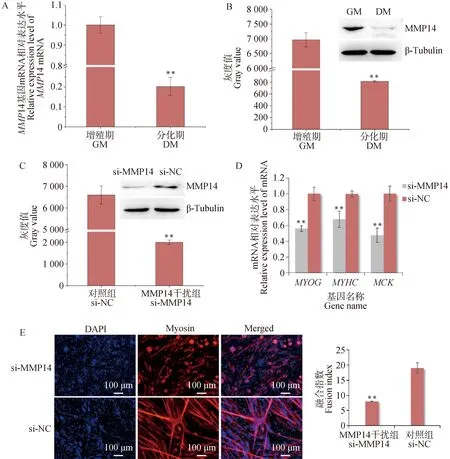
A.qRT-PCR檢測衛星細胞增殖期(GM)和分化期(DM,24 h)MMP14基因的mRNA水平。B.Western blot檢測衛星細胞增殖期(GM)和分化期(DM)MMP14蛋白表達水平。C.Western blot檢測si-MMP14干擾效果,柱狀圖為條帶灰度值分析。D&E. 在衛星細胞中轉染si-MMP14,誘導細胞分化48 h:D.通過qRT-PCR檢測分化標志基因表達水平;E.利用免疫熒光試驗檢測肌管(Myosin,紅光),細胞核用DAPI染色(藍光),標尺為100 μm。qRT-PCR試驗中每組設3個生物學重復,試驗數據以“均值±標準差”的形式呈現,*. P<0.05,**. P<0.01。Western blot試驗和qRT-PCR均以β-Tubulin為內參A. qRT-PCR was performed to detect the expression level of MMP14 gene in satellite cells in proliferation and differentiation status. B. Western blot analysis was performed to detect the expression level of MMP14 protein in satellite cells in proliferation and differentiation status. C. Western blot analysis was performed to detect interference effect of si-MMP14. The gray value analysis of the bands was represented by a bar chart. D&E. si-MMP14 was transfected into satellite cells, and the cells were then induced to differentiate for 48 h: The expression level of differentiation marker genes was detected by qRT-PCR (D), and myotubes (Myosin, red) were detected by immunofluorescence assay (E). Nucleus was stained with DAPI (blue) scale bars: 100 μm. β-Tubulin was used as the internal control. Triplicate samples were analyzed for each treatment, and the results were presented as the “mean±s.e.m”. *. P<0.05,**. P<0.01. β-Tubulin was used as the internal control in both Western blot and qRT-PCR圖1 MMP14在衛星細胞肌源性分化過程中的功能Fig.1 Function of MMP14 in satellite cell myogenic differentiation
2.2 DIA-seq初步篩選衛星細胞中MMP14調控的蛋白
為了進一步研究MMP14蛋白調控衛星細胞發育的分子機制,通過si-RNA抑制衛星細胞中MMP14蛋白的表達,在衛星細胞增殖期收集細胞進行DIA定量蛋白質組學測序分析。經生物信息學分析發現,試驗組(si-MMP14)與對照組(si-NC)相比,對照組數據的彌散程度更高(圖2A),共篩選到549個差異蛋白,其中包括66個上調蛋白和483個下調蛋白(圖2B&2C)。
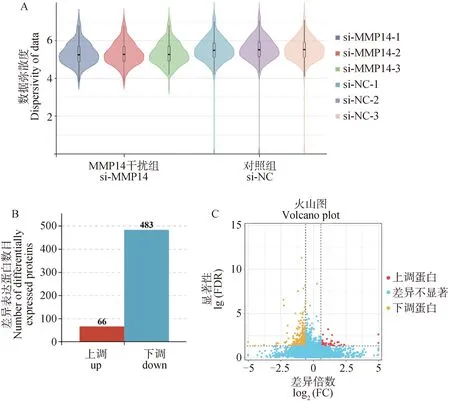
A.小提琴圖用來展示多組數據的分布狀態以及概率密度,圖形縱軸方向長度代表數據彌散程度,橫軸方向長度代表在某縱坐標位置數據分布多少。B.紅色柱子代表上調蛋白數,藍色表示下調蛋白數。C.黃色圓點代表下調蛋白數,紅色圓點表示上調蛋白數A. The violin chart is used to display the distribution status and probability density of multiple sets of data. The length along the vertical axis of the graph represents the degree of data dispersion, while the length along the horizontal axis represents the distribution of data at a certain vertical coordinate position. B. The red column represents the number of up-regulated proteins, while the blue column represents the number of down-regulated proteins. C. Yellow dots represent the number of down regulated proteins, while red dots represent the number of up regulated proteins圖2 DIA-seq分析差異蛋白Fig.2 Differential proteins analysis using DIA-seq
2.3 差異蛋白功能注釋和富集分析
本研究利用基因本體論(Gene Ontology,GO)對上述差異蛋白進行功能分析。對GO功能注釋的3個本體進行統計發現,在生物學過程(biological process,BP)分析中,差異蛋白主要富集在細胞進程、單有機體過程、代謝過程等與肌肉細胞成分相關的生物學過程;在分子功能(molecular function,MF)分析中,差異蛋白主要富集在肌動蛋白結合、催化活性等分子信號傳導相關的功能中;在細胞組成(cellular component,CC)分析中,差異蛋白主要富集在細胞構成、細胞器的構成以及細胞膜的完整性等與細胞骨架結構的完整性相關的組分(圖3)。選取了生物學功能相關的前20個GO條目進行分析,發現差異蛋白主要富集在肌動蛋白的細胞骨架組織、染色質結構組成、染色質凝縮以及蛋白質的轉運及翻譯等過程(圖4A)。
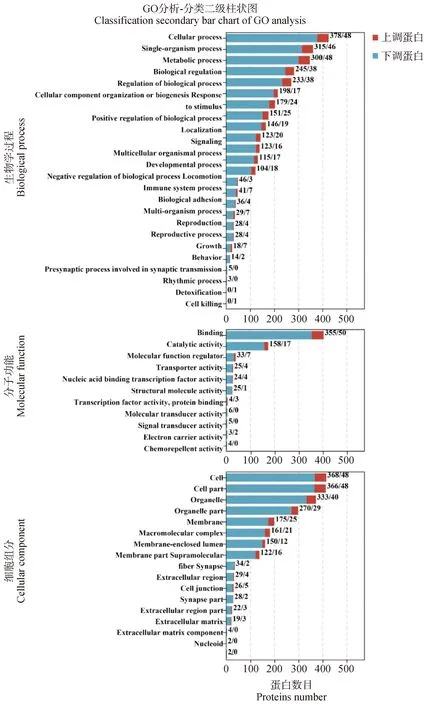
藍色代表下調基因的蛋白數,紅色代表上調基因的蛋白數Blue represents the number of proteins downregulated by genes, while red represents the number of proteins upregulated by genes圖3 差異蛋白功能富集分析Fig.3 Functional enrichment analysis of differential proteins
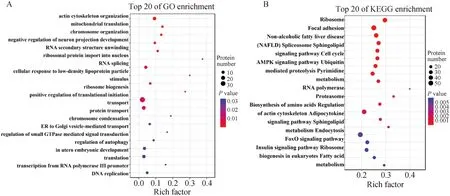
A.差異蛋白GO分析;B.差異蛋白通路富集分析。氣泡大小代表該條目所包含的蛋白數,氣泡顏色代表該條目的富集顯著程度A. GO analysis of differential proteins; B. Pathway analysis of differential proteins. The size of the bubble represents the number of proteins contained in each term, and the color of the bubble represents the significance of the enrichment of each term圖4 差異蛋白GO分析和通路分析Fig.4 Pathway and GO analysis of differentially expressed proteins
為了探究MMP14在小鼠骨骼肌衛星細胞發育過程中的功能,進一步應用京都基因與基因組百科全書(Kyoto Encyclopedia of Genes and Genomes,KEGG)對蛋白質組學檢測獲得的差異蛋白進行通路分析(圖4B)。結果表明,MMP14調控的蛋白富集在6 類通路中,包括有機系統,人類疾病,新陳代謝,環境信息過程、分子過程、基因信息過程。根據P值篩選出前20條信號通路,主要包括細胞黏附、細胞骨架調控通路、脂肪酸代謝、肌動蛋白骨架脂肪細胞因子氨基酸的生物合成等信號通路。
2.4 MMP14參與調控細胞命運決定以及H3-K9組蛋白修飾
本研究進一步對差異蛋白進行了基因集富集分析(gene set enrichment analysis,GSEA)。結果表明,抑制MMP14會影響衛星細胞的細胞命運調控、肌細胞的分化以及H3-K9組蛋白修飾通路,但脂肪酸的生物合成通路顯著上調(圖5A-D)。基于GO、KEGG以及GSEA分析,對差異蛋白進行熱圖分析。結果表明,抑制MMP14蛋白的表達導致與成肌分化相關的蛋白顯著上調,而與成脂分化以及H3-K9甲基化相關的蛋白顯著下調。進一步說明MMP14參與調控衛星細胞分化以及細胞命運決定和異染色質結構等過程(圖5E)。
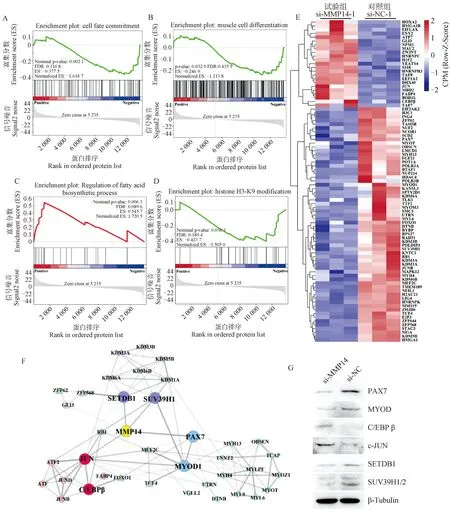
A-D.差異蛋白GSEA分析。E.差異蛋白熱圖分析,紅色代表上調基因,藍色代表下調基因。F.差異蛋白互作網絡分析。G.Western blot檢測肌源性決定因子(PAX7和MYOD)、脂肪分化決定因子(JUN和C/EBPβ)以及H3-K9組蛋白甲基轉移酶(SETDB1和SUV39H1)的表達水平,β-Tubulin作為內參蛋白A-D. GSEA analysis of differential proteins. E. Heat map of differential proteins. Red represents up-regulated genes, blue represents down-regulated genes. F. Interaction network analysis of differential proteins. G. Western blot was performed to detect the expression level of myogenic determination factors (PAX7 and MYOD), lipogenic regulatory factors (JUN and C/EBPβ), and H3-K9 histone methyltransferase (SETDB1 and SUV39H1). β-Tubulin was used as the internal control圖5 MMP14調控衛星細胞命運決定和異染色質結構Fig.5 MMP14 regulated satellite cell fate determination and heterochromatin structure
為了進一步分析MMP14調控衛星細胞分化的通路,應用STRING數據庫中的互作關系分析工具對差異蛋白進行互作網絡分析,并且利用Cytoscape構建互作關系網絡圖。互作分析結果表明,MMP14作為重要節點蛋白,與肌源性分化相關蛋白、脂肪生成相關蛋白以及異染色質結構調控蛋白直接互作(圖5F)。進一步篩選關鍵蛋白并應用Western blot進行驗證。結果表明,抑制MMP14蛋白可導致肌源性分化決定因子(MYOD和PAX7)以及H3-K9組蛋白甲基轉移酶(SETDB1和SUV39H1)的表達水平明顯下調,而成脂調控因子(JUN和C/EBPβ)的表達明顯上調(圖5G)。
3 討 論
衛星細胞作為骨骼肌祖細胞,不僅可以分化為肌纖維,還可以調節細胞外基質的組成,從而影響骨骼肌發育[23]。骨骼肌的發育和再生依賴于衛星細胞肌源性特征的維持,如增殖、分化和自我更新的能力。Foster等[24]研究發現,衛星細胞一旦轉入分化狀態就會停止增殖,并伴隨著細胞形態的改變,形成具有雙極邊緣的紡錘形,最后互相融合形成大的多核肌管。
本課題組前期的研究發現,隨著骨骼肌發育衛星細胞的分化能力呈逐漸衰減的趨勢。這個過程涉及到一系列胞內和胞外的調控因子,其中MMP14是關鍵調控因子之一。Lluri和Jaworski等[25]的研究表明MMP14的表達影響骨骼肌的生長。Christensen和Purslow[26]研究發現,在牛和小鼠的骨骼肌組織中MMP14均有表達,表明MMP14 參與肌管生成,可能是影響肌管形成的因素。本研究通過檢測衛星細胞增殖期和分化期MMP14的表達水平,結果發現MMP14基因表達水平在小鼠骨骼肌衛星細胞增殖期顯著上調,而在分化期下調。抑制MMP14蛋白表達可以有效地抑制衛星細胞分化,表明MMP14可以參與調控細胞分化,但這種調控作用可能發生在分化啟動前而不是在細胞分化期。研究表明,許多功能基因雖然不直接參與終末端分化,但會在細胞分化啟動前(遷移、激活或增殖期)發揮作用,進而影響后續肌源性效應因子表達和肌管融合等過程[27-29]。本研究進一步通過DIA定量蛋白質組學測序分析探究了MMP14調控衛星細胞分化的分子機制。通過對篩選到的差異蛋白進行互作網絡分析發現,MMP14可與衛星細胞肌源性調控因子PAX7和MYOD蛋白直接互作。此外,抑制MMP14蛋白表達可導致PAX7和MYOD蛋白水平下調(圖5G)。PAX7和MYOD的表達在骨骼肌衛星細胞的活化、增殖和分化中起重要作用,PAX7和MYOD的表達增加表明衛星細胞在高度增殖[30]。PAX7是衛星細胞的標志蛋白,它的表達缺失會導致衛星細胞數量減少以及MYOD蛋白表達水平下調,衛星細胞肌源性分化潛力下降[31]。MYOD是骨骼肌特異性轉錄因子,在衛星細胞分化啟動過程中發揮重要作用,可在分化啟動時瞬時高表達,進而上調下游MRFs家族基因表達水平,從而促進衛星細胞分化[32-33]。因此推測,MMP14可能通過調節PAX7和MYOD的表達影響衛星細胞的肌源性潛能和分化啟動,進而影響衛星細胞的成肌分化。當細胞進入分化進程后MMP14蛋白水平下調,表明MMP14對衛星細胞肌源性分化的調控作用發生在分化啟動前,而不是直接參與調控分化啟動后的肌源性效應因子的表達和肌管融合。
在本研究中,蛋白組學分析共篩選得到549個差異蛋白,通過對這些差異蛋白進行GO、KEGG以及GSEA分析,發現MMP14可參與調控細胞黏附、脂肪酸代謝通路、細胞命運決定以及染色質結構等生物學過程和通路。蛋白互作分析表明,除了肌源性調控因子PAX7[11-13]和MYOD之外,MMP14還與成脂調控因子(JUN和C/EBPβ)以及H3-K9組蛋白甲基轉移酶(SETDB1和SUV39H1)直接互作。抑制MMP14蛋白可下調SETDB1和SUV39H1蛋白表達水平,上調JUN和C/EBPβ蛋白表達水平(圖5)。JUN又名活化蛋白1(AP-1),是一種轉錄復合物。Lee等[34]對JUN作為轉錄因子在脂肪細胞分化中的作用進行研究,結果發現小鼠3T3-L1前脂肪細胞中JUN過表達顯著抑制脂肪細胞分化。C/EBPβ是CCAAT/增強子結合蛋白的成員,是促進脂肪形成的主要轉錄因子之一[35]。Zhao等[36]的研究證明,敲除C/EBPβ會減少棕櫚酸處理的HepG2細胞中的脂質積聚并增加脂解。H3-K9組蛋白位于細胞核外源,是一種與轉錄沉默相關的組蛋白[37]。H3-K9me2/3是異染色質區的表觀遺傳標志,標記表達沉默的基因,優先富集在染色體的基因貧乏區域,形成轉錄抑制的異染色質區,而相關基因在異染色質區的分布會影響基因的表達[38-39]。McCarthy等[40-41]的研究表明,H3K9me2/3的標志性蛋白異染色質蛋白1 (HP1)與H3-K9組蛋白甲基轉移酶(Setdb1、SUV39H1)相互作用,影響SETDB1和SUV39H1蛋白的穩定性。Ambrosio等[42]的研究發現,H3-K9me2/3的甲基化水平在增殖的衛星細胞中表達較高,可以調控MyoD因子的表達。在成肌細胞的增殖階段,H3-K9組蛋白甲基轉移酶SUV39H1與MyoD相互作用募集H3-K9me2/3抑制標記,從而抑制衛星細胞的分化[43]。因此推測,MMP14可以通過調控H3-K9組蛋白的甲基化來影響異染色質區域結構,并且直接與成肌和成脂關鍵調控因子互作,參與調控衛星細胞分化和命運決定。
4 結 論
本研究初步分析了MMP14調控骨骼肌衛星細胞分化機制。研究發現,MMP14調控衛星細胞的肌源性潛能和啟動分化前的細胞狀態,進一步影響細胞分化和肌纖維發育過程,而不是直接參與衛星細胞的終末端分化。此外MMP14可能通過H3-K9組蛋白甲基化參與衛星細胞命運決定以及成肌與成脂分化的轉換。本研究結果將為金屬基質蛋白酶參與調控骨骼肌發育的分子機制提供理論依據。

