綿羊肺炎支原體小鼠感染模型的建立
杜改梅,王 月,茅慧華,雷衛強,儲岳峰,劉茂軍,3,4*
(1.金陵科技學院動物科學與食品工程學院,南京 210038;2.中國農業科學院蘭州獸醫研究所/蘭州大學動物醫學與生物安全學院/動物疫病防控全國重點實驗室,蘭州 730000;3.江蘇省農業科學院獸醫研究所,農業農村部獸用生物制品工程技術重點實驗室,南京 210014;4.獸用生物制品(泰州)國泰技術創新中心,泰州 225300)
綿羊肺炎支原體(Mycoplasmaovipneumoniae,Mo)是引起綿羊和山羊支原體肺炎的主要病原體之一,該病呈全球性流行,不同年齡的羊均可感染,羔羊最易感,發病率高達90%[1-2]。羊感染后病變主要在肺組織,剖解可見肺尖葉、心葉有實變區[3-4],主要臨床表現為咳嗽、流涕、呼吸困難、生長發育遲緩、消瘦等,這給養殖業造成巨大經濟損失,嚴重威脅著養羊業的健康快速發展。目前,該病主要通過疫苗免疫和藥物進行防治。疫苗研究國內外雖有較多報道,但由于Mo分離株之間存在高度基因多態性,致使菌株間毒力和免疫原性差異較大,使疫苗的交叉保護力不理想[5]。藥物防治主要以抗生素為主,其雖具有一定療效,但不能從根源上消除感染,疾病容易復發,且易產生細菌耐藥性和藥物殘留等[6],給生態環境、人類和動物健康造成嚴重危害。目前在Mo致病機制、免疫機制等方面也尚未得到明確的結論。闡明該病的致病機理,研制出有效預防該病的疫苗和治療用新型藥物是該病防控的關鍵。而穩定的感染動物模型是疫苗評估和藥物療效反應的基礎保障,也是研究闡明病原體和宿主相互作用機制的必要平臺。
實驗用Mo陰性羊篩選困難,Mo人工感染羊發病模型難建立,現雖已有較多羊發病模型的研究報道[7-10],但研究結果差異較大,不同品種羊對綿羊肺炎支原體易感性不同[11],致使后續研究進展緩慢,且實驗羊成本高和飼養條件等諸多因素均阻礙了綿羊肺炎支原體致病和免疫機制的研究以及疫苗和藥物的研發。小鼠是應用最為廣泛的一種實驗動物,其成本低,飼養方便,是建立病理模型較常用的實驗動物,具有較好的穩定性,且易于標準化。而目前尚未見綿羊肺炎支原體小鼠發病模型的相關研究報道。因此,本研究通過體外分離培養Mo,感染小鼠,通過分析感染小鼠肺病變特點、肺組織抗原載量、血清抗體水平,篩選出綿羊肺炎支原體感染小鼠方法,為綿羊肺炎支原體感染模型的建立提供新思路和新方法,為今后該病的致病機理、免疫機制和防治策略等研究奠定重要基礎。
1 材料與方法
1.1 材料
病料樣品來自于某羊場疑似綿羊支原體肺炎的病羊肺組織,酶標二抗(Goat anti-mouse IgG-HRP)購自BETHYL。SPF健康BALB/c小鼠購于江寧區青龍山動物繁殖場。
1.2 分離培養
將肺組織病樣用支原體培養基清洗3~5次,培養基組成:MEM培養基55 mL、1.7%水解乳蛋白Hank′s緩沖液35 mL、25%酵母液2 mL、健康馬血清10 mL、青霉素200 IU·mL-1、0.4%酚紅0.18 mL。然后將肺組織置于培養液中用無菌剪刀在超凈工作臺剪碎為1 mm3小碎塊,再用移液器反復吹打,使組織塊盡量破裂,用0.45 μm微孔過濾器過濾,將濾液放置于37 ℃恒溫培養箱中靜置培養,每天觀察記錄培養基顏色變化情況和清澈度情況。連續培養5~7 d后觀察有無支原體生長。變黃的菌液保存于-20 ℃備用。
1.3 分離培養物的PCR鑒定
采用PCR方法對本研究分離培養的病原菌進行分子生物學鑒定,具體方法為:取分離培養的變黃菌液5 mL,10 000 r·min-1離心20 min,用1 mL滅菌雙蒸水將沉淀吹吸混勻,使用天根DNA提取試劑盒提取DNA進行Mo PCR檢測,同時以雙蒸水為DNA模板做陰性對照。參照GenBank中公布的HSP70基因序列,使用Primer 6.0軟件設計擴增引物,上游引物序列:5′-ATGAAAGGAAAACAT-AATATGGC-3′,下游引物序列:5′-TTAGTTTTGTTTGATTTCAGCAT-3′,由南京擎科生物科技有限公司合成。PCR反應體系為20 μL:2×Rapid Taq Master Mix 10 μL,上下游引物各1 μL,DNA模板4 μL,ddH2O 4 μL。PCR擴增反應程序:95 ℃預變性5 min;95 ℃ 30 s,50 ℃ 30 s,72 ℃ 1 min,共32個循環;72 ℃ 10 min。將PCR產物進行1.6%瓊脂凝膠電泳檢測,觀察凝膠電泳成像結果,拍照。將PCR擴增條帶回收進行序列測定。
1.4 感染菌液制備及含量測定
將鑒定為Mo的分離培養病原菌進行傳代培養,連續傳5代后,將新鮮培養物用于小鼠攻毒試驗;同時,采用顏色變化單位(CCU)測定培養物濃度。方法為將傳代菌液以1∶10接種于支原體培養基中,依次10倍倍比稀釋10個梯度濃度,每次設4個平行重復,同時設置陰性對照,置于37 ℃恒溫培養箱中靜置培養,每天觀察記錄,連續培養10 d后,最終以管中顏色不再變化為止,且對照無變化,不再發生顏色變化的稀釋倍數為菌液CCU。
1.5 動物試驗
隨機將60只8周齡的SPF健康BALB/c雄性小鼠(22 g±2 g)分為對照組、Mo感染組1、感染組2、感染組3和感染組4(n=12),所有小鼠自由飲水和采食,適應飼養一周后進行試驗。小鼠感染Mo的詳細試驗方案見表1。
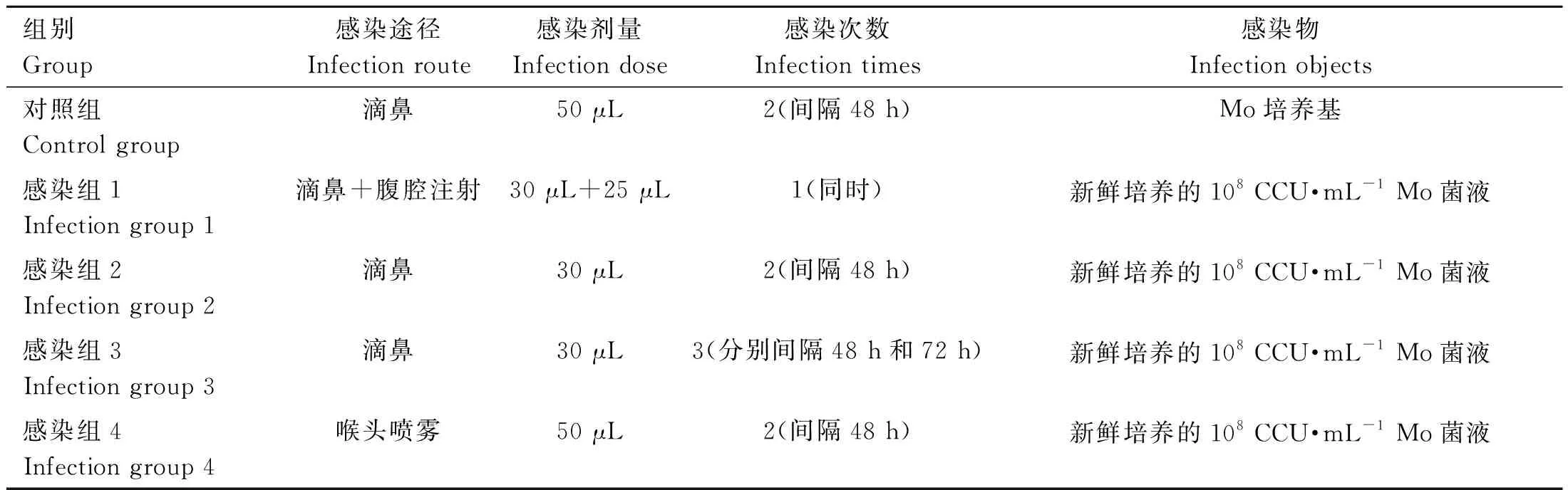
表1 小鼠感染綿羊肺炎支原體(Mo)的試驗方案(n=12)Table 1 Experiment scheme of mice Mycoplasma ovipneumoniae (Mo) infection (n=12)
攻毒后每天觀察小鼠的臨床表現,分別在攻毒后第0、7和14 天禁食稱量小鼠體重。試驗第14天眼球采血并分離血清,乙醚麻醉后處死,剖檢觀察肺病理變化并進行病理評分[12],將肺病變評定為0~5分(無病變計為0分,出現病變記為1分,病變面積每超過20%累加1分)。HE染色進行肺組織病理學檢查。qPCR檢測小鼠肺組織中Mo載量(DNA拷貝數),間接ELISA檢測血清中Mo IgG抗體水平。稱量小鼠脾和肝質量,計算臟器系數。
1.6 肺組織病理組織學檢查(HE染色)
將小鼠肺組織進行組織固定,常規脫水、石蠟包埋、切片和HE染色后,光鏡下觀察組織病理學改變,并對其病理損傷程度進行評分。形態改變根據輕重標記為“1分”“2分”“3分”“4分”,分別表示輕微、輕度、中度、重度,無病變標記為“0分”。
1.7 Mo DNA拷貝數檢測
Mo感染后第14天,采集小鼠肺組織并稱重,加裂解液研磨,采用動物組織DNA提取試劑盒(購自天恩澤生物技術有限公司)提取DNA。測定Mo全菌DNA標準品濃度,計算拷貝數,采用標準曲線法通過qPCR檢測肺組織中Mo DNA拷貝數[13]。用滅菌雙蒸水將Mo全菌DNA標準品進行10倍倍比稀釋,101~108copies·μL-1。將標準品稀釋物和待測樣品DNA各取1 μL作為qPCR反應模板,同時以水做陰性對照。qPCR使用的引物Mo F:5′-ATGTTGACCACGGAAAAACC-3′,Mo R:5′-GG-CATAGTGACGCTTGTCTG-3′。qPCR反應體系為20 μL:2×Taq Pro Universal SYBR qPCR Master Mix 10 μL,上下游引物各0.5 μL,DNA模板2 μL,ddH2O 7.0 μL。qPCR擴增反應程序:95 ℃預變性5 min;95 ℃ 30 s,60 ℃ 30 s,共38個循環;60 ℃收集熒光信號,根據標準曲線計算得到每個待測樣品的Mo DNA拷貝數。
1.8 血清Mo抗體檢測方法
小鼠眼球采血,3 000 r·min-1離心15 min,分離血清。采用間接ELISA方法檢測血清中Mo lgG抗體水平,參考文獻[14]方法改進建立,將待檢血清按1∶50稀釋,HRP-山羊抗小鼠IgG按1∶4 000稀釋,一抗和二抗作用時間均為37 ℃ 60 min,底物顯色10 min,酶標儀檢測OD450 nm值。PBS空白孔中以PBS緩沖液替代樣品,陰性對照孔中以陰性小鼠血清替代樣品。
1.9 統計學處理
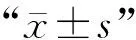
2 結 果
2.1 分離培養和PCR鑒定
從肺組織中分離培養的菌株在培養基中37 ℃恒溫培養5 d后,1∶10和1∶20稀釋接種培養的培養基顏色均由紅色變為黃色,且清亮不渾濁,陰性對照瓶培養基顏色仍為紅色,沒有發生變化。采用PCR方法從分離培養的菌液中擴增出一條與預期目的基因片段大小相符的DNA條帶,大小約為1 815 bp,對照組沒有條帶(圖1)。PCR擴增條帶回收進行了測序分析,由測序結果可知,擴增條帶的基因序列與Mo代表株NCTC10151(GenBank: LR215028.1)序列相似性為98.3%,表明分離菌株為綿羊肺炎支原體,命名為NJ01株。
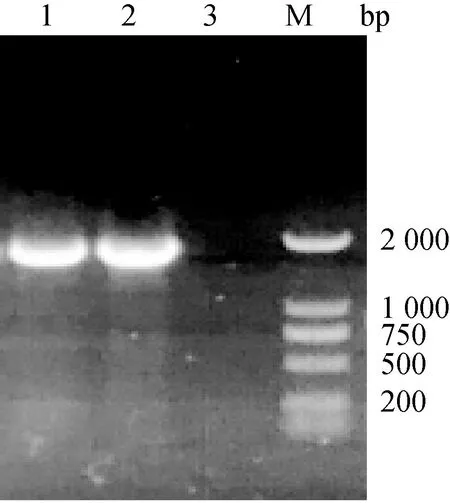
M. DNA相對分子質量標準;1和2. 分離培養物;3. 空白對照M. DNA marker; 1 and 2. Isolated strain; 3. Blank control圖1 綿羊肺炎支原體PCR鑒定Fig.1 PCR identification of Mycoplasma ovipneumoniae
2.2 小鼠臨床表現
感染Mo后小鼠臨床表現異樣,Mo感染組1在感染后第6天出現被毛粗亂,但沒有呼吸異常現象;感染組2和組4的小鼠在感染后第4天出現被毛粗亂和嚴重扎堆現象(圖2),第13天因呼吸困難而各死亡1只,剖檢發現肺嚴重充血和出血。感染組3小鼠第5天出現被毛粗亂,第8天1只小鼠呼吸加快。
2.3 Mo對小鼠體重的影響
從圖3得知,對照組小鼠體重呈逐漸上升趨勢,其它組小鼠體重在接種后第7天出現下降趨勢,Mo感染組3和組4小鼠體重分別比對照組顯著降低5.4%(P<0.05)和6.1%(P<0.05);第14天時各組小鼠體重呈逐漸上升趨勢,但Mo感染組小鼠體重均顯著低于對照組,感染組2和組4分別比對照組顯著降低17.2%(P<0.05)和21.6%(P<0.05),且感染組2和組4顯著低于感染組1和組3,這表明給小鼠攻毒Mo會影響其生長性能,使生長緩慢,2次滴鼻和喉頭噴霧感染影響顯著。
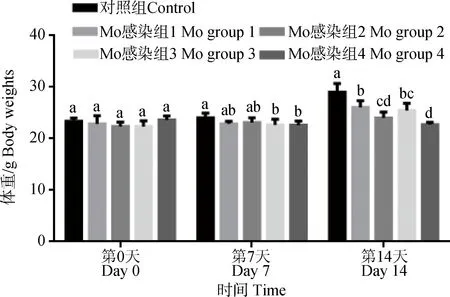
不同日齡點間差異用字母表示,字母不同表示差異顯著(P<0.05)Means not sharing common letter differ significantly (P<0.05)圖3 Mo感染對小鼠體重的影響(n=12)Fig.3 The effect of Mo infection on body weight of mice(n=12)
2.4 小鼠肺剖檢病變觀察及病理評分
對照組小鼠未見異常表現和肺病變。Mo感染組小鼠肺部出現不同程度的充血、出血和實變(箭頭),其中Mo感染組2和組4小鼠肺部實變和出血嚴重,感染組1和組3有輕微出血和實變(圖4)。Mo感染組1、組2、組3和組4的小鼠肺病變平均評分分別為2.0、3.5、2.5和3.3,其中Mo感染組2和組4均顯著高于感染組1(P<0.05)和組3(P<0.05)(圖5),這表明連續2次滴鼻或喉頭噴霧攻毒均可以使小鼠感染并出現肺部嚴重病變。
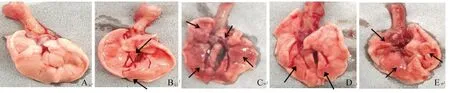
A. 對照小鼠肺;B~E. Mo感染組1~4小鼠肺A. Lung of control group mice, B-E. Lung of mice in Mo infected group 1-4圖4 Mo感染后第14天小鼠肺病理變化Fig.4 Pathological anatomy of lung in mice on the 14th day post infection with Mo
2.5 小鼠肺組織病理組織學檢查
如圖6所示,對照組小鼠肺組織結構正常、完整,肺泡未見萎縮、塌陷,肺泡間隔未見明顯充血、水腫及炎細胞浸潤,各級支氣管未見明顯病理變化,標記為0分;Mo感染組1小鼠肺支氣管/血管周圍可見輕微炎細胞浸潤,標記為1分,表示輕微;Mo感染組2小鼠肺可見輕微間質性肺炎,肺泡間隔增寬,其內可見少量單核細胞為主的炎細胞浸潤,支氣管管腔有輕度滲出及少量脫落支氣管上皮細胞,標記為3分,表示中度;Mo感染組3小鼠肺可見輕度間質性肺炎,肺泡內可見以單核細胞為主的炎細胞浸潤,標記為2分,表示輕度;Mo感染組4小鼠肺可見中度間質性肺炎,肺泡間隔增寬,其內可見以單核細胞為主的炎細胞浸潤,支氣管管腔內可見輕微滲出及少量脫落的支氣管上皮細胞,標記為4分,表示重度。
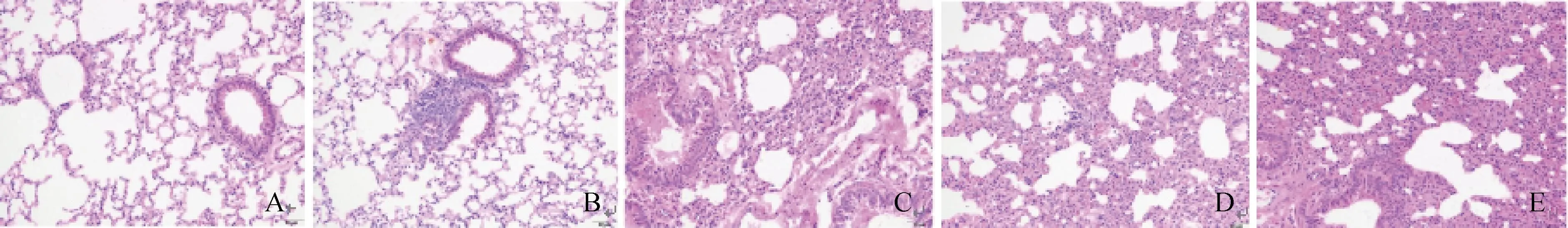
A. 對照小鼠肺組織;B~E. 依次為Mo感染組1-4小鼠肺組織A. Lung tissues of control group mice; B-E. Lung tissues of mice in Mo infected group 1-4圖6 Mo感染第14天小鼠肺組織病理學檢查(HE染色,200×)Fig.6 Histopathological examination of lung in mice on the 14th day post infection with Mo (HE staining,200×)
2.6 qPCR檢測小鼠肺組織中Mo DNA拷貝數
根據標準曲線換算得到Mo感染組小鼠肺組織中Mo載量。由圖7可知,對照組沒有檢測到Mo,Mo感染組1小鼠肺臟組織中DNA拷貝數為102.56拷貝·g-1;感染組3為103.21拷貝·g-1,且顯著高于組1(P<0.05);Mo感染組2和組4的小鼠肺組織中Mo DNA拷貝數分別為103.84拷貝·g-1和103.77拷貝·g-1,均顯著高于Mo感染組1(P<0.05)和組3(P<0.05)。這表明連續2次滴鼻或噴霧攻毒Mo可以使小鼠肺臟組織中Mo載量明顯升高。
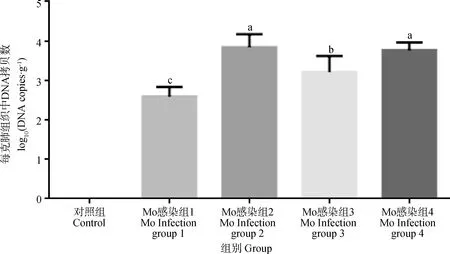
圖7 Mo感染組小鼠肺組織中Mo拷貝數DNA(n=12)Fig.7 Mo DNA copy number of mice lung tissues in Mo infected groups(n=12)
2.7 Mo對小鼠血清中Mo IgG抗體水平的影響
圖8結果顯示,Mo IgG ELISA檢測小鼠血清的OD450 nm平均值,對照組為0.11,Mo感染組1為0.63,顯著高于對照組(P<0.05),但顯著低于其它三個感染組(P<0.05);Mo感染組2為1.05,顯著高于對照組(P<0.05)、感染組1(P<0.05)和組3(P<0.05);Mo感染組3為0.81,感染組4為0.99,并顯著高于對照組(P<0.05)和感染組1(P<0.05),提示4個感染組小鼠均不同程度感染了Mo。
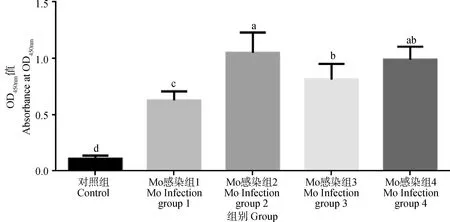
圖8 小鼠血清中Mo抗體水平(n=12)Fig.8 Mo antibody secretion levels in mouse serum in infected and control groups(n=12)
2.8 Mo對小鼠臟器系數的影響
Mo感染組小鼠的肝和脾均出現不同程度的腫大,對照組小鼠臟器未觀察到病變。由圖9可知,感染組1小鼠肝臟系數比對照組和感染組4分別顯著升高17.27%(P<0.05)和15.34%(P<0.05);感染組1和組3的小鼠脾分別比對照組顯著增加70.70%(P<0.05)和69.70%(P<0.05),比感染組2分別顯著增加65.05%(P<0.05)和64.08%(P<0.05)。這表明2次滴鼻或喉頭噴霧感染后小鼠肝和脾嚴重腫大。
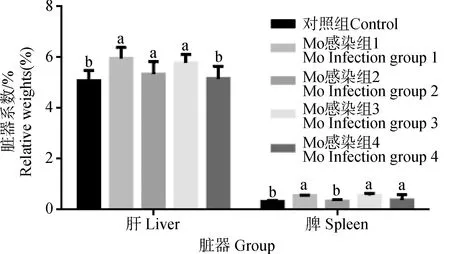
圖9 Mo對小鼠臟器系數的影響(n=12)Fig.9 Effect of Mo on relative weights of organs in infected and control groups(n=12)
3 討 論
綿羊肺炎支原體感染導致羊生長性能和免疫力低下,易繼發細菌或病毒出現混合感染,導致死亡,給養羊業造成重大經濟損失[15]。動物感染模型是研究疫病發病機制、研發有效治療藥物和疫苗的關鍵和保障條件。人工感染動物模型的建立受菌株、動物品種、感染途徑和劑量等多種因素的影響[16-17]。多數動物支原體菌株致病力較弱,即使是臨床分離株也不易導致本動物發病。而羊的品種較多,不同品種對綿羊肺炎支原體的易感性不同[18-19]。已有研究報道,將盤羊和巴什拜的雜交羊經鼻腔滴注和氣管注射Mo,結果雜交羊比巴氏拜羊對Mo較易感[20];給不同品種羊人工感染Mo,結果白山羊病變明顯,死亡率高,且羔羊易感染性更高[8]。同時,感染方式在感染模型的建立中至關重要,主要有肌內注射、腹腔注射、皮下注射、滴鼻、滴眼等方式[21-22]。為了提高感染模型的穩定性,同時降低試驗費用,探索研究小鼠的發病模型不僅可以為實驗操作提供便利,還為該病的防治研究工作提供重要保障。
小鼠是研究免疫和疫苗的有價值的常用實驗動物模型,其來源廣泛、易于飼養、價格低、操作簡便易行,廣泛用于細菌學研究,且野生鼠類極易感染鼠類呼吸道支原體病,大鼠和小鼠感染不同支原體后均出現明顯的炎性癥狀和典型的病理變化[23-25]。有報道,煙熏過的小鼠鼻滴攻毒肺炎支原體感染率可高達93%[26]。因此,推測小鼠是綿羊肺炎支原體感染動物模型的理想選擇,但到目前為止尚未見相關報道。本研究選擇小鼠為感染對象,通過滴鼻或喉頭噴霧途徑,感染不同劑量的Mo,結果發現連續2次滴鼻或喉頭噴霧攻毒,攻毒后第13天,小鼠出現氣喘,呼吸困難而死亡。本研究小鼠僅通過感染綿羊肺炎支原體而出現發病表現,沒有采用煙熏等其它途徑,這樣更能排除發病的非綿羊肺炎支原體感染原因。
羔羊感染綿羊肺炎支原體后,體溫升高,出現咳嗽、流鼻涕等輕微癥狀,血清中Mo抗體上升為陽性,剖檢時見肺的病變顯著,顏色由紅色至灰色不等,肺出現不同程度的壞死[27]。本研究小鼠感染綿羊肺炎支原體后第14天剖檢發現肺部嚴重出血和實變,與文獻報道的支原體感染病變相近。
目前用于檢測綿羊肺炎支原體的實驗室技術較多,如PCR技術、間接ELISA、細菌分離培養等[28-29]。支原體感染小鼠模型病原體多以檢測組織中病原體載量為依據,煙熏并感染肺炎支原體后小鼠組織中病原體拷貝數顯著高于單獨感染組77%[26]。本文采用qPCR檢測到小鼠感染后第14天,4個感染組肺組織中均有Mo病原,且Mo載量高達103.84拷貝·g-1,而對照組沒有檢測到該病原;感染組血清Mo IgG水平顯著高于對照組,肝和脾嚴重腫大。本研究表明,小鼠Mo感染模型實驗操作方法簡便,不僅可靠穩定,安全性高,而且與實驗羊相比,在人力和經濟上具有更低成本效益,符合動物試驗中減少、替代和優化的“3R”原則,本研究為該病病原生物學特性研究、疫苗和藥物研發等提供了重要基礎保障。
4 結 論
滴鼻或喉頭噴霧攻毒Mo均可以引起小鼠發病,以間隔48 h滴鼻或喉頭噴霧兩次感染發病嚴重,肺剖檢顯示嚴重出血和實變,肺組織病理學檢查呈重度,可見中度間質性肺炎,肺泡內可見以單核細胞為主的炎細胞浸潤,支氣管管腔內可見輕微滲出及少量脫落的支氣管上皮細胞,臨床表現、病理變化和病變評分相一致;肺Mo載量達103.84拷貝·g-1,與陽性血清抗體檢測結果也一致。這些結果表明應用報道的方法成功建立了Mo小鼠感染動物模型。

