馬鞭草治療血瘀型閉經的作用機制
馮君 陳西婭 程力

摘要:目的 探討馬鞭草治療血瘀型閉經的作用機制。方法 通過TCMSP數據庫篩選馬鞭草有效成分,在SwissTargetPrediction數據庫進行靶點預測,在GeneCards、DrugBank、OMIM數據庫中檢索閉經相關疾病靶點,借助STRING數據庫構建PPI網絡,在Metascape數據庫進行生物富集分析,利用AutoDockVina、Ligplot、PyMOL軟件進行分子對接。結果 保留馬鞭草有效成分7種,藥物靶點213個,60個與閉經相關,疾病靶點2350個。GO富集涉及核雌激素受體結合等307條生物學過程;KEGG富集涉及內分泌抵抗等43條信號通路。分子對接顯示,馬鞭草核心有效成分槲皮素、木犀草素、香葉木素、山奈酚、蒿黃素與核心靶點AKT1、EGFR、SRC、IGF1R、MMP9均有較強的結合能力。結論 馬鞭草可能作用于內分泌抵抗等多條信號通路,通過抗炎、抗氧化、降解卵泡細胞外基質、促進卵泡血管重塑、誘導原始卵泡活化等作用治療血瘀型閉經。
關鍵詞:馬鞭草;閉經;網絡藥理學;分子對接
閉經主要表現為無月經或月經停止,增加了女性發生應激性或脆性骨折的風險,18歲以前出現的功能性下丘腦性閉經還會不可逆地損害峰值骨量,影響成年后最終身高和骨成熟度[1]。中藥馬鞭草性味苦、涼,歸肝、脾經,有活血散瘀、清熱解毒之功,主治癥瘕積聚、痛經經閉。《本草撮要》記載:“馬鞭草味苦微寒,入足厥陰經,功專破血通經”。現代藥理研究表明,馬鞭草主要化學成分揮發油、黃酮等具有抗炎、抗腫瘤等多種生物活性,臨床多用于治療支氣管哮喘、肝癌等,少有用于治療閉經者[2]。本研究簡要探討馬鞭草治療血瘀型閉經的作用機制。
1資料與方法
1.1 網絡藥理學
以“馬鞭草”為關鍵詞在TCMSP數據庫中檢索后,導入SwissADME平臺篩選胃腸道吸收為“High”,且符合類藥性五原則(DL YES≥2;0 violation)的化合物,導入SwissTargetPrediction數據庫進行靶點預測;以“Amenorrhea”為關鍵詞分別在GeneCards、DrugBank、OMIM數據庫中檢索得到疾病靶點,獲取二者的交集靶點。
將有效成分、交集靶點導入Cytoscape3.9.1軟件篩選出核心有效成分;將交集靶點導入STRING數據庫構建PPI網絡并進行拓撲分析,篩選核心PPI網絡后保留度值前10的基因為關鍵基因。
將關鍵基因導入Metascape數據庫進行生物富集分析,篩選P值較小的前20個通路作圖;將有效成分、關鍵基因、KEGG通路信息導入Cytoscape3.9.1軟件,篩選度值排序前5的靶點為核心靶點。
1.2 分子對接
分別在TCMSP、PDB數據庫中獲取核心有效成分、核心靶點的分子結構,導入AutoDockVina軟件進行半柔性對接,篩選生成氫鍵結合能最低的5組對接關系通過PyMOL、Ligplot軟件構建對接模式圖。
2結果
2.1 網絡藥理學
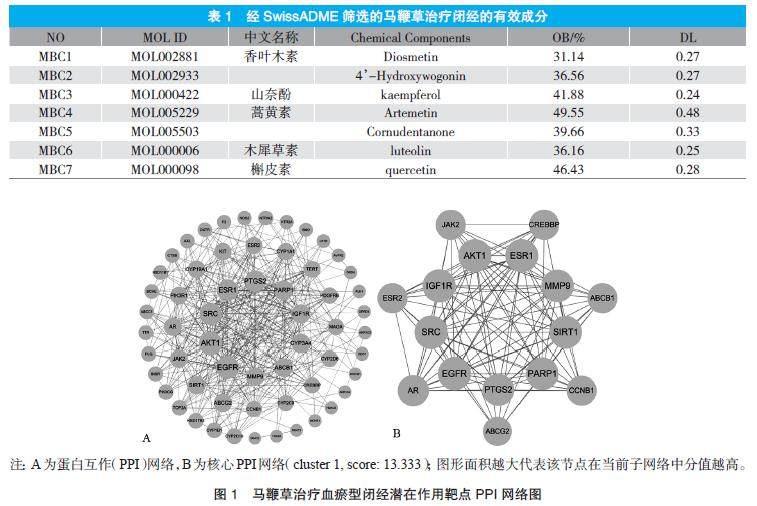
保留有效成分7種(表1)、疾病靶點2350個、藥物靶點213個,交集靶點60個。導入Cytoscape3.9.1軟件,篩選出槲皮素、山奈酚、木犀草素、香葉木素、蒿黃素為核心有效成分;將導入STRING數據庫構建PPI網絡(圖1A),篩選核心PPI網絡(圖1B),推測EGFR、SRC、IGF1R、AKT1、ESR1、MMP9、SIRT1、PARP1、PTGS2、AR可能在馬鞭草治療血瘀型閉經中發揮關鍵調控作用。
將關鍵基因導入Metascape數據庫進行生物富集分析。KEGG富集主要涉及內分泌抵抗等43條信號通路;GO富集分析主要涉及一氧化氮合酶調節活性等307條生物學過程,其中富集在內分泌抵抗信號通路上的基因顯著性最高。導入Cytoscape3.9.1軟件,篩選出AKT1、EGFR、SRC、IGF1R、MMP9可能是核心作用靶點。
2.2 分子對接
核心有效成分與核心靶點均能有效結合,其中槲皮素、木犀草素、香葉木素與MMP9,山奈酚、蒿黃素與AKT1生成氫鍵結合能最低(表2),對接關系模式圖顯示,5組對接關系中的有效成分與靶點均通過形成氫鍵以及疏水作用力相互作用。
3討論
閉經病名首見于《內經》,古稱“女子不月”、“月事不來”等,脾腎虧虛、血虛血瘀、痰濕阻滯均可導致本病,以“虛則補而通之,實則瀉而通之”為基本治則。血瘀型閉經又分為氣滯血瘀、寒凝血瘀兩種證型。現代藥理研究表明,馬鞭草總黃酮可通過抑制AKT/mTOR信號通路誘導細胞自噬來抑制肝癌細胞增殖,但少有針對馬鞭草治療閉經的藥理學研究[3~4]。
研究發現,卵泡膜細胞和卵巢顆粒細胞的細胞外基質(ECM)及卵泡液中存在大量明膠蛋白、纖維蛋白和 IV型膠原蛋白等,這些活性蛋白的有效水解能夠改變卵泡發育的微環境,有利于卵泡細胞增殖、遷移、分化[5]。
基質金屬蛋白酶(MMPs)屬于金屬蛋白酶超家族,后者是一個多結構域鋅依賴的內肽酶家族。MMPs的表達可被絲裂原活化蛋白激酶、p38、粘著斑激酶、胞外信號調節激酶1或蛋白激酶B(AKT)的磷酸化而改變的細胞信號所誘導,并傾向于與炎癥、免疫細胞滲透和腫瘤發生密切相關[6]。MMPs包含23個家族成員,其中基質金屬蛋白酶2和基質金屬蛋白酶9(MMP9)均屬于明膠酶,二者結構域相似,均含有3個重復的纖維連接蛋白Ⅱ型模塊結構域,能在體外裂解ECM蛋白,從而促進胚胎生長和發育、組織重塑、炎癥和傷口愈合,磷酸化的AKT還可誘導AKT依賴性FOXO蛋白磷酸化并從細胞核內移除,觸發原始卵泡活化[7~8]。
本研究保留7種有效成分,60個交集靶點,核心有效成分是槲皮素、木犀草素、香葉木素、山奈酚、蒿黃素,核心靶點是AKT1、EGFR、SRC、IGF1R、MMP9。分子對接結果顯示,核心有效成分與核心靶點均能較好地結合,其中槲皮素、木犀草素、香葉木素與MMP9,山奈酚、蒿黃素與AKT1生成氫鍵結合能最低。由此可見,ECM蛋白水解失調、血管重塑失敗、原始卵泡活化受阻均可導致卵泡生長受限,最終導致閉經的發生,提示MMP9、AKT是本病的關鍵治療靶點。本研究通過生物富集分析得到43條通路和307個生物學過程,發現KEGG主要與內分泌抵抗等信號通路有關,且內分泌抵抗信號通路上富集的基因顯著性最高(P值最小),提示該條信號通路可能是馬鞭草治療血瘀型閉經的關鍵信號通路。
綜上所述,馬鞭草主要成分槲皮素、木犀草素、香葉木素、山奈酚、蒿黃素作用于AKT1、EGFR、SRC、IGF1R、MMP9等基因靶點,參與多種生物學過程,調控內分泌抵抗等多條信號通路,可通過抗炎、抗氧化、降解卵泡細胞外基質、促進卵泡血管重塑、誘導原始卵泡活化等作用治療血瘀型閉經。
參考文獻:
[1]張志鵬,鄧李紅,王壽富,等.超高效液相色譜指紋圖譜與化學模式識別馬鞭草藥材質量評價研究[J].中國醫藥導報,2022,19(21):21-25.
[2]蔡小兵,胡欣,金鵬飛.對《中華人民共和國藥典》2010年版(一部)的分析和探討[J].中國新藥雜志,2012,21(16):1874-1877.
[3]李振雨,梁月儀,呂渭升,等.馬鞭草藥材UPLC指紋圖譜建立及指標性成分的測定[J].天然產物研究與開發,2023,35(4):551-561.
[4]王夢月,賈敏如.馬鞭草在民間的藥用情況概述[J].中國民族民間醫藥雜志,2002(3):156-158.
[5]王夢月,賈敏如.25個民族藥用馬鞭草情況概述[J].中國民族醫藥雜志,2002(2):20-21.
[6]杜超群,楊最素.馬鞭草對治療生殖器官疾病的研究進展[J].醫學理論與實踐,2012,25(15):1843-1844.
[7]王燕,朱向東,王歡,等.馬鞭草的臨床應用及其用量探究[J].長春中醫藥大學學報,2021,37(2):278-281.
[8]馬設召.陽和湯加減聯合桂枝茯苓丸、益母草、馬鞭草治療子宮肌瘤的臨床療效觀察[J].智慧健康,2021,7(2):153-155.

