米諾地爾治療橋本氏甲狀腺炎合并脫發(fā)1例
韓樂 蔣雨辰
[關(guān)鍵詞] 橋本氏甲狀腺炎;自身免疫性甲狀腺疾病;脫發(fā);斑禿;休止期脫發(fā)
[中圖分類號(hào)] R581; R758.71 [文獻(xiàn)標(biāo)識(shí)碼] B [文章編號(hào)] 1004-4949(2024)09-0144-03
甲狀腺疾病(Thyroid disease)是臨床常見的內(nèi)分泌疾病,包括甲狀腺功能異常、甲狀腺結(jié)節(jié)及自身免疫性甲狀腺疾病等,其發(fā)病率呈現(xiàn)逐年上升的趨勢(shì)[1]。目前已有研究表明[2,3],甲狀腺疾病常可能合并或?qū)е露喾N類型的脫發(fā),如斑禿、休止期脫發(fā)、雄激素性脫發(fā)等,其中自身免疫性甲狀腺疾病與脫發(fā)關(guān)系最為密切。自身免疫性甲狀腺疾病包括Graves病以及橋本氏甲狀腺炎,二者均可能導(dǎo)致甲狀腺功能改變及毛發(fā)異常,使患者更易出現(xiàn)包括斑禿在內(nèi)的多種類型脫發(fā)[4]。有研究表明[5,6],患有斑禿的患者,也更容易合并甲狀腺異常,該現(xiàn)象的具體機(jī)制目前尚不完全清楚,可能與免疫、遺傳等因素有關(guān)[7]。以往的病例報(bào)道多為甲狀腺疾病與斑禿之間的研究,罕有橋本氏甲狀腺炎同時(shí)與多種類型脫發(fā)合并的報(bào)道,本研究報(bào)道1例甲狀腺功能正常的橋本氏甲狀腺炎合并多種類型脫發(fā)的患者,采用糖皮質(zhì)激素聯(lián)合米諾地爾進(jìn)行治療,探究其臨床療效,現(xiàn)報(bào)道如下。
1 臨床資料
1.1 病例資料 患者女,62歲,因脫發(fā)伴情緒欠佳9月余,于2024年1月9日至我科脫發(fā)門診就診。患者因家庭變故出現(xiàn)情緒欠佳及睡眠障礙,后逐漸出現(xiàn)彌漫性脫發(fā),以頂部、顳部及枕部為主。患者既往有血糖升高史,未達(dá)到糖尿病診斷標(biāo)準(zhǔn),無高血壓、心臟病等慢性病史,無鼻炎、哮喘、甲亢等過敏性疾病或自身免疫性疾病病史,直系親屬有甲亢病史,無腫瘤病史及家族史。體格檢查:系統(tǒng)查體未見明顯異常,頭皮頂部、顳部、枕部毛發(fā)呈彌漫性稀疏,頭皮及頭發(fā)油膩,少許黏著性鱗屑附著,拉發(fā)試驗(yàn)陽性,指趾甲未見明顯異常,全身皮膚較干燥。實(shí)驗(yàn)室檢查:餐后血糖11.32 mmol/L;促甲狀腺激素1.9007 mIU/ml(正常范圍為0.35~4.94 mIU/ml),血清游離甲狀腺素15.78 pmol/L(正常范圍為9.01~19.05 pmol/L),游離三碘甲狀腺原氨酸4.72 pmol/L(正常范圍為2.43~6.01 pmol/L),血清總甲狀腺素106.2 nmol/L(正常范圍為62.68~150.84 nmol/L),抗甲狀腺過氧化物酶抗體615.7 IU/ml↑,抗甲狀腺球蛋白抗體89.06 IU/ml↑。血常規(guī)、肝腎功能、C反應(yīng)蛋白、乙肝兩對(duì)半、丙肝抗體、梅毒抗體、HIV抗體等檢查均未見明顯異常。甲狀腺彩超:甲狀腺形態(tài)正常,雙側(cè)葉對(duì)稱性不大,輪廓規(guī)則,表面光整,內(nèi)部回聲增粗,分布欠均勻。CDFI:甲狀腺內(nèi)見點(diǎn)條狀血流信號(hào)。雙側(cè)頸部未見明顯異常腫大淋巴結(jié)。皮膚鏡檢查:頂部、顳部、枕部毛發(fā)均顯示出毛囊口變細(xì)、消失或者閉鎖,毛發(fā)尖端變細(xì),粗細(xì)不均,呈現(xiàn)感嘆號(hào)樣發(fā),可見黃點(diǎn)征,毛干變細(xì)、短縮或者消失,同時(shí)毛干出現(xiàn)色素減退,毛囊周圍色素沉著,毳毛增多,單個(gè)毛囊單位以單根毛囊為主。患者治療前情況,見圖1、圖2。
1.2 臨床診斷 橋本氏甲狀腺炎,斑禿,休止期脫發(fā),睡眠障礙,焦慮狀態(tài),抑郁狀態(tài)。
1.3 方法 使用復(fù)方倍他米松注射液1 ml肌肉注射,3周/次;使用5%米諾地爾酊劑(浙江萬晟藥業(yè)有限公司,國(guó)藥準(zhǔn)字H20010714,規(guī)格:10 ml∶0.5 g)于睡前外用于頭皮,2 ml/次;谷維素片口服,3次/d,2片/次,以改善患者心理狀態(tài)及調(diào)節(jié)患者睡眠。
2 結(jié)果
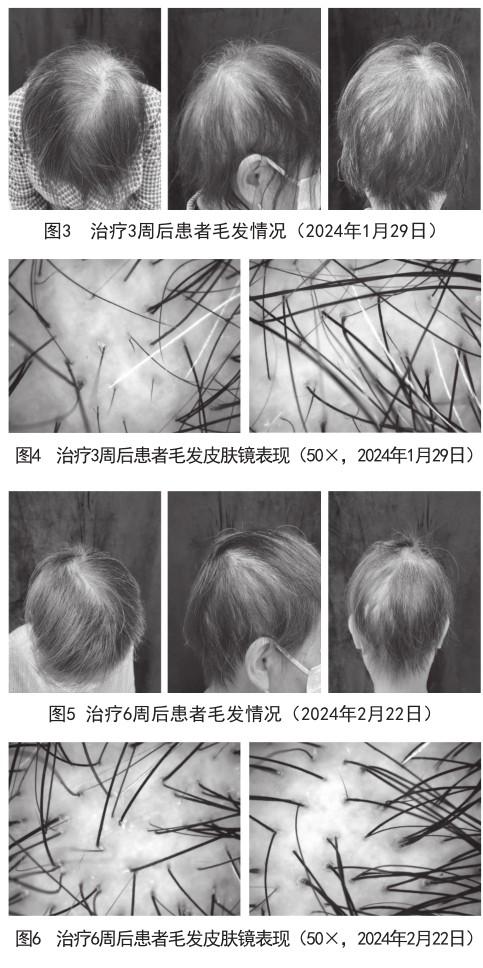
治療3周后第1次隨訪復(fù)查(2024年1月29日):患者脫發(fā)量明顯減少,新生毛發(fā)不明顯,但拉發(fā)試驗(yàn)轉(zhuǎn)為陰性。皮膚鏡檢查顯示:毛發(fā)密度較前增加,感嘆號(hào)樣發(fā)比例減少,仍有毛干色素減退,可見新生毳毛,毛囊口較多皮脂附著。隨著脫發(fā)量減少,患者焦慮、抑郁等情緒減輕,睡眠狀態(tài)較前改善。患者治療3周后情況,見圖3、圖4。
治療6周后第二次隨訪復(fù)查(2024年2月22日):患者脫發(fā)量持續(xù)減少,可見較多新生毛發(fā),拉發(fā)試驗(yàn)陰性。復(fù)查皮膚鏡顯示:毛發(fā)密度增加,毛干直徑均勻,顏色加深,較少感嘆號(hào)樣發(fā),大部分毛發(fā)恢復(fù)正常,仍可見新生毳毛。患者焦慮、抑郁等情緒明顯改善,極少出現(xiàn)睡眠障礙等問題。目前患者仍在繼續(xù)隨訪治療中。患者治療3周后情況,見圖5、圖6。

3 討論
自身免疫性甲狀腺疾病常表現(xiàn)為Graves病及橋本氏甲狀腺炎,其發(fā)病機(jī)制尚不完全清楚,可能與抗甲狀腺抗體的產(chǎn)生、T/B淋巴細(xì)胞的浸潤(rùn)有關(guān),并可能導(dǎo)致甲狀腺激素分泌異常[8]。斑禿是非瘢痕性脫發(fā)中最常見的脫發(fā)類型,其與毛囊免疫豁免機(jī)制喪失,導(dǎo)致CD8+ T細(xì)胞攻擊毛囊相關(guān)[9,10]。目前現(xiàn)有的關(guān)于自身免疫性甲狀腺疾病與斑禿的機(jī)制研究中已經(jīng)揭示了調(diào)節(jié)性T細(xì)胞共同參與了兩者的發(fā)病[11]。有研究顯示[12],HLADQB1*03與斑禿及抗體誘發(fā)的甲狀腺功能減退均密切相關(guān)。這進(jìn)一步為自身免疫性甲狀腺疾病導(dǎo)致斑禿或者斑禿常常合并自身免疫性甲狀腺疾病提供了機(jī)制上的解釋。
對(duì)于該患者來說,皮膚鏡不僅能發(fā)現(xiàn)該患者有斑禿的典型表現(xiàn),還發(fā)現(xiàn)其有毛囊口閉鎖、色素減退等休止期脫發(fā)的表現(xiàn)。休止期脫發(fā)與多種內(nèi)源性和外源性因素相關(guān),包括手術(shù)、重大疾病、甲狀腺疾病、分娩、營(yíng)養(yǎng)不良等[13]。其中,甲狀腺激素可能會(huì)干擾人體正常的毛囊生長(zhǎng)周期,從而導(dǎo)致休止期脫發(fā)。有證據(jù)表明[14],甲功T3、T4不僅能影響體外毛發(fā)在其生長(zhǎng)期的生長(zhǎng)長(zhǎng)度,還能影響人體頭皮毛囊線粒體的能量代謝。此外,相關(guān)免疫因素也可能共同介導(dǎo)休止期脫發(fā)的發(fā)生。因此,對(duì)于該患者合并休止期脫發(fā)的可能原因,除了自身家庭變故等情緒應(yīng)激之外,橋本氏甲狀腺炎導(dǎo)致的甲狀腺病變也是重要的發(fā)病因素。
本病例提示,橋本氏甲狀腺炎患者早期可能未出現(xiàn)甲狀腺功能異常而處于亞臨床期,即使此時(shí)患者甲狀腺功能正常,也應(yīng)注意觀察患者是否出現(xiàn)脫發(fā)或出現(xiàn)其他并發(fā)癥,應(yīng)對(duì)甲狀腺功能進(jìn)行監(jiān)測(cè),并給予治療。同時(shí),合并斑禿、休止期脫發(fā)等多種類型脫發(fā)的患者應(yīng)注意檢查甲狀腺功能,明確脫發(fā)是否存在某些原發(fā)性甲狀腺疾病或共患病的可能,給予綜合性處理。另外,本病例還提示,使用系統(tǒng)激素聯(lián)合外用米諾地爾對(duì)這自身免疫性甲狀腺疾病合并脫發(fā)的患者有較好的治療效果,這兩種藥物對(duì)毛發(fā)生長(zhǎng)有協(xié)同作用。米諾地爾可以通過增加頭皮血流及延長(zhǎng)毛發(fā)生長(zhǎng)期來刺激毛發(fā)生長(zhǎng),而糖皮質(zhì)激素的抗炎作用既可以治療脫發(fā)又可以為米諾地爾的起效營(yíng)造良好的環(huán)境。但不管是甲狀腺疾病還是脫發(fā)均可能對(duì)患者心理產(chǎn)生不同程度的影響,故應(yīng)注意關(guān)注患者心理狀況并加強(qiáng)其心理疏導(dǎo),給予其個(gè)體化、系統(tǒng)化治療,進(jìn)而達(dá)到綜合性改善的目的。
[參考文獻(xiàn)]
[1]Zhang X,Wang X,Hu H,et al.Prevalence and trends of thyroid disease among adults,1999-2018[J].Endocr pract,2023,29(11):875-880.
[2]Hussein RS,Atia T,Bin Dayel S.Impact of thyroid dysfunction on hair disorders[J].Cureus,2023,15(8):e43266.
[3]Aboalola D,Aouabdi S,Ramadan M,et al.An update on alopecia and its association with thyroid autoimmune diseases[J].TouchREV Endocrinol,2023,19(2):54-59.
[4]Naik PP,F(xiàn)arrukh SN.Association between alopecia areata and thyroid dysfunction[J].Postgrad Med,2021,133(8):895-898.
[5]Lee S,Lee YB,Kim BJ,et al.Screening of thyroid function and autoantibodies in patients with alopecia areata: a systematic review and meta-analysis[J].J Am Acad Dermatol,2019,80(5):1410-1413.
[6]Moseley IH,Thompson JM,George EA,et al.Immunemediated diseases and subsequent risk of alopecia areata in a prospective study of US women[J].Arch Dermatol Res,2023,315(4):807-813.
[7]Naik PP,F(xiàn)arrukh SN.Association between alopecia areata and thyroid dysfunction[J].Postgrad Med,2021,133(8):895-898.
[8]Bogus?awska J,Godlewska M,Gajda E,et al.Cellular and molecular basis of thyroid autoimmunity[J].Eur Thyroid J,2022,11(1):e210024.
[9]Seok J,Cho SD,Lee J,et al.A virtual memory CD8+ T celloriginated subset causes alopecia areata through innatelike cytotoxicity[J].Nat Immunol,2023,24(8):1308-1317.
[10]Rajabi F,Drake LA,Senna MM,et al.Alopecia areata: a review of disease pathogenesis[J].Br J Dermatol,2018,179(5):1033-1048.
[11]Wan S,Xu W,Xie B,et al.The potential of regulatory T cell-based therapies for alopecia areata[J].Front Immunol,2023,14:1111547.
[12]Popa A,Carsote M,Cretoiu D,et al.Study of the thyroid profile of patients with alopecia[J].J Clin,2023,12(3):1115.
[13]Asghar F,Shamim N,F(xiàn)arooque U,et al.Telogen effluvium: a review of the literature[J].Cureus,2020,12(5):e8320.
[14]Zhang QY,Ye XP,Zhou Z,et al.Lymphocyte infiltration and thyrocyte destruction are driven by stromal and immune cell components in Hashimotos thyroiditis[J].Nat Commun,2022,13(1):775.
收稿日期:2024-4-4 編輯:劉亦洋

