聚焦中考化學金屬的冶煉熱點題型


摘? 要:工業上冶煉金屬的原料、原理、設備、產品等問題一直是各省、市中考化學命題的熱點,多以工藝流程的形式考查化學方程式的書寫、反應類型的判斷等.本文對中考化學金屬冶煉的考查內容及其常見熱點題型進行了分類和總結.
關鍵詞:題型;冶煉金屬;中考化學
中圖分類號:G632??? 文獻標識碼:A??? 文章編號:1008-0333(2024)14-0134-03
收稿日期:2024-02-15
作者簡介:王琳(1971.12—),女,北京人,本科,中學高級教師,從事初中化學教學研究.
基金項目:甘肅省教育科學“十四五”規劃2022年度重點課題“新中考改革背景下的化學課堂轉型實踐研究”(立項號:GS[2022]GHBZ141).
金屬的冶煉一直是中考化學命題的重點內容,包括一氧化碳還原氧化鐵實驗、工業煉鐵等內容.重點考查反應原理、實驗操作步驟先后順序的確定、實驗現象、尾氣處理等,主要以填空題、簡答題和計算題等形式出現[1].
1 考查冶煉金屬的反應原理
例1? 我國古代制取黃銅的原理是:C+ZnCO3+Cu2O高溫2CO2↑+2Cu+Zn.下列說法正確的是(? ).
A.黃銅的硬度比純銅小
B.反應中Cu2O發生氧化反應
C.氣體產物中可能含有CO
D.黃銅是鋅、銅組成的復合材料
解析? 合金的硬度比組成它的純金屬的硬度大,黃銅的硬度比純銅大,A錯誤;反應中Cu2O失去了氧,發生了還原反應,B錯誤;碳與氧結合能生成一氧化碳,氣體產物中可能含有CO,C正確;合金是指在一種金屬中加熱熔合其他金屬或非金屬而形成的具有金屬特性的物質,屬于金屬材料,黃銅不是鋅、銅組成復合材料,D錯誤.
答案:C
2 考查實驗室模擬煉鐵
例2? (2023·四川瀘州)工業上可用焦炭與赤鐵礦冶煉鐵.實驗室用如圖1所示裝置模擬冶煉鐵并探究其產物.回答下列問題:
(1)酒精噴燈加熱前,先打開活塞K1和K2,關閉K3,將氣囊中N2鼓入.通N2的目的是.
(2)通適量N2后,關閉活塞K1和K2,打開K3,點燃酒精噴燈進行實驗.B裝置中盛放的試劑是(選填“稀硫酸”“澄清石灰水”或“氯化鈣溶液”),用于檢測氣體產物之一(填化學式).
(3)裝置C的作用是.
(4)當A裝置藥品完全變黑后,停止實驗.移走酒精噴燈停止加熱前的操作是.
(5)用簡單的化學方法證明已經冶煉出鐵.取少量黑色產物于試管中,滴加(選填“稀硫酸”“澄清石灰水”或“硫酸銅溶液”),觀察到,說明鐵已生成.
解析? (1)加熱前通N2的目的是排凈裝置內的空氣;(2)焦炭與氧化鐵高溫下反應會生成二氧化碳,二氧化碳可以使澄清的石灰水變渾濁,因此B裝置中盛放的試劑是澄清石灰水,用于檢測氣體產物之一中的二氧化碳,化學式為CO2;(3)一氧化碳與氫氧化鈣不反應,一氧化碳也不溶于水,因此裝置C的作用是收集一氧化碳氣體;(4)當A裝置藥品完全變黑后,停止實驗,移走酒精噴燈停止加熱前的操作是先把K3關閉,以防產生倒吸,發生危險;(5)鐵能夠與稀硫酸反應產生硫酸亞鐵和氫氣,觀察到有氣泡產生.
3 考查古文獻中冶煉金屬的方法
例3? (2023·四川巴中)明代宋應星所著《天工開物》一書,介紹了“火法煉鋅”的方法,把爐甘石(ZnCO3)和煤炭餅裝入煉鋅罐,如圖2所示,泥封、“其底鋪薪,發火煅紅”“冷定毀罐取出”.下列說法錯誤的是(? ).
A.爐甘石(ZnCO3)加入鋅罐之前,將其粉碎的目的是增大反應物之間的接觸面積
B.反應區中發生的反應之一:C+2ZnO高溫2Zn+CO2↑,該反應中體現了C的還原性
C.“冷定毀罐取出”的目的是防止鋅在較高溫度下再次被氧化
D.“火法煉鋅”符合低碳發展理念
解析? 將爐甘石進行粉碎的目的是增大反應物之間的接觸面積,讓反應更加充分,A正確;碳具有還原性,可將氧化鋅還原成鋅單質,B正確;為了防止熱的鋅與空氣中的氧氣發生反應,故“冷定”后方能“毀罐”取鋅,C正確;“火法煉鋅”會產生二氧化碳,不符合低碳原理,D錯誤.
答案:D
4 考查工業上冶煉金屬的相關計算
例4? (2023·四川眉山)磁鐵礦石(主要成分為Fe3O4)是常用的煉鐵原料,工業上可通過如下反應:Fe3O4+4CO高溫3Fe+4CO2,將其中的Fe3O4轉化為Fe.
(1)Fe3O4中鐵、氧的微觀粒子數目之比為.
(2)假設煉鐵過程中鐵沒有損耗,用含348噸Fe3O4的磁鐵礦石理論上可以煉出含鐵96%的生鐵的質量是多少?
解析? (1)由四氧化三鐵的化學式可知,Fe3O4中鐵、氧的微觀粒子數目之比為3∶4.
(2)設理論上可以煉出鐵的質量為x.
Fe3O4+4CO? 高溫? 3Fe+4CO2
232168
348 tx×96%
232∶168=348 t∶96%? x
x=262.5 t
5 考查冶煉金屬的定性、定量綜合實驗
此類試題一般借助于冶煉金屬的實驗,通過定性分析和定量計算來探究物質的組成成分以及含量等.試題的綜合性較強,常以填空題或實驗探究題呈現,難度也較大.
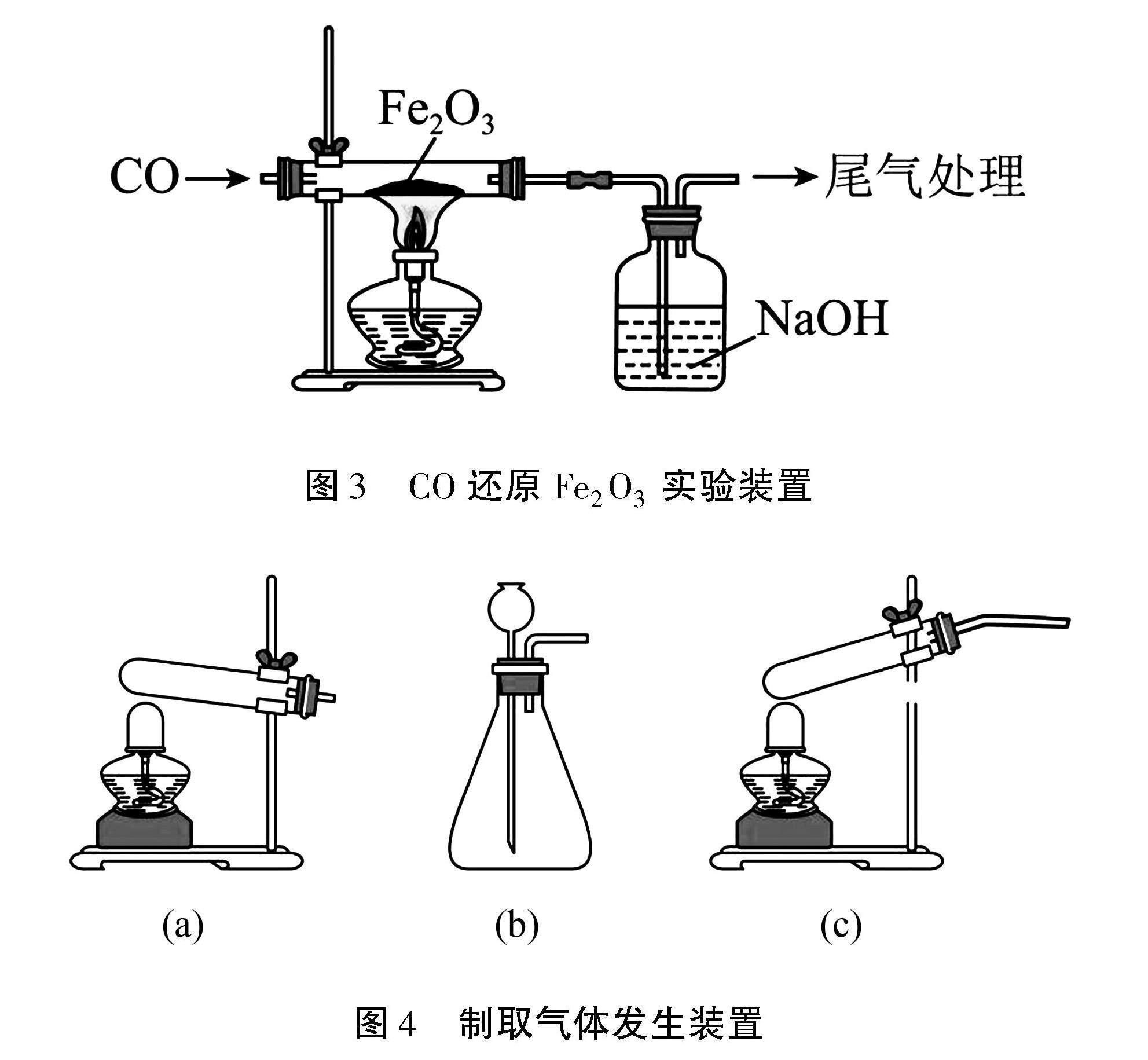
例5? (2023·廣東廣州)某小組采用圖3所示實驗裝置探究CO還原Fe2O3時,出現了爭論.甲同學觀察到固體由紅色變成黑色,推斷黑色固體是Fe;乙同學提出疑問,認為黑色固體可能是Fe3O4,并查閱了資料:Fe3O4可被磁鐵吸引,幾乎不溶于稀酸溶液.
(1)制備CO的原理是:HCOOH濃硫酸△CO↑+H2O(HCOOH在常溫下為液態),圖4所示三種氣體發生裝置中,可用于制備CO的是(填標號).
(2)若甲同學推斷正確,反應的化學方程式為.
(3)對乙同學提出的質疑進行分析和驗證.
①定量分析物質組成可知,該反應生成Fe3O4是合理的,理由是.
②該小組通過對黑色固體進行檢驗,證明同時含有Fe3O4和Fe.檢驗的操作和現象是:取樣于試管中,.
(4)該小組為了探索CO還原Fe2O3與溫度的關系,走訪了某鋼鐵廠.工程師用SDTQ熱分析儀對該反應進行研究,根據不同溫度下所得固體的質量,推導對應的固體成分,結果如圖5所示.
①用CO煉鐵時,還原Fe2O3的溫度應不低于(填“400”“600”或“800”)℃.
②圖中x=.
③該小組查閱資料得知酒精燈加熱溫度為600 ℃左右,他們發現上述對黑色固體成分的檢驗結果與圖像有矛盾,推測黑色固體在冷卻過程中發生了以下反應:=Fe3O4+.
解析? (1)由制備CO的原理可知,反應屬于液液加熱型,圖4所示三種氣體發生裝置中,可用于制備CO的是C.(2)甲同學推斷黑色固體是Fe,則對應反應為一氧化碳和氧化鐵在高溫下生成鐵和二氧化碳,化學方程式為:3CO+Fe2O3高溫2Fe+3CO2.(3)①定量分析物質組成可知,該反應生成 Fe3O4是合理的,理由是反應前有鐵、氧元素,根據質量守恒定律可知,反應后元素種類不變;②該小組通過對黑色固體進行檢驗,證明同時含有Fe3O4和Fe,可加入稀鹽酸,Fe3O4幾乎不溶于稀鹽酸,鐵和稀鹽酸反應生成氯化亞鐵和氫氣,故檢驗的操作和現象是取樣于試管中,滴入稀鹽酸,觀察到有氣泡生成,形成淺綠色溶液,有黑色固體不溶解,則原黑色固體同時含有Fe3O4和Fe.(4)①用CO煉鐵得鐵單質,結合圖5,還原Fe2O3的溫度應不低于800 ℃;②由圖5可知,最初氧化鐵固體的質量為48.0 g,其中鐵元素全部轉化為鐵單質,則Fe的質量為48.0 g×48 g×112160×100%=33.6 g×100%=33.6 g,則x=33.6;③由圖5可知,600 ℃左右固體為氧化亞鐵,可能是在冷卻過程中氧化亞鐵分解為四氧化三鐵和鐵,化學方程式為4FeOFe3O4+Fe.
6 結束語
總之,工業上冶煉金屬的一般原理是在高溫的條件下,用還原劑(如一氧化碳、碳等)將金屬從含金屬的礦石中還原出來,原料和產品都涉及的是不純物質的質量,計算時一定要進行換算,把純凈物的質量代入化學方程式計算.
參考文獻:[1] 人民教育出版社,課程教材研究所,化學課程教材研究開發中心.義務教育教科書·化學[M].北京:人民教育出版社,2015.
[責任編輯:季春陽]

