發根農桿菌介導的甜瓜CRISPR/Cas9系統靶位點的檢測





摘 " "要:選取甜瓜栽培材料龍慶八號作為受體材料,構建CmCURT1A基因CRISPR/Cas9基因編輯載體,經發根農桿菌介導檢測靶位點的編輯情況,為后續甜瓜遺傳轉化試驗提供載體基礎。以甜瓜CmCURT1A基因(ID:MELO3C006053.2)為靶基因構建雙靶位點敲除載體,經發根農桿菌K599介導的簡單遺傳轉化技術使甜瓜組織長出不定根,經PCR測序發現在不定根中分別存在65 bp、72 bp不同堿基片段的缺失。該方法成功進行了甜瓜CRISPR/Cas9載體靶位點敲除情況的檢測,簡單高效,實現了在甜瓜中基因編輯靶點的快速鑒定,為研究甜瓜基因功能和遺傳改良奠定基礎。
關鍵詞:甜瓜;CRISPR/Cas9;發根農桿菌;基因敲除
中圖分類號:S652 文獻標志碼:A 文章編號:1673-2871(2024)08-015-09
Detection of target sites of CRISPR/Cas9 system in melon by Agrobacterium rhizogenes system
ZHU Lei
(Daqing Branch of Heilongjiang Academy of Agricultural Sciences, Daqing 163711, Heilongjiang, China)
Abstract: The cultivation melon Long Qing No. 8 was used as the receptor material to construct the CRISPR/Cas9 editing vector of CmCURT1A gene. The targe site was detected through Agrobacterium rhizogenes, which provided the vector basis for subsequent genetic transformation experiment of melon. A double target knockout vector was constructed using the CmCURT1A gene(ID: MELO3C006053.2) as the target gene. Through a simple genetic transformation technique mediated by Agrobacterium rhizome K599, adventitious roots were grown. PCR sequencing revealed that different base fragments of 65 bp and 72 bp were absent in the adventitious roots. The method was simple and efficient for the detection of CRISPR/Cas9 vector target site knockout in melon, realizing rapid identification of gene editing targets, and laying a foundation for studying the gene function and genetic improvement in melon.
Key words: Melon; CRISPR/Cas9 system; Agrobacterium rhizogenes; Gene knockout
甜瓜為葫蘆科甜瓜屬作物,其含有豐富的可溶性固形物和維生素等營養物質,同時也是典型的喜光、耐熱植物,是我國重要的水果型經濟作物。葉片是甜瓜進行光合作用的主要場所,葉片中的葉綠體吸收光能轉為化學能,進而積累有機物供給植物生長發育。類囊體是葉綠體細胞器中重要的片層結構,類囊體的結構、數量、大小都可能會影響葉綠體的結構,進而影響植物的光合作用[1-2]。隨著甜瓜全基因組測序工程的完成,有關甜瓜葉綠體發育相關基因的研究正在穩步進行,甜瓜葉綠體基因組中約有115個基因,且有高度保守性[3]。這些基因主要分為三大類:光合作用相關基因,葉綠體轉錄、翻譯、表達相關基因,其他蛋白質編碼基因等[4]。研究發現,在鹽脅迫下,CmCUTR1A基因的表達顯著下調,且葉綠體超微結構顯示類囊體排列不均勻、不清晰且數量減少[5]。因此,深入研究甜瓜葉綠體相關基因CmCUTR1A,為促進甜瓜有機物的生成和產量的提高奠定了研究基礎。
近年來,利用基因工程和細胞工程等技術改良園藝作物品質已取得重大進展。基因編輯技術實現了精準地對靶標基因進行定向修飾,使DNA雙鏈斷裂,并利用DNA自身的修復特性對靶標基因進行敲除、替換、插入、突變等人工修飾[6]。CRISPR/Cas9系統因具有簡單、高效、精準等優點成為當前廣泛應用到擬南芥[7]、水稻[8]、玉米[9]、大豆[10]、棉花[11]、番茄[12]等重要作物中的基因編輯系統[13]。CRISPR/Cas9系統在尋找靶位點時,可能會受到基因組中其他高度相似序列的干擾,導致在非目標位置發生切割,即脫靶效應[14-15]。
CRISPR/Cas9基因編輯系統在研究甜瓜基因功能方面非常重要,因此高效、準確地實現靶位點的切割是進行甜瓜基因功能分析的重要基礎。由于甜瓜的遺傳轉化周期較長、過程復雜繁瑣、轉化效率偏低等,利用發根農桿菌(Agrobacterium rhizogenes)[16]介導的遺傳轉化技術促使甜瓜產生不定根進行靶位點檢測是當前可以快速獲得甜瓜靶位點切割情況的方式。發根農桿菌的工作原理是利用其能力誘導植物傷口形成不定根,并通過攜帶T-DNA的Ri質粒侵入細胞,將T-DNA插入植物基因組中[17]。發根農桿菌介導的植物遺傳轉化技術已經廣泛應用于大豆、黃瓜、西瓜、甜瓜等植物中[18-21]。
甜瓜遺傳轉化過程復雜,周期較長,且CRISPR/Cas9基因編輯系統存在一定的脫靶風險。2016年,Chandrasekaran等[22]報道了利用pKSE402基因編輯載體在黃瓜中成功敲除eIF4E單個核苷酸,但轉化率不足1%;Feng等[23]利用添加了GRF/GIF生長因子基因的CRISPR/Cas9載體使得西瓜材料TC的基因編輯效率達到47.02%;2022年,Xin等[24]對甜瓜基因型、侵染時間和條件等進行優化,通過觀察GFP熒光信號的強弱獲得最優的遺傳轉化體系。因此,為了快速檢測靶位點的敲除情況,便于后續甜瓜遺傳轉化試驗的順利進行,筆者構建了甜瓜CmCUTR1A基因雙靶點基因敲除載體,并利用發根農桿菌介導甜瓜外植體產生不定根,通過不定根中GFP熒光信號的強弱進行篩選并測序,為實現甜瓜基因組編輯及基因功能的驗證奠定基礎。
1 材料與方法
1.1 材料
試驗選取的甜瓜栽培材料龍慶八號為黑龍江省農業科學院大慶分院自主選育的薄皮甜瓜品種,其具備可溶性固形物含量高、抗逆性強等優良性狀,且再生能力較強,種質資源保存在黑龍江省農業科學院大慶分院。
1.2 田間試驗設計與時間安排
2023年3月,挑選甜瓜栽培材料龍慶八號飽滿種子進行催芽、育苗,于黑龍江省安達市育種基地育苗溫室內進行。
2023年4-5月,選取長勢一致、健壯幼苗20株,定植于黑龍江省安達市育種基地,設置隨機區組,株行距30 cm×50 cm,常規肥水管理,使用地膜覆蓋,田間管理采用多蔓整枝,嚴格控制人工自交授粉,后期進行疏花疏果,每株留1~2個瓜為宜。
2023年7月,果實成熟后采收,將采收的種子涮洗、晾干后,挑選成熟、飽滿的籽粒裝袋,注明品種與采收日期,以備后續試驗使用。
1.3 分子試驗設計
1.3.1 植物材料 分子試驗材料為甜瓜栽培材料龍慶八號幼嫩葉片組織總RNA和龍慶八號成熟飽滿種子。
1.3.2 菌株材料 基因克隆所使用的載體為pMD-18T,CRISPR-Cas9基因編輯載體為pKSE402、PCBC-DT1T2,載體由黑龍江省八一農墾大學園藝學院提供。大腸桿菌(E. coli)DH5α菌株和發根農桿菌K599菌株分別購自上海唯地生物技術有限公司。
1.3.3 試驗設計 2023年5月提取幼嫩葉片總RNA,反轉錄為cDNA,設計特異性引物,采用TA克隆進行CmCUTR1A基因克隆并分析序列差異;2023年7-8月構建甜瓜CRISPR/Cas9敲除載體,并進行發根農桿菌介導的甜瓜遺傳轉化試驗。
1.4 植物總RNA的提取與cDNA的反轉錄
取甜瓜幼嫩葉片于2 mL離心管中,在液氮中速凍、研磨,迅速加入裂解液,后續操作按照植物總RNA快速抽提試劑盒(上海生工)說明書進行,利用高速微型離心機進行低溫、高速離心。
cDNA的反轉錄利用HiScript II Q Select RT SuperMix for qPCR(+gDNA wiper)進行,反轉錄后的cDNA置于-20 ℃保存,避免反復凍融。
1.5 CmCUTR1A基因的克隆及序列差異分析
參考葫蘆科基因組數據庫CuGenDB(Cucurbit Genomics Database)獲得CmCUTR1A基因參考序列,利用Primer Premier 5.0設計基因擴增引物。上游引物clone-F:ATGGCAGCCACGGCCTCCCCT,下游引物clone-R:TTATTCGGTTCCAGCAATCTTC。
在無RNA酶的200 μL離心管中添加:稀釋5倍的cDNA 2 μL、10 μmol·L-1 clone-F/R各1 μL、2 × Rapid Taq Master Mix 12.5 μL、ddH2O 8.5 μL,用瞬時離心機進行混勻。PCR擴增程序:95 ℃預變性3 min;95 ℃變性15 s,56 ℃退火15 s,72 ℃延伸20 s,35個循環數;72 ℃延伸5 min。反應后用1%瓊脂糖凝膠電泳檢測目的基因條帶,并利用DNA純化試劑盒FastPure Gel DNA Extraction Mini Kit進行切膠回收。
將目的基因與pMD-18T載體按照載體說明書進行連接,然后將反應液轉化入大腸桿菌DH5α感受態細胞中。接著,在含有50 mg·L-1氨芐青霉素的LB固體平板上倒置過夜培養于37 ℃。第2天,挑取白色飽滿的單菌落,利用預先設計的引物和PCR擴增程序進行PCR檢測,隨后將陽性菌液送至上海生工進行測序。最后,利用DNAMAN進行序列差異比對分析。
1.6 雙靶位點的選擇
本研究所選取的敲除基因為甜瓜類囊體結構蛋白關鍵基因CmCUTR1A(Gene ID:MELO3C006053.2),在使用在線靶位點設計軟件CRISPR-P2.0(http://crispr.hzau.edu.cn/CRISPR2/)進行靶位點設計時,需要根據 CRISPR/Cas9 系統的特點來識別目標序列中含有PAM序列的區域。通常情況下,為確保編輯效果,在選擇靶位點時會考慮其GC含量不低于40%。同時,為避免試驗中出現脫靶現象,會對所選的靶位點進行特異性分析。為了提高編輯效率,選擇2個靶位點進行編輯。
1.7 CRISPR/Cas9敲除載體的構建
(1)本試驗所用的CRISPR/Cas9載體為pKSE402載體(以pHSE401載體為骨架改造優化),以稀釋100倍的pCBC-DT1T2為模板進行4引物PCR擴增,引物序列見表1。DT1-BsF/DT2-BsR引物稀釋至10 μmol·L-1;DT1-F0/DT2-R0引物稀釋至5 μmol·L-1。
(2)純化回收上述PCR產物,建立如下酶切連接體系:PCR產物50 ng、10× ligase buffer 1 μL、T4 DNA ligase 0.5 μL、BsaI-HF 0.5 μL、ddH2O補足至10 μL體系。PCR擴增程序設置:37 ℃酶切2 min,16 ℃連接5 min,50個循環數;80 ℃酶失活5 min。
(3)將5 μL上述連接產物轉化入DH5α感受態細胞后,涂布于含有50 mg·L-1卡那霉素的LB固體平板上,然后在37 ℃下倒置過夜進行培養。第2天,挑選白色飽滿的單菌落,利用特異性引物U626-IDF和U629-IDR進行菌液PCR檢測。陽性菌液送往上海生工進行測序(測序引物選用特異性引物U626-IDF和U629-IDR)。
(4)從測序正確的菌液中提取重組質粒,取1 μg重組質粒利用轉化法導入100 μL發根農桿菌K599感受態中,依次進行冰浴5 min、液氮5 min、37 ℃水浴5 min、冰浴5 min,加入700 μL無抗生素的TY液體培養基;28 ℃,200 r·min-1振蕩2~3 h。涂布于含有50 mg·L-1卡那霉素和50 mg·L-1鏈霉素的TY固體平板上,28 ℃倒置培養2~3 d。挑取白色飽滿單菌落,利用特異性引物U626-IDF和U629-IDR進行PCR檢測陽性菌液。
1.8 發根農桿菌介導的甜瓜遺傳轉化
(1)從成熟甜瓜種子中,選取籽粒飽滿、大小均勻、平整的龍慶八號甜瓜種子進行試驗,將其浸泡在55 ℃溫水中處理2 h,去除種皮。接下來,在HDL潔凈工作臺(北京東聯哈爾儀器制造有限公司)中進行以下操作:用75%酒精消毒30 s,然后用無菌水沖洗3次,隨后用10% NaClO消毒10 min,最后再用無菌水沖洗5次。將處理后的種子放置于含有8%瓊脂的培養基中,每個培養皿30~40粒種子。將培養皿置于28 ℃連續黑暗條件下培養2 d,直至甜瓜種子萌發。
(2)選取萌發飽滿的甜瓜種子,將下胚軸切掉并刮去生長點子葉一分為二,切去上半部分,便于發根農桿菌的侵染。
(3)將PCR檢驗正確的菌液接種于50 mL離心管中繼續培養(10 mL TY液體+50 mg·L-1卡那霉素和50 mg·L-1鏈霉素),待菌液濃度達到OD600約0.6時,4000 r·min-1離心,用滅菌的MS液體重懸菌體,調節重懸液濃度OD600約0.2。將切好的甜瓜子葉節置于20 mL注射器中,吸取10 mL菌液抽真空2 min后,取出晾干,平鋪于覆有一層濾紙的MS固體培養基(MS+3.0%蔗糖+NAA α-萘乙酸 0.5 mg·L-1)中,25 ℃暗培養2 d。
(4)2 d后將暗培養的子葉節取出,用無菌水沖洗干凈并晾干后,置于MS固體培養基(MS+3.0%蔗糖+NAA α-萘乙酸 0.5 mg·L-1+特美汀200 mg·L-1)上,26 ℃、光16 h/暗8 h培養,約2周左右觀察生根情況。
1.9 甜瓜不定根靶位點的檢測
利用CTAB法提取不定根組織的DNA[25],根據靶位點的位置及理論敲除長度在靶點前后設計特異性引物CmCUTR1A-F和CmCUTR1A-R,并進行PCR擴增驗證。對1%瓊脂糖凝膠電泳目的片段條帶正確的PCR產物進行膠回收,并送往生工生物工程有限公司測序,檢測分析靶位點的編輯情況。
2 結果與分析
2.1 CmCUTR1A基因序列差異分析
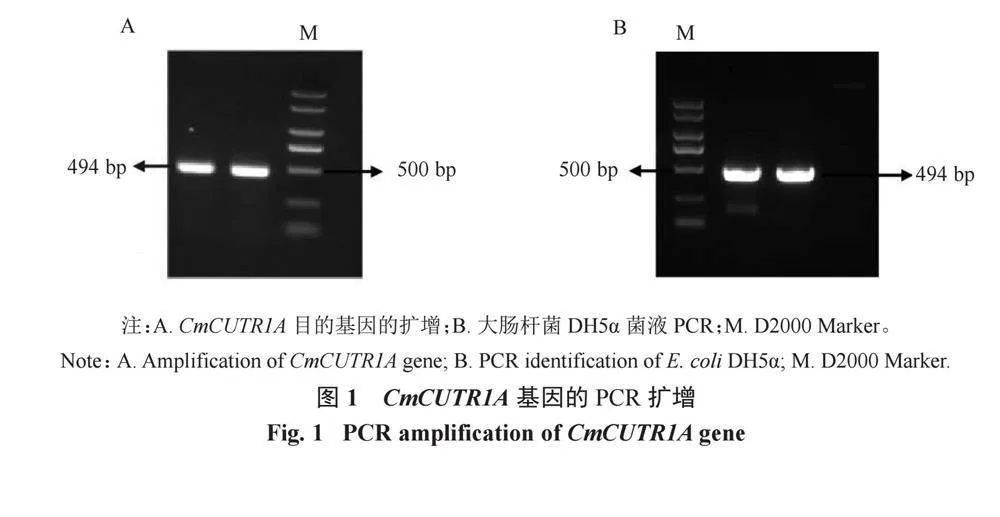
取龍慶八號甜瓜栽培材料幼嫩葉片,提取葉片組織的總RNA,后反轉錄為cDNA。以CmCUTR1A基因的特異性引物(表2)進行PCR擴增,1%瓊脂糖凝膠電泳顯示該目的基因片段長度為494 bp(圖1-A),將PCR擴增產物進行膠回收后連接克隆載體并轉入大腸桿菌感受態細胞,進行菌液PCR鑒定,條帶約為494 bp(圖1-B),將陽性菌液進行測序,測序結果經DNAMAN進行序列比對,發現龍慶八號與葫蘆科甜瓜參考基因組數據庫中MELO3C006053.2基因相比無突變產生(圖2),故可以用龍慶八號甜瓜品種進行發根農桿菌的侵染及后續試驗。
2.2 雙靶位點載體的構建
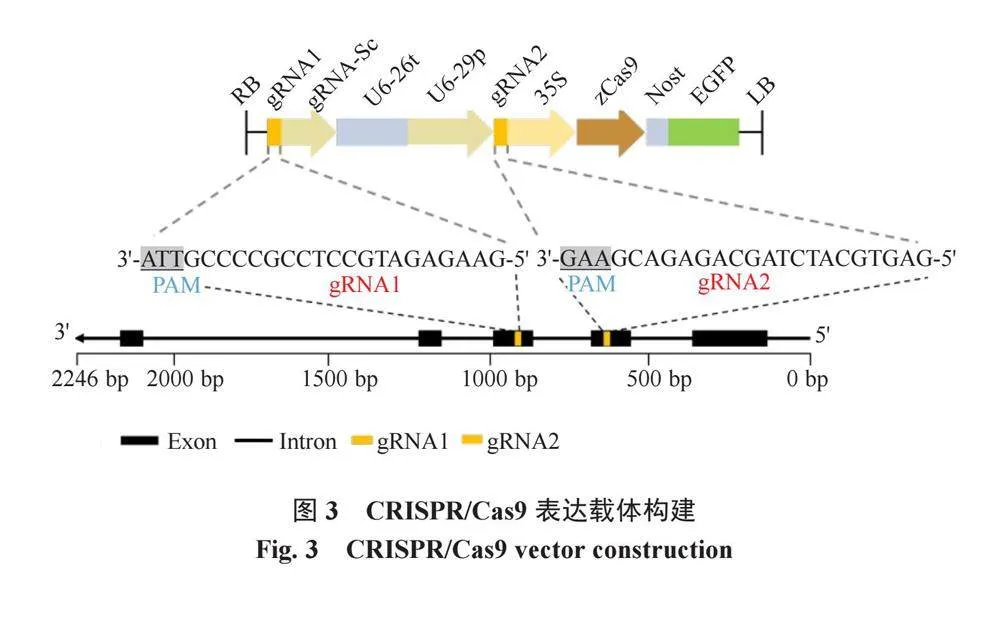
根據CRISPR-P2.0在線工具設計了雙靶位點,分別位于第2外顯子和第3外顯子上。以PCBC-DT1T2載體為中間模板進行四引物擴增,擴增雙靶點基因敲除所需要的作用元件sgRNA與兩個靶位點 gRNA1、gRNA2,利用CRISPR/Cas9系統重組載體構建示意圖(圖3)。
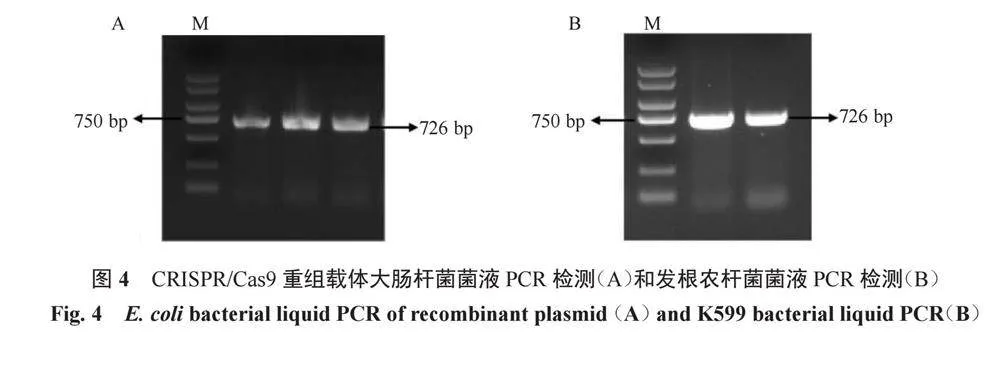
PCR擴增得到的中間產物,利用T4連接酶連接到pKSE402載體上,并轉入大腸桿菌感受態細胞中以特異性引物U626-IDF和U629-IDR進行菌液PCR以驗證陽性菌液,PCR檢測特異性條帶大小在1%瓊脂糖凝膠檢測下應為726 bp(圖4-A),測序結果顯示所添加的作用元件sgRNA和2個靶位點的序列均正確無誤(圖5)。以上結果表明,CRISPR/Cas9敲除載體已經構建成功。提取測序成功菌液中的重組質粒并轉入發根農桿菌K599感受態細胞中,輕挑取白色單克隆菌落并進行陽性菌液PCR檢測,經1%瓊脂糖凝膠電泳檢測片段長為726 bp(圖4-B),證明該重組質粒已成功轉入發根農桿菌中,可以用于后續侵染試驗。
2.3 發根農桿菌介導的甜瓜轉化技術檢測靶位點的可行性
通過發根農桿菌K599介導的甜瓜轉化體系對CRISPR/Cas9表達載體靶位點的可行性進行驗證,龍慶八號種子萌發后(圖6-A),將切好的甜瓜子葉節放入20 mL無菌注射器中添加10 mL菌液并進行抽真空5 min,25 ℃暗培養3 d(圖6-B),用無菌水脫菌后,將子葉節表面晾干后放置于生根篩選的MS培養基上進行光照培養。在含有NAA的MS培養基上進行不定根的培養約7 d后能觀察到不定根的伸長(圖6-C),利用路陽365L熒光檢測燈能觀察到明顯的綠色熒光信號(圖6-D)。
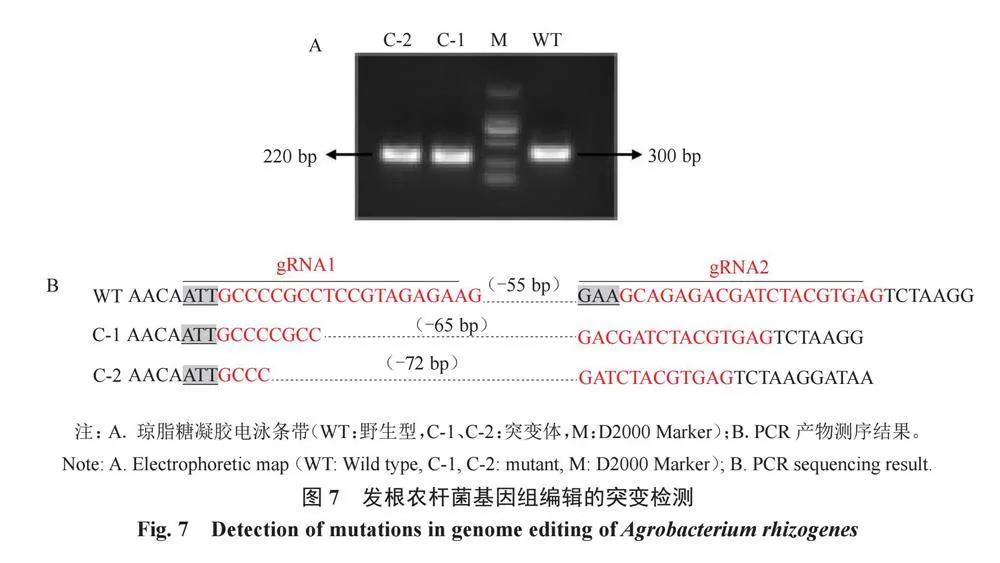
待培養至20 d后提取甜瓜不定根組織的DNA,根據雙靶位點在CmCUTR1A基因上的位置,在雙靶位點附近設計了特異性引物CmCUTR1A-F和CmCUTR1A-R,利用該引物對DNA進行PCR擴增,采用1%瓊脂糖凝膠電泳對目的片段進行檢驗,結果發現未經敲除的WT條帶大小約300 bp,編輯后的不定根產生的條帶經電泳后大小約220 bp(圖7-A),將目的片段進行回收純化并送往上海生工生物工程有限公司進行測序。利用GFP熒光信號篩選不定根,共進行PCR測序檢測產生不定根的外植體16個,測序結果顯示,經基因敲除后的不定根組織的DNA中存在兩種獨立的不同堿基的缺失,在C-1、C-2的測序結果中顯示均從第1個PAM序列進行識別,并敲除至第2個PAM序列產生,但DNA在雙鏈斷裂的過程中會產生堿基互補配對進而進行DNA的修復。由于重新修復補充上的堿基數量不等,導致敲除片段存在長度上的差異。C-1的測序結果顯示缺失65 bp,C-2顯示缺失72 bp(圖7-B)。經計算,產生GFP熒光信號的外植體16個,測序獲得的獨立編輯事件為2個,初步估算本研究中以pKSE402載體和甜瓜栽培品種龍慶八號為受體材料的基因編輯效率為12.5%。結果表明,該方法成功實現了在甜瓜不定根中的基因編輯,發生了堿基的缺失,說明該基因編輯載體具有基因編輯的功能,可用于甜瓜材料龍慶八號的穩定遺傳轉化試驗。
3 討論與結論
甜瓜的光合作用是通過葉綠體進行的,而葉綠體中的類囊體結構可能直接或間接地影響甜瓜葉片光合速率。筆者之前在甜瓜的研究中發現了一個基因CmCUTR1A[5],該基因可能控制著甜瓜中類囊體的結構。基于這一發現進行了后續試驗以進一步探究其基因結構與功能。
由于甜瓜基因型的不同會導致甜瓜在遺傳轉化過程中所用激素濃度不同[26],筆者選擇了具有較強再生能力的龍慶八號甜瓜材料作為研究對象。隨著基因編輯技術的廣泛應用,提高植物基因編輯效率并實現精準靶向基因敲除位點越來越受到重視。傳統育種方法中的物理和化學誘變產生新突變體具有隨機性[27],需要進行大規模操作,從而導致巨大的工作量。然而,CRISPR/Cas9系統的引入解決了這一生產技術上的難題,通過構建確定的雙靶位點等載體,CRISPR/Cas9系統能夠高效、精準靶向編輯相關基因,實現基因的精準定點突變,這一技術為基因功能的研究及新品種選育提供了新的策略。
CRISPR/Cas9系統在甜瓜上的應用已經逐漸擴大。從2019年至今,通過基因編輯技術已經獲得了大多數甜瓜基因的功能信息如CmPDS[28]、CmROS1[29]、CmeIF4E[30]等。與此同時,甜瓜遺傳轉化體系也在逐步優化[24],使得甜瓜品種的基因優化改良不再成為困難。然而,甜瓜的基因編輯進程仍然較為緩慢,并且常常存在一定程度的脫靶風險。為了解決這個問題,一種利用發根農桿菌介導的方法被提出來檢測靶位點編輯情況。通過評估載體的可利用性,可以有效地進行后續的基因功能驗證工作。通過構建雙靶位點CRISPR/Cas9基因敲除系統,并利用發根農桿菌K599誘導甜瓜不定根的生成,筆者成功地獲得了敲除突變體,這一方法已被證明是有效的。此外,一些研究表明,在煙草、蒲公英等植物中,利用發根農桿菌誘導產生的不定根[31-32],可以經過脫分化和再分化的過程培育成完整的轉基因植株。在南瓜中也成功地通過誘導不定根形成了愈傷組織[33],為培育出完整的轉基因植株提供了新途徑。這些研究結果為甜瓜不定根的脫分化和再生提供了新的方向。
本研究結果表明,經基因克隆比對,龍慶八號甜瓜栽培材料中類囊體結構蛋白CmCUTR1A基因與甜瓜參考基因組該基因序列無突變差異;構建了CmCUTR1A基因雙靶點CRISPR/Cas9載體,并經發根農桿菌介導使甜瓜子葉節產生不定根,且經檢測不定根中存在多種片段缺失,證明此CRISPR/Cas9載體具有一定的基因敲除功能,為后續進行甜瓜遺傳轉化試驗奠定了基礎。
參考文獻
[1] 徐振彪,宋林霞.葉綠體的遺傳工程應用研究[J].安徽農業科學,2007,35(23):7085-7087.
[2] 周云龍.載色體與葉綠體的區別和聯系[J].生物學教學,2014,39(6):39-40.
[3] RODRIGUEZ-MORENO L,GONZALEZ V M,BENJAK A,et al.Determination of the melon chloroplast and mitochondrial genome sequences reveals that the largest reported mitochondrial genome in plants contains a significant amount of DNA having a nuclear origin[J].BMC Genomics,2011,12:424.
[4] 朱強龍,朱子成,王鵬飛,等.葫蘆科作物線粒體和葉綠體基因組研究進展[J].中國瓜菜,2016,29(8):1-8.
[5] LIU T,AMANULLAH S,XU H C,et al.RNA-Seq identified putative genes conferring photosynthesis and root development of melon under salt stress[J].Genes,2023,14(9):1728.
[6] 方銳,暢飛,孫照霖,等.CRISPR/Cas9介導的基因組定點編輯技術[J].生物化學與生物物理進展,2013,40(8):691-702.
[7] 瞿禮嘉,郭冬姝,張金喆,等.CRISPR/Cas系統在植物基因組編輯中的應用[J].生命科學,2015,27(1):64-70.
[8] WANG F J,WANG C L,LIU P Q,et al.Enhanced rice blast resistance by CRISPR/Cas9-targeted mutagenesis of the ERF transcription factor gene OsERF922[J].PLOS ONE,2016,11(4):e0154027.
[9] FENG C,YUAN J,WANG R,et al.Efficient targeted genome modification in maize using CRISPR/Cas9 system[J].Journal of Genetics and Genomics,2016,43(1):37-43.
[10] CAI Y P,CHEN L,LIU X J,et al.CRISPR/Cas9-mediated targeted mutagenesis of GmFT2a delays flowering time in soya bean[J].Plant Biotechnology Journal,2018,16(1):176-185.
[11] WANG P C,ZHANG J,SUN L,et al.High efficient multisites genome editing in allotetraploid cotton(Gossypium hirsutum)using CRISPR/Cas9 system[J].Plant Biotechnology Journal,2018,16(1):137-150.
[12] BEMER M,KARLOVA R,BALLESTER A R,et al.The tomato FRUITFULL homologs TDR4/FUL1 and MBP7/FUL2 regulate ethylene-independent aspects of fruit ripening[J].Plant Cell,2012,24(11):4437-4451.
[13] BHATTA B P,MALLA S.Improving horticultural crops via CRISPR/Cas9:current successes and prospects[J].Plants-Basel,2020,9(10):1360.
[14] TSAI S Q,ZHENG Z,NGUYEN N T,et al.GUIDE-seq enables genome-wide profiling of off-target cleavage by CRISPR-Cas nucleases[J].Nature Biotechnology,2015,33(2):187-197.
[15] GANTZ V M,BIER E.The mutagenic chain reaction:A method for converting heterozygous to homozygous mutations[J].Science,2015,348(6233):442-444.
[16] SMITH E F,TOWNSEND C O.A plant-tumor of bacterial origin[J].Science,1907,25(643):671-673.
[17] CHILTON M D,DRUMMOND M H,MERIO D J,et al.Stable incorporation of plasmid DNA into higher plant cells:The molecular basis of crown gall tumorigenesis[J].Cell,1977,11(2):263-271.
[18] JACOBS T B,LAFAYETTE P R,SCHMITZ R J,et al.Targeted genome modifications in soybean with CRISPR/Cas9[J].BMC Biotechnology,2015,15:16.
[19] WANG X T,JIN B Y,YAN W J,et al.Cucumber abscisic acid 8`-hydroxylase Csyf2 regulates yellow flesh by modulating carotenoid biosynthesis[J].Plant Physiology,2023,193(2):1001-1015.
[20] 張月喬,葛潔,田樹娟,等.利用發根農桿菌體系檢測西瓜CRISPR/Cas9系統的靶位點[J].中國瓜菜,2020,33(4):7-11.
[21] 王平勇,徐永陽,趙光偉,等.發根農桿菌介導甜瓜轉基因過表達體系的建立[J].中國瓜菜,2019,32(12):15-18.
[22] CHANDRASEKARAN J,BRUMIN M,WOLF D,et al.Development of broad virus resistance in nontransgenic cucumber using CRISPR/Cas9 technology[J].Molecular Plant Pathology,2016,17(7):1140-1153.
[23] FENG Q,XIAO L,HE Y,et al.Highly efficient genotype-independent transformation and gene editing in watermelon (Citrullus lanatus) using a chimeric ClGRF4-GIF1 gene[J].Journal of Integrative Plant Biology,2021,63(12):2038-2042.
[24] XIN T,TIAN H,MA Y,et al.Targeted creating new mutants with compact plant architecture using CRISPR/Cas9 genome editing by an optimized genetic transformation procedure in cucurbit plants[J].Horticulture Research,2022,9:uhab086.DOI:10.1093/hr/uhab086.
[25] 王懷松,賀超興,張志斌,等.甜瓜白粉病抗性AFLP連鎖標記的初步研究[J].中國瓜菜,2009,22(2):4-6.
[26] 祁宏英,徐洪國,王秀文,等.甜瓜再生體系的建立[J].中國瓜菜,2021,34(5):105-108.
[27] COLBERT T,TILL B J,TOMPA R.High-throughput screening for induced point mutations[J].Plant Physiology,2001,126(2):480-484.
[28] HOOGHVORST I,LOPEZ C,NOGUES S.Efficient knockout of phytoene desaturase gene using CRISPR/Cas9 in melon[J].Scientific Reports,2019,9:17077.
[29] GIORDANO A,SANTO D M,QUADRANA L,et al.CRISPR/Cas9 gene editing uncovers the roles of constitutive triple response 1 and repressor of silencing 1 in melon fruit ripening and epigenetic regulation[J].Journal of Experimental Botany,2022,73(12):4022-4033.
[30] PARSA H S,SABET M S,MOIENI A,et al.CRISPR/Cas9-mediated cytosine base editing using an improved transformation procedure in melon (Cucumis melo L.)[J].International Journal of Molecular Sciences,2023,24(13):11189.
[31] ALTAMURA M M,ARCHILLETTI T,CAPONE I,et al.Histological analysis of the expression of Agrobacterium rhizogenes rolB-GUS gene fusions in transgenic tobacco[J].New Phytologist,1991,118(1):69-78.
[32] LEE M H,YOON E S,JEONG J H,et al.Agrobacterium rhizogenes-mediated transformation of Taraxacum platycarpum and changes of morphological characters[J].Plant Cell Reports,2004,22(11):822-827.
[33] BALEN B,LELJAK-LEVANIC D,MIHAIJEVI? S,et al.Formation of embryogenic callus in hairy roots of pumpkin(Cucurbita pepo L.)[J].In Vitro Cellular and Developmental Biology Plant,2004,40(2):182-187.

