化合物A34對糖尿病小鼠的降糖作用及機制探討



摘 要:為研究一種新型可溶性環氧化物水解酶(soluble epoxide hydrolase,sEH)抑制劑(A34)對糖尿病小鼠的降糖作用,探討其作用機制,連續5天給小鼠腹腔注射鏈脲佐菌素(streptozotocin,STZ,50 mg/(kg·d),誘導1型糖尿病(type 1 diabetes mellitus,T1DM)小鼠模型。通過飲水給藥,考察A34對糖尿病小鼠飲水攝食量、非禁食血糖、空腹血糖、葡萄糖耐量和血漿胰島素水平的影響,研究A34的降糖作用;通過研究胰島中sEH表達水平、胰島形態變化及血漿中細胞因子干擾素-γ(INF-γ)和白介素-4(IL-4)的含量,分析A34降糖的作用機制。結果表明:與模型組相比,A34有效改善了糖尿病小鼠多飲、多食癥狀及葡萄糖耐量情況(p<0.01),降低了空腹血糖和非禁食血糖(p<0.01),提高了血漿胰島素水平(p<0.05);小鼠胰島中sEH表達量降低(p<0.01),胰島受損減輕,血漿中IFN-γ與IL-4含量比值降低(p<0.05)。A34可能通過調控促炎和抗炎細胞因子的動態平衡,保護胰島β細胞免受損傷,從而改善小鼠胰島β細胞功能,發揮降糖作用。
關鍵詞:藥物化學;可溶性環氧化物水解酶;1型糖尿病;葡萄糖耐量;胰島β細胞;細胞因子
中圖分類號:TQ463;R914.4
文獻標識碼:A
DOI:10.7535/hbkd.2024yx05003
Anti-diabetic effect and mechanism of compound A34 in diabetic mice
SUN Yanping ZHANG Xueyu TIAN Ye3,CHEN Meng DOU Shanshan LI Shuo
ZHANG Huimin SONG Huijia ZHAO Yanfang3,GAO Zibin1,2
(1.School of Chemical and Pharmaceutical Engineering,Hebei University of Science and Technology,
Shijiazhuang,Hebei 050018, China;
2.Hebei Province Key Laboratory of Molecular Chemistry for Drug, Shijiazhuang,Hebei 050018, China;
3.School of Pharmaceutical Engineering,Shenyang Pharmaceutical University, Shenyang,Liaoning 110016, China)
Abstract: In order to detemine the anti-diabetic effect and potential mechanism of a novel soluble epoxide hydrolas inhibitor (A34) on diabetic mice. Type 1 diabetes mellitus (T1DM) mice were induced by streptozotocin (50 mg/(kg·d) for 5 days, ip)and the hypoglycemic effect of A34 were evaluated by water and food intake, non-fasting and fasting blood glucose, glucose tolerance and plasma insulin level in diabetic mice after water administration.The underlying mechanism was explored via measuring the expression level of sEH in islets, the morphological change of islets and the concerntration of cytokines INF-γ and IL-4 in plasma. Compared with diabetic model group, the water and food intake(p<001, p<005), blood glucose (p<001), glucose tolerance (p<001) and plasma insulin level (p<005 ) were improved in A34 group. Additionally, A34 could protect pancreatic islet morphology, suppress sEH expression in islet (p<001), reduce the ratio of INF-γ to IL-4 in plasma(p<005 ). These results showed that A34 prevents hyperglycemia and β-cell dysfunction through regulating the dynamic balance of pro-inflammatory and anti-inflammatory cytokines in diabetic mice.
Keywords:medicinal chemistry;soluble epoxide hydolase;type 1 diabetes mellitus;glucose tolerance;islet β cell;cytokines
可溶性環氧化物水解酶(soluble epoxide hydrolase,sEH)是一種以環氧脂肪酸為底物的酶,能夠將多不飽和脂肪酸的CYP450酶活性代謝產物——環氧脂肪酸水解成活性較低的二羥基脂肪酸[1]。環氧脂肪酸具有抗炎、抗氧化作用,在預防和治療代謝性疾病和神經系統疾病中發揮著重要作用[2-3]。sEH在人體廣泛分布,通過抑制sEH活性可以減少環氧脂肪酸的降解,起到治療疾病的作用。近年來,多個sEH的小分子抑制劑被設計合成出來,并在多種疾病模型中表現出良好的治療效果[4-5]。研究表明,患糖尿病時sEH在胰島[6]、心臟[7]、視網膜[8]、肝臟[9]、腦血管[10]等的表達和活性升高,使用sEH抑制劑或基因敲除能夠緩解高血糖癥狀,提高對胰島素的敏感性,預防和治療糖尿病及其并發癥[11-12]。sEH的抑制劑GSK2256294已完成Ⅱ期臨床研究,肥胖患者用藥后可抑制其體內sEH活性,降低氧化應激[13]。
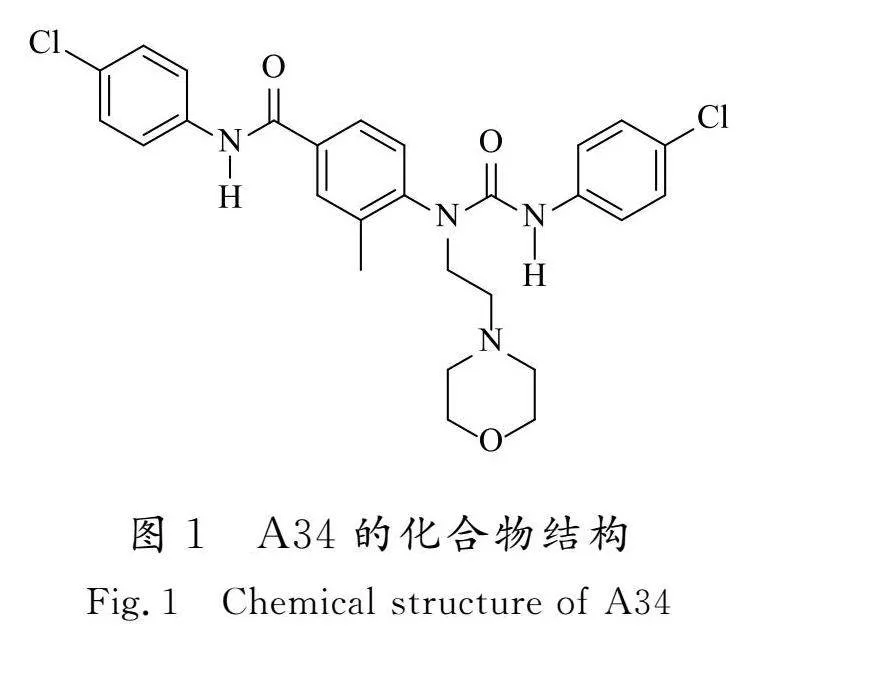
1型糖尿病(type 1 diabetes mellitus,T1DM)的發病與自身免疫缺陷相關,β細胞的自身免疫性破壞導致胰島素分泌不足,血糖升高[14]。盡管sEH抑制劑能夠通過多種作用途徑發揮降血糖的作用[15-17],但其對T1DM中自身免疫反應的影響尚不明確。化合物N-(4-氯苯基)-4-(3-(4-氯苯基)-1-(2-嗎啉代乙基)脲基)-3-甲基苯甲酰胺(A34)是本研究團隊設計合成的新型sEH抑制劑,其結構見圖1。
A34在體外具有良好的sEH抑制活性(IC50為0.04 nmol),在體內也表現出良好的抗炎活性[18]。目前,國內外尚無sEH抑制劑類藥物上市。本文通過考察A34對T1DM的治療作用,初步探討其對免疫平衡的影響,為sEH抑制劑的研發提供實驗依據,為糖尿病的治療提供新的思路。
1 實驗材料
1.1 主要藥品及試劑
A34,由沈陽藥科大學合成;鏈脲佐菌素,STZ,Sigma公司提供;超敏小鼠胰島素試劑盒,易致生物科技有限公司提供;HE染色試劑盒,Sigma公司提供;干擾素-γ(INF-γ)、白介素-4(IL-4)檢測試劑盒,南京建成生物工程研究所提供;兔SP試劑盒、DAB顯色試劑盒,北京中杉金橋生物技術有限公司提供;Tris-EDTA抗原修復液、EPHX2兔多克隆抗體,Proteintech中國公司提供。
1.2 主要儀器
酶標儀,美國伯騰(BioTek)儀器有限公司提供;血糖測試儀,羅氏診斷產品有限公司提供;組織病理切片機,金華市華速科技有限公司提供;快速混勻器,常州博遠實驗分析儀器廠提供;生物顯微鏡,徠卡公司提供;電子天平,型號AL204、XP205,梅特勒-托利多儀器(上海)有限公司提供;高速冷凍離心機,安徽中科中佳科學儀器有限公司提供。
1.3 實驗動物
SPF級雄性Balb/c小鼠(6~8周,體質量18~20 g),購自河北伊維沃生物科技有限公司,合格證編號為SCXK(冀)2020-002。將小鼠于室溫(22 ± 2)℃、相對濕度55%±5%,以及12 h/12 h明暗交替環境下飼養。
2 實驗方法
2.1 動物分組、造模及給藥
將小鼠適應性喂養1周后,隨機分為3組,正常對照組(Con組)、模型組(Mod組)和給藥組(A34組)[19],其中正常對照組6只,模型組和給藥組均12只,每籠6只進行喂養。模型組和給藥組連續5 d按50 mg/kg劑量腹腔注射STZ的檸檬酸緩沖溶液(0.1 mol/L,pH值為4.5)進行造模;正常對照組注射同等劑量的檸檬酸鹽緩沖液。實驗期間,正常對照組飲用蒸餾水,模型組飲用2.5%羥丙基-β-環糊精水溶液,給藥組造模前2天開始飲用2.5%羥丙基-β-環糊精增溶的質量濃度為0.025 mg/mL的A34水溶液,直至6周實驗結束。
2.2 動物實驗方案
每周測定小鼠飲水攝食量、非禁食血糖及空腹血糖;分別于造模第4周和第6周進行葡萄糖耐量實驗;第6周糖耐量實驗結束后第2天,采血分離小鼠血漿,測定血漿中胰島素、INF-γ和IL-4含量,將小鼠胰腺組織制成石蠟切片,HE染色觀察胰腺病理形態,通過免疫組織化學染色檢測胰腺組織中sEH表達情況。
2.3 血糖檢測
每周一上午9:00,對小鼠尾靜脈采血,采用血糖測定儀測定小鼠非禁食血糖,隨后禁食6 h(自由飲水),于下午15:00測定空腹血糖。
2.4 腹腔注射葡萄糖耐量實驗(IPGTT)
將小鼠禁食6 h(9:00~15:00,自由飲水),測定空腹血糖,記為0 min血糖值,隨后根據小鼠體質量按
1 g/kg劑量腹腔注射葡萄糖液,分別于糖負荷后的15、30、60、120 min尾靜脈采血,測定血糖值,并計算時間血糖值曲線下面積AUC(min·mmol/L):
AUC=15×(BG0+BG15)/2+15×(BG15+BG30)/2+30×(BG30+BG60)/2+
60×(BG60+BG120)/2 。 (1)
式中:BG0、BG15、BG30、BG60、BG120分別代表0、15、30、60、120 min的血糖值。
2.5 血漿樣品制備
從小鼠眼球取血,放入EDTA-K2抗凝管中,于室溫、4 000 r/min條件下離心15 min,分離血漿,分裝后于-20 ℃保存。
2.6 胰腺石蠟切片制備
采用頸椎脫臼方法,從小鼠腹腔剪取胰尾部分組織,用生理鹽水沖洗干凈后,置于4%多聚甲醛固定液中,于4 ℃條件固定24 h,用流水沖洗后,常規石蠟包埋,5 μm切片。
2.7 ELISA實驗
參照各檢測試劑盒說明書,檢測各組小鼠血漿樣品中胰島素、IFN-γ和IL-4的含量。
2.8 HE染色
參照HE染色試劑盒說明書,石蠟切片脫臘水化后,用蘇木素染色5 min,分化液分化30 s,用自來水沖洗2 min,伊紅染色10 s,脫水透明封片,在生物顯微鏡下觀察獲得的圖像。
2.9 免疫組織化學檢測
參照兔SP試劑盒說明書,石蠟切片脫臘水化后,進行常規抗原修復、阻斷、封閉操作。每個樣本滴加適量稀釋后的一抗,于37 ℃孵育1 h,PBS沖洗20 min,滴加生物素標記山羊抗兔lgG,室溫孵育13 min,PBS沖洗20 min,再滴加辣根酶標記鏈酶卵白素工作液,室溫孵育13 min,PBS沖洗20 min,DAB顯色,蘇木素復染細胞核,脫水封片,顯微鏡下觀察采集的圖像。采用Image-Pro Plus軟件分析免疫組化圖像,根據積分光密度(IOD)計算染色強度。
2.10 統計學處理
數據以均數±標準差(x±s)表示,采用SPSS統計軟件進行數據處理。2組比較采用t檢驗,多組比較采用單因素方差分析(one-way ANOVA),兩兩比較分析采用Bonferroni法。假設檢驗水準按α=0.05判定,p<0.05為差異有統計學意義。
3 實驗結果
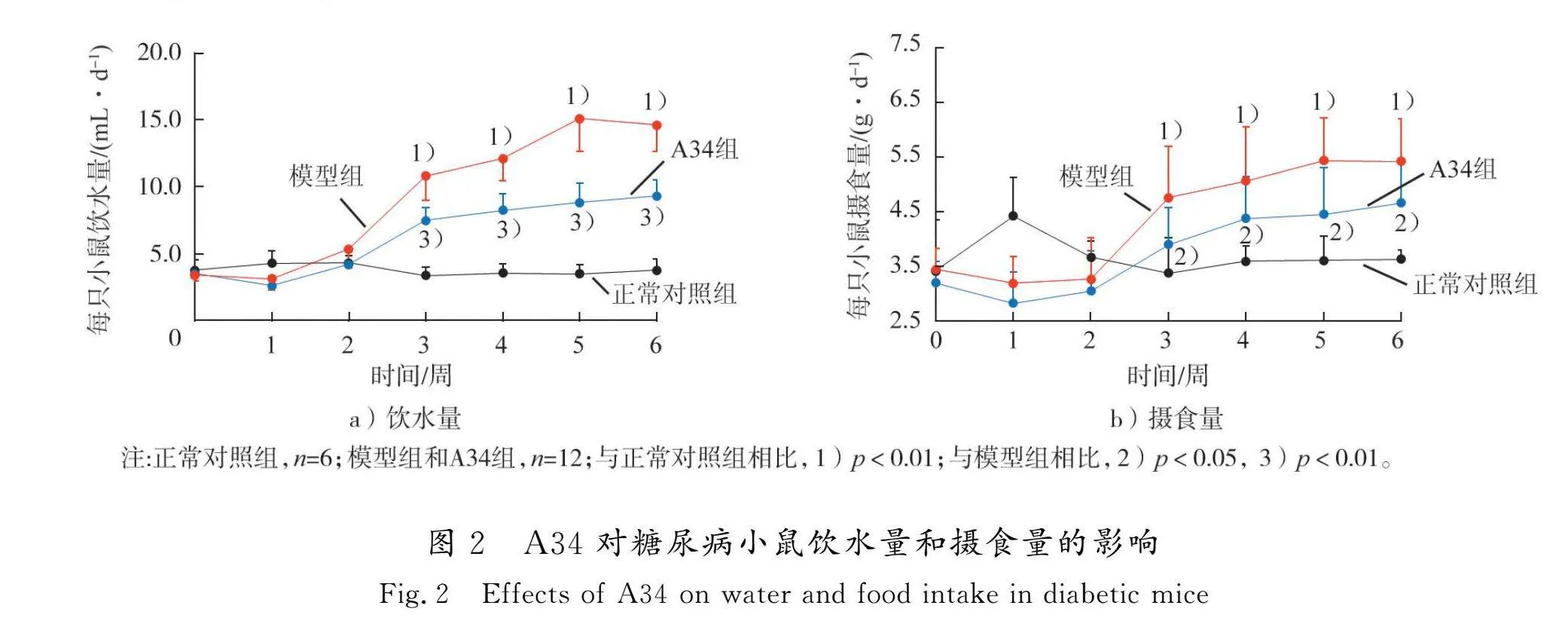
3.1 A34對糖尿病小鼠飲食量的影響
在整個實驗周期內,正常對照組小鼠飲水量和攝食量維持在初始水平;造模3周后,與正常對照組相比,模型組小鼠飲水量和攝食量逐漸增加(p<0.01);與模型組相比,給予A34干預后,糖尿病小鼠飲水量和攝食量均降低(p<0.01,p<0.05),表明A34改善了糖尿病小鼠“多飲多食”的癥狀。結果見圖2。
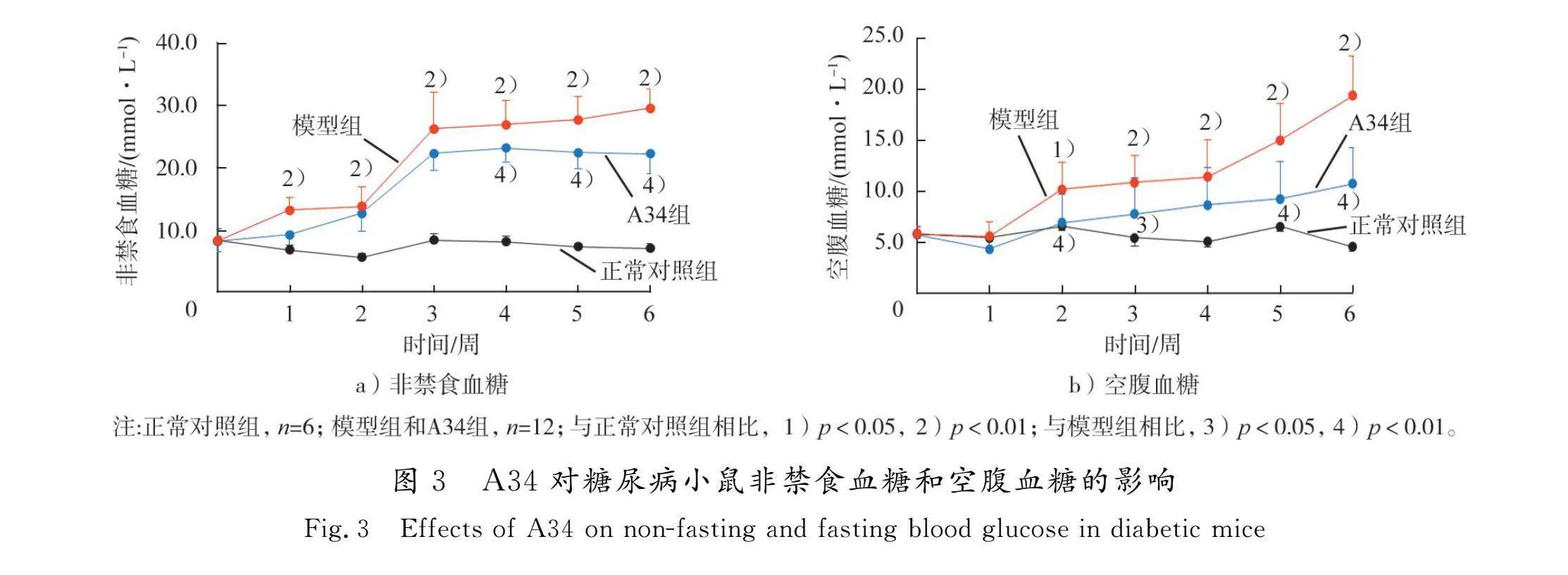
3.2 A34對糖尿病小鼠血糖的影響
如圖3所示,實驗期間,正常對照組小鼠非禁食血糖和空腹血糖保持平穩。模型組小鼠非禁食血糖和空腹血糖均隨造模時間延長逐漸升高,并分別于造模1周、2周后明顯高于正常對照組(p<0.01,p<0.05);A34組非禁食血糖和空腹血糖隨造模時間延長亦有升高趨勢,但升高程度低于模型組,分別于造模4周、2周后顯著低于模型組(p<0.01)。結果表明,A34能夠緩解糖尿病小鼠的非禁食血糖和空腹血糖的升高,具有降糖作用。
3.3 A34對糖尿病小鼠葡萄糖耐量的改善作用
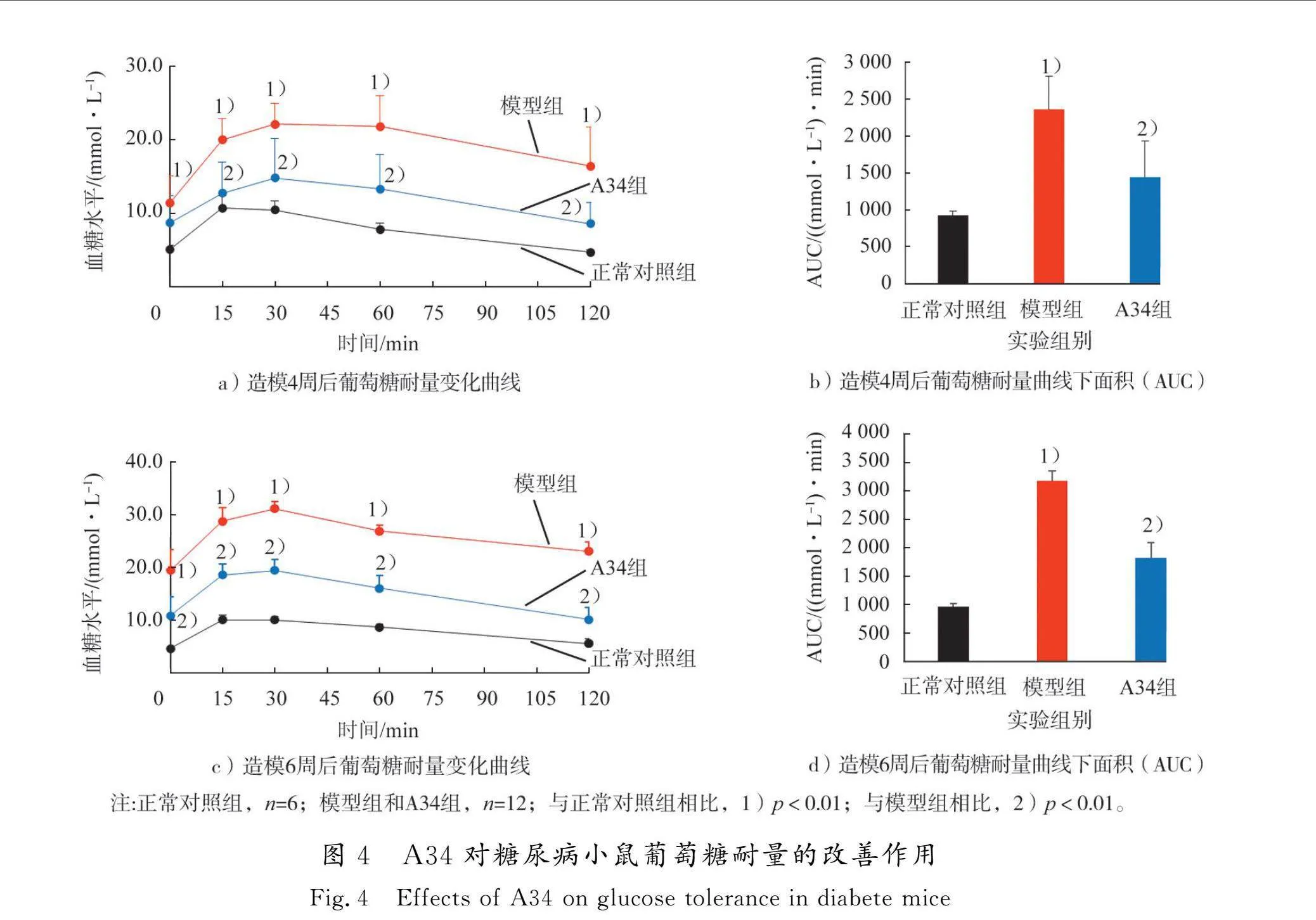
葡萄糖耐量實驗是評價機體葡萄糖代謝能力的經典方法。分別于小鼠造模4周和6周時進行葡萄糖耐量實驗,結果見圖4。給予葡萄糖后,正常對照組小鼠血糖15 min達到峰值并于120 min時恢復至初始水平;模型組小鼠血糖30 min到達峰值,120 min時未恢復至初始水平;A34組小鼠血糖30 min達到峰值并于120 min時恢復至初始水平;與模型組相比,A34組注射葡萄糖后,血糖值與血糖曲線下面積均明顯低于模型組(p<0.01)。結果表明:正常對照組小鼠胰島功能良好,給予葡萄糖后,能迅速釋放胰島素調節血糖的穩態;模型組小鼠胰島功能明顯受損,胰島素分泌延遲且不足。A34能夠減輕STZ誘導的胰島損傷,改善糖尿病小鼠對葡萄糖的調控能力,保護胰島功能。
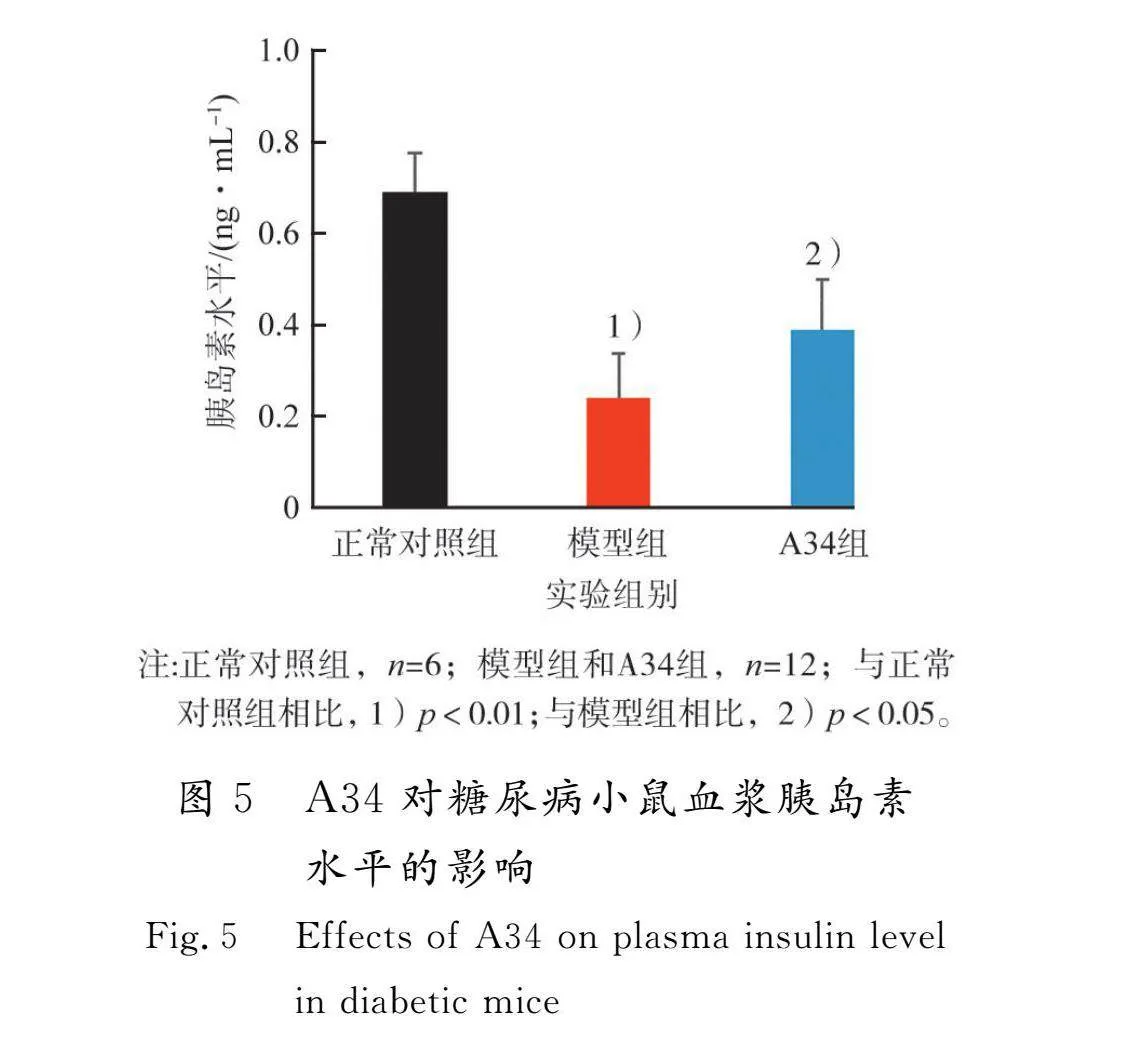
3.4 A34對糖尿病小鼠血漿胰島素水平的影響
采用ELISA法測定血漿胰島素含量,結果如圖5所示。
由圖5可知:正常對照組小鼠血漿胰島素含量維持在較高水平((0.69±0.20)ng/mL),STZ能夠破壞胰島細胞,影響胰島素分泌功能,導致模型組血漿胰島素水平顯著降低((0.24±0.10)ng/mL)(p<0.01);A34干預后,緩解了STZ造成的胰島素缺乏((0.39±0.11)ng/mL)(p<0.05),保護了胰島細胞功能。
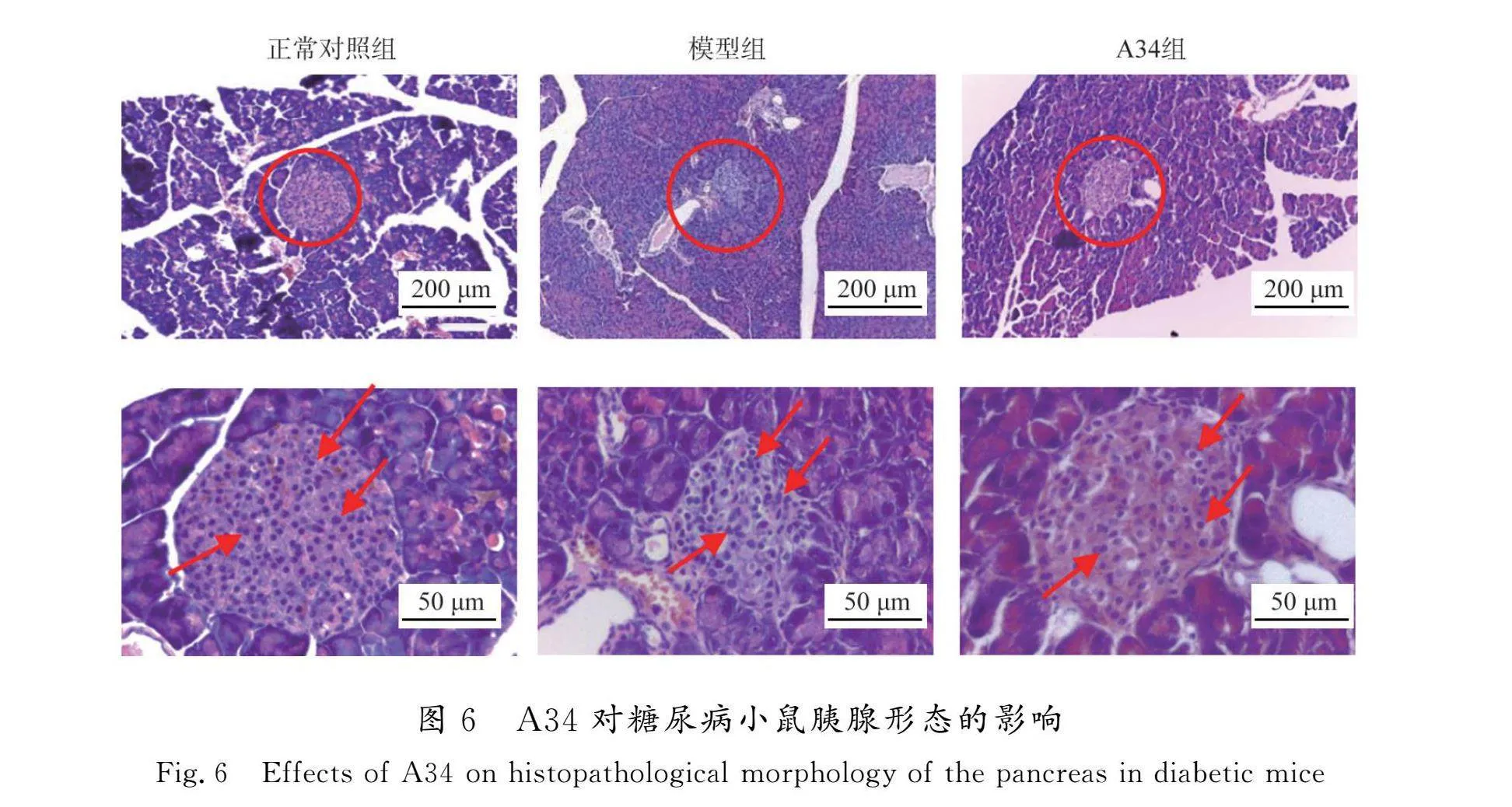
3.5 A34對糖尿病小鼠胰島形態的影響
HE染色結果如圖6所示。
由圖6可以看出:正常對照組小鼠的胰島呈橢圓形,結構完整、邊緣清晰,胰島內β細胞大小均勻、飽滿充盈、排列緊密;模型組小鼠的胰島萎縮變形,邊緣不清,結構紊亂,胰島內β細胞腫脹、變形;與模型組相比,A34組小鼠胰島形態結構較完整,β細胞腫脹、變形情況減輕。結果表明,A34能夠緩解STZ誘導的胰島萎縮變形和β細胞腫脹情況。
3.6 A34對糖尿病小鼠胰腺sEH表達量的影響
采用免疫組織化學染色考察胰島中sEH的表達情況。結果如圖7所示。
由圖7可知:胰腺中sEH主要在胰島細胞中表達,與正常對照組相比,模型組小鼠胰島中sEH表達量明顯增多(p<0.01);與模型組相比,給藥組小鼠胰島中sEH表達量明顯降低(p<0.01)。結果表明,STZ誘導的糖尿病小鼠模型中,胰島中sEH表達升高,A34能夠降低糖尿病小鼠胰島中sEH的表達量。
3.7 A34對糖尿病小鼠炎癥因子IFN-γ與IL-4的影響
糖尿病是由T細胞介導的自身免疫性疾病,涉及慢性炎癥過程。本研究采用ELISA法測定了小鼠血漿中促炎因子IFN-γ與抗炎因子IL-4水平,結果見表1。其中:正常對照組,n=6;模型組和A34組,n=9。
由表1可知:與正常對照組相比,模型組小鼠血漿IFN-γ水平、IFN-γ/IL-4比值均增高(p<0.05);與模型組相比,A34組小鼠血漿IL-4水平增高(p<0.01),IFN-γ/IL-4比值降低(p<0.05),INF-γ水平比較差異無統計學意義。這表明A34能夠調控糖尿病小鼠血漿細胞因子水平,降低促炎因子和抗炎因子的比例,改善由細胞因子失衡導致的β細胞的炎性損傷。據有關文獻報道,sEH抑制劑可以通過抑制NF-κB活化發揮抗炎作用[20]。根據本研究結果推測,A34可能是通過抑制NF-κB信號通路,減少機體炎癥反應,降低胰島β細胞凋亡,從而保護胰島細胞功能,發揮降糖作用。
4 討 論
T1DM是一種T細胞介導的自身免疫性疾病[21],其發病過程有多種免疫細胞參與,其中CD4+T淋巴細胞扮演了很重要的角色。CD4+T細胞根據分泌的細胞因子不同可分為T輔助細胞1(Th1)和T輔助細胞2(Th2)2種細胞亞群。在體內,Th1細胞主要分泌IFN-γ、TNF-α等促炎因子,Th2細胞主要分泌IL-4、IL-10等抗炎因子。正常機體內,Th1和Th2細胞亞群互相制約,達到平衡,維持機體免疫平衡。當平衡被破壞,Th1細胞亞群占優勢時,就會誘發一系列炎癥反應,炎癥因子與免疫系統相互作用,引起胰島β細胞結構與功能障礙[22],導致T1DM發生。
sEH是環氧脂肪酸的主要代謝酶,在多種疾病中sEH表達量增高、活性增強,而sEH抑制劑或者基因敲除sEH能夠在疾病控制方面發揮重要作用。sEH抑制劑在胃腸道炎癥模型小鼠中抑制了sEH活性,與模型組小鼠相比,sEH抑制劑治療組顯著減少了炎性細胞浸潤,降低了促炎細胞因子IFN-γ和TNF-α的水平,下調了LTB4和5-HETE炎癥介質,降低了活動性潰瘍的發生率,延緩了疾病進展[23]。在蛙皮素或精氨酸誘導的小鼠急性胰腺炎模型中,胰腺中sEH表達量和活性均增強,而進行sEH基因敲除或使用sEH抑制劑TPPU之后,抑制了NF-κB炎癥信號通路,減少了細胞死亡,改善了胰腺炎癥狀[24-25]。sEH抑制劑還能有效改善類風濕性關節炎[26]、牙周炎[27]等炎癥性疾病。此外,在高脂飲食誘導的2型糖尿病小鼠模型及糖尿病患者中,胰島β細胞中sEH表達量顯著升高,而基因敲除sEH或者抑制sEH活性,減輕了胰島β細胞氧化應激、細胞凋亡及去分化,改善了糖尿病癥狀[3]。在STZ誘導的T1DM小鼠模型中,基因敲除sEH或者通過sEH抑制劑治療之后,能夠減少胰島細胞凋亡,增強胰島β細胞葡萄糖刺激胰島素分泌功能,改善胰島素的敏感性,降低血糖[28-29]。
5 結 語
1)本文以新型sEH抑制劑A34作為藥物,通過多參數考察驗證了其對T1DM小鼠的降糖作用機制。結果表明,A34通過調控促炎和抗炎細胞因子的動態平衡,保護胰島β細胞免受損傷,改善T1DM小鼠多飲、多食狀況,緩解T1DM小鼠血糖的增長,提高糖尿病小鼠血漿胰島素水平及對血糖的調控能力,具有顯著的降血糖作用。
2)A34能夠降低T1DM小鼠血漿IFN-γ/IL-4比值,這表明胰島β細胞保護功能可能是通過調控淋巴細胞因子的釋放、調節Th1/Th2 失衡狀態以及減輕STZ所起的炎癥免疫反應實現的。本研究的發現提示,A34可能對與炎癥反應相關的一些其他疾病也有一定的治療作用。
本研究僅對A34的降糖機制進行了初步探索,尚有不足之處。例如:未進行A34在體內對sEH抑制作用的研究;未明確A34的降糖作用是否通過抑制sEH、提高或維持環氧脂肪酸的水平來實現。后續還需通過體外細胞實驗、基因敲除或過表達、液質聯用技術等多種手段確認A34的降糖機制。
參考文獻/References:
[1] SPECTOR A A.Arachidonic acid cytochrome P450 epoxygenasepathway[J].Journal of Lipid Research,2009,50 (supl):S52-S56.
[2] WAGNER K M,MCREYNOLDS C B,SCHMIDT W K,et al.Soluble epoxide hydrolase as a therapeutic target for pain,inflammatory and neurodegenerative diseases[J].Pharmacology & Therapeutics,2017,180:62-76.
[3] DOS S L R B,FLEMING I.Role of cytochrome P450-derived,polyunsaturated fatty acid mediators in diabetes and the metabolic syndrome[J].Prostaglandins & Other Lipid Mediators,2020. DOI:10.1016/j.prostaglandins.2019.106407.
[4] MALLIGA R I,KUNDU B,WOOD C M.Soluble epoxide hydrolase inhibitors:an overview and patent review from the last decade[J].Expert Opinion on Therapeutic Patents,2022,32(6):629-647.
[5] ZARRIELLO S,TUAZON J P,COREY S,et al.Humble beginnings with big goals:Small molecule soluble epoxide hydrolase inhibitors for treating CNS disorders[J].Progress in Neurobiology,2019,172:23-39.
[6] KOIKE S,HSU M F,BETTAIEB A,et al.Genetic deficiency or pharmacological inhibition of soluble epoxide hydrolase ameliorates high fat diet-induced pancreatic β-cell dysfunction and loss[J].Free Radical Biology & Medicine,2021,172:48-57.
[7] DEWEY S,LAI Xianyin,WITZMANN F A,et al.Proteomic analysis of hearts from Akita mice suggests that increases in soluble epoxide hydrolase and antioxidative programming are key changes in early stages of diabetic cardiomyopathy[J].Journal of Proteome Research,2013,12(9):3920-3933.
[8] HU Jiong,DZIUMBLA S,LIN Jihong,et al.Inhibition of soluble epoxide hydrolase prevents diabetic retinopathy[J].Nature,2017,552(7684):248-252.
[9] ZHANG Lening,VINCELETTE J,CHEN D,et al.Inhibition of soluble epoxide hydrolase attenuates endothelial dysfunction in animal models of diabetes,obesity and hypertension[J].European Journal of Pharmacology,2011,654(1):68-74.
[10]JOUIHAN S A,ZULOAGA K L,ZHANG Wenri,et al.Role of soluble epoxide hydrolase in exacerbation of stroke by streptozotocin-induced type 1 diabetes mellitus[J].Journal of Cerebral Blood Flow and Metabolism,2013,33(10):1650-1656.
[11]LURIA A,BETTAIEB A,XI Yannan,et al.Soluble epoxide hydrolase deficiency alters pancreatic islet size and improves glucose homeostasis in a model of insulin resistance[J].Proceedings of the National Academy of Sciences of the United States of America,2011,108(22):9038-9043.
[12]ANITA N Z,SWARDFAGER W.Soluble epoxide hydrolase and diabetes complications[J].International Journal of Molecular Sciences,2022. DOI:10.3390/IJMS23116232.
[13]JAMES R,JUSTIN R,DAVID W,et al.GSK2256294 Decreases sEH (soluble epoxide hydrolase) activity in plasma,muscle,and adipose and reduces f2-isoprostanes but does not alter insulin sensitivity in humans[J].Hypertension,2021,78(4):1092-1102.
[14]LI Ping,CHEN Yanli,LUO Luxiang,et al.Immunoregulatory effect of acanthopanax trifoliatus (L.) Merr. polysaccharide on T1DM mice[J].Drug Design,Development and Therapy,2021,15:2629-2639.
[15]LUO Pengcheng,CHANG Hsinhsin,ZHOU Yiqiang,et al.Inhibition or deletion of soluble epoxide hydrolase prevents hyperglycemia,promotes insulin secretion,and reduces islet apoptosis[J].The Journal of Pharmacology and Experimental Therapeutics,2010,334(2):430-438.
[16]CHEN Lingdan,FAN Cheng,ZHANG Yi,et al.Beneficial effects of inhibition of soluble epoxide hydrolase on glucose homeostasis and islet damage in a streptozotocin-induced diabetic mouse model[J].Prostaglandins & Other Lipid Mediators,2013,104/105:42-48.
[17]TIAN Ye,LI Shuo,DONG Kuan,et al.Discovery of benzamide derivatives containing urea moiety as soluble epoxide hydrolase inhibitors[J].Bioorganic Chemistry,2022. DOI:10.1016/J.BIOORG.2022.105898.
[18]崔玉琴,趙鶯歌,田瑞瓊,等.羧甲基殼聚糖接枝聚丙烯酸水凝膠的制備及體內外評價[J].河北科技大學學報,2015,36(5):504-510.
CUI Yuqin,ZHAO Yingge,TIAN Ruiqiong,et al.Preparation of carboxymethyl chitosan grafted polyacrylic acid hydrogel and its evaluation in vitro and in vivo[J].Journal of Hebei University of Science and Technology,2015,36(5):504-510.
[19]SHEN H C,HAMMOCK B D.Discovery of inhibitors of soluble epoxide hydrolase:A target with multiple potential therapeutic indications[J].Journal of Medicinal Chemistry,2012,55(5):1789-1808.
[20]侯文睿,謝勝男,魯憬莉,等.RegⅢ/胰島素原雙基因質粒的構建及其對1型糖尿病小鼠的治療作用[J].藥學學報,2010,45(8):987-994.
HOU Wenrui,XIE Shengnan,LU Jingli,et al.Recombination of RegⅢ-proinsulin-pBudCE4.1 plasmid and its therapeutic effect on STZ-induced type 1 diabetes mellitus[J].Acta Pharmaceutica Sinica,2010,45(8):987-994.
[21]陳小娟,何福根,周迪夷.杜仲多糖對自發性2型糖尿病db/db小鼠糖脂代謝的影響[J].中國藥學雜志,2020,55(17):1433-1438.
CHEN Xiaojuan,HE Fugen,ZHOU Diyi.Effect of Eucommiaulmoides polysaccharide on db/db diabetic mice′s glycolipid metabolism[J].Chinese Pharmaceutical Journal,2020,55(17):1433-1438.
[22]ZHANG Wanying,YANG A L,LIAO Jie,et al.Soluble epoxide hydrolase gene deficiency or inhibition attenuates chronic active inflammatory bowel disease in IL-10(-/-) mice[J].Digestive Diseases and Sciences,2012,57(10):2580-2591.
[23]BETTAIEB A,CHAHED S,TABET G,et al.Effects of soluble epoxide hydrolase deficiency on acute pancreatitis in mice[J].PLoS One,2014. DOI:10.1371/journal.pone.0113019.
[24]BETTAIEB A,CHAHED S,BACHAALANY S,et al.Soluble epoxide hydrolase pharmacological inhibition ameliorates experimental acute pancreatitis in mice[J].Molecular Pharmacology,2015,88(2):281-290.
[25]TRINDADE D S C A,CLEMENTE N J `T,ABDALLA H B,et al.Soluble epoxide hydrolase inhibitor,TPPU,increases regulatory T cells pathway in an arthritis model[J].FASEB Journal,2020,34(7):9074-9086.
[26]TRINDADE D S C A,BETTAIEB A,NAPIMOGA M H,et al.Soluble epoxide hydrolase pharmacological inhibition decreases alveolar bone loss by modulating host inflammatory response,RANK-related signaling,endoplasmic reticulum stress,and apoptosis[J].The Journal of Pharmacology and Experimental Therapeutics,2017,361(3):408-416.
[27]LUO Pengcheng,CHANG H H,ZHOU Yiqiang,et al.Inhibition or deletion of soluble epoxide hydrolase prevents hyperglycemia,promotes insulin secretion,and reduces islet apoptosis[J].The Journal of Pharmacology and Experimental Therapeutics,2010,334(2):430-438.
[28]CHEN L D, FAN C,ZHANG Y,et al.Beneficial effects of inhibition of soluble epoxide hydrolase on glucose homeostasis and islet damage in a streptozotocin-induced diabetic mouse model[J].Prostaglandins Other Lipid Mediat,2013,104/105:42-48.
[29]LUO P C,CHANG H H,ZHOU Y Q,et al.Inhibition or deletion of soluble epoxide hydrolase prevents hyperglycemia,promotes insulin secretion,and reduces islet apoptosis[J].Journal of Pharmacology and Experimental Therapeutics,2010,334:430-438.

